
第一章化学反应与能量变化测试题(二)
一、选择题
1.“焓”是指()
A.物质所具有的能量 B.反应热的变化
C.化学键所具有的能量 D.物质的一种化学性质
2.甲烷是一种高效清洁的新能源,0.5mol甲烷完全燃烧生成液态水时放出445 KJ热量,则下列热化学方程式中正确的是()
A.2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l);ΔH = +890 KJ·mol-1
B.CH4(g) + 2O2(g) == CO2(g) +2H2O(l);ΔH = +890 KJ·mol-1
C.CH4(g) + 2O2(g) == CO2(g) +2H2O(l);ΔH = -890 KJ·mol-1
D.2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l);ΔH = -890 KJ·mol-1
3.在U形管中,用惰性电极电解硫酸钠和石蕊的混合液,一段时间后,下列说法不正确的是()
A.电解后溶液仍显中性 B.两极均有气体产生
C.阳极附近的颜色变红 D.阴极附近的颜色变红
4.用惰性电极和相同电量分别电解①HCl ②NaNO3③CuCl2④AgNO3四种电解质溶液,在理论上生成气体的总体积(同温同压下)由多到少的顺序是()
A.④③②① B.①②③④ C.④②①③ D.③④①②
5.下图中能验证氯化钠溶液(含酚酞)电解产物的装置是()
6.下列说法中,正确的是()
A.构成原电池两个电极的材料必须是两种金属
B.由铜,锌作电极与硫酸铜溶液组成的原电池中铜是正极
C.电子通过外导线由锌流向铜,通过硫酸溶液被氢离子得到放氢气
D.铜,锌原电池工作时,若有13g锌溶解,电路中有0.2mol电子通过
7.下列说法中正确的是()
A.原电池的正极和电解池的阳极都是发生氧化反应
B.用铂做电极电解NaOH溶液,因溶质的质量不变,所以浓度也不变
C.在电解池中,阳离子向阳极移动,在原电池中,阳离子向负极移动
D.电解食盐水时,阴极区溶液里OH-离子的浓度相对增大,使酚酞试液变红
8.下列关于实验现象的描述不正确的是()
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.若镀层被破坏,镀锡铁比镀锌铁更易被腐蚀
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
9.有X、Y、Z、M四种金属,已知:X可以从Y 的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z 的离子共存于电解液中,Y离子先放电;M的离子的氧化性强于Y的离子,则这四种金属的活动性由强到弱的顺序是()
A.X > Y > Z > M B.X > Z > M > Y
C.M > Z > X > Y D.X > Z > Y > M
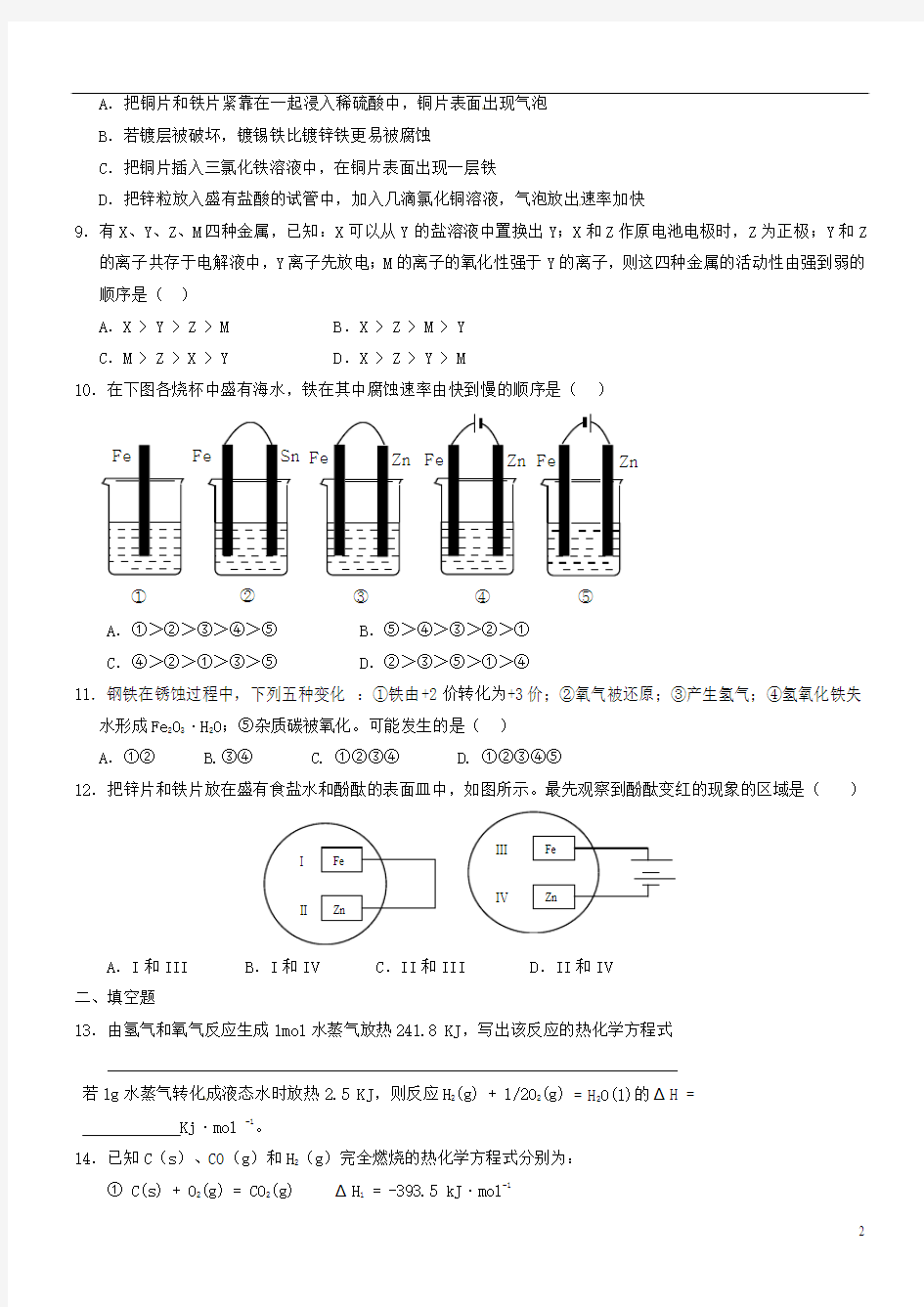
10.在下图各烧杯中盛有海水,铁在其中腐蚀速率由快到慢的顺序是()
⑤
④
③
②
①
A.①>②>③>④>⑤B.⑤>④>③>②>①
C.④>②>①>③>⑤D.②>③>⑤>①>④
11.钢铁在锈蚀过程中,下列五种变化:①铁由+2价转化为+3价;②氧气被还原;③产生氢气;④氢氧化铁失水形成Fe2O3·H2O;⑤杂质碳被氧化。可能发生的是()
A.①② B.③④ C. ①②③④ D. ①②③④⑤
12.把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示。最先观察到酚酞变红的现象的区域是()
A.I和III B.I和IV C.II和III D.II和IV
二、填空题
13.由氢气和氧气反应生成1mol水蒸气放热241.8 KJ,写出该反应的热化学方程式
若1g水蒸气转化成液态水时放热2.5 KJ,则反应H2(g) + 1/2O2(g) = H
2O(l)的
ΔH =
Kj·mol -1。
14.已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
① C(s) + O2(g) = CO2(g) ΔH1 = -393.5 kJ·mol-1