
精细有机合成课程提纲及练习(供参考)
9.利用卤素交换制备氟代烷反应, 此类反应在DMSO 中进行,反应速度比在甲醇中快107倍。为什么?
答: 卤素交换制备氟代烷反应,其反应过程可用下式表示:
此反应是一个双分子的亲核取代反应,亲核试剂(或离子)的亲核能力越强,反应速度越
快。甲醇是质子传递性溶剂,是氢键给体,F -离子能与醇中的氢形成氢键,由于F -
离子的
电荷密度大,因此溶剂化的作用很强,因而在甲醇中F -
的亲核能力很弱。在DMSO 中,DMSO 是非质子传递极性溶剂,它可使正离子专一性的溶剂化而不能使负离子专一性溶剂
化,负离子成为活泼的“裸负离子”,因此以DMSO 为溶剂的F -
离子的亲核能力很强。因此卤素交换制备氟代烷反应,在DMSO 中进行比在甲醇中快很多。 10.2-萘酚与苄基溴反应,采用不同的溶剂,得到的产物不同。
答:在二甲基酰胺的极性非质子溶剂中,由于溶剂对负离子的溶剂化作用很小,得到的主要产物为O-烷基化产物;而在质子溶剂(H 2O )中,由于萘酚负离子与水分子形成牢固的氢键,使氧的反应中心受到溶剂的屏蔽,而主要以C-烷化产物为优势。
11.已知下列负离子的电荷密度大小顺序为:F –
>C l –
>PhO –
>Br –
>I –
>CN –
,试讨论说明它们在质子传递性溶剂中和非质子传递极性溶剂中亲核活性次序。
答:在质子传递性溶剂中,负离子可与溶剂的质子形成氢键,即溶剂化。负离子的电荷密度越大,则溶剂化能力越强,因而其亲核活性越小,因此在质子传递性溶剂中,负离子的亲核活性次序为F –
< Cl –
< PhO –
< Br –
< I –
<CN –
在非质子传递极性溶剂中,溶剂可使正离子专一性的溶剂化而不能使负离子专一性溶剂
,因此负离子的电荷密度越大,则其亲核能力越强。所以在非质子传递极性溶剂中,负离子的亲核活性次序为F –
>Cl –
>PhO –
>Br –
>I –
>CN –
CH 2Br
+
DMF
H 2O
++NaBr
NaBr
ONa
OCH 2
CH 2
ONa
3—I
F
CH 3+I £
-
δ-δ-F
CH 3
I
CH 3I CH 3F ++
I ―
F ―
5.卤素对双键进行亲电加成和自由基加成的机理;卤化氢对双键进行亲电加成和自由基加成的机理(只能是HBr );加成的定位规律;次氯酸与丙烯进行亲电加成的机理。
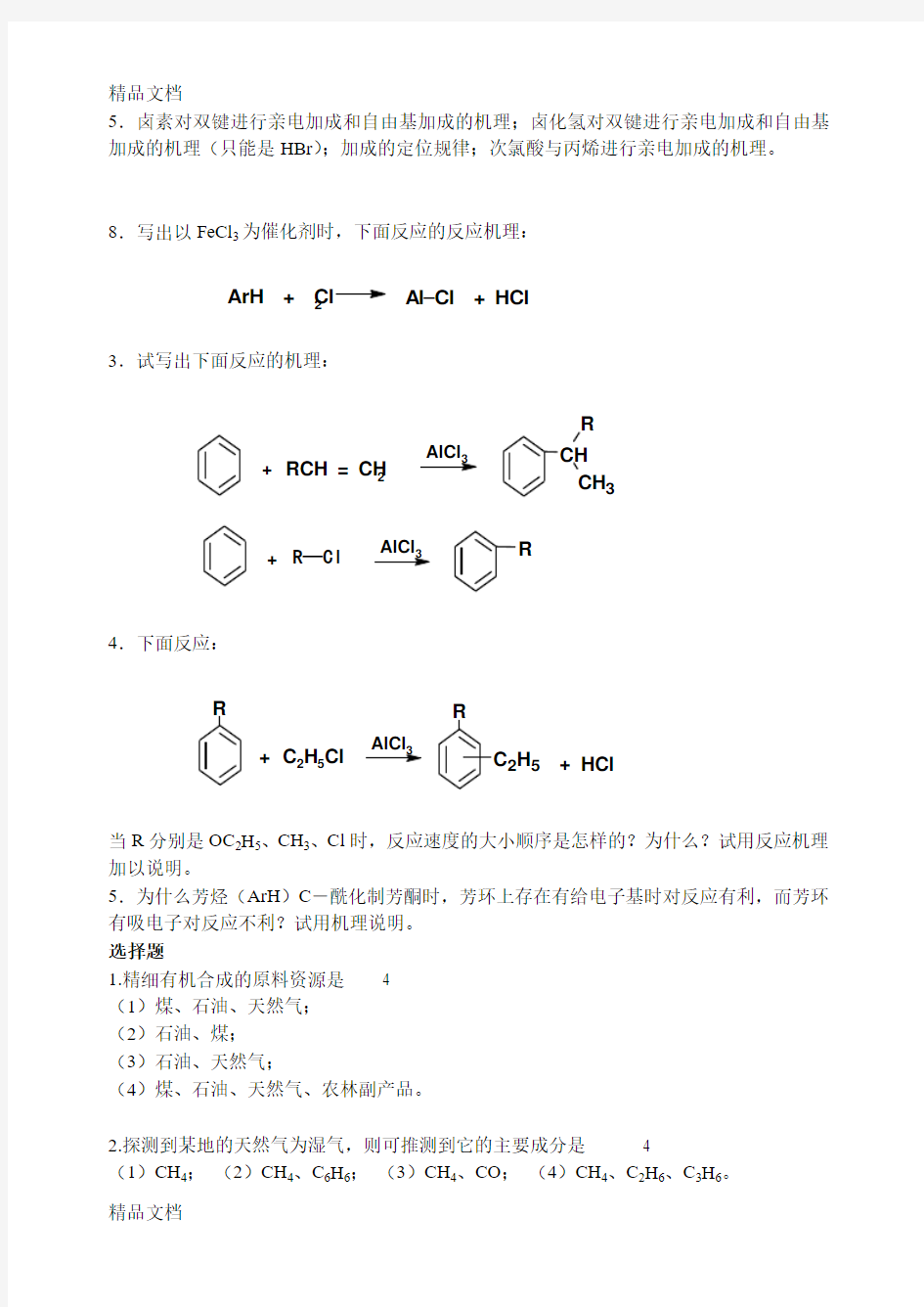
8.写出以FeCl 3为催化剂时,下面反应的反应机理:
3.试写出下面反应的机理:
4.下面反应:
当R 分别是OC 2H 5、CH 3、Cl 时,反应速度的大小顺序是怎样的?为什么?试用反应机理加以说明。
5.为什么芳烃(ArH )C -酰化制芳酮时,芳环上存在有给电子基时对反应有利,而芳环有吸电子对反应不利?试用机理说明。 选择题
1.精细有机合成的原料资源是 4 (1)煤、石油、天然气; (2)石油、煤; (3)石油、天然气;
(4)煤、石油、天然气、农林副产品。
2.探测到某地的天然气为湿气,则可推测到它的主要成分是 4
(1)CH 4; (2)CH 4、C 6H 6; (3)CH 4、CO ; (4)CH 4、C 2H 6、C 3H 6。 R
+ HCl
3
C 2H 5Cl
R
C 2H 5 + ArH + Cl 2
Al
Cl + HCl
+ RCH = CH 2
CH R
3 + R—Cl
AlCl 3
3
R
3.对于一个复杂的精细化学品的合成,下面说法错误的是 3 (1)可以采用同一原料,不同的单元反应来完成; (2)可以采用不同的原料,不同的单元反应来完成; (3)只能采用一种合成路线来完成; (4)可以采用不同的合成路线来完成。
4.动植物油脂水解可得到: 4 (1)葡萄糖和果糖;
(2)可以得到脂肪醇和甘油; (3)可以得到乙醇和丙酮;
(4)可以得到各种脂肪酸和甘油。
5.关于芳香族的π络合物与σ络合物,下面的说法不正确的是 1 (1)π络合物是亲电试剂已与芳环上的某一碳原子形成了σ键; (2)σ络合物是亲电试剂已与芳环上的某一碳原子形成了σ键; (3)π络合物是生成σ络合物的过渡态,它们之间存在平衡; (4)σ络合物在溶液中可导电。
6.关于下面的亲电取代反应,下列说法正确的是2
(1)亲电试剂E +极活泼,生成的产物选择性好;
(2)亲电试剂E +极活泼,生成的产物a 、b 、c 数量相当; (3)亲电试剂E +极不活泼,生成的产物选择性差; (4)亲电试剂E +极不活泼,几乎不生成a 和c 。 7.某一脂肪族亲核取代反应的反应历程可表示如下:1
下面说法正确的是:
(1)它是一个二步反应,属于单分子反应历程; (2)它是一个二步反应,属于双分子反应历程; (3)第一步是控制步骤,反应速度=k[RX][Nu:] CH 3
E
+
+CH 3
E +
+CH 3
E CH 3
(a)
(b)
(c)
X
-
R
X
慢
R ++快
Nu:
-
R
Nu
+R +
(4)第二步是控制步骤,反应速度=k[RX]。 8.某一卤代烷发生水解反应
下面说法正确的是2
(1)当R -X 为CH 3-X 时,属于S N 1反应; (2)当R -X 为(CH 3)3-X 时,属于S N 1反应;
(3)当R -X 为(CH 3)3-X 时,介于S N 1和S N 2之间的反应 (4)当R -X 为CH 3-X 时,属于S N 2反应。
9.对于下面两个反应
下面说法正确的是:2 (1)a 为E 2,b 为S N 2; (2)a 为S N 2,b 为E 2; (3)a 、b 都为S N 2; (4)a 、b 都为E 2
10.下面反应的主要产物是1
(1)a (2)b (3)c (4)a ,b ,c
11.一个游离基反应的完成,可以下几个阶段来描述 1 (1)游离基的生成、反应链的传递、反应链的终止; (2)反应链的传递、反应链的终止、游离基的生成; HX
R X ROH ++HOH H 3CH 2C
C
CH CH 3
33
Br
-HBr NaOH H 3CH 2C C C CH 3
3
3
H 3CH 2C C
CH CH 3H 33
H 3CH 2C C CH CH 3
23
++(a)
(b)
(c)
CH 2CH 2Br H +C 2H 5OH CH 2=CH 2++C 2H 5O -+C 2H 5OCH 2CH 3Br
-
+CH 2
CH 3
Br
a b
C 2H 5O -Br -
(3)反应链的终止、游离基的生成、反应链的传递;
(4)光照产生游离基、产生的游离基在受热下反应、游离基相互碰撞而终止反应。
12.一种化工产品的合成路线,指的是 1
(1)选用什么原料,经由哪几步单元反应来制备; (2)原料的预处理和反应物的后处理; (3)采用间歇式操作还是采用连续式操作;
(4)反应物的分子比,主要反应物的转化率以及反应过程的温度、压力和时间等。 13.关于间歇式操作,下面说法错误的是 4
(1)是将各种反应原料按一定的顺序加到反应器中,并在一定温度、压力下经过一定时间完成特定的反应,然后将反应好的物料从反应器中放出; (2)反应物的组成随时间而改变;
(3)反应物的温度和压力也可以随时间而改变; (4)间歇式操作仅适于反应时间要求很长的反应。 14.关于连续操作的说法错误的是: 3
(1)连续操作是将各种反应原料按一定的比例和恒定的速度不断地加入到反应器中,并且从反应器中以恒定的速度不断地排出反应物;
(2)对于连续操作,在常操作的条件下,反应器中某一特定部位的反应物料组成、温度和压力原则上是不变的;
(3)在连续操作过程中,无法实现传质与传热。
(4)相对于间歇式操作而言,连续操作容易实现高度自动控制,而且也容易实现节能。 15.对于理想混合型反应器,下面说法正确的是: 1 (1)反应器中各处的物料组成、温度相同;
(2)流出物料的组成、温度与反应器中的物料组成和温度不相同; (3)不具有返混;
(4)各物料质点的停留时间相同。 16.对于理想置换型反应器,说法错误的是 2
(1)在垂直于物料流向的任何一个截面上,所有的物系参数都相同(组成、温度、压力、流速);
(2)适合于间歇操作; (3)不具有返混;
(4)各物料质点在反应器中的停留时间相同。
17.对于下面的放射性标记碘负离子I *–与碘甲烷之间的碘交换反应,分别选择水和DMF (N,N-二甲基甲酰胺)作为反应介质,其反应速度 3
(1)在两种溶剂中的反应速度相同; I
↓
+CH 3I
k
CH 3
I ↓
δ
-I
δ-
↓
CH 3I
+
(2)在水中反应速度快;
(3)在DMF中反应速度快;
(4)由于这两种介质是非极性溶剂,所以反应不能发生。
18.质子传递型溶剂一定是 1
(1)极性溶剂;
(2)非极性溶剂;
(3)水;
(4)无机化合物。
19.非质子传递极性溶剂, 3
(1)能起氢键给体作用;
(2)使负离子专一性的溶剂化;
(3)使正离子专一性的溶剂化;
(4)是电子对受体溶剂。
20.下面说法正确的是 2
(1)溶剂的介电常数越大,则溶剂的溶剂化能力越强;
(2)溶剂的介电常数越大,则使离子对离解为独立离子的能力越强;
(3)溶剂的介电常数越大,则溶剂的酸性越强;
(4)溶剂的介电常数越大,则其导电能力越强。
21.水常常作为离子型反应的溶剂,这是因为 1
(1)水的介电常数特别高( =78.4),使异性电荷之间的静电引力降低,从而使离子对完全离解;
(2)水既是氢键给体,又是氢键受体;
(3)水能溶解大多数离子体化合物;
(4)水无色无味无毒,价格低廉。
22.(C4H9)4N+·HSO4–是季铵盐,可作为相转移催化剂使用。(C4H9)4N+通常被认为是较软的正离子,若水溶液中同时有F–、Cl–、Br–、I–几种负离子存在,则这几种负离子被季铵正离子提取到非极性溶剂中的容易程度是:2
(1)F–>Cl–>Br–>I–;
(2)F–<Cl–<Br–<I–;
(3)F–= Cl–= Br–= I–;
(4)无法比较。
23.下面说法错误的是3
(1)列管式固定床反应器中,催化剂固定在反应床层上,反应进行时,催化剂是固定的;(2)在流化床反应器中,反应进行时,催化剂处于流态化,漂浮在气体中做不规则运动;(3)在气固相接触催化反应中,催化剂是气体,反应原料是固体;
(4)在气固相接触催化反应中,催化剂是固体,反应原料是气体。反应原料气态混合物在一定温度、压力下通过固体催化剂来完成反应。
24.关于催化剂具有的基本特征,下列说法错误的是:4
(1)产生中间产物,改变反应途径,因而降低反应活化能和加速反应速率;
(2)不能改变平衡状态和反应热,催化剂同时加速正反应和逆反应的速率;
(3)具有选择性,可使化学反应朝所期望的方向进行,抑制不需要的副反应。
(4)在反应过程中不参与中间反应,但降低反应物的活化能。
25.固体催化剂通常由下面几部分构成: 1
(1)催化活性物质、助催化剂和载体;
(2)固体和气体;
(3)能加速正反应而不能加速副反应的固体物质及能起粘结作用的载体;
(4)能产生活性中心的固体物质及比表面积很大的毒物。
26.催化剂的选择性是指:1
(1)催化剂专门对某一化学反应起加速作用的性能;
(2)催化剂能加速所有的化学反应;
(3)用少量的催化剂就可生成大量的目的产物;
(4)催化剂在加速一个化学反应的同时,还必须抑制另一个反应。
27.催化剂中毒的原因不是因为 3
(1)原料中有可使催化剂中毒的物质而使催化剂中毒;
(2)在催化剂的制备过程中带入了使催化剂中毒的物质而使催化剂中毒;
(3)由于大量的反应原料气体包覆了催化剂;
(4)毒物破坏或遮盖了催化剂的活性中心。
28.催化剂失活的原因不是因为 2
(1)由于毒物的存在使催化剂中毒而失去活性;
(2)由于使用的时间太长;
(3)由于积炭、焦油物等物质将催化剂的孔道堵塞而使催化剂失去活性;
(4)由于热的作用,使催化剂的结构发生了变化。
29.催化剂的优劣主要采用下面哪几个指标来评价? 1
(1)选择性、活性、稳定性;
(2)机械强度、比表面积、稳定性;
(3)活性、比表面积、稳定性;
(4)选择性、活性、比表面积。
30.固体催化剂中的助催化剂的作用是 2 (1)对目的反应具有良好的催化作用;
(2)本身没有催化活性或催化活性很小,但是能提高催化活性物质的活性、选择性或稳定性;
(3)是催化活性物质的支持物、粘结物或分散体; (4)增强催化剂的机械强度。
31.溴化氢在光照条件下与丙烯发生反应,得到的产物是: 1
32.下面反应,溶剂极性增加,预计反应速度会: 3
(1)不变; (2)加快; (3)减慢;
(4)先减慢,到一定程度后又会加快。 33.下面反应得到的主要产物是 1
(1)a ; (2)b ; (3)a 和b ; (4)都没有。
34.下面几种烯烃与卤化氢在AlCl 3的作用下进行加成,烯烃的反应能力的大小顺序是:4
CH CH 2
R C
H 2CH 2
C
H 2CHCl CH
CH
R R
a
b
c
d CH 2CH 2Br C H 3CH
CH 3
C H 3CH
CH 2
BrH 2C CH
CHBr C H 3(1)(2)
(3)(4)
CH 2
Br C H 3+NaOH
CH 2
OH C H 3+NaBr
CH 3
+Cl 2
CH
3
Cl
FeCl 3
+
CH 2Cl
a
b
(1)a >b >c >d ; (2)b >c >d >a ; (3)c >b >a >d ; (4)d >a >b >c 。
35.利用单质溴使芳环溴化的过程中,一般向体系中加入氧化剂,其目的是:1 (1)将生成的HBr 氧化成Br 2,以充分利用溴素; (2)氧化参加反应的Br 2;
(3)因为溴化是一个可逆反应,加入氧化剂可使反应进行彻底; (4)氧化剂是作为溴化反应的催化剂。
36.利用单质碘使芳环直接碘化的过程中,一般向体系中加入氧化剂,其目的是:3 (1)作为反应的助催化剂; (2)作为反应的催化剂;
(3)因为碘化是一个可逆反应,加入氧化剂可使反应进行彻底;
(4)生成的HI 是强酸,会影响芳环的碘化,加入氧化剂以破坏HI 的强酸性。
37.对于下面的反应,氯化深度是指:3
(1)该反应属于连串反应; (2)反应中k 1<k 2<k 3;
(3)每摩尔苯所消耗的氯气量(摩尔); (4)生成产物的酸强度。
38.工业硫酸有以下几种规格 1 (1)92.5% H 2SO 4和98% H 2SO 4; (2)20% H 2SO 4和65% H 2SO 4;
(3)92.5% H 2SO 4、98% H 2SO 4和104.5% H 2SO 4; (4)65% H 2SO 4和98% H 2SO 4。
39.工业发烟硫酸有以下几种规格 2 (1)92.5% H 2SO 4和98% H 2SO 4; (2)20% H 2SO 4和65% H 2SO 4;
(3)92.5% H 2SO 4、98% H 2SO 4和104.5% H 2SO 4; C 6H 6+
Cl 2
C 6H 5Cl
HCl +
1+Cl
2
C 6H 4Cl 3HCl
+
C 6H 4Cl 2k +Cl 2C 6H 4Cl 2HCl +C 6H 5Cl k 2
(4)65% H 2SO 4和98% H 2SO 4。
40.当以浓H 2SO 4或发烟为磺化剂时,磺化反应的速度可用下式表示:
2
2]
[1
][3
O H ArH k SO ?
'=υ 式中ArH 表示被磺化的芳烃,则此式说明了: 2
(1)磺化反应的速度与体系中生成的水的量有关,水越多,反应速度越快; (2)磺化反应的速度与体系中生成的水的量有关,水越少,反应速度越快; (3)磺化反应的速度与体系中生成的水的量无关;
(4)磺化反应的速度与体系中生成的水的量的关系不明确。
41.磺化反应过程中,为了为避免磺化剂浓度局部过高和可能发生局部过热现象而导致副反应,可采取下列措施:1
(1)搅拌; (2)加热; (3)冷却; (4)加入水。 42.在溶剂中用SO 3磺化时,溶剂的目的是2 (1)作为冷却剂;
(2)稀释反应物,控制反应速度,抑制副反应; (3)作为反应物;
(4)稀释反应中生成的水。
43.下列几种磺化剂:SO 3、Cl-SO 3H 、H 2SO 4·SO 3、H 2SO 4,它们的磺化能力大小顺序是1 (1)SO 3>Cl-SO 3H >H 2SO 4·SO 3>H 2SO 4; (2)Cl-SO 3H >SO 3>H 2SO 4·SO 3>H 2SO 4; (3)SO 3>H 2SO 4·SO 3>H 2SO 4>Cl-SO 3H ; (4)H 2SO 4>H 2SO 4·SO 3>SO 3>Cl-SO 3H 。
44.用混酸硝化芳烃,混酸是指 1 (1)硝酸与硫酸的混合物; (2)硝酸与盐酸的混合物; (3)硝酸与磷酸的混合物; (4)硫酸与盐酸的混合物。
45.某芳烃用混酸硝化,考察其动力学过程,属于动力学型,这说明 2 (1)芳烃与混酸硝化反应的速度很快;
(2)芳烃在两相界面处发生反应的数量远远少于芳烃扩散到酸相中发生反应的数量; (3)芳烃在两相界面处发生反应的数量远远大于芳烃扩散到酸相中发生反应的数量;
(4)反应在两相的界面上发生。
46.甲苯在66.6% ~71.6% H2SO4中硝化,其动力学特征是慢速传质型,此时反应速度受传质的控制。则下面说法正确的是: B
A. 甲苯硝化发生在有机相中;
B. 反应主要在酸膜中或两相的边界层上进行;
C. 甲苯与混酸硝化反应的速度很慢;
D. 甲苯在两相界面处发生反应的数量远远少于甲苯扩散到酸相中发生反应的数量。
47.在间歇硝化过程中,反应的开始阶段,突然停止搅拌或由于搅拌桨叶脱落而导致搅拌失效是非常危险的,这是因为: 1
(1)停止搅拌,两相很快分层,大量活泼的硝化剂在酸相中积累,若再次开动搅拌,将会突然发生激烈反应,瞬间放出大量热,温度失去控制,因而发生事故;
(2)硝酸将会分解而发生爆炸;
(3)停止搅拌会使反应物的粘度增加很快;
(4)反应中生成的热量无法及时移走。
48.硝化反应中的相比是指 2
(1)硝酸和被硝化物的分子比;
(2)混酸与被硝化物的重量比;
(3)混酸和被硝化物的摩尔比;
(4)混酸中硝酸与硫酸的分子比。
49.烷基苯或多烷基苯用混酸硝化时,若硝化条件不适宜,硝化液会发黑变暗,其原因是1 (1)硝化过程中硝酸用量不足;
(2)硝化过程中硝酸用量过量;
(3)硝化过程中硫酸用量不足;
(4)硝化过程中生成了大量的NO2。
50.关于还原反应,下列说法错误的是4
(1)在还原剂的参与下,能使某原子得到电子或电子云密度增加的反应称为还原反应;(2)在有机分子中增加氢或减少氧的反应称为还原反应。
(3)氢化是还原反应的一种形式;
(4)有机化合物从电解槽的阳极上获得电子而完成的反应称为还原反应。
51.关于Raney Ni,下面说法正确的是:2
(1)Raney Ni由Al-Ni合金构成;
(2)是一种具有高度孔隙的、外观为灰黑色粉末状的、可作为催化氢化催化剂的骨架镍。
(3)可保存在空气中;
(4)属于载体型催化剂。
52.关于液相催化氢化,下面的说法正确的是1
(1)氢化在液相介质中进行,是气-液-固多相反应;
(2)氢化在液相介质中进行,是气-液相反应;
(3)氢化在液相介质中进行,是液-液相反应;
(4)其基本过程是吸附-反应-再吸附。
53.在催化氢化反应中,氢气的来源不可以是:4
(1)将氯化钠的水溶液电解;
(2)将天然气转化;
(3)水煤气净化;
(4)将空气深冷分离。
54.用铁屑还原硝基化合物,向体系中加入电解质,其目的是1
(1)增加介质的导电能力,加快反应速度;
(2)电解质是该反应的催化剂,所以必须加入;
(3)电解质可起到盐析作用,使产物分离;
(4)加入的电解质本身就是还原剂。
55.用铁屑还原硝基化合物时,铸铁作为还原剂的效果比熟铁粉要好,这是因为1 (1)铸铁中含有的杂质多,可形成微电池,所以效果好;
(2)熟铁粉中含有太多的杂质,所以效果不好;
(3)铸铁本身可起到电解质的作用,所以效果好;
(4)因为熟铁粉无法进行铁的预蚀,所以效果不好。
56.某人用锌粉还原硝基苯希望得到苯胺,可他得到的是氢化偶氮苯,这可能是因为3 (1)反应是在酸性条件下进行的;
(2)反应是在中性条件下进行的;
(3)反应是在碱性条件下进行的;
(4)锌粉中含有杂质铁。
57.有人想将间二硝基苯还原为间硝基苯胺,你认为他可以采用哪种还原剂?3
(1)铁屑;
(2)锌粉;
(3)二硫化钠;
(4)铝氢化锂。
58.脂肪族伯胺与亚硝酸进行重氮化反应,生成的的重氮盐不会1
(1)分解而放出N2;
(2)发生亲核取代反应,生成伯醇;
(3)发生重排和加成等副反应生成仲醇、卤代烷和烯烃化合物;
(4)稳定地存在。
59.芳香族伯胺进行重氮化反应时,反应体系中必须1
(1)亚硝酸过量及始终呈强酸性;
(2)亚硝酸不能过量及始终呈强酸性;
(3)体系呈弱酸性;
(4)用盐酸作为酸性物质。
60.重氮化反应进行时,反应体系中的亚硝酸始终是过量的,过量的亚硝酸可用下面的方法来检测。1
(1)用碘化钾淀粉试纸;
(2)用酚酞变色;
(3)用甲基橙色;
(4)通过尝味道。
61.重氮化反应进行时,反应完成后,体系中过量的亚硝酸可用下面的方法来除掉:1 (1)加入尿素或氨基磺酸分解亚硝酸;
(2)加热分解;
(3)将它过滤;
(4)进行减压蒸馏。
62.下面反应得到的主要产物是1
(1)a;(2)b;(3)a和b;(4)都没有。
63.下面反应得到的主要产物是1
NH2
+C
H2CH CN NHCH
2CH
2
CH3
N
H CH CN
NH2
Br-CH2-CF3NHCH
2
CF3NHCF
2CH2 a b
(1)a;(2)b;(3)a和b;(4)都没有。
64.硫酸二甲酯和硫酸二乙酯这二种化学试剂,1
(1)是非常强烈的烷基化试剂,但是有剧毒;
(2)是非常强烈的烷基化试剂,而且没有毒性;
(3)烷基化的能力非常弱;
(4)没有烷基化能力。
65.关于平平加O或匀染剂O,下面说法错误的是:4
(1)它高碳伯醇的聚氧乙烯醚;
(2)它是非离子表面活性剂;
(3)它是由高碳伯醇与环氧乙烷反应而成;
(4)它由高碳伯醇与亚硝酸重氮化得到的。
66.关于Friedel-Crafs反应,指的是3
(1)N-烃化;(2)O-烃化;(3)C-烃化;(4)S-烃化。
67.关于三氯化铝(AlCl3),下面说法不正确的是2
(1)在一般使用温度是二聚体,二聚体失去缺电子性,所以二聚体对于付-克反应没有催化作用;
(2)它的价格很贵,而且其催化活性不是很高,所以在付-克反应中很少用它作催化剂;(3)它既可作为卤代烃,又可作为烯烃烷基化的催化剂;
(4)它在一定的温度下会升华。
68.羧酸与醇的酯化是一个可逆反应,为了破坏平衡,使反应朝右进行,哪种措施是无效4 (1)采用过量的醇或酸;
(2)从酯化混合物中蒸出酯;
(3)用带水剂从酯化混合物中蒸出生成的水;
(4)采用酯化催化剂。
69.用酰氯与芳烃反应制备芳酮,采用三氯化铝作为催化剂,则每摩尔酰氯消耗的三氯化铝摩尔数为?1
(1)0mol;(2)1mol;(3)2mol;(4)3mol。
70.自动氧化是指1
(1)某些有机物在室温遇到空气所发生的缓慢氧化反应;
(2)在空气中用氧化剂氧化某些有机物;
(3)氧气与有机物发生的游离基反应;
(4)凡是用空气作为氧化剂的氧化反应。
71.将油脂置于空气中,油脂会逐渐酸败,这是由于什么原因引起的?1
(1)油脂的自动氧化;
(2)油脂中存在微生物,会使油脂分解;
(3)油脂中含有发臭的物质; (4)由于光照的结果。
72.自动氧化反应过程中,所谓“自阻现象”是指2
(1)反应体系中存在有能与游离基结合形成稳定化合物的物质; (2)在氧化反应过程中,会有阻化剂生成; (3)生成的目的产物会分解;
(4)反应过程中会生成有机过氧化氢物。 73.氨氧化是指1
(1)将带有甲基的有机物与氨和空气的气态混合物在高温下通过固体催化剂制取腈类的反应;
(2)有机物在有氨和氧气存在的条件下进行反应; (3)是指将邻二甲苯氧化制备邻苯二甲酸酐的反应; (4)是指氨与氧反应生成一氧化氮和水的反应。 74.浓HNO 3和稀HNO 3都可作为氧化剂,1
由此可得出结论:
(1)稀HNO 3氧化性比浓HNO 3弱; (2)稀HNO 3氧化性比浓HNO 3强;
(3)稀HNO 3氧化性与浓HNO 3氧化性相同; (4)稀HNO 3与浓HNO 3都不具备氧化性。
75.在中性或碱性水介质中可发生如下氧化反应, 2
冠醚在此反应中的作用是: (1)溶剂;
(2)相转移催化剂;
(3)可与卤代烷完全互溶; (4)液-固相非均相催化剂。
1、蒽醌在发烟硫酸中磺化,为了使生成的产物以α-蒽醌磺酸为主,则要在反应液中需加下列哪种定位催化剂?( a )
A 、汞盐
B 、铜盐
C 、AlCl3
D 、HF
2、对于苯的一磺化反应,当苯环上存在下列哪种取代基时,将不利于磺化反应的进行?( a )
A 、-Br
B 、-OH 、
C 、-CH3
D 、-NH2 3、写出以下磺化反应的方法和大致反应条件。 3e ++
E 0 = 0.96V 2H 2O E 0 =0.80V
稀HNO 3浓HNO 3
NO 3ˉ4H ++NO e
+NO 3ˉ2H ++NO 2+
H 2O
R-CH 2Br +K 2CrO 4
R-CHO
答(1)用烘焙磺化法。大致反应条件:邻二氯苯为介质,约180℃,18h ,收率93% (2)过量发烟硫酸磺化法。大致反应条件:约30℃,4h ,收率89%
4、写出由苯制苯胺—2,4—二磺酸的合成路线、各步反应的名称、磺化反应的详细名称和磺化的大致反应条件。
答:苯经混酸一硝化、硝基还原得苯胺,后者在邻二氯苯中用理论量浓硫酸在180℃左右
进行烘焙磺化得对氨基苯磺酸,最后再用过量发烟硫酸进行二磺化,即得到苯胺-2,4-磺酸。
其合成路线如下:
第三章14.KMnO 4中性水溶液与癸烯-1在室温下不反应,若加入少量季铵盐,则立刻激烈反应。试解释原因并说明原理。
答:KMnO4中性水溶液与癸烯-1在室温下不反应,是因为KMnO4水溶液中的MnO4-
与癸烯-1处在互不相溶的两相,分子间不能发生碰撞,因而反应不能发生。向体系中加
入少量季铵盐,季铵盐可作为相转移催化剂,通过离子交换季铵盐将MnO4-
带入有机相癸烯-1中,即发生相转移催化反应,所以反应很快发生。反应原理可表示如下: 水相
有机相
界面Q +X -目的产物
K +X -
Q +MnO 4-
++
阴离子交换
+Q +Y
-
+有机反应物
CH 3(CH 2)7CH=CH 2CH 3(CH 2)7COOH
KMnO 4Q +MnO 4-
第四章11题试说明为何当丙烯与次氯酸进行加成反应时,得到的产物1-氯-2-丙醇和2-氯-1-丙醇的比例为9︰1。
答:丙烯与次氯酸加成过程可表示如下:
(C 8H 17)3N +
CH 3·Clˉ
25℃
CH 3(CH 2)7CH=CH 2
KMnO CH 3(CH 2)7COOH
NH 2
SO 3H
NH 2
NH 2
SO 3H
NH 2
(1)
(2)
SO 3H NH 2NH 2SO 3H NH 2NO 2
SO 3H
丙烯与次氯酸加成是一个亲电加成的过程,得到的中间体a 较中间体b 不稳定,因此中间体b 更容易生成,因而得到的产物1-氯-2-丙醇和2-氯-1-丙醇的比例为9︰1。
第四章13题试预测下列各烯烃与溴进行加成溴化时相对速度的大小 :
答:
第五章第7.配制10Kg 10.5%的发烟H 2SO 4,分别需要98% 的浓H 2SO 4和20%的发烟H 2SO 4多少?
解:设分别需要98% 的浓H 2SO 4和20%的发烟H 2SO 4为x 、y 克 10.5%的发烟H 2SO 4和20%的发烟H 2SO 4换算为硫酸浓度分别为w 1、w 2 则
%
5.104%20225.0%100%3
6.102%5.10225.0%10021=?+==?+=w w
于是有:x+y=10, 0.98x+1.045y=10×1.0236 则:x=3.29;y=6.71 答:
第六章6.如何计算D.V.S 和F.N.A?硫酸脱水值与混酸硝化能力有何关系?试计算下述体+ H +HOCl H 2+OCl H 2+
OCl
Cl + + H 2O
CH C
H 3CH 2Cl
OH CH C
H 3CH 2+9
1
CH
CH 2C H 3Cl +
+CH
CH 2
+
C H 3CH
+
CH 2C H 3
+
2O
a
b
CH 2=CH 2CH 3CH=CH 2(CH 3)2C=CH 2
(CH 3)2C=CHCH 3
CH 2=CHCN
HOOCCH=CHCOOH (CH 3)2C=CHCH 3
(CH 3)2C=CH 2CH 3CH=CH 2CH 2=CH 2
CH 2=CHCN HOOCCH=CHCOOH <<<<<
系的D.V.S 值,设HNO 3的浓度为65%, H 2SO 4的浓度为96%。 解:(1)D.V .S 和F.N.A 可分别用下面的公式进行计算:
硝化生成的水质量混酸中含水质量混酸中含硫酸质量
废酸中含水质量废酸中含硫酸质量+==
S V D ..
废酸质量
废酸中含硫酸质量
=
...A N F
混酸的硫酸脱水值越大,则混酸的硝化能力越强。
(2)对于第一种混酸,
混酸中所含硫酸质量为:275×1.84×96%=485.76 混酸中含水的质量为:275×1.84×(1-96%)+275×1.42×(1-65%)=156.915 硝化时生成的水的质量为: 52.721863
%
6542.1275=???
代入计算式得:
12.252
.72915.15676
.485..=+=+=
硝化生成的水质量混酸中含水质量混酸中含硫酸质量S V D
(3)对于第二种混酸
21
.418
63
%
6542.1125%)651(42.1125%)961(84.1275%
9684.1275..=???+-??+-????=
+=硝化生成的水质量
混酸中含水质量混酸中含硫酸质量
S V D
第六章7.怎样分离邻二硝基苯(或对二硝基苯)与间二硝基苯的混合物?
答:可采用化学方法进行分离。邻二硝基苯与对二硝基苯在碱性条件下磺化或水解变为可溶于水的化合物,但间二硝基苯不发生类似的反应,因而可将它们进行分离。
第七章13.某人用金属锌还原硝基苯,以期得到苯胺。可最后他得到的是氢化偶氮苯,请你分析他失败的原因,并用方程式加以说明。
答:主要是因为选择介质的pH 值不正确。因为金属还原硝基苯,在不同的介质条件下,所得的产物不同:
在碱性条件下,硝基化合物用锌粉还原,由于发生双分子还原反应,得到的产物是氢化偶氮苯,而不是苯胺,其还原过程可表示如下:
第10章第4题下面反应:
NO +
Na SO NO 2
NO 2NO 2
SO
3Na NO 2
SO
3
+
NO 2
NO +
NaOH NO 2
NO
2NO 2
ONa
NO 2
+
NO
Zn + H +
NH 2
NHOH
苯胲,苯基羟胺
NH
NH
氢 化 偶 氮 苯
ArNO 2
N
N Ar Ar NH NH Ar Ar
当R分别是OC2H5、CH3、Cl时,反应速度的大小顺序是怎样的?为什么?试用反应机理加以说明。
答:这是C-烷基化反应,其反应历程为亲电取代反应,反应历程可表示如下:
+AlCl
3
分子络合物
慢
+Ar-H
快
离子对或离子络合物
Ar C2H5+AlCl
3
+HCl
[AlCl
3
]
δ+δ-
C2H
C2H
+Ar
4
ˉ
C
2
H
5
+AlCl
4
ˉ
……C2H5+AlCl
4
ˉ
+
Ar
H
C2H
AlCl
4
ˉ
因为是亲电取代反应,所以当苯环上存在有推电子基时,推电子基使苯环活化,所以它的存在会有利于亲电取代反应的进行,反应速度加快;反之当苯环上有吸电子基时,由于吸电子基会使苯环钝化,因此反应速度减慢。由于OCH3、CH3、Cl的推电子能力逐渐减小,因此几种物质的反应速度大小顺序为:
OC2H5
CH3
Cl
<<
合成复习例题:
1.
学号:20115051217 学年论文 学院化学化工学院 专业化学 年级2011级 姓名马韵会 论文题目现代有机合成 指导教师金春雪职称教授 成绩 2013年12月18日
目录 摘要 (1) 关键词 (1) Abstract (1) Keywords (1) 引言 (1) 1开发“原子经济性[5]”反应 (2) 2选用更“绿色化”的起始原料和试剂 (2) 3采用无毒无害的高效催化剂 (3) 4采用无毒无害的溶剂 (3) 结束语 (4) 参考文献 (4)
现代有机合成 学生姓名:马韵会学号:20115051217 化学化工学院化学 指导老师:金春雪职称:教授 摘要:有机合成是综合应用各类有机反应及其组合、有机合成新技术[1]、有机合成设计及策略以获得目标产物的过程。有机合成既与材料、生命、环保、能源四大支柱学科密切相关,也与我们社会的现代文明和日常生活密切相关。近年来绿色化学[2]、洁净技术、环境友好过程已成为合成化学追求的目标和方向。可见21世纪有机合成所关注的不仅仅是合成了什么分子,而是如何合成,其中有机合成的有效性、经济性、环境影响和反应速率将是有机合成研究的重点,尤其是绿色有机合成的研究[3]。 关键词:有机合成;绿色化学;绿色合成 Abstract:Organic synthesis is a comprehensive application and combination of various types of organic reactions,organic synthesis technology[1],the process of design and organic synthesis strategies to obtain the desired https://www.doczj.com/doc/419200391.html,anic synthesis is closely related to both materials,life,environmental protection,energy four pillars of discipline, but also closely related to the daily life of modern civilization and our society.In recent years,green chemistry[2],clean technology,environmental-friendly process has become the pursuit of the goals and direction of synthetic chemistry.Visible in the21st century is not only of concern to the organic synthesis of what synthesized molecules,but how synthesis,where the validity of organic synthesis,economy,environmental impact and the reaction rate will be the focus of research in organic synthesis,especially green organic synthesis study[3]. Keywords:Organic Synthesis;Green Chemistry;Green synthesis 引言 有机合成是指利用化学方法将原料制备合成新的有机物的过程。它是一个极富创造性的领域。早期的有机合成主要是合成自然界中已存在的但含量稀少的有机化合物。后来根据结构与性质关系的规律性和实际需求,进一步合成了自然界不存在的、具有理论和实际价值的有机化合物。
精细有机合成原理期末模拟题1 一、填空题 1、精细化工产品的特点是(小批量、多品种)、(高技术密集)、(附加值高)、(综合生产工艺流程和多用途)、(商品性强); 2、石油是由(碳)、(氢)、(氧)、(氮)、(硫)五种元素组成的,这五种元素可以构成(烃类)和(非烃类)两类化合物; 3、化学反应器按催化剂运动状态可分为(固定床)、(流化床)和(移动床); 4、全混流反应器的基本假设之一是,器内各处浓度、温度(相同),且等于(出口)的浓度和温度; 5、单层绝热床反应器适用于热效应(小)的化学反应,否则用(多层)绝热床反应器; 6、精细有机合成中,溶剂的作用主要有(溶解作用)和(影响化学反应); 7、催化剂的使用要求有(活性)、(选择性)、(寿命)和(机械强度); 8、催化剂失活的原因有(热失活)和(中毒)两种; 9、均相配位催化反应的优点是(活性高)、(选择性好)、(有体系预见性); 10、卤代苯(氟苯、氯苯、溴苯、碘苯)的一硝化是一个(亲电取代)反应,由于氟的电负性最大,其负的(吸电诱导)效应也最大,一硝化时异构产物中(对)位的比例大。 11、常用磺化剂有(浓硫酸)、(发烟硫酸)、(氯磺酸)和(三氧化硫)。 12、写出三种不同类型的氢化催化剂(铁粉)、(硫化钠)、(NaBH4)。 13、天然石油中含有(烷烃)、(环烷烃)、(芳烃)三种烃类化合物; 14、催化剂寿命指的是保持其(平衡活性a e)的时间。 二、单选题 1、下列试剂哪一个不是亲电试剂? (a)NO2+(b)Cl2(c)Fe2+(d)Fe3+ 2、按极性分类,下列溶剂中哪一个是非极性溶剂?
(a)丙酮 (b)环己烷 (c) 水 (d)甲醇 3、 下面哪一个不是自由基生成(链引发)的方式? (a)加压 (b)加热 (c)加过氧化苯甲酰 (d)光照 4、 下面哪一个化合物最容易发生硝化反应? (a)苯 (b)一硝基苯 (c) 二硝基苯 (d)苯胺 5、1摩尔硝基苯还原生成1摩尔苯胺,理论上需要铁粉的摩尔数为 (a)1.0 (b)1.25 (c)2.0 (d)2.25 6、下面哪一个是H 酸?(b) HO3S NH2OH (a)(b) H N OH HO S 23 3(c) HO NH 2HO 3S (d) HO 3S SO 3H OH 7、某化学反应的计量方程式为: 2P A 已知:n A0=10mol,n A =1mol,n P =12mol,则: (a)Sp=1/3 (b)Sp=2/3 (c)Yp=3/10 (d)Yp=1/10 8、最常用的胺基化剂是: (a)氨水 (b)气氨 (c)液氨 (d)碳酸氢氨 9、2-氯蒽醌胺解制备2-氨基蒽醌的催化剂是:
一、名词解释 1.卤化: 在有机化合物分子中引入卤原子,形成碳—卤键,得到含卤化合物的反应被称为卤化反应。根据引入卤原子的不同,卤化反应可分为氯化、溴化、碘化和氟化. 2.磺化 :向有机分子中引入磺酸基团(-SO3H)的反应称磺化或者硫酸盐化反应。. 3. 硝化:在硝酸等硝化剂的作用下,有机物分子中的氢原子被硝基(—NO2)取代的反应叫硝化反应。 4.烷基化: 烷基化反应指的是在有机化合物分子中的碳、硅、氮、磷、氧或硫原子上引入烃基的反应的总 称。引入的烃基可以是烷基、烯基、炔基和芳基,也可以是有取代基的烃基,其中以在有机物分子中引入烷基最为重要 5.酰化:在有机化合物分子中的碳、氮、氧、硫等原子上引入脂肪族或芳香族酰基的反应称为酰化反应。 6.氧化:广义地说,凡是失电子的反应皆属于氧化反应。 狭义地说,凡能使有机物中氧原子增加或氢原子减少的反应称为氧化反应。 7.磺化的π值:当硫酸的浓度降至一定程度时,反应几乎停止,此时的剩余硫酸称为“废酸”;废酸浓度用 含SO3的质量分数表示,称为磺化的“π值”。磺化易,π值小;磺化难,π值大。 8.硫酸的D.V.S: :硫酸的脱水值是指硝化结束时,废酸中硫酸和水的计算质量之比。 9.还原:广义:在还原剂作用下,能使某原子得到电子或电子云密度增加的反应称为还原反应。 狭义:能使有机物分子中增加氢原子或减少氧原子,或两者兼尔有之的反应称为还原反应。 10.氯化深度: 氯与甲苯的物质的量比. 11.废酸的F.N.A:废酸计算浓度(F.N.V)是指混酸硝化结束时,废酸中硫酸的计算浓度(也称硝化活性因素)。 12.相比:指硝酸与被硝化物的量比。 13.硝酸比:指硝酸与被硝化物的量比。 14.氨解:氨解反应是指含有各种不同官能团的有机化合物在胺化剂的作用下生成胺类化合物的过程。氨解 有时也叫做“胺化”或“氨基化”,但是氨与双键加成生成胺的反应则只能叫做胺化不能叫做氨解 (1)Claisen-Schmidt反应; 芳香醛或脂肪酮混合交叉缩合。反应是在氢氧化钠溶液或乙醇溶液中进行,得到很高产率的α、β-不饱和醛或酮。这一反应叫Claisen-Schmidt反应。 (2)Darzen反应; 醛酮(主要是芳醛)与α-卤代酸酯在强碱存在下反应,生α、β-环氧酸酯的反应叫达尔森反应,也称为缩水甘油酯的反应。 (3)Mannich反应; 含活泼H原子的化合物和甲醛及胺(伯胺或仲胺,氨)进行缩合反应,结果活泼氢原子被
有机合成题 1、以乙炔和1, 3-二溴丙烷为原料合成1, 6-庚二烯(无机试剂任选)。 2、以丙烯、乙炔为原料合成正辛烷(无机试剂任选)。 3、以乙烯为原料(无机试剂任选)合成乙基正丁基醚。 4、完成转化: 5、用C3以下的不饱和烃为原料合成1, 7-辛二烯-4-炔(其它试剂任选)。 6、以甲苯和乙炔为原料(无机试剂任选)合成: 7、以乙烯为原料(无机试剂任选)合成丙烯酸。 8、以苯乙烯为原料(其它试剂任选)合成(Z)-1-苯基丙烯: 9、以甲苯为原料(无机试剂任选)合成: 10、以甲苯为原料(其它试剂任选)合成: 11、以丙烯为原料(无机试剂任选)合成烯丙基腈。 12.(本小题5分)以苯、甲苯及必要的原料合成下列化合物: (1)O CH2CH2CH3 NO2 COOH NO2 Br (6) (5) (4) (3) (2) (1) 目标分子 (1) 解: CH3Br NO2 HOOC NO2 CH3 NO2 HOOC NO2 (2) H3CH3 SO3H CH3 NO2 SO3H CH3 NO2 H2SO4 100℃ 浓 浓 浓HNO3 H2SO4 H3O+ (3) CH3CH3 Br CH3 Br NO2 浓H2SO4 浓HNO3 Br2 FeBr3 13.(本小题4分)完成转化: .CH 3 CHCH3 Br CH3CH2CH2Br CH3CHCH3 Br KOH/C2H5OH CH3CH=CH2+HBr ROOR CH3CH2CH2Br 14.(本小题5分)以乙炔、丙烯为原料(无机试剂任选)合成正戊醛。 参考答案: 1、 2、(
3、 4、 5、 6、 7、
精细有机合成原理期末模拟题 1 一、填空题 1、精细化工产品的特点是(小批量、多品种)、(高技术密集)、(附加值高)、(综合生产工艺流程和多用途)、(商品性强); 2、石油是由(碳)、(氢)、(氧)、(氮)、(硫)五种元素组成的,这五种元素可以构成(烃类)和(非烃类)两类化合物; 3、化学反应器按催化剂运动状态可分为(固定床)、(流化床)和(移动床); 4、全混流反应器的基本假设之一是,器内各处浓度、温度(相同),且等于(出口)的浓度和温度; 5、单层绝热床反应器适用于热效应(小)的化学反应,否则用(多层)绝热床反应器; 6、精细有机合成中,溶剂的作用主要有(溶解作用)和(影响化学反应); 7、催化剂的使用要求有(活性)、(选择性)、(寿命)和(机械强度); 8、催化剂失活的原因有(热失活)和(中毒)两种; 9、均相配位催化反应的优点是(活性高)、(选择性好)、(有体系预见性); 10、卤代苯(氟苯、氯苯、溴苯、碘苯)的一硝化是一个(亲电取代)反应,由于氟的电负性最大,其负的(吸电诱导)效应也最大,一硝化时异构产物中(对)位的比例大。 11、常用磺化剂有(浓硫酸)、(发烟硫酸)、(氯磺酸)和(三氧化硫)。 12、写出三种不同类型的氢化催化剂(铁粉)、(硫化钠)、(NaBH4)。 13、天然石油中含有(烷烃)、(环烷烃)、(芳烃)三种烃类化合物; 14、催化剂寿命指的是保持其(平衡活性a e)的时间。 二、单选题 1、下列试剂哪一个不是亲电试剂? (a)NO2+(b)Cl2(c)Fe2+(d)Fe3+ 2、按极性分类,下列溶剂中哪一个是非极性溶剂? (a)丙酮(b)环己烷(c) 水(d)甲醇 3、下面哪一个不是自由基生成(链引发)的方式? (a)加压(b)加热(c)加过氧化苯甲酰(d)光照 4、下面哪一个化合物最容易发生硝化反应? (a)苯(b)一硝基苯(c) 二硝基苯(d)苯胺 5、1摩尔硝基苯还原生成1摩尔苯胺,理论上需要铁粉的摩尔数为 (a) (b) (c) (d) 6、下面哪一个是H酸?(b) 7、某化学反应的计量方程式为: 2P A S 已知:n A0=10mol,n A=1mol,n P=12mol,则: (a)Sp=1/3 (b)Sp=2/3 (c)Yp=3/10 (d)Yp=1/10 8、最常用的胺基化剂是: (a)氨水(b)气氨(c)液氨(d)碳酸氢氨 9、2-氯蒽醌胺解制备2-氨基蒽醌的催化剂是: (a)CuCl (b)CuCl+SnCl2(c)CuCl+FeCl2(d)CuSO4 10、下面哪一个重氮盐偶合时的反应活性最高? (a)Cl-Ar-N=N+(b)O2N-Ar-N=N+(c)H3C-Ar-N=N+ (d)H3CO-Ar-N=N+ 11、用混酸(浓硫酸和硝酸)硝化时,关于浓硫酸的作用,下面哪一个说法是错误的?
精细化工工艺学复习题及答 案 -标准化文件发布号:(9456-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII
1、精细化学品的定义是什么? 精细化学品是与大宗化学品相对应的一类化工产品,是指对化学工业生产的初级或次级产品进行深加工而制成的具有某些或某些种特殊功能的化学品2、精细化学品的分类:精细有机化学品、精细无机化学品、精细生物制品 特点:生产特性,小批量、多品种、复配型居多;技术密集度高;多采用间歇式生产装置;生产流程多样化 经济特性,投资效率高、附加价值高、利润率高; 商业特性,市场竞争激烈、重视市场调研、适应市场需求、重视技术的应用服务、要求技术保密、独家经营; 产品特性,具有一定的物理功能、化学功能和生物活性 3、选择聚合物助剂是应注意:与树脂的配伍性、耐久性、对加工条件的适应性、制品用途对助剂的制约、协同效应 4、常用的塑料加工助剂有增塑剂、稳定剂、阻燃剂、润滑剂、抗静电剂、着色剂、发泡剂 5、DOP邻苯二甲酸二辛酯、DBP邻苯二甲酸二丁酯、TPP磷酸三苯酯、DOA 己二酸二辛酯 6、表面活性剂分为哪几类各自具有什么特点? 阴离子表面活性剂一般都具有好的渗透、润湿、乳化、分散、增溶、起泡、去污等作用 阳离子表面活性剂它除用作纤维柔软剂、抗静电剂、防水剂、染色助剂等之外,还用作矿物浮选剂、防锈剂、杀菌剂、防腐剂等 两性活性剂由阳离子部分和阴离子部分组成的表面活性剂 非离子表面活性剂在水中不电离,其亲水是主要是由具有一定数量的含氧基团(一般为醚基和羟基)构成 7、化妆品的辅助原料有哪些? 表面活性剂、香料、色素、防腐剂、保湿剂、营养剂、防晒剂、收敛剂 8、亲水亲油平衡值(HLB)是指:反应表面活性剂的亲水基和亲油基之间在大小和力量上的平衡程度的量 计算:非离子型聚乙二醇和多元醇类(亲水基的分子量*100)/(表面活性剂分子量*5)=(亲水基的分子量*100)/(疏水基分子+亲水基分子量)*5 多元醇脂肪酸酯 20(1—S/A) S酯的皂化值 A原料脂肪酸的酸值 聚乙二醇类 EO/5 EO聚环氧乙烷部分的质量分数 离子型 7+∑亲水基基团数+∑亲油基基团数 9、常用食品防腐剂主要有哪四类?试简要说明 苯甲酸及其盐类食品中可大量食用 山梨酸及其盐类 对羟基苯甲酸酯类防腐效果好,毒性低,无刺激性 丙酸及丙酸盐新型防腐剂,对人体无毒副作用 10、日允许摄入量ADI:人一生中每日从食物或饮水中摄取某种物质而对健康无明显危害的量
《有机合成》测试卷 出题者:20072401171 单项选择(10 X 1' = 10',每空一分) 1.下列反应应用何种试剂完成 ( ) A .LiAlH 4 B. NaBH 4 C. Fe + CH 3COOH (D) Pt + H 2 D. 2.下列化合物有顺反异构的是 ( ) A.CH 3CH=CHCH 3 B .CH 3CH 2CH 2CH=CH 2 C .CH 3CH=C(CH 3)2 D . CH3C CCH 3 3. 尼龙-66是一种聚酰胺,其单体为: ( ) (A) 己内酰胺 (B) 己二酸己二胺盐 (C) 己二酸 + 尿素 (D) 丁二酰亚胺 主要产物是 ( ) (A) C 6H 5CH 2OH C 6H 5652COOCOCH 3 (C) C 6H 5CH=CHCOOCOCH 3 (D) C 6H 5CH=CHCOOH 5.下列反应不能使碳链剪断的是 ( ) A .氯仿反应 B.Hofmann 反应 C.酯化反应 D.脱羧反应 6.下列反应不属于合成的原则的是 ( ) A .合成路线复杂 B.经济易得 C.对环境造成污染小 D.反应条件温和 7比较取代羧酸FCH 2COOH,ClCH 2COOH,BrCH 2COOH,ICH 2COOH 的酸性最大的是: ( ) (A) FCH 2COOH (B) ClCH 2COOH (C) BrCH 2COOH (D) ICH 2COOH 8.以下物质不具有手性的是 ( ) A.酒石酸 B.二氯甲烷 C.二氯乙烯 D.一氯甲烷 9.四氢吡喃醚对以下试剂不稳定的是 ( ) A .碱 B.Grignard 试剂 C.烷基锂 D.酸 10.以下方法不可以用来合成酚的是 ( ) A . 苯磺酸盐碱熔法 B.氯苯水解法 C. 醇脱水法 D. 异丙苯水解法 O 3C 6H 5CHO +(CH 3CO)2O
练习题 1、从苯及不超过3个C 的有机原料合成 Br Br CH 2CH 2CH 3 2、用苯和不超过3个碳的有机物为原料合成 CH 2CH 2CH 3 Br 3、选择合适的试剂合成下面的化合物 C-CH 2CH 3CH 3OH 4、选择合适的试剂合成下面的化合物 CH 2OH NO 2 5、用甲苯为原料合成 Br COOH 6、由指定原料合成下列产物 OH CH 2 7、由指定原料合成下列产物 CHO 8、由乙酰乙酸乙酯合成下列化合物
O CCH 3 9、选择合适的试剂合成下面的化合物 O CH 3CCH 2CH 3CCH 2CH 2CH 2OH O 10、用苯和不超过4个碳的有机物合成 OH O 11、由指定原料合成下列产物 CH 3O 2N CN CH 3 12、由不超过三个碳的有机原料及必要的无机试剂合成下列产物 O CH 3CH 2CHCHCOCH 2CHOCH 2CH 3 OH 3CH 3 13、用不超过4个碳的有机物和适当的无机试剂合成下列化合物 O CH 3CCH 2CH 2CH 2CH 2N CH 3 CH 3 14、用不超过4个碳的有机物合成(4分) O 15、用不超过4个碳的有机物合成 O O CH 2CH 2CH 2CH 3 16、由指定原料合成下列产物(6分) CHCOOH NO 2 NO 2CH 3 17、用不超过4个碳的有机物为原料合成
OH CH 3CH 2CH 2CH 2CHCH 2CH 2CH 2CH 2CH 3 18、由指定原料合成下列产物 CH 3CH 2CH 2Br (CH 3)2CHCOOH 19、选择合适的试剂合成下面的化合物 CH 2OH NO 2 20、由1,3-丙二醇合成螺庚烷酸合成下列化合物 COOH 21、由指定的主要原料出发合成下列化合物 O COOC 2H 5 Ph Ph C HO +CO CH 3 22、由苯及不超过3个C 的有机原料合成下列产物 COOH I CH 2CH 2CH 3 24、用丙二酸二乙酯及不超过4个碳的有机物合成下列化合物(6分) COOH 25、由苯及不超过3个C 的有机原料合成下列产物 Br CH 2CH 2CH 3 26、由丙二酸二乙酯及不超过3个碳的有机物合成下列化合物 O EtO 2C 27、由已二酸及不超过三个碳的有机原料合成下列产物
现代有机合成的新方法 摘要: 方法是有机合成化学发展的基础,新方法的产生和发展可为有机合成开拓新的研究领域和 发展方向. 介绍现代有机合成中一些新方法, 结合具体的有机合成反应实例阐述有机合成在这些 新方法方面取得的新成果和进展, 现代有机合成发展方向和应重视的研究领域. 关键词: 现代有机合成; 新方法; 进展 The new method of the modern organic synthesis Abstract: the method of synthetic organic chemistry the development foundation, the new method for generating and development for organic synthesis, open up new areas of research and development direction of modern organic synthesis. This paper introduces some new methods, combined with specific examples of organic synthesis organic synthesis in these new methods to achieve new results and progress, the modern organic synthesis development direction and importance should be attached to the research area. Key words: modern organic synthesis; new method; progress 有机合成化学作为有机化学的一个分支, 已经有一百多年的历史. 现代的有机合成不但能合成大量的结构复杂而多样的次生生物代谢物和基因、蛋白质等复杂的生命物质, 而且能合成大量的自然界中没有的具有独特功能性分子的物质. 现代有机合成不只是合成什么的问题, 更重要的是如何合成和怎样合成的问题. 有机合成与21 世纪的三大发展学科: 材料科学、生命科学和信息科学有着密切的联系, 为三大学科的发展提供理论、技术和材料的支持. 新世纪有机合成将进一步在这三大学科领域中发挥作用并开辟新的领域. 随着生命科学和材料科学的发展, 尤其进入后基因组时代后, 需要有机合成快速提供各种具有特定生理和材料功能的有机分子, 而要获得有新结构的功能类型分子往往取决于新的合成方法, 新的方法往往又取决于新的理论. 因此, 21 世纪有机合成的发展, 需要从方法、结构与功能方面入手. 1 现代有机合成的新方法 有机合成的发展一方面得益于有机金属试剂的开发与应用, 另一方面得益于新的反应方式, 如自由基反应、卡宾反应、环加成反应与高效合成反应等. 这里就一些新方法给出若干实例. 1.1 自由基反应 自由基化学已为有机合成提供了许多新方法.主要表现在以下 4 个方面: 新型自由基原子转移供体, 如(MeSi)、SiH; 成环模型, 跨环环化反应; 在分子内自由基加成反应中自由基加成的模式, 即endo/exo 型; 自由基加成反应立体选择性的控制[ 1] .在多烯烃的体系内串联式自由基加成反应为多环化合物的合成提供了高效方法[ 2] .
复习思考习题 1.写出制备的合成路线。 2.写出由对硝基甲苯制备以下芳磺酸的合成路线。 (1) (2)(3) 3.写出由苯制备苯胺-2,4-二磺酸的合成路线、各步反应的名称和磺化反应的主 要反应条件。 4.简述由甲苯制备以下化合物的合成路线和工艺过程。 (1) (2) (3) 5.写出由苯制备3-硝基-4-氯苯磺酸氯的合成路线、各步反应的名称、主要反应条 件和产物的分 离方法。 6.写出由环氧乙烷制备2-氨基乙基磺酸钠的几个合成路线和各步反应的名称? 7.对以下操作进行评论: (1)氯苯在过量氯磺酸中进行氯磺化生成4-氯苯磺酰氯,然后向磺化液中滴加 硝酸进行硝化 得3-硝基-4-氯苯磺酰氯。 (2)在制备1-亚硝基-2-萘酚时将C10H7OH、NaOH、NaNO2按1:1的比例的摩 尔比配成混合 水溶液,然后慢慢滴入到稀硫酸中进行亚硝化。 8.简述由甲苯制备的以下卤化产物的合成路线、主要反应过程和主要反应条件?
(1) (2) (3) (4) (5) (6) 9.写出制备2,6-二氯苯胺的几条合成路线 10.写出由氯苯制备3-氨基-4-甲氧基苯磺酸的2种可用于工业生产的合成路线。 11.在以下反应所用的HF酸属于哪种类型的试剂? (1) (2) 12.氯化苄和苯甲酸在水介质中反应生成苯甲酸苄酯时,如何使反应顺利进行? 13.写出由苯,甲苯,氯苯或硝基苯为原料制备3,3'-二氨基-N-苯甲酰苯胺和4,4'- 二氨基-N-苯 甲酰苯胺的合成路线。 14.列出以下化合物在空气液相氧化时由难到易的次序 (1)(2)(3) (4) 15.简述制备以下产品的合成路线和主要工艺过程。 (1) (2)
专题总结------有机合成题 一、引言 1.设计合成路线的3个指标 (1)途径简捷;(2)原料易得;(3)总产率高。 2.设计合成路线的步骤和方法 (1)分析目标分子的结构,进行合理的“切断” ①化合物的类型分析目标化合物是哪一类(如酯、醛、酮、醇、醚)。例1:用简单的原料合成 分析: 解: 例2:由简单化合物合成 分析:
②碳架分析碳链是开链还是环状,是增长还是缩短,碳架是脂环、芳环还是杂环。 例:从乙烯、丙烯合成正辛烷 分析: 解: ③分子的立体构型 例:从乙烯、丙烯合成顺-4-辛烯、反-4-辛烯 分析: (2)选择廉价、易得的原料 例:用简单的化合物合成
分析: 解: (3)注意基团保护例1: 解: 例2:由甲苯制备 解: 例3:完成转化
(保护酮羰基) 解: 例4: 完成转化 (保护醛基) 解: 二、增长碳链的方法(形成碳-碳键的方法) 1.亲核取代 (1)卤代烃氰解——制多一个碳的羧酸 (增加一个C的羧酸) 例:由丁二烯合成己二酸。 解: (2)卤代烃与炔化钠反应
例:由乙烯、丙烯制正辛烷。 (3)三乙负离子与卤烃反应——制甲基酮 (4)丙二负离子与卤烃反应——制取代乙酸 2.亲核加成 (1)格氏反应 (2)醛、酮加氰氢酸 (3)羟醛缩合 (4)Perkin反应 (5)Knoevenagel反应 (6)Reformasky反应——制β羟基酸(酯) (7)Claisen酯缩合反应 (8)Michel加成 3.芳环上亲电取代
4.其他方法 (1)环化加成 例:由丁二烯合成己二酸。 (2)重氮盐放氮 (3)重氮甲烷与酰氯反应——制多一个碳的羧酸 例: (4)Skraup合成法——制喹啉类化合物 见“专题总结Ⅲ”中“四、重要的有机合成反应”。
精细有机合成原理期末模拟题1 一、 填空题 1、精细化工产品的特点是(小批量、多品种)、(高技术密集)、(附加值高)、(综合生产工艺流程和多用 途)、(商品性强); 2、石油是由(碳)、(氢)、(氧)、(氮)、(硫)五种元素组成的,这五种元素可以构成(烃类)和(非烃 类)两类化合物; 3、化学反应器按催化剂运动状态可分为(固定床)、(流化床)和(移动床); 4、全混流反应器的基本假设之一是,器内各处浓度、温度(相同),且等于(出口)的浓度和温度; 5、单层绝热床反应器适用于热效应(小)的化学反应,否则用(多层)绝热床反应器; 6、精细有机合成中,溶剂的作用主要有(溶解作用)和(影响化学反应); 7、催化剂的使用要求有(活性)、(选择性 )、(寿命)和(机械强度); 8、催化剂失活的原因有(热失活)和(中毒)两种; 9、均相配位催化反应的优点是(活性高)、(选择性好)、(有体系预见性); 10、卤代苯(氟苯、氯苯、溴苯、碘苯)的一硝化是一个(亲电取代)反应,由于氟的电负性最大,其负 的(吸电诱导)效应也最大,一硝化时异构产物中(对)位的比例大。 11、常用磺化剂有(浓硫酸)、(发烟硫酸)、 (氯磺酸)和(三氧化硫)。 12、写出三种不同类型的氢化催化剂(铁粉)、(硫化钠)、(NaBH 4)。 13、天然石油中含有(烷烃)、(环烷烃)、 (芳烃)三种烃类化合物; 14、催化剂寿命指的是保持其(平衡活性a e )的时间。 二、 单选题 1、 下列试剂哪一个不是亲电试剂? (a)NO 2+ (b)Cl 2 (c)Fe 2+ (d)Fe 3+ 2、 按极性分类,下列溶剂中哪一个是非极性溶剂? (a)丙酮 (b)环己烷 (c) 水 (d)甲醇 3、 下面哪一个不是自由基生成(链引发)的方式? (a)加压 (b)加热 (c)加过氧化苯甲酰 (d)光照 4、 下面哪一个化合物最容易发生硝化反应? (a)苯 (b)一硝基苯 (c) 二硝基苯 (d)苯胺 5、1摩尔硝基苯还原生成1摩尔苯胺,理论上需要铁粉的摩尔数为 (a)1.0 (b)1.25 (c)2.0 (d)2.25 6、下面哪一个是H 酸?(b) HO3S NH2OH (a)(b) H N OH HO S SO H 23 3(c) HO NH 2HO 3S (d) HO 3S SO 3H OH 7、某化学反应的计量方程式为: 2P A
一、名词解释(每题3分) 1卤化 : 2 磺化: 3. 硝化: 4 烷基化: 5 酰化: 6. 氧化: 7 .磺化的π值:; 8.硫酸的D.V.S: 9 还原: 10.氯化深度: 11.废酸的F.N.A: 12 相比: 13 硝酸比: 14 .氨解: 二、填空题(每空1分) 1.从天然气和石油中可获得_______、、、等脂肪烃。 2.萘在低温磺化时主要产物为,在较高温度下为_____________。 3.SO3在室温下有 ____、、、四种聚合形式。其中为液态。 4.用SO3磺化要注意防止_________、、、等副反应。 5. 共沸去水磺化法适用于________________。 6. 氯磺酸磺化时要注意。 7.硝化方法常见有______种,工业上常采用______________________,主要适用于。 8.硝化加料方法有_______ 、、三种。 9.硝化反应的主要活泼质点是___________________________。 10.自由基产生有 _____________、___________、____________三种方法。 11.从天然气和石油中可获得_______、、等芳香烃。 12.硝化反应器常用制成,因此要控制废酸浓度不低于防腐。 13.废酸处理有、、、等方法。 14. 烘培磺化多用于________________。 15.氟化物制备可通过_______________、、。16.链反应有_____________、___________、____________ 三步。 17 卤化技术按其方法可分为_____________、___________、____________三种类型。 18 芳环上的卤化反应属于_____________反应 19 工业发烟硫酸有两种规格,一种含游离SO3约 ,另一种含游离SO3,约 20 在连续分离器中,可加入以加速硝化产物与废酸分离。 21硝酸比指
现代有机合成 技术简介报告 姓名:田雅明 学号:2009291029 学院:化学化工学院 专业:应用化学
近百年来,有机化学对人类文明进程的巨大推动作用与卓越的贡献是不争的事实,而有机合成技术的长足发展又为有机化学的不断创新和其多样性、选择性以及经济性等方面提供了坚实的保障。 有机合成是综合应用各类有机反应及其组合、有机合成新方法、新技术、有机合成设计及策略以获得目标产物的过程。有机合成既与材料、生命、环保、能源四大支柱学科密切相关,也与我们社会的现代文明和日常生活密切相关。尤其在当今,新材料和新药物的需求、资源的合理开发和利用、减少或消除环境污染等可持续发展问题为有机合成提出了更高的要求。早期的有机合成主要是合成自然界中已存在的但含量稀少的有机化合物。后来根据结构与性质关系的规律性和实际需求,进一步合成了自然界不存在的、新的、具有理论和实际价值的有机化合物。所以,有机合成今后的任务将不再是盲目追求更多新化合物的合成,而是去设计合成预期的、有特异性能或有重大意义的有机化合物。 有机合成的发展趋势可以概括为两点: 其一是合成什么,包括合成在生命、材料学科中具有特定功能的分子和分子聚集体;其二是如何合成,包括高选择性合成、绿色合成、高效快速合成等。“如何合成”是合成化学家主要关注的问题。另外,有机合成的迅猛发展是缘由其它学科的需求,反过来有机合成也有力地促进了其它学科的进步。应该说,与有机合成关系最密切的学科是材料科学、生命科学和环境科学,当然能源、信息等其它科学也还是直接或间接相关的。其中环境科学中的绿色化学问题与有机合成密切相关。绿色化学当今已
不仅为学术界,而且也为社会上广为知晓的名词。在国际上有专门的刊物“Green Chemistry”,在美国有专门的奖项。绿色化学包括多方面的内容,但仔细分析这些内容就可以发现,其核心是有机合成。目前,绿色有机合成是十分重要的课题,又是十分艰难的课题,尤其是可以工业化的、理想的绿色有机合成。绿色有机合成今后长时期内将会是有机化学中最具挑战性的一个领域。 绿色合成不是治理污染而是防止污染产生的一种新观念,它是开发从源头解决污染问题的一门科学。对环境保护及社会的可持续发展具有重大意义。那么实现绿色合成的方法、技术与途径是:1. 开发“原子经济性”反应2. 提高烃类氧化反应的选择性3. 选用更“绿色化”的起始原料和试剂4. 采用无毒、无害的高效催化剂5. 采用无毒、无害的溶剂6. 反应方式的改变7. 采用高效合成法8. 固态反应9. 利用可再生的生物质资源。 目前应用于实践的绿色合成有:1、微波辐照有机合成2、有机声化学合成3、高效合成方法----一锅合成4、相转移催化反应5、有机电化学合成6、有机光化学合成7、等离子体有机合成8、超临界有机合成9、固相合成10、组合合成。其中,我对高效合成方法----一锅合成法和相转移催化反应印象颇深。 传统的有机合成是一步一步地进行反应的,难免步骤多、产率低、选择性差,且操作十分繁杂。采用一锅合成的方法,可将多步反应或多次操作置于一个反应器内完成,不再分离许多中间产物。采用一锅合成法,目标产物将可能从某种新颖、简捷的途径获得。通常,一锅
精细有机合成课程讲稿 水解的方法很多,包括卤素化合物的水解、芳磺酸及其盐类的水解、芳环上硝基的水 也可使用廉价的温和碱性剂,例如,碳酸钠和氢氧化钙
1975年,环氧乙烷的生产已可用乙烯的空气直接氧化法。丙烯的空气直接氧化法还不成熟,因甲基也会被氧化。环氧丙烷的另一个工业生产方法是丙烯的间接氧化法,国外已实现了工业化生产。 电化氯醇法是利用氯化钠(或氯化钾、溴化钠、碘化钠的水溶液,经电解生成氯气和氢氧化钠的原理。在阳极区通入丙烯,生成氯丙醇;在阴极区氯丙醇与氢氧化钠作 11.1.3苯氯甲烷衍生物的水解 苯环侧链甲基上的氯也相当活泼,其水解反应可在弱碱性缚酸剂或酸性催化剂的存在下进行。通过这类水解反应可以制得一系列产品。 一、苯一氯甲烷(一氯苄)水解制苯甲醇 苯甲醇的工业生产方法主要是氯苄的碱性水解法,分为间歇法和连续法。 间歇法是将一氯苄与碳酸钠水溶液充分混合并在80~90℃反应,水解产物经油水
连续法是将氯化苄与碱的水溶液在高温180~℃及加压1~6.8MPa下充分混合后通过反应区,反应只需要几分钟。采用塔式反应器,用质量分数10%的碳酸钠水溶液℃及1.8MPa下水解反应可得到纯度为98%的苯甲醇,收率98%。 芳环上卤基的水解 氯基水解是制备邻、对硝基酚类的重要方法,还可以制得的硝基酚类有 -3-硝基苯磺酸等,将这些硝基酚类还原可制得相应氨基酚类,它们都
在这里,用浓硫酸水解法的原因,一方面是为了使反应物溶解,另一方面是因为碱性水解法会引起副反应。 用类似的反应条件还可以从1-氨基-2,4-二氯蒽醌的水解制备 芳磺酸及其盐类的水解 酸性水解是磺化反应的逆反应,是亲电取代反应历程。酸性水解可用来除去芳环上的 生成的酚钠盐用无机酸如H2SO4酸化,即转变为游离酚。 一、碱熔反应的影响因素
1、精细化学品与精细化工的概念与特点。 精细化学品:凡能增进或赋予一种(类)产品以特定功能,或本身具有特定功能 的小批量或高纯度化学品”。 精细化学品的特点:① 产品功能性强(专用性)② 批量小③ 品种多④ 利润率 高⑤更新换代快 精细化工“生产精细化学品的工业”。“它属于一类化工产品的生产行业”。 精细化工的特点:① 多品种、小批量②综合生产流程和多功能生产装置 ③ 高技术密集度④大量应用复配技术⑤ 新产品开发周期长,费用高⑥ 商品 性强、市场竞争激烈 2、新领域精细化学品的类别。 食品添加剂、饲料添加剂、电子化学品、造纸化学品、塑料助剂、皮革化学品、表面活性剂、水处理剂等。 3、精细化率的定义、我国目前的精细化率。 精细化工率(精细化率)=精细化工品的总值值 100% 精细化率是一个国家或地区化学工业发达程度和化工科技水平高低的重要标志。我国目前的精细化率为45%。 4、世界精细化工的发展趋势。 发达国家新领域精细化工发展迅速、重视化境友好绿色精细化学品和超高功能及超高附加值产品,发展绿色化生产与生物工程技术。传统精细化工向发展中国家转移。 5、我国精细化工的现状与存在的主要问题。 ?我国精细化工产品的自我供应能力已有了大幅度的提升,传统精细化工产品不 仅自给有余,而且大量出口;新领域精细化工产品的整体市场自给率达到70%左 右。一些产品在国际市场上具有较大的影响力。 ?目前国内精细化工产品尚难以满足细分市场需求。以中低档产品为主,难以满 足高端市场要求,以电子化学品为代表的高端精细化学品严重依靠进口。 ?在快速变化的市场面前,我国的研发力量还很不足的,特别是薄弱的精细化工 的基础性研究已成为我国开发新技术和新产品的重要制约因素。 ?部分国家以保护环境和提高产品安全性为由,陆续实施了一批新的条例和标 准;我国也在不断加大与人民生活息息相关的工业品的安全管理力度和提
精细有机合成课程提纲及练习(供参考) 9.利用卤素交换制备氟代烷反应, 此类反应在DMSO 中进行,反应速度比在甲醇中快107倍。为什么? 答: 卤素交换制备氟代烷反应,其反应过程可用下式表示: 此反应是一个双分子的亲核取代反应,亲核试剂(或离子)的亲核能力越强,反应速度越 快。甲醇是质子传递性溶剂,是氢键给体,F -离子能与醇中的氢形成氢键,由于F - 离子的 电荷密度大,因此溶剂化的作用很强,因而在甲醇中F - 的亲核能力很弱。在DMSO 中,DMSO 是非质子传递极性溶剂,它可使正离子专一性的溶剂化而不能使负离子专一性溶剂化,负 离子成为活泼的“裸负离子”,因此以DMSO 为溶剂的F - 离子的亲核能力很强。因此卤素交换制备氟代烷反应,在DMSO 中进行比在甲醇中快很多。 10.2-萘酚与苄基溴反应,采用不同的溶剂,得到的产物不同。 答:在二甲基酰胺的极性非质子溶剂中,由于溶剂对负离子的溶剂化作用很小,得到的主要产物为O-烷基化产物;而在质子溶剂(H 2O )中,由于萘酚负离子与水分子形成牢固的氢键,使氧的反应中心受到溶剂的屏蔽,而主要以C-烷化产物为优势。 11.已知下列负离子的电荷密度大小顺序为:F – >C l – >PhO – >Br – >I – >CN – ,试讨论说明它们在质子传递性溶剂中和非质子传递极性溶剂中亲核活性次序。 答:在质子传递性溶剂中,负离子可与溶剂的质子形成氢键,即溶剂化。负离子的电荷密度越大,则溶剂化能力越强,因而其亲核活性越小,因此在质子传递性溶剂中,负离子的亲核活性次序为F – < Cl – < PhO – < Br – < I – <CN – CH 2Br + DMF H 2O ++NaBr NaBr ONa OCH 2 CH 2 ONa 3—I F CH 3+I £ - δ-δ-F CH 3 I CH 3I CH 3F ++ I ― F ―
1.浓硝酸作为硝化剂时,参加硝化反应的活性质点是NO2+,稀硝酸作为硝化剂时,参加硝化反应的活性质点是NO+。 是(邻对位)定位基;-COOH是(间位)定位基。2.在芳香族的亲电取代反应中,苯环上的-OCH 3 3.(间歇操作)是将各种反应原料按一定的顺序加到反应器中,并在一定的温度、压力下经过一定时间完成特定的反应,然后将反应好的物料从反应器中放出。 4.在连续操作的反应器中,有两种极限的流动模型是(理想混合型和理想置换型) 10% 的发烟硫酸换算成硫酸的浓度是。 5.按照原料单体的种类和数目不同,缩聚反应可以分为(均缩聚、异缩聚、共缩聚)三类。 6.一氯苯的生产工艺经过了三个阶段的变革即(单锅间歇生产工艺、多锅连续生产工艺、塔式沸腾连续生产工艺)。 7.芳环的取代卤化属于亲电反应,在这个反应中,卤素做亲电试剂。 8.(芳伯胺)化合物转变成重氮化合物的反应称为重氮化反应。 9.在铁屑还原法还原硝基时,铁屑的高纯度对反应利。 10.羟基是第 1 类定位基。 三 1以季铵盐为例,简述相转移催化的原理,并画出示意图 在互不相溶的两相体系中,亲核试剂M+Nu-只溶于水相而不溶于有机相,而有机反应物R-X+只溶于有机溶剂而不溶于水相。两者不易相互靠拢而发生化学反应。在上述体系中加入季铵盐Q+X-,它的季铵盐正离子Q+具有亲油性,因此季铵盐既能溶于水相又能溶于有机相。当季铵盐与水相中的亲核试剂M+Nu-接触时,亲核试剂中的负离子Nu-可以同季铵盐中的负离子X-进行交换生成Q+Nu-离子对。这个离子对可以从水相转移到有机相,并且与有机相中的反映物R-X发生亲核取代反应而生成目的产物R+Nu-,在反应中生成的Q+X-离子对又可以从有机相转移到水相,从而完成相转移催化的催化循环,使上述的亲核取代反应顺利完成。 2.在进行芳香族重氮化反应时,往往加入亚硝酸钠,然后再用淀粉-碘化钾试纸鉴定有过量的亚硝基存在时,再加入脲,把过量的亚硝基除去,才进行下一步的反应。解释这一系列的变化并写出可能的反应方程式。 在重氮化时,要用到亚硝酸做重氮化试剂,而且在反应中应保持亚硝酸微过量,可用淀粉-碘化钾试纸检验,微过量的亚硝酸可以将试纸中的碘化钾氧化,游离出碘单质使试纸变为蓝色。反应为 2HNO2 + 2KI +2H2O I2 +2kCl +2NO 而重氮化反应完毕,过量的亚硝酸对下一步反应不利,因此常加入尿素或氨基磺酸将过量的亚硝酸分解