表3 志愿者口服试验制剂和参比制剂后主要药代动力学参数(x ±sd)
制剂t 1/2(A )/h t 1/2(B )/h T peak/h C max /
L g ?ml -1
AUC/L g ?m l ?h -10-240-∞F(%)
T 0.843±0.294 5.329±1.895 1.5±0.2959.981±2.234
33.923±5.34341.526±6.290
99.132±0.069
R
1.060±0.397
5.297±2.394
2.0±0.343
8.281±1.665
34.332±5.590
42.693±8.225
2.3 试验制剂和参比制剂血药浓度-时间曲线
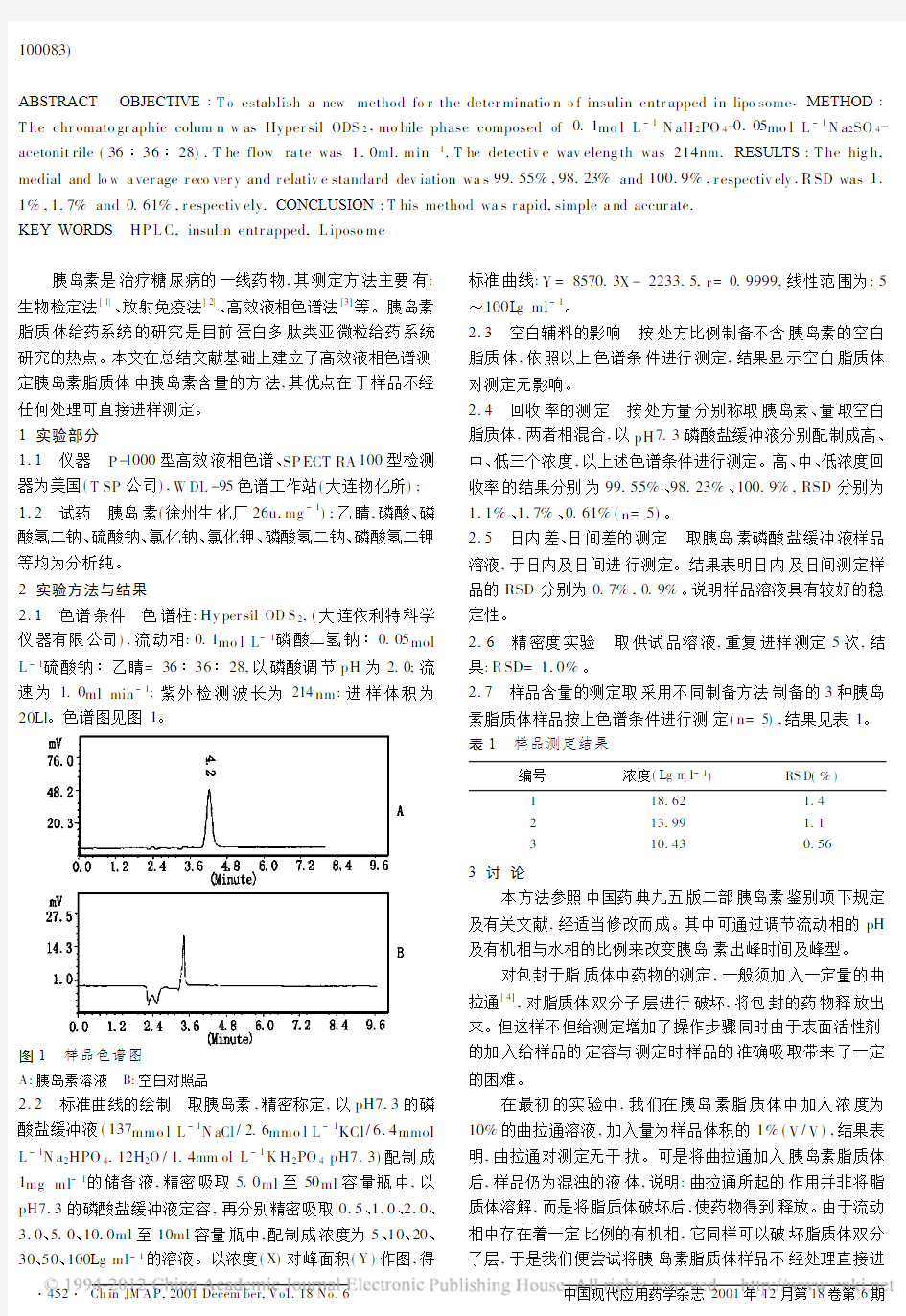
志愿者口服试验制剂和参比制剂血药浓度均值-时间实测曲线如图2
所示。
图2 18名志愿者口服试验制剂和参比制剂血浓度均值-时间实测曲线
2.4 生物等效性
两制剂主要药代动力学参数方差分析、单双侧t 检验和(1-2A )置信区间分析示两制剂为生物等效制剂。如表4所示。
表4 生物等效性评价结果
参数t 1t 290%可信限AU C 0-∞10.80010.60696.0-104.5AU C 0-2413.86615.31793.7-104.1t 1/2(B ) 3.169 2.52664.1-141.0C max 7.687 4.15790.5-123.3T pea k
36.306
7.489
84.8-98.5
≥t(1-A )∶1.7460
3 讨 论
本实验建立了高效液相色谱法测定醋氯芬酸血药浓度的方法,该法专一性强,灵敏度高,符合生物等效性试验要求。
多因素方差分析显示,醋氯芬酸试验制剂和参比制剂单剂口服双交叉试验主要药动学参数(A U C 0-∞、A U C 0-24)无显著性差异,进一步双单侧t 检验和(1-2A )置信区间分析个体间、周期间和剂型间符合生物等效的假设,即醋氯芬酸片和市售的Beofenac 具有生物等效性。参考文献
1
Bort R,Pon soda X,Carras co E,et
al.
M etabolism of
aceclofenac in humans.Drug M etab Dis pos.1996,24(8):8342
Brogden RN and Wis em an LR .Acecloenac :a review of its pharmacodynamic properties and th erapeu tic potential in the treatmen t of r heum atic dis orders and in p ain managem ent.Dru gs,1996,52(1):113
3高立勤,刘文英,邢久东.固相萃取反向冲洗-反相HPLC 法测定血浆中醋氯芬酸浓度.药物分析杂志,1998,18(4):14柳晓泉,陈西敬,赵陆华,等.高效液相色谱法测定血浆中醋氯芬酸及其在犬体内药代动力学.药学学报,1997,32(7):5465柳晓泉,陈西敬,赵陆华,等.醋氯芬酸在大鼠体内的药代动力学.中国药科大学学报,1998,29(4):308
收稿日期:2000-08-16
HPLC 法测定胰岛素脂质体中胰岛素的含量
张 火亘 张 强 齐宪荣(北京100083北京大学药学院药剂教研室)
摘要 目的:胰岛素脂质体中胰岛素含量的测定。方法:采用高效液相色谱法,色谱柱为Hyper sil O DS 2,流动相为0.1mol L -1磷酸二氢钠-0.05mo l L -1硫酸钠-乙睛=36∶36∶28,流速为1ml m in -1,检测波长为214nm 。结果:高、中、低的回收率分别为99.55%,98.23%,100.9%,R SD 分别为1.1%,1.7%和0.61%。在5~100L g ml -1测定范围内,线性良好,r =0.9999。结论:方法可靠,准确。
关键词 高效液相色谱法;胰岛素;脂质体
Determination of insulin entrapped in liposome by HPLC
Zhang Xuan ,Zhang Qiang ,Qi Xianr ong (School of P har maceutical Science ,Beij ing M edical U niv er sity ,B eij ing ,
100083)
ABSTRACT OBJECTIVE :T o establish a new method fo r the deter minatio n o f insulin entr apped in lipo some .METHOD :
T he chr omato gr aphic colum n w as Hyper sil ODS 2,mo bile phase composed of 0.1mo l L -1N aH 2PO 4-0.05mo l L -1N a 2SO 4-acetonit rile (36∶36∶28).T he flow ra te was 1.0ml.min -1.T he detectiv e wav eleng th was 214nm.RESULTS :T he hig h,medial and lo w a ver age r eco ver y and r elativ e standard dev iation wa s 99.55%,98.23%and 100.9%,r espectiv ely .R SD was 1.1%,1.7%and 0.61%,r espectiv ely.CONCLUSION :T his method wa s r apid,simple a nd accur ate.KEY WORDS HP L C,insulin entr apped,L iposo me 胰岛素是治疗糖尿病的一线药物,其测定方法主要有:生物检定法[1]、放射免疫法[2]、高效液相色谱法[3]等。胰岛素脂质体给药系统的研究是目前蛋白多肽类亚微粒给药系统研究的热点。本文在总结文献基础上建立了高效液相色谱测定胰岛素脂质体中胰岛素含量的方法,其优点在于样品不经任何处理可直接进样测定。1 实验部分
1.1 仪器 P -1000型高效液相色谱、SP ECT RA 100型检测器为美国(T SP 公司),W DL -95色谱工作站(大连物化所);1.2 试药 胰岛素(徐州生化厂26u.mg -1
);乙睛,磷酸、磷
酸氢二钠、硫酸钠、氯化钠、氯化钾、磷酸氢二钠、磷酸氢二钾
等均为分析纯。2 实验方法与结果
2.1 色谱条件 色谱柱:Hy per sil OD S 2,(大连依利特科学仪器有限公司),流动相:0.1mo l L -1磷酸二氢钠∶0.05mol L -1硫酸钠∶乙睛=36∶36∶28,以磷酸调节pH 为2.0;流速为1.0ml min -1;紫外检测波长为214nm :进样体积为20L l 。色谱图见图1
。
图1 样品色谱图
A:胰岛素溶液 B:空白对照品
2.2 标准曲线的绘制 取胰岛素,精密称定,以pH7.3的磷酸盐缓冲液(137mmo l L -1N aCl /2.6mmo l L -1KCl /6.4mmol L -1N a 2HPO 4.12H 2O /1.4mm ol L -1K H 2PO 4pH7.3)配制成1mg ml -1的储备液,精密吸取5.0ml 至50ml 容量瓶中,以pH7.3的磷酸盐缓冲液定容,再分别精密吸取0.5、1.0、2.0、
3.0、5.0、10.0ml 至10ml 容量瓶中,配制成浓度为5、10、20、30、50、100L g ml -1的溶液。以浓度(X)对峰面积(Y )作图,得
标准曲线:Y =8570.3X -2233.5,r =0.9999,线性范围为:5~100L g ml -1。
2.3 空白辅料的影响 按处方比例制备不含胰岛素的空白脂质体,依照以上色谱条件进行测定,结果显示空白脂质体对测定无影响。
2.4 回收率的测定 按处方量分别称取胰岛素、量取空白脂质体,两者相混合,以pH 7.3磷酸盐缓冲液分别配制成高、中、低三个浓度,以上述色谱条件进行测定。高、中、低浓度回收率的结果分别为99.55%、98.23%、100.9%,RSD 分别为1.1%、1.7%、0.61%(n =5)。
2.5 日内差、日间差的测定 取胰岛素磷酸盐缓冲液样品溶液,于日内及日间进行测定。结果表明日内及日间测定样品的RSD 分别为0.7%,0.9%。说明样品溶液具有较好的稳定性。
2.6 精密度实验 取供试品溶液,重复进样测定5次,结果:R SD=1.0%。
2.7 样品含量的测定取采用不同制备方法制备的3种胰岛素脂质体样品按上色谱条件进行测定(n=5),结果见表1。表1 样品测定结果
编号浓度(L g m l -1)
RS D(%)118.62 1.4213.99 1.13
10.43
0.56
3 讨 论
本方法参照中国药典九五版二部胰岛素鉴别项下规定及有关文献,经适当修改而成。其中可通过调节流动相的pH 及有机相与水相的比例来改变胰岛素出峰时间及峰型。
对包封于脂质体中药物的测定,一般须加入一定量的曲拉通[4],对脂质体双分子层进行破坏,将包封的药物释放出来。但这样不但给测定增加了操作步骤同时由于表面活性剂
的加入给样品的定容与测定时样品的准确吸取带来了一定的困难。
在最初的实验中,我们在胰岛素脂质体中加入浓度为10%的曲拉通溶液,加入量为样品体积的1%(V /V ),结果表明,曲拉通对测定无干扰。可是将曲拉通加入胰岛素脂质体后,样品仍为混浊的液体,说明:曲拉通所起的作用并非将脂质体溶解,而是将脂质体破坏后,使药物得到释放。由于流动相中存在着一定比例的有机相,它同样可以破坏脂质体双分子层,于是我们便尝试将胰岛素脂质体样品不经处理直接进
452?
样测定。方法学研究证明其可行。
因此本文所建立的测定胰岛素脂质体中胰岛素含量的高效液相色谱法,操作简便,重现性好,结果准确。
参考文献
1中国药典二部.1995:753.
2段明星,乐志操,马 红,等.氰基丙烯酸酯包裹胰岛素纳米颗
粒的结构.中国药学杂志,1999,34(1):23.
3朱延勤,严汉英,刘学丽,等.RH-HPLC测定胰岛素滴眼液的含量.中国药学杂志.1995,30(7):432.
4吕万良,齐宪荣,孙华东,等.阿霉素隐行脂质体的研制及其在小鼠体内的组织分布.中国药学杂志,1999,34(5):310.
收稿日期:2000-09-18
呋喃西林凝胶剂的研制
虞和永 孙 碧 夏晓萍(杭州310006浙江大学附属妇产科医院)
摘要 目的:研制呋喃西林凝胶剂,建立质量控制方法。方法:以Carbopo l934为凝胶基质,采用分光光度法测定含量,加速实验法考察稳定性。结果:所得制剂均匀,分散性好;含量测定平均回收率100.91%,相对标准偏差RSD(%)为0.48。结论:该制剂制备工艺简单,质量可控。
关键词 呋喃西林;凝胶剂
Preparation of Furacilin gel
Yu Heyo ng,Sun Bi,Xia Xiaoping(T he Af f iliated H osp ital f or Gy necology and O bs tetrics,Zhej iang University, H angz hou,310006)
ABSTRACT OBJEC TIVE:T o study the pr escription and pr eparat ion of F uracilin gel.and set up the method of contr ol quality.METHODS:Car bopol934was used as base,the co ntent w as deter mined by spect ro pho tomet ry.RESULTS:T he prepara tio n was w ell-distr ibuted.T he aver age r ecov ery of t he F uracilin w as100.91%(R SD=0.72n=6).CONCLUSION: T he prepar atio n pr ocess was simple and the quality can be co nt ro lled.
KEY WORDS F uracilin,gel
呋喃西林为常用的局部抗菌药。能干扰细菌氧化酶系统而发挥抑菌或杀菌作用,抗菌谱广,用于多种革兰氏阳性及阴性细菌引起的皮肤、粘膜感染[1]。目前临床应用的主要有溶液剂、栓剂、散剂,末见有凝胶剂产品。以呋喃西林、硼酸配伍的制剂对细菌性阴道病,轻度宫颈糜烂有确切的疗效[2]。为了患者用药的方便,更好地发挥药效,我们用新型药物辅料Car bo pol934为基质研制了呋南西林凝胶剂,对该制剂的处方及制备工艺、含量测定方法,初步稳定性进行了研究,为该制剂的进一步开发提供了科学依据。
1 仪器与试剂
1.1 仪器 D U-640分光光度计(美国Backman);
M ET T L ED-T OL EDO分析天平;
PHS-10A数字酸度/离子计
1.2 试剂 呋喃西林(济南金达药化有限公司)
Carbo po l934(上海人民制药厂)
2 实验方法与结果2.1 处方 呋喃西林10g,硼酸10g,Car bo po l93410g,甘油100g,无水乙醇200ml,碘酸钾、薄荷脑,三乙醇胺适量,蒸馏水加至1000g。
2.2 制备工艺 取Carbo po l934分次撒入适量蒸馏水中,使其缓慢溶胀,加入甘油,搅拌,使成透明凝胶基质。另取薄荷脑溶于乙醇,碘酸钾、硼酸溶于适量水中,三项合并,搅匀。边搅拌边撒入呋喃西林粉,以三乙醇胺调P H,加水至足量,搅匀,分装。成品pH为4.5~5.5。
2.3 含量测定
2.3.1 测定波长的选择 分别配制呋喃西林水溶液,辅料和凝胶基质的水溶液,在200~400nm范围内扫描。结果可见:呋喃西林在373±1nm处有最大吸收,其它基质和辅料在此均无吸收,故选择373nm波长进行含量测定。
2.3.2 标准曲线 精密称取呋喃西林10mg置50ml量瓶中,用水溶解,稀释至刻度,摇匀。分别吸取0.5,1.0,2.0, 2.5,3.0,4.0,5.0ml于50ml量瓶中,加水至刻度,摇匀。在
本法系比较胰岛素标准品(S)与供试品(T)引起小鼠血糖下降的作用,以测定供试品的效价。标准品溶液的配制精密称取胰岛素标准品适量,按标示效价,加入每100ml中含有苯酚0.2g并用盐酸调节pH值为2.5的0.9%氯化钠溶液,使溶解成每1ml中含20单位的溶液,分装于适宜的容器内,4~8℃贮存,如无沉淀析出,可在3个月内使用。标准品稀释液的配制试验当日,精密量取标准品溶液适量,按高低剂量组(ds<[2]>、ds<[1]>)加0.9%氯化钠溶液(pH2.5)配成两种浓度的稀释液,高低剂量的比值(r)不得大于1:0.5。高浓度稀释液一般可配成每1ml中含0.06~0.12单位,调节剂量使低剂量能引起血糖明显下降,高剂量不致引起血糖过度降低,高低剂量间引起的血糖下降有明显差别。供试品溶液与稀释液的配制按供试品的标示量或估计效价(A<[T]>),照标准品溶液与其稀释液的配制法配成高、低两种浓度的稀释液,其比值(r)应与标准品相等,供试品和标准品高低剂量所致的反应平均值应相近。检定法取健康无伤、同一来源、同一性别、出生日期相近的成年小鼠,体重相差不得超过3g,按体重随机分成4组,每组不少于10只,逐只编号, 各组小鼠分别自皮下注入一种浓度的标准品或供试品稀释液,每鼠0.2~0.3ml,但各鼠的注射体积(ml)应相等。注射后40分钟,按给药顺序分别自眼静脉丛采血,用适宜的方法,如葡萄糖氧化酶-过氧化酶法测定血糖值。第一次给药后间隔至少3小时,按双交叉设计,对每组的各鼠进行第二次给药,并测定给药后40分钟的血糖值。照生物检定统计法(附录ⅩⅣ)中量反应平行线测定双交叉设计法计算效价及实验误差。本法的可信限率(FL%)不得大于25%。
胰岛素设计性实验报告 篇一:实验设计-修订版 胰岛素所致的低血糖休克及药物 和激素对血糖的影响 第一临床医学院XX级医学检验一班 设计人:郭英刘雨霏刘妮彭超 XX年3月12日 【题目】胰岛素所致低血糖休克及药物和激素对血糖的影响 【背景】 胰岛素是重要的内分泌激素之一,主要生理作用是全面地调节糖类代谢,同时也相应地调节脂肪和蛋白代谢。正常动物由于神经系统的调节和激素的相互作用,血液中胰岛素浓度是相对稳定的。若给正常动物注射胰岛素,可造成人胰岛素性低血糖症状。血糖浓度持续降低而出现交感神经兴奋性增高和脑功能障碍症群而导致的综合症就是低血糖休克。在实验条件下如果给动物注射过量的胰岛素,使动物体内胰岛素量骤然升高,可造成动物实验性低血糖,会使神经组织的正常代谢和功能发生障碍,以至产生痉挛昏迷,外部表现为惊厥,称之为胰岛素休克。小鼠的低血糖休克实验属于经典实验.传统的胰岛素休克实验目的是观察人工胰岛素性低血糖休克以及注射葡萄糖后的消失过程,以加深对胰岛素
生理作用的理解.但实验中一般不测定小鼠血糖的变化,只是观察胰岛素造成低血糖休克时的行为变化。 现阶段对胰岛素降低血糖的原理研究较多,其他药物和激素如甲状腺素、生长激素、糖皮质激素对血糖的研究也以较多,但都是单量试验,并未将多种激素和药物联合起来观察对血糖影响的研究。本次试验将通过制作胰岛素低血糖休克模型来同时观察多种药物和激素对血糖的影响。 体内降低血糖的激素只有胰岛素一种,但升高血糖的激素却不止胰高血糖素一种。糖皮质激素是一种胰岛素拮抗激素,可以增强肝脏中的糖原异生,促进肝糖原分解,抑制外周组织对葡萄糖的摄取和利用,从而导致血糖升高。而甲状腺素有促进生长发育的作用,也能够促进糖的吸收和糖异生,也可升高血糖。生长激素的主要生理功能是促进神经组织以外的所有其他组织生长;促进机体合成代谢和蛋白质合成;促进脂肪分解;对胰岛素有拮抗作用;抑制葡萄糖利用而使血糖升高等作用。但其剂量不同,对血糖的影响亦不同,本次试验就胰岛素等临床常见的与血糖有关的药物和激素对血糖的影响做相应的探讨。 【目的】 学习检测血糖的方法,观察胰岛素及药物和激素对血糖的影响,同时验证不同剂量的生长激素对血糖的影响不同,从而加深理解药物和激素影响血糖水平的机制。
小鼠胰岛素定量分析酶联免疫检测试剂盒 本试剂盒仅供科研使用。用于体外定量检测小鼠血清、血浆或细胞培养上清液中的胰岛素浓度。使用前请仔细阅 读说明书并检查试剂组分是否完整, 如有疑问请与上海巧伊生物科技有限公司联系,我们将提供力所能及的帮助。 如您有其它需求,请登录上海巧伊生物科技有限公司网站或致电本公司。 胰岛素简介: 胰岛素是糖代谢中最主要的激素之一。胰腺的?细胞岛细胞产生胰岛素前体蛋白,前体蛋白被加工成C肽和胰岛素。它们以等摩尔浓度进入血循环中。成熟的胰岛素由A、B两条链组成。这两条链是通过两个二硫键桥接形成有功能的胰岛素分子。 血浆葡萄糖浓度的变化是胰岛素产生并分泌的最主要刺激因素,产生的胰岛素具有一些代谢调节作用。其最主要的作用是,将外周血中糖转运到肝脏中贮存起来。一些诸如肝糖生成障碍或在促进血糖升高的激素诸如胰高血糖素、肾 上腺素、生长激素和皮质醇等作用下促进肝糖分解都可拮抗胰岛素的作用。 检测原理: 本试剂盒采用双抗体夹心ELISA法检测样本中胰岛素的浓度。胰岛素捕获抗体已预包被于酶标板上,当加入标本或参考品时,其中的胰岛素会与捕获抗体结合,其它游离的成分通过洗涤的过程被除去。当加入与HRP耦连的抗胰岛素抗体后,抗小鼠胰岛素抗体与胰岛素接合,形成夹心的免疫复合物,其它游离的成分通过洗涤的过程被除去。最后加入显色剂,若样本中存在胰岛素将会形成免疫复合物,辣根过氧化物酶会催化无色的显色剂氧化成蓝色物质,在加入终止液后呈黄色。通过酶标仪检测,读其450nm处的OD值,胰岛素浓度与OD450值之间呈正比,通过参考品绘制标准曲线,对照 未知样本中OD值,即可算出标本中胰岛素浓度。 小鼠胰岛素定量分析酶联免疫检测试剂盒组成: 组分 规格(96T/48T) 小鼠胰岛素预包被板 12条/6条 标准品稀释液 10ml/5ml 小鼠胰岛素标准品 2支/1支(冻干) 小鼠胰岛素抗体HRP结合物 10ml/5ml 浓缩洗涤液 20× 30ml/15ml TMB底物 10ml/5ml 终止液 5ml/3ml 封板胶纸 3/2张 说明书 1份 标本收集: 1.标本的收集请按下列流程进行操作; A.细胞上清标本离心去除悬浮物后即可; B.血清标本应是自然凝固后,取上清,避免在冰箱中凝固血液; C.血浆标本,推荐用EDTA的方法收集若待测样本不能及时检测, D.标本收集后请分装,冻存于-20℃,避免反复冻融。 2.血清标本不应添加任何防腐剂或抗凝剂; 3.标本应清澈透明,检测前样本中如有悬浮物应通过离心去除。 4.请勿使用溶血,高血脂或污染的标本检测,否则结果将不准确。 注意事项: 1.试剂盒请保存在2~8℃。 2.浓缩洗涤液因在低温下可能有结晶,请水浴加热使结晶完全溶解后再配制工作液。 3.标准品复溶加样后,剩余部分请丢弃。 4.底物请勿接触氧化剂和金属。
小老鼠胰岛素惊厥实验报告 组员:胡欣、郑宁博、朱靖、马凯、於梦秋 (1)原理: 胰岛素是调节机体血糖水平的激素之一。给动物注射大量胰岛素后,引起血糖降低,动物出现惊阙现象。 (2)准备 小白鼠、注射器、胰岛素溶液、酸性生理盐水、生理盐水、10%葡萄糖。 (3)操作步骤 1.取4只体重相近的小鼠,分为实验组与对照组,每组二只。(实验前饥饿26小时) 2.给实验组小鼠腹腔注射胰岛素溶液(0.1毫克/10克体重),胰岛素溶液浓度为2 国际单位/毫升。 腹腔注射方法:左手提起并固定小鼠,使小鼠腹部朝上,鼠头略低于尾部,右手持注射器将针头在下腹部靠近腹白线的两侧进行穿刺,针头刺入皮肤后进针3mm左右,接着使注射针头与皮肤呈45°角刺入腹肌,穿过腹肌进入腹膜腔,当针尖穿过腹肌进入腹膜腔后抵抗感消失。固定针头,保持针尖不动,回抽针栓,如无回血、肠液和尿液后即可注射药液。 胰岛素溶液的配制:用pH2.5-3.5的酸性生理盐水配制胰岛素。 酸性生理盐水配制:将10毫升0.1N HCl 加入300毫升生理盐水中,调pH 值为2.5-3.5。 3.给对照组小鼠腹腔注射等量生理盐水。 4.将两组动物做好标记后,放在室温下观察,比较两组动物的神态、姿势及活动情况。 5.当动物出现抽搐、翻滚等惊阙反应时,记录时间,并将其中一只立即皮下注射10%葡萄糖(0.1毫升/10克体重)。 皮下注射方法:选项背或大腿内侧的皮肤。操作时,常规消毒注射部位皮肤,然后将皮肤提起,注射针头取一钝角角度刺入皮下,把针头轻轻向左右摆动,易摆动则表示已刺入皮下,再轻轻抽吸,如无回血,可缓慢地将药物注入皮下。拔针时左手拇、食指捏住进针部位片刻,以防止药物外漏。 6.比较对照组动物、注射葡萄糖的动物、以及出现惊阙而未经注射葡萄糖的动物的活动情况,分析所得结果。 (4)实验结果及结论
简单介绍胰岛素的测定方法 摘要:胰岛素是体内一类重要的多肽激素,同时它也是临床上治疗糖尿病的一线药物。因此不论是在体测定胰岛素的含量,还是在复杂的药物体系中对胰岛素准确定量,意义都非常重大。正如我们所知,为了正确评价不同剂型中的胰岛素在人体中的确切疗效和安全性,必须研究胰岛素在动物和人体内的药代动力学、吸收、分布、代谢和排泄的规律,这是解释生理学、药效学和毒理学正确合理地进行临床试验必不可少的重要资料,而对胰岛素的准确定量正是这些研究工作的基础。另外,对于药剂本身而言,对胰岛素的准确定量,不但是质量标准的建立的基础,而且也是评价药物处方的关键。 关键词:胰岛素;生物检定;免疫学 与传统药物相比,胰岛素类药物属生物技术药物,它们本身具有种属特异性、免疫原性和非预期的多向性活性等特点,这就给胰岛素类药物的分析方法提出了特殊的要求。特别是药代动力学研究,它的前提就是建立可靠的测定方法。好的胰岛素测定方法的主要标志是:特异性高,灵敏度高、重现性好、回收率高、线性范围宽。如何专一地识别胰岛素又不受其它组分的干扰是检测方法建立的主要难题,另外胰岛素的给药量一般极低,更要求高灵敏度测定方法。许多常规的药物分析方法在用于胰岛素分析时在特异性、灵敏度和精确度方面都有所欠缺。本文扼要介绍目前用于胰岛素测定的主要方法。 1. 生物检定法 生物检定法的基本原理是在体内和体外组织,或细胞对被测药物的某种特异反应,通过剂量(或浓度)效应曲线对目标生物技术药物定量分析(绝对量或比活性单位),一般分为在体分析和离体组织(细胞)分析两种。整体生物分析法测定过程对实验条件的要求较严格,操作程序较多,而许多活性细胞因子已建国际通用的标定国际单位的特定依赖细胞株和标准方法,利用这些系统进行研究是相对可靠的。对于体内实验,一般需要建立动物模型,观察指标也需要建立相应的检查方法,因而耗时数周才能完成,价格昂贵又费时,而且观察终点受主观因素影响,造成灵敏度较低。但是生物检定法是以药物的活性为评价标准,因而其最大优点是能反映生物活性。尤其是胰岛素的生物活性不仅取决于一级结构而且与三级结构有关,因此生物检定法迄今在对胰岛素的研究及应用中有特殊的地位,常常是首先建立的测定方法。胰岛素最常用的生物检定法有小鼠(或兔)血糖法(毛细管法)和小鼠惊厥法。有人对这两种方法进行比较,认为小鼠血糖法可以消除人为误差,更为准确。目前国内外药典中胰岛素类系列制品效价测定,已将经典的生物检定法全部改为高效液相色谱法(HPLC)。 2. 免疫学方法(immune methods) 免疫学方法是利用蛋白多肽药物抗原决定簇部位的单克隆或多克隆抗体特异地识别被检药物,再以放射计数,比色等方法予以定量,即将特异的抗原抗体反应配以灵敏检测的方法。免疫学方法的缺点在于它测定的是蛋白多肽的免疫活性而不是生物活性;不能同时测定代谢物,而且具有抗原决定簇的代谢片段可能增加结果误差;不同来源的抗体与相同的蛋白多肽反应可能有较大的差别;还可能受到内源物质的干扰。但免疫法毕竟是一种迅速、灵敏、适于批处理的方法,已有数十种蛋白多肽被开发成能满足药物动力学研究的商品药盒。其他以免疫为基础的有助于生物技术药物分离和鉴定的分析方法还有免疫沉淀法亲和层析法和免疫印迹法。常用的免疫学方法有以下四种。 2.1 放射免疫法(Radioimmuno assays, RIA)
小鼠胰岛素(Insulin)酶联免疫分析(ELISA) 试剂盒使用说明书 本试剂仅供研究使用目的:本试剂盒用于测定小鼠血清样本中胰岛素(Insulin)含量。 实验原理: 本试剂盒应用双抗体夹心法测定标本中小鼠胰岛素(Insulin)水平。用纯化的小鼠胰岛素(Insulin)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入胰岛素(Insulin),再与HRP标记的胰岛素(Insulin)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的胰岛素(Insulin)呈正相关。用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中小鼠胰岛素(Insulin)含量。 试剂盒组成: 试剂盒组成48孔配置96孔配置保存说明书1份1份 封板膜2片(48)2片(96) 密封袋1个1个 酶标包被板1×481×962-8℃保存 标准品:18mIU/L0.5ml×1瓶0.5ml×1瓶2-8℃保存标准品稀释液 1.5ml×1瓶 1.5ml×1瓶2-8℃保存酶标试剂3ml×1瓶6ml×1瓶2-8℃保存样品稀释液3ml×1瓶6ml×1瓶2-8℃保存显色剂A液3ml×1瓶6ml×1瓶2-8℃保存显色剂B液3ml×1瓶6ml×1瓶2-8℃保存终止液3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存 样本处理及要求: 1.血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。仔细收集上 清,保存过程中如出现沉淀,应再次离心。 2.血浆:应根据标本的要求选择EDTA、柠檬酸钠或肝素作为抗凝剂,混合10-20分钟后, 离心20分钟左右(2000-3000转/分)。仔细收集上清,保存过程中如有沉淀形成,应该再次离心。 3.尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。仔细收集上清,保存过程 中如有沉淀形成,应再次离心。胸腹水、脑脊液参照实行。 4.细胞培养上清:检测分泌性的成份时,用无菌管收集。离心20分钟左右(2000-3000转/ 分)。仔细收集上清。检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。通过反复冻融,以使细胞破坏并放出细胞内成份。离心20分钟左右(2000-3000转/分)。仔细收集上清。保存过程中如有沉淀形成,应再次离心。
生理解剖实验报告 实验名称:胰岛素的降血糖作用及小鼠解剖 实验人:林鸿运 同组者:蒋仕新刘辉 实验日期:2011.04.26 一、实验目的 1. 掌握小鼠的抓取和固定方法; 2. 掌握小鼠的解剖方法; 3. 了解一般实验动物的抓取和固定方法 二、实验内容 1、观察胰岛素对小鼠的降血糖作用 2、掌握小鼠的腹腔注射方法 3、学会对普通动物的实验解剖 三、实验对象及器材 昆明鼠一只,蛙板一块,固定针2根,手术剪,眼科剪,玻璃分针两根,注射器及消毒棉等。实验药品有50%的葡萄糖溶液、胰岛素溶液、麻醉剂,生理盐水。 四.实验步骤 1、小鼠的抓取与固定 正确的抓取固定动物,是为了不损害动物健康,不影响观察指标,并防止被动物咬伤,保证实验顺利进行。抓取固定动物的方法依实验内容和动物类而定。抓取固定动物前,必须对各种动物的一般习性有所了解,抓取固定时既要小心仔细,不能粗暴,又要大胆敏捷,确实达到正确抓取固定动物的目的. 小鼠性情较温顺,挣扎力小,比较容易抓取和保定。抓取时,用左手拇指和食指捏住小鼠尾巴中部(图1)放在格板或铁笼上。趁着小鼠试图挣脱的瞬间,迅速用另外三个手指压住小鼠的尾巴根部握入手掌(图2);放松拇指和食指,用另外三个手指控制小鼠,然后用食指和拇指捏住小鼠头部两边疏松的皮肤提起小鼠(图3),完成抓取保定。注意,抓小鼠尾巴应抓住尾巴中部或根部,不能仅捏住小鼠尾巴的尾端,因为这时小鼠的重量全部集中到尾端,如果小鼠挣扎,有可能弄破尾端。
2、胰岛素的降低血糖的作用(将小鼠分为2组,一组注射0.3ml的胰岛素溶液另一组注射等量的葡萄糖溶液观察两组小鼠的变化情况)。 3、小鼠被毛去除 有剪毛法,拔毛法,剃毛法,用硫化钠脱毛法(我们用剪毛法) 4、小鼠的麻醉 麻药有挥发性的和非挥发性两种。给药途径有吸入性麻醉,注射给药。小鼠一般用腹部麻醉的方法。用水合氯醛300ml/kg,根据小鼠的体重给药0.25ml。抓取小鼠后,使针头和腹部成30度的角,刺入腹腔,回抽若无回血或者肠内容物可以注入。注入麻药5分钟后,小鼠昏迷。 5、解剖 从腹部开始,查看腹部脏器,以肝脏胃脾肾输尿管姨小肠大肠膀胱前列腺性腺顺序。然后再看胸部,看到肺脏心脏胸腺等器官,并在直视的情况下进行了心脏的采血。然后再看颈部的解剖。最后解剖头部。 三讨论和结论: 通过此次实验,我们学到了实验动物的一般操作技术,如抓取和固定、编号被毛的去除给药途径麻醉采血和处死等方法。为以后进入临床进行实验研究做好了初步的准备。 思考与讨论 1、胰岛素的作用机制 胰岛素是动物机体内唯一降低血糖的激素,也是唯一同时促进糖原、脂肪、蛋白质合成的激素。作用机理属于受体酪氨酸激酶机制。 胰岛素能促进全身组织对葡萄糖的摄取和利用,并抑制糖原的分解和糖原异生,因此,胰岛素有降低血糖的作用。胰岛素分泌过多时,血糖下降迅速,脑组织受影响最大,可出现惊厥、昏迷,甚至引起胰岛素休克。 2、胰岛素的注射 腹腔注射方法:左手提起并固定小鼠,使小鼠腹部朝上,鼠头略低于尾部,右手持注射器将针头在下腹部靠近腹腔白线的两侧进行穿刺,针头刺入皮肤后进针3mm左右,接着使注射针头与皮肤呈45°角刺入腹肌,穿过腹肌进入腹膜腔,当针尖穿过腹肌进入腹膜腔后抵抗感消失。固定针头,保持针尖不动,回抽针栓,如无回血、肠液和尿液后即可注射药液。
苦瓜皂苷对糖尿病小鼠的降血糖作用和对胰岛素水平的影响 发表时间:2012-11-22T15:18:26.467Z 来源:《医药前沿》2012年第23期供稿作者:张尚武1 张雅琴2 [导读] 观察苦瓜皂苷提取物对糖尿病小鼠的降血糖作用和胰岛素水平的影响。 张尚武1 张雅琴2(1苏州大学附属第一人民医院普外科江苏苏州 215006)(2 苏州卫生职业技术学院病理教研室江苏苏州 215009) 【摘要】目的观察苦瓜皂苷提取物对糖尿病小鼠的降血糖作用和胰岛素水平的影响。方法昆明小鼠以链脲佐菌素制备糖尿病模型并使用苦瓜皂苷提取物治疗,观察苦瓜皂苷的降血糖作用和对胰岛素水平的影响。结果与糖尿病小鼠相比,苦瓜皂苷治疗组小鼠血糖显著降低,胰岛素水平明显上调,胰岛素抵抗指数显著升高,胰岛素敏感指标显著降低。结论苦瓜皂苷对糖尿病小鼠有明显的降血糖作用,影响胰岛素分泌,使胰岛素抵抗指数显著升高,胰岛素敏感指标显著降低。 【关键词】苦瓜皂苷胰岛素抵抗 胰岛素抵抗(Insulin Resistance,IR)是指胰岛素作用的靶器官对胰岛素作用的敏感性下降,即正常剂量的胰岛素产生低于正常生物学效应的一种状态。中医药对IR的研究渐趋活跃,并逐渐成为中医药防治胰岛素抵抗的研究热点。苦瓜皂苷是苦瓜中有效成分之一,主要在苦瓜果实中存在,苦瓜种子、茎叶中也含有一定量的苦瓜皂苷[1]。本研究观察了苦瓜皂苷提取物对胰岛素抵抗小鼠的降血糖作用和胰岛素水平的影响。 1 材料与方法 1.1 实验动物 昆明种小白鼠50只(6~8周龄),体质量18~22g雄性,购自苏州大学医学院实验动物中心。 1.2 实验动物的分组及实验方法 实验动物随机分为五组,分别为空白对照组、糖尿病模型组、苦瓜皂苷低剂量组、苦瓜皂苷中剂量组和苦瓜皂苷高剂量组,每组10只小鼠。糖尿病模型组、苦瓜皂苷低剂量组、苦瓜皂苷中剂量组和苦瓜皂苷高剂量组小鼠按36mg/kg?d腹腔注射链脲佐菌素,连续给药30天制备模型,随后苦瓜皂苷低剂量组、苦瓜皂苷中剂量组和苦瓜皂苷高剂量组分别给于1g/kg?d,2g/kg?d和4g/kg?d剂量治疗,连续给药15天,分别于第1天、15天、30天和45天禁食8小时测定空腹血糖值,最后一次给药前禁食,给药后8小时内眼眶采血收集血液标本。 1.3 实验动物血糖、胰岛素水平的检测和胰岛素抵抗指数的计算 实验小鼠分别于给药的第1天、15天、30天和45天禁食8小时采取尾动脉微量血,使用强生稳豪倍易型血糖仪及血糖试纸测定空腹血糖值(FPG)。最后一次给药结束后8小时内眼眶采血收集血液标本,4℃静置半小时,吸取上层血清,使用小鼠胰岛素水平检测试剂盒ELISA测定空腹血清胰岛素水平(FIN),使用公式计算胰岛素抵抗指数HOMA-IR=[FPG(mmol/L)×FIN(mIU/L)]/22.5。 1.4 数据统计 所有实验结果采用SPSS10.0软件进行统计分析,结果以x-±s的形式表示。组间差异采用t检验。 2 结果 2.1 小鼠第1天、15天、30天和45天空腹血糖值(FPG) 注:每组小鼠数量n=10;与空白对照组相比,*p<0.01, **p<0.01, △ p<0.01, △△ p<0.01 2.2 小鼠空腹胰岛素水平(FIN)及胰岛素抵抗指数(HOMA-IR)计算 注:每组小鼠数量n=10;与空白对照组相比,* p<0.01, ** p<0.01, △ p<0.01, △△ p<0.01 3 讨论 近些年来,国内外对苦瓜治疗IR和糖尿病的研究都取得了很大的进展,现代医学研究表明[2],苦瓜全株,尤其是果实和种子具有降血糖、抗肿瘤、抗病毒、抗生育及堕胎、抗虫等多种显著的生理活性,其中苦瓜皂苷提取物具有抗氧化、免疫调节作用,可修复受损的胰腺,降低糖尿病高血糖引起的氧化应激水平。有研究表明[3],苦瓜皂苷可使剧烈运动大鼠血清,骨骼肌和肝脏中SOD(超氧化歧化酶)维持较高活力,及时清除体内产生的过氧化物,其机理是苦瓜皂苷能够增强巨噬细胞分泌,而具有诱导和增强SOD和GSH-Px (谷胱甘肽过氧化酶)的活力。此外,苦瓜皂苷也可明显增强体外培养胸腺细胞内SOD的活性,并降低MDA(丙二醛)的产生量。本实验通过链脲佐菌素制备糖尿病模型,使用苦瓜皂苷提取物治疗,观察苦瓜皂苷的降血糖作用和对胰岛素水平的影响,研究显示苦瓜皂苷是一种潜在的降糖、降脂的活性成分,苦瓜皂苷对糖尿病小鼠有明显的降血糖作用,影响胰岛素分泌,使胰岛素抵抗指数显著升高,胰岛素敏感指标显著降低。参考文献 [1]关健,赵余庆.苦瓜化学成分的研究[J].中草药.2007,38(12): 1777-1779. [2]Chen Q, Chan LL, Li ETO. Bitter melon(momordica charntia) reduces adiposity, lowers serum insulin and normalizes glucose tolerance in rats fed a high fat diet[J]. J Nutr, 2003. 133(4): 1088-1093. [3]李健,黄艳,陈诛娟等. 苦瓜皂甙生物活性的研究进展[J].食品研究与开发,2008,29(3):144-146.