
2015-2016学年江苏省泰州市泰兴一中高二(下)第二次段考化
学试卷
一、单项选择题:本题包括10小题,每小题2分,共计20分.每小题只有一个选项符合题意.
1.下列物质中,不属于卤代烃的是()
A.CH2Cl2B.CCl2F2C.D.
2.涂改液是一种使用率较高的文具,很多同学都喜欢使用涂改液.经实验证实涂改液中含有许多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,二氯甲烷就是其中的一种.下列有关说法中不正确的是()
A.涂改液危害人体健康、污染环境,中小学生最好不要使用或慎用涂改液
B.二氯甲烷沸点较低
C.二氯甲烷易溶于水,涂改液沾到手上时,用水很容易洗去
D.二氯甲烷为四面体的结构,不存在同分异构体
3.常温常压下为无色液体,而且密度大于水的是()
①苯②硝基苯③溴苯④四氯化碳⑤溴乙烷⑥乙酸乙酯.
A.①⑥B.②③④⑥C.②③④⑤D.③④⑤⑥
4.下列分子中,核磁共振氢谱中有3个峰的是()
A.一氯甲烷 B.溴乙烷C.1﹣氯丙烷D.邻氯甲苯
5.下列化学用语表达不正确的是()
A.丙烷的球棍模型为
B.丙烯的结构简式为CH3CHCH2
C.符合通式C n H2n
的一定是烷烃
+2
D.O2、O3属于同素异形体
6.下列卤代烃在KOH醇溶液中加热不反应的是()
①C6H5Cl ②(CH3)2CHCH2Cl ③(CH3)3CCH2Cl ④CHCl2﹣CHBr2 ⑤
⑥CH2Cl2.
A.①③⑥ B.②③⑤ C.全部 D.②④
7.从溴乙烷制取1.2﹣二溴乙烷,下列转化方案中最好的是()
A.CH3CH2Br CH3CH2OH CH2=CH2CH2BrCH2Br
B.CH3CH2Br CH2BrCH2Br
C.CH3CH2Br CH2=CH2CH2BrCH3CH2BrCH2Br
D.CH3CH2Br CH2=CH2CH2BrCH2Br
8.化学工作者从有机反应RH+Cl2(g)RCl(l)+HCl(g)受到启发提出的在农药和有机合成工业中可获得副产品HCl的设想已成为现实,试指出由上述反应产物分离得到盐酸的最佳方法是()
A.水洗分液法B.蒸馏法
C.升华法D.有机溶剂萃取法
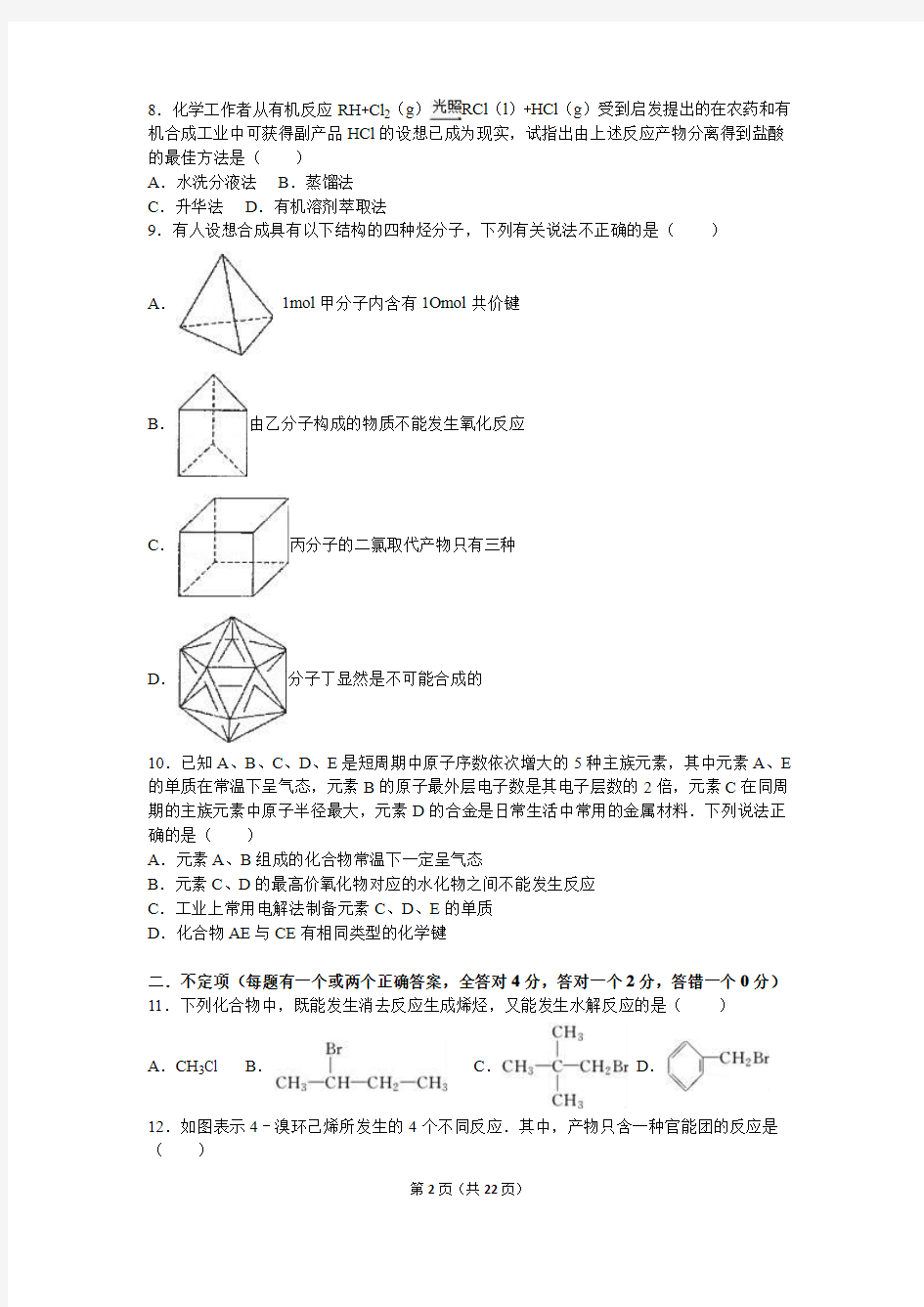
9.有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是()
A.1mol甲分子内含有1Omol共价键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子的二氯取代产物只有三种
D.分子丁显然是不可能合成的
10.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E 的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是()
A.元素A、B组成的化合物常温下一定呈气态
B.元素C、D的最高价氧化物对应的水化物之间不能发生反应
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE有相同类型的化学键
二.不定项(每题有一个或两个正确答案,全答对4分,答对一个2分,答错一个0分)11.下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是()
A.CH3Cl B.C.D.
12.如图表示4﹣溴环己烯所发生的4个不同反应.其中,产物只含一种官能团的反应是()
A.①B.②C.③D.④
13.下列说法正确的是()
A.丙烷是直链烃,所以分子中3个碳原子也在一条直线上
B.丙烯所有原子均在同一平面上
C.所有碳原子一定在同一平面上
D.至少有16个原子共平面
14.在一定条件下,萘可以被硝硫混酸硝化生成二硝基物,它是1.5﹣二硝基萘()
和1.8﹣二硝基萘()的混合物.后者可溶于质量分数大于98%的硫酸,而前者不
能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8﹣二硝基萘,应彩的方法是()A.蒸发浓缩结晶 B.向滤液中加入水后过滤
C.用Na2CO3溶液处理滤液D.将滤液缓缓加入水中过滤
15.柠檬烯具有特殊香气.可溶于乙醇或乙醚,不溶于水,其结构简式如图所示:
,有关柠檬烯的说法正确的是()
A.柠檬烯分子为非极性分子
B.柠檬烯分子中所有碳原子处于同一个平面上
C.柠檬烯能与酸性高锰酸钾溶液发生取代反应
D.柠檬烯的分子式为C10H16,能使溴的四氯化碳溶液褪色
二、第Ⅱ卷
16.在实验室鉴定氯酸钾晶体和1﹣氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化.(填序号)
(1)鉴定氯酸钾中氯元素的操作步骤依次是
(2)鉴定1﹣氯丙烷中氯元素的操作步骤依次是.
17.下列物质①O2②氯仿③CH3CH2CH2OH
④O3⑤CHCl3⑥CH3OH⑦C⑧⑨ C (填序号)
互为同分异构体的是,属于同位素的是.
18.(1)分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简式
(2)写出2﹣甲基﹣1﹣戊烯的结构简式:.
19.已知:CH3﹣CH═CH2+HBr﹣→(主要产物),1mol某烃A充分燃烧后
得到8mol CO2和4mol H2O.
该烃A在不同条件下能发生如下所示一系列变化.
(1)A的结构简式:.
(2)上述反应中,①是反应,⑦是反应.(填反应类型)
(3)写出C的结构简式:
(4)写出D﹣→F反应的化学方程式:
写出B﹣→E反应的化学方程式:.
20.现通过以下步骤由制备
(1)写出A、B的结构简式:A:B:.
(2)从左到右依次填写每步反应所属的反应类型(a.取代反应,b.加成反应,c.消去反应,只填字母代号):.
(3)写出④的反应方程式:
(4)写出的含有六元碳环的同分异构体:
(5)写出该制备方法的合成路线图,有机合成路线图示例如下:CH3CHO
CH3COOH CH3COOCH2CH3.
21.醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷和1﹣溴丁烷的反应如下:NaBr+H2SO4═HBr+NaHSO4①R﹣OH+HBr﹣→R﹣Br+H2O②可能存在的副反应有:醇在
Br﹣Br
)溴代烃的水溶性(填)相应的醇,其原因是.
(2)将1﹣溴丁烷粗产品置于分液漏斗中,加水振荡后静置,产物在(填“上层”“下层”或“不分层”).
(3)制备操作中,加入的浓硫酸必须进行稀释,其目的是(填字母).
A.减少副产物烯和醚的生成B.减少Br2的生成
C.减少HBr的挥发D.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是(填字母).
A.NaI B.NaOH C.NaHSO3D.KCl
(5)在制备溴乙烷时,采用边反应边蒸馏产物的方法,目的是:
但在制备1﹣溴丁烷时却不能边反应边蒸馏,其原因:.
元素原子基态时的电子排布式.
(2)C元素的第一电离能比氧元素的第一电离能(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是,其在水中溶解度大,理由:
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有(填序号);
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为(填序号).
a.平面正方形b.正四面体c.三角锥形d.V形
1mol[E(CA3)4]2+中含有σ键的数目为.
23.钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.
(1)写出Se的基态原子的外围电子排布式.
(2)酒石酸钛配合物广泛应用于药物合成.酒石酸(结构如图1所示)中羧基氧原子的轨道杂化类型分别是,1mol酒石酸中π键的数目是.
(3)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于晶体;NO3﹣离子的空间构型为.
(4)主族元素A和钛同周期,具有相同的最外层电子数,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键.元素A、元素B和钛三者形成的晶体的晶胞如图2所示,写出该晶体的化学式(用元素符号表示).
2015-2016学年江苏省泰州市泰兴一中高二(下)第二次
段考化学试卷
参考答案与试题解析
一、单项选择题:本题包括10小题,每小题2分,共计20分.每小题只有一个选项符合题意.
1.下列物质中,不属于卤代烃的是()
A.CH2Cl2B.CCl2F2C.D.
【考点】有机物分子中的官能团及其结构.
【分析】烃中的氢原子被卤素原子取代后生成的有机物为卤代烃,卤代烃必须满足:分子中除了碳氢元素以外,只含有卤素原子,不能含有其它元素,以此解答该题.
【解答】解:A.CH2Cl2可以看作甲烷中2个氢原子被2个氯原子取代,CH2Cl2属于卤代烃,故A不选;
B.CCl2F2可以看作甲烷中氢原子分别被F、Cl取代,属于卤代烃,故B不选;
C.为硝基苯,不含卤素原子,故C选;
D.为溴苯,为苯中氢原子被溴原子取代完成的,溴苯属于卤代烃,故D不选.故选C.
2.涂改液是一种使用率较高的文具,很多同学都喜欢使用涂改液.经实验证实涂改液中含有许多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,二氯甲烷就是其中的一种.下列有关说法中不正确的是()
A.涂改液危害人体健康、污染环境,中小学生最好不要使用或慎用涂改液
B.二氯甲烷沸点较低
C.二氯甲烷易溶于水,涂改液沾到手上时,用水很容易洗去
D.二氯甲烷为四面体的结构,不存在同分异构体
【考点】有机物的结构和性质;常见的生活环境的污染及治理.
【分析】二氯甲烷为涂改液的主要成分,常温下为液体,为卤代烃,难溶于水,易挥发,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,危害人体健康、污染环境,中小学生最好不要使用或慎用涂改液,以此解答该题.
【解答】解:A.由题给信息可知,涂改液中含有许多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,则改液危害人体健康、污染环境,中小学生最好不要使用或慎用涂改液,故A正确;
B.二氯甲烷常温下为液体,易挥发,沸点较低,故B正确;
C.二氯甲烷难溶于水,不能用水冲洗,故C错误;
D.二氯甲烷具有甲烷的结构特点,可由氯原子取代生成,为四面体结构,不存在同分异构体,故D正确.
故选C.
3.常温常压下为无色液体,而且密度大于水的是()
①苯②硝基苯③溴苯④四氯化碳⑤溴乙烷⑥乙酸乙酯.
A.①⑥B.②③④⑥C.②③④⑤D.③④⑤⑥
【考点】苯的性质;溴乙烷的化学性质.
【分析】根据有机物大多不溶于水,再结合物质的颜色和密度来解答.
【解答】解:①苯的密度比水小,常温、常压下为无色;
②硝基苯的密度比水大,常温、常压下为无色;
③溴苯的密度比水大,常温、常压下为无色;
④四氯化碳的密度比水大,常温、常压下为无色;
⑤溴乙烷的密度比水大,常温、常压下为无色;
⑥乙酸乙酯的密度比水小,常温、常压下为无色;
显然只有②③④⑤符合题意,
故选C.
4.下列分子中,核磁共振氢谱中有3个峰的是()
A.一氯甲烷 B.溴乙烷C.1﹣氯丙烷D.邻氯甲苯
【考点】常见有机化合物的结构.
【分析】根据有机物分子中有几种H原子,核磁共振氢谱有几种吸收峰,结合等效氢判断.【解答】解:A.一氯甲烷CH3Cl,分子中只有一种氢原子,核磁共振氢谱一种,故A不符合;
B.溴乙烷CH3CH2Br,分子中含有两种氢原子,核磁共振氢谱两种,故B不符合;
C.1﹣氯丙烷CH3CH2CH2Cl,分子中含有两种氢原子,核磁共振氢谱三种,故C符合;D.邻氯甲苯分子中含有五种氢原子,核磁共振氢谱五种,故D不符合;
故选C.
5.下列化学用语表达不正确的是()
A.丙烷的球棍模型为
B.丙烯的结构简式为CH3CHCH2
C.符合通式C n H2n
的一定是烷烃
+2
D.O2、O3属于同素异形体
【考点】有机物分子中的官能团及其结构;电子式、化学式或化学符号及名称的综合.【分析】A.球棍模型中,用大小不同的小球表示原子,用短棍表示共价键;
B.丙烯的结构简式中没有标出其官能团碳碳双键;
C.C n H2n
为饱和链烃的通式;
+2
D.O2、O3为同种元素构成的不同单质.
【解答】A.丙烷为含有3个碳原子的烷烃,丙烷的球棍模型为,故A
正确;
B.丙烯的官能团为碳碳双键,结构简式中需要标出官能团,丙烯的结构简式为CH3CH=CH2,故B错误;
C.C n H2n
中C原子全部成键,为烷烃,故C正确;
+2
D.O2、O3为同种元素构成的不同单质,互为同素异形体,故D正确.
故选B.
6.下列卤代烃在KOH醇溶液中加热不反应的是()
①C6H5Cl ②(CH3)2CHCH2Cl ③(CH3)3CCH2Cl ④CHCl2﹣CHBr2 ⑤
⑥CH2Cl2.
A.①③⑥ B.②③⑤ C.全部 D.②④
【考点】卤代烃简介.
【分析】消去反应是指在一定条件下,有机物脱去小分子生成含有不饱和键的有机物.卤代烃的消去反应是在碱的醇溶液中加热,连接﹣X的碳的相邻碳原子上的一个H和﹣X一同被脱去,而生成不饱和烃和卤化氢.
【解答】解:①有机物发生消去反应发生后将会形成不饱和键,而氯苯中相邻的碳原子是苯环的一部分,没有氢原子,故不能发生消去反应,故①正确;
②和氯相连的碳的相邻碳原子上有氢,故能消去,生成对应的烯烃和氯化钾,故②错误;
③和氯相连的碳的相邻碳原子上没有氢,所以不能发生消去反应.故③正确;
④和氯或溴相连的碳相邻碳原子上有氢,故能消去,生成对应的烯烃或炔烃和氯化钾,故
④错误;
⑤和溴相连的碳上有氢,故能发生消去反应,生成对应的烯烃和溴化钾,故⑤错误;
⑥二氯甲烷只有一个碳,没有相邻的碳,所以不能发生消去反应.故⑥正确;
故选A.
7.从溴乙烷制取1.2﹣二溴乙烷,下列转化方案中最好的是()
A.CH3CH2Br CH3CH2OH CH2=CH2CH2BrCH2Br
B.CH3CH2Br CH2BrCH2Br
C.CH3CH2Br CH2=CH2CH2BrCH3CH2BrCH2Br
D.CH3CH2Br CH2=CH2CH2BrCH2Br
【考点】溴乙烷的化学性质;乙烯的化学性质.
【分析】在有机物的制备反应中,应选择的合成路线是步骤尽量少,合成产率尽量高,据此解答即可.
【解答】解:A.转化中发生三步转化,较复杂,消耗的试剂多,反应需要加热,故A不选;B.发生取代反应的产物较多,引入杂质,且反应不易控制,故B不选;
C.转化中发生三步转化,较复杂,且最后一步转化为取代反应,产物不纯,故C不选;D.发生消去、加成两步转化,节约原料、转化率高、操作简单、产物纯净,故D选;
故选D.
8.化学工作者从有机反应RH+Cl2(g)RCl(l)+HCl(g)受到启发提出的在农药和有机合成工业中可获得副产品HCl的设想已成为现实,试指出由上述反应产物分离得到盐酸的最佳方法是()
A.水洗分液法B.蒸馏法
C.升华法D.有机溶剂萃取法
【考点】物质分离、提纯的实验方案设计.
【分析】RH+Cl2(g)RCl(l)+HCl(g),从反应产物中分离得到盐酸,利用溶解性即可.
【解答】解:RH+Cl2(g)RCl(l)+HCl(g),从反应产物中分离得到盐酸,因RCl 不溶于水,HCl极易溶于水,
则水洗分液法可得到盐酸,
故选A.
9.有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是()
A.1mol甲分子内含有1Omol共价键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子的二氯取代产物只有三种
D.分子丁显然是不可能合成的
【考点】有机化合物中碳的成键特征.
【分析】A.根据烃的物质的量以及1个甲分子中含有6个碳碳共价单键、4个碳氢共价单键;
B.根据烃能燃烧,发生氧化还原反应;
C.根据一氯取代产物中氢原子的种类;
D.根据碳原子最外层只有4个电子,最多可形成4个共价键,不能形成5个共价键,【解答】解:A.1个甲分子中含有6个碳碳共价单键、4个碳氢共价单键,即1个甲分子中含有10个共价键,所以1mol甲分子内含有1Omol共价键,故A正确;
B.烃能燃烧,发生氧化还原反应,故B错误;
C.丙分子的一氯代物只有一种,其分子中含有3种氢原子,所以丙分子的二氯取代产物只有三种,故C正确;
D.分子丁中碳原子形成5个共价键,所以不可能合成,故D正确;
故选:B;
10.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E 的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是()
A.元素A、B组成的化合物常温下一定呈气态
B.元素C、D的最高价氧化物对应的水化物之间不能发生反应
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE有相同类型的化学键
【考点】原子结构与元素的性质.
【分析】元素B的原子最外层电子数是其电子层数的2倍,B为2个电子层时,B为C,为3个电子层时为S,A、E的单质在常温下呈气态,元素C在同周期的主族元素中原子半径最大,则C为Na元素,元素D的合金是日常生活中常用的金属材料,则D为Al,结合原子序数依次增大,则E为Cl,B只能为C,A为H,然后结合元素及其化合物的性质来解答.
【解答】解:元素B的原子最外层电子数是其电子层数的2倍,B为2个电子层时,B为C,为3个电子层时为S,A、E的单质在常温下呈气态,元素C在同周期的主族元素中原子半径最大,则C为Na元素,元素D的合金是日常生活中常用的金属材料,则D为Al,结合原子序数依次增大,则E为Cl,B只能为C,A为H,
A.元素A、B组成的化合物常温下可能为气态、液体、固体,如烷烃中C原子数少于4个为气体,随碳原子个数增多,为液体、固体,故A错误;
B.元素C、D的最高价氧化物对应的水化物分别为NaOH、氢氧化铝,能发生反应,故B 错误;
C.C、D、E的单质为Na、Al、Cl2,工业上常用电解熔融的NaCl制备Na,电解熔融的氧化铝制备铝,电解氯化钠溶液制备氯气,故C正确;
D.化合物AE为HCl,含共价键,CE为NaCl,含离子键,化学键类型不同,故D错误;故选C.
二.不定项(每题有一个或两个正确答案,全答对4分,答对一个2分,答错一个0分)11.下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是()
A.CH3Cl B.C.D.
【考点】有机物的结构和性质.
【分析】选项中均为卤代烃,与﹣X相连C的邻位C上有H可发生消去反应生成烯烃,﹣X可发生水解反应转化为﹣OH,以此来解答.
【解答】解:A.没有邻位C,不能发生消去反应,故A不选;
B.可发生消去反应生成1﹣丁烯或2﹣丁烯,水解生成2﹣丁醇,故B选;
C.与﹣X相连C的邻位C上没有H,不能发生消去反应,故C不选;
D.与﹣X相连C的邻位C上没有H,不能发生消去反应,故D不选;
故选B.
12.如图表示4﹣溴环己烯所发生的4个不同反应.其中,产物只含一种官能团的反应是()
A.①B.②C.③D.④
【考点】有机物的结构和性质.
【分析】由结构可知,有机物中含C=C和﹣Br,①为氧化反应,②为水解反应,③为消去反应,④为加成反应,以此来解答.
【解答】解:由结构可知,有机物中含C=C和﹣Br,①为氧化反应,得到两种官能团;
②为水解反应,得到﹣C=C和﹣OH两种官能团;
③为消去反应,产物中只有C=C;
④为加成反应,产物中只有﹣Br,
则有机产物只含有一种官能团的反应是③④,
故选CD.
13.下列说法正确的是()
A.丙烷是直链烃,所以分子中3个碳原子也在一条直线上
B.丙烯所有原子均在同一平面上
C.所有碳原子一定在同一平面上
D.至少有16个原子共平面
【考点】常见有机化合物的结构.
【分析】A.直链烃是锯齿形的;
B.甲烷是正四面体结构;
C.因为环状结构不是平面结构;
D.苯环是平面结构,该分子中在同一条直线上的原子有8个.
【解答】解:A.丙烷3个碳原子是锯齿形的,故A错误;
B.CH3﹣CH═CH2中甲基上至少有一个氢不和它们共平面,故B错误;
C.因为环状结构不是平面结构,所以所有碳原子不可能在同一平面上,故C错误;
D.该分子中在同一条直线上的原子有8个(),再加上其中一个苯
环上的8个原子,所以至少有16个原子共平面,故D正确.
故选D.
14.在一定条件下,萘可以被硝硫混酸硝化生成二硝基物,它是1.5﹣二硝基萘()
和1.8﹣二硝基萘()的混合物.后者可溶于质量分数大于98%的硫酸,而前者不
能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8﹣二硝基萘,应彩的方法是()A.蒸发浓缩结晶 B.向滤液中加入水后过滤
C.用Na2CO3溶液处理滤液D.将滤液缓缓加入水中过滤
【考点】物质的分离、提纯的基本方法选择与应用.
【分析】根据题中信息,1.8﹣二硝基萘可溶于质量分数大于98%的硫酸,当对溶液进行稀释时,1.8﹣二硝基萘在稀酸溶液中析出,注意稀释浓硫酸时不能将水直接加入酸中,因硫酸溶于水会放出大量的热而导致液体飞溅,应将浓酸加入到水中,很明显加入Na2CO3溶液处理滤液会造成原料的损耗,不利于循环利用.
【解答】解:A、1.8﹣二硝基萘可溶于质量分数大于98%的硫酸,蒸发不会使1.8﹣二硝基萘析出,故A错误;
B、因硫酸溶于水会放出大量的热而导致液体飞溅,应将浓酸加入到水中,故B错误;
C、加入Na2CO3溶液处理滤液会造成原料的损耗,不利于循环利用,故C错误;
D、将滤液缓缓加入水中过滤,防止硫酸溶于水会放出大量的热而导致液体飞溅,1.8﹣二硝基萘可溶于质量分数大于98%的硫酸,当对溶液进行稀释时,1.8﹣二硝基萘在稀酸溶液中析出,故D正确.
故选D.
15.柠檬烯具有特殊香气.可溶于乙醇或乙醚,不溶于水,其结构简式如图所示:
,有关柠檬烯的说法正确的是()
A.柠檬烯分子为非极性分子
B.柠檬烯分子中所有碳原子处于同一个平面上
C.柠檬烯能与酸性高锰酸钾溶液发生取代反应
D.柠檬烯的分子式为C10H16,能使溴的四氯化碳溶液褪色
【考点】有机物的结构和性质.
【分析】柠檬烯中含有2个碳碳双键,可发生加成、加聚、氧化反应,结合结构特点解答该题.
【解答】解:A.可溶于乙醇或乙醚,不溶于水,由相似相溶原理可知柠檬烯分子为非极性分子,故A正确;
B.可溶于乙醇或乙醚,不溶于水,但结构不对称,为极性分子,故B错误;
C.含有碳碳双键,可与酸性高锰酸钾发生氧化还原反应,故C错误;
D.由结构简式可知有机物分子式为C10H16,可与溴发生加成反应,能使溴的四氯化碳溶液褪色,故D正确.
故选AD.
二、第Ⅱ卷
16.在实验室鉴定氯酸钾晶体和1﹣氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化.(填序号)
(1)鉴定氯酸钾中氯元素的操作步骤依次是④③⑤⑦①
(2)鉴定1﹣氯丙烷中氯元素的操作步骤依次是②③⑦①.
【考点】常见离子的检验方法.
【分析】(1)氯酸钾与二氧化锰混合加热反应,反应后的物质加水溶解,把二氧化锰过滤掉,取用滤液,滴加硝酸银溶液,再加稀硝酸,观察反应现象;
(2)鉴定1﹣氯丙烷中存在氯元素,应在碱性条件下水解,然后在用硝酸酸化,加入硝酸银进行检验.
【解答】解:(1)由题意可知:氯酸钾与二氧化锰混合加热反应,反应后的物质有氯化钾和二氧化锰;加水溶解,把二氧化锰过滤掉,取用滤液,再滴加硝酸银溶液,观察反应现象;如果生成白色沉淀,滴加稀硝酸白色沉淀不消失,则证明氯酸钾中含氯元素,操作步骤依次为:④③⑤⑦①,
故答案为:④③⑤⑦①;
(2)1﹣氯丙烷不溶于水,在酸性或碱性条件下水解,其中碱性条件下水解程度较大,碱性条件下水解生成氯离子,然后在用硝酸酸化,加入硝酸银进行检验,以排除氢氧根离子的干扰,操作步骤为:②③⑦①,
故答案为:②③⑦①.
17.下列物质①O2②氯仿③CH3CH2CH2OH
④O3⑤CHCl3⑥CH3OH⑦C⑧⑨ C (填序号)
互为同分异构体的是③⑧,属于同位素的是⑦⑨.
【考点】同分异构现象和同分异构体;同位素及其应用.
【分析】具有相同分子式而结构不同的化合物互为同分异构体;具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素.
【解答】解:③CH3CH2CH2OH⑧具有相同分子式而结构不同,互为同分异
构体;
⑦C⑨C具有相同质子数,不同中子数,互为同位素;
故答案为:③⑧;⑦⑨.
18.(1)分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简
式
(2)写出2﹣甲基﹣1﹣戊烯的结构简式:CH2=CH(CH3)CH2CH2CH3.
【考点】芳香烃、烃基和同系物.
【分析】(1)苯环上的一溴取代物只有一种,说明苯环上只有一种氢原子;
(2)含有C=C双键的碳链有5个碳原子,双键处于端位置,从C=C双键一端编号,甲基在2号碳原子上.
【解答】解:(1)苯环上的一溴取代物只有一种,说明苯环上只有一种氢原子,则2个碳原
子不可能是形成1个乙基,只能是2个甲基,且处于对角位置,其结构简式为,
故答案为:;
(2)2﹣甲基﹣1﹣戊烯分子中含有C=C双键的碳链有5个碳原子,双键处于端位置,从
C=C双键一端编号,甲基处于2号碳原子上,其结构简式为CH2=CH(CH3)CH2CH2CH3,故答案为:CH2=CH(CH3)CH2CH2CH3.
19.已知:CH3﹣CH═CH2+HBr﹣→(主要产物),1mol某烃A充分燃烧后
得到8mol CO2和4mol H2O.
该烃A在不同条件下能发生如下所示一系列变化.
(1)A的结构简式:.
(2)上述反应中,①是加成反应,⑦是酯化反应.(填反应类型)
(3)写出C的结构简式:
(4)写出D﹣→F反应的化学方程式:+NaOH+NaBr
写出B﹣→E反应的化学方程式:+2NaOH
+2NaBr+2H2O.
【考点】有机物的推断.
【分析】1mol某烃A充分燃烧后得到8mol CO2和4mol H2O,由原子守恒可知A的分子式
为C8H8,A的不饱和度为=5,与溴发生加成反应得到B,B发生取代反应得到E,E与溴发生加成反应得到C8H6Br4,可推知A中含有1个碳碳双键,可推知A为
,B为,E为.苯乙烯发生加聚反应生成C为
.结合信息可知苯乙烯与HBr发生加成反应生成D为,D发
生水解反应生成F为,F与醋酸发生酯化反应得到H为.【解答】解:1mol某烃A充分燃烧后得到8mol CO2和4mol H2O,由原子守恒可知A的分
子式为C8H8,A的不饱和度为=5,与溴发生加成反应得到B,B发生取代反应得到E,E与溴发生加成反应得到C8H6Br4,可推知A中含有1个碳碳双键,可推知A为
,B为,E为.苯乙烯发生加聚反应生成C为
.结合信息可知苯乙烯与HBr发生加成反应生成D为,D发
生水解反应生成F为,F与醋酸发生酯化反应得到H为.
(1)A的结构简式:,故答案为:;
(2)上述反应中,①是加成反应,⑦是酯化反应,故答案为:加成;酯化;
(3)C的结构简式:,故答案为:;
(4)D→F反应的化学方程式: +NaOH+NaBr;
B→E反应的化学方程式: +2NaOH+2NaBr+2H2O,
故答案为: +NaOH+NaBr;
+2NaOH+2NaBr+2H2O.
20.现通过以下步骤由制备
(1)写出A、B的结构简式:A:B:.
(2)从左到右依次填写每步反应所属的反应类型(a.取代反应,b.加成反应,c.消去反应,只填字母代号):bcbcb.
(3)写出④的反应方程式:+2NaOH++2O
(4)写出的含有六元碳环的同分异构体:
(5)写出该制备方法的合成路线图,有机合成路线图示例如下:CH3CHO
CH3COOH CH3COOCH2CH3.
【考点】有机物的合成.
【分析】由转化关系可知,氯苯与氢气发生加成反应生成A为,A在氢氧化钠醇溶
液、加热条件下发生消去反应生成B为,环己烯再与氯气发生加成反应生成,
再发生消去反应生成C为,与氯气发生加成反应得到.
【解答】解:由转化关系可知,氯苯与氢气发生加成反应生成A为,A在氢氧化钠
醇溶液、加热条件下发生消去反应生成B为,环己烯再与氯气发生加成反应生成
,再发生消去反应生成C为,与氯气发生加成反应得到.
(1)A的结构简式为:,B的结构简式为:,
故答案为:;;
(2)由上述分析可知,①为加成反应,②为消去反应,③为加成反应,④为消去反应,⑤为加成反应,
故答案为:bcbcb;
(3)④的反应方程式: +2NaOH+2NaCl+2H2O,
故答案为: +2NaOH+2NaCl+2H2O;
(4)的含有六元碳环的同分异构体:,
故答案为:;
(5)该制备方法的合成路线图:
,
故答案为:
.
21.醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷和1﹣溴丁烷的反应如下:NaBr+H2SO4═HBr+NaHSO4①R﹣OH+HBr﹣→R﹣Br+H2O②可能存在的副反应有:醇在
Br﹣Br
溴代烃的水溶性小于(填其原因是醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键.
(2)将1﹣溴丁烷粗产品置于分液漏斗中,加水振荡后静置,产物在下层(填“上层”“下层”或“不分层”).
(3)制备操作中,加入的浓硫酸必须进行稀释,其目的是ABC(填字母).
A.减少副产物烯和醚的生成B.减少Br2的生成
C.减少HBr的挥发D.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是C(填字母).
A.NaI B.NaOH C.NaHSO3D.KCl
(5)在制备溴乙烷时,采用边反应边蒸馏产物的方法,目的是:平衡向生成溴乙烷的方向移动(或反应②向右移动)
但在制备1﹣溴丁烷时却不能边反应边蒸馏,其原因:1﹣溴丁烷和正丁醇的沸点相差不大.
【考点】制备实验方案的设计.
【分析】(1)醇能和水形成氢键的物质而易溶于水;1﹣溴丁烷的密度大于水,且和水不互溶;
(2)浓硫酸具有强氧化性,能氧化溴离子为溴单质,易发生消去反应,浓硫酸溶解溶液温度升高易使溴化氢挥发;
(3)1﹣溴丁烷和正丁醇的沸点相差较小,不能采用蒸馏的方法分离;
(4)溴代烷在碱溶液中水解,碘化钠和溴单质反应生成碘单质,氯化钠不能除去溴单质;(5)根据平衡移动原理分析采用边反应边蒸出产物的原因;根据1﹣溴丁烷和正丁醇的沸点的沸点大小判断.
【解答】解:(1)醇能和水形成氢键的物质而易溶于水,溴代烃和水不反应也不能和水形成氢键,所以溴代烃的水溶性小于相应的醇;
故答案为:小于;醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键;(2)1﹣溴丁烷和水不能形成氢键所以不易溶于水,且密度大于水,所以将1﹣溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在下层,
故答案为:下层;
(3)A.浓硫酸和1﹣丁醇反应发生副反应消去反应生成烯烃、分子间脱水反应生成醚,稀释后不能发生类似反应减少副产物烯和醚的生成,故a正确;
B.浓硫酸具有强氧化性能将溴离子氧化为溴单质,稀释浓硫酸后能减少Br2的生成,故b 正确;
C.反应需要溴化氢和1﹣丁醇反应,浓硫酸溶解溶液温度升高,使溴化氢挥发,稀释后减少HBr的挥发,故c正确;
D.水是产物不是反应的催化剂,故d错误;
故答案为:ABC;
(4)欲除去溴代烷中的少量杂质Br2,
A.NaI和溴单质反应,但生成的碘单质会混入,故a错误;
B.溴单质和氢氧化钠反应,溴代烷也和NaOH溶液发生水解反应,故b错误;
C.溴单质和NaHSO3溶液发生氧化还原反应,可以除去溴单质,故c正确;
D.KCl不能除去溴单质,故d错误;
故答案为:C;
(5)根据题给信息知,乙醇和溴乙烷的沸点相差较大,采用边反应边蒸出产物的方法,可以使平衡向生成溴乙烷的方向移动,而1﹣溴丁烷和正丁醇的沸点相差较小,所以不能边反应边蒸出产物,
故答案为:平衡向生成溴乙烷的方向移动(或反应②向右移动);1﹣溴丁烷和正丁醇的沸点相差不大.
元素原子基态时的电子排布式1s2s2p3s3p sd4s.
(2)C元素的第一电离能比氧元素的第一电离能大(填“大”或“小”).
(3)CA3分子中C原子的杂化类型是sp3,其在水中溶解度大,理由:NH3与H2O 分子间形成氢键
(4)A、C、E三种元素可形成[E(CA3)4]2+,其中存在的化学键类型有①③(填序号);
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为a(填序号).
a.平面正方形b.正四面体c.三角锥形d.V形
1mol[E(CA3)4]2+中含有σ键的数目为16mol.
【考点】位置结构性质的相互关系应用.
【分析】A原子的1s轨道上只有1个电子,则A为H元素;B是电负性最大的元素,则B 为F元素;C的基态原子2p轨道中有三个未成对电子,核外电子排布为1s22s22p3,故C为N元素;E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,则E为Cu;D是主族元素且与E同周期,其最外层上有两个运动状态不同的电子,则D为Ca,据此解答.【解答】解:A原子的1s轨道上只有1个电子,则A为H元素;B是电负性最大的元素,则B为F元素;C的基态原子2p轨道中有三个未成对电子,核外电子排布为1s22s22p3,故C为N元素;E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,则E为Cu;D 是主族元素且与E同周期,其最外层上有两个运动状态不同的电子,则D为Ca.
(1)E为Cu元素,核外电子排布式是:1s22s22p63s23p6sd104s1,
故答案为:1s22s22p63s23p6sd104s1;
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,氮元素原子2p能级为半满稳定状态,第一电离能高于氧元素的,
故答案为:大;
(3)NH3分子中N原子价层电子对个数是4且含有一个孤电子对,所以N的杂化轨道类型是sp3,NH3极易溶于水的主要原因是:NH3与H2O分子间形成氢键,
故答案为:sp3;NH3与H2O分子间形成氢键;
(4)[Cu(NH3)4]2+配离子中,铜离子与氨气分子之间形成配位键,氨气分子中N原子与氢原子之间形成极性共价键,
[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代能得到两种不同结构的产物,[Cu(NH3)4]2+的空间构型为平面正方形,
[Cu(NH3)4]2+中含有4个配位键、12个N﹣H键,1mol[Cu(NH3)4]2+中含有σ键的数目为16mol,
故答案为:①③;a;16mol.
23.钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途.
(1)写出Se的基态原子的外围电子排布式4s24p4.
(2)酒石酸钛配合物广泛应用于药物合成.酒石酸(结构如图1所示)中羧基氧原子的轨道杂化类型分别是sp2、sp3,1mol酒石酸中π键的数目是2N A.
(3)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于分子晶体晶体;NO3﹣离子的空间构型为平面三角形.
(4)主族元素A和钛同周期,具有相同的最外层电子数,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键.元素A、元素B和钛三者形成的晶体的晶胞如图2所示,写出该晶体的化学式CaTiO3(用元素符号表示).
【考点】晶胞的计算;原子核外电子排布;判断简单分子或离子的构型.
【分析】(1)Se的原子核外有34个电子,最外层有6个电子;
(2)羧基氧原子的价层电子对数判断;双键中含有一个π键;
(3)分子晶体的熔沸点较低;NO3﹣的价层电子对数=成键电子对数+孤电子对数,然后判断杂化类型和空间构型;
(4)主族元素A和钛同周期,具有相同的最外层电子数,则最外层含有2个电子,A为Ca元素,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键,已知N、O、F的氢化物能形成氢键,则B为O,Ca占据晶胞的顶点,O占据面心,Ti在晶胞内部,根据均摊法计算.
【解答】解:(1)Se的原子核外有34个电子,最外层有6个电子,则其核外电子分4层排布,最外层为电子排布为4s24p4,故答案为:4s24p4;
(2)羧基的结构式为﹣﹣O﹣H,两个O原子的价层电子对数分别为3、4,则杂化类型
分别为sp2、sp3;酒石酸分子中含有2个羧基,每个羧基含有一个C=O,双键中含有一个π键,则一分子酒石酸中含有2个π键,所以1mol酒石酸中π键的数目是2N A;
故答案为:sp2、sp3;2N A;
(3)已知TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,分子晶体的熔沸点较低,
则TiCl4属于分子晶体;NO3﹣中N原子的价层电子对数=3+(5+1﹣3×2)=3,属于sp2
杂化,没有孤电子对,所以离子的构型为平面三角形;
故答案为:分子晶体;平面三角形;
2019-2020学年八年级(上)期末数学试卷 一.选择题(共6小题) 1.下列交通标志图案是轴对称图形的是() A.B.C.D. 2.下列各数:,﹣3.14,,2π,无理数有() A.1个B.2个C.3个D.4个 3.点P(1,﹣2)关于y轴对称的点的坐标是() A.(﹣1,﹣2)B.(1,2)C.(﹣1,2)D.(﹣2,1)4.已知一次函数y=kx+b的图象经过第一、二、三象限,则b的值可以是()A.﹣2 B.﹣1 C.0 D.2 5.下列各组数是勾股数的是() A.6,7,8 B.1,,2 C.5,4,3 D.0.3,0.4,0.5 6.在△ABC中,∠C=90°,∠B=60°,下列说法中,不一定正确的是() A.BC2+AC2=AB2 B.2BC=AB C.若△DEF的边长分别为1,2,,则△DEF和△ABC全等 D.若AB中点为M,连接CM,则△BCM为等边三角形 二.填空题(共10小题) 7.1﹣π的相反数是. 8.17.85精确到十分位是. 9.已知△ABC≌△A'B'C',∠A=60°,∠B=40°,则∠C′=. 10.点P(﹣5,12)到原点的距离是. 11.若函数y=2x+3﹣m是正比例函数,则m的值为.
12.如图,△ABC中,D是BC上一点,AC=AD=DB,∠C=70°,则∠B=°. 13.如图,Rt△ABC中,∠C=90°,AD是∠BAC的平分线,CD=4,AB=16,则△ABD的面积等于. 14.一次函数y1=ax+3与y2=kx﹣1的图象如图所示,则不等式kx﹣1<ax+3的解集是. 15.已知A(x1,y1)、B(x2,y2)是一次函数y=(2﹣m)x+3图象上两点,且(x1﹣x2)(y1﹣y2)<0,则m的取值范围为. 16.如图,平面直角坐标系中,若点A(3,0)、B(4,1)到一次函数y=kx+4(k≠0)图象的距离相等,则k的值为. 三.解答题(共10小题) 17.(1)计算:
江苏省泰兴中学高二政治周末作业(必修) 经济生活第二单元 一、单项选择题 1、右图是中国3G标识,通过3G手机可以实现视频通话、宽带上网、观看手机电视等。手机新功能带来生活和娱乐 方式新变化,这说明() A.消费对生产有反作用 B.生产决定消费水平和消费方式 C.新的消费热点能给企业带来经济效益 D.生产是消费的目的和动力 2.十七大报告指出,促进经济增长由主要依靠投资、出口拉动向依靠消费、投资、出口协调拉动转变。增加“消费”与投资、出口协调拉动经济增长,这是因为() A.只要增加居民收入,就能拉动经济增长 B.生产决定消费,没有生产就没有消费 C.消费的发展能促进生产的发展 D.有效需求不足会制约经济的增长 3.生产决定消费,消费对生产具有重要反作用。下列选项体现消费对生产具有重要反作用的是 A.数字技术的发展,为人们提供了视听效果更完美的产品 B.随着收入水平的不断提高,旅游成为人们生活的一部分 C.网上购物方式不仅方便了消费者,而且降低了企业成本 D.人们对健康的关注,推动了绿色食品业的迅速发展 4.据调查,目前我国至少有85%的新迁住户要装修居室,家庭居室装修业成了新的经济增长点。家庭居室装修业的兴起说明()A.转变经济增长方式必须扩大内需 B.超前消费反映了人们消费观念的转变 C.生存资料消费是居民最基本的消费 D.新的消费热点能够带动相关产业的发展 5、近几年来,人们休闲方式不断“升级”,昔日打网球、保龄球等“贵族运动”,如今已成为平民时尚。人们对休闲服务的个性 化需求也在增加。人们休闲方式不断升级的根本原因是() A.居民收入稳步增长B.社会经济不断发展 C.商品、服务价格持续下降D.居民消费结构日益优化 6、据《人民日报》报道,既不同于集体经济占主导的“苏南模式”,也有别于私营经济唱主角的“温州模式”,务实的宁波人似 乎并不在意什么模式,他们追求的则是“不看成份看发展,不看比例看贡献,不看规模看效益”的目标。材料充分体现了()A.我国公有制经济居于主体地位 B.国有经济的实现形式可以多样化 C.符合“三个有利于”的所有制形式可以而且应当用来为社会主义服务 D.非公有制经济是社会主义经济的重要组成部分 7、2010年10月1日是我国《物权法》实施三周年。物权法规定:国家、集体、私人的物权和其他权利人的物权受法律保护, 任何单位和个人不得侵犯。这一规定() ①有利于维护社会主义市场经济秩序 ②重在保护个人的私有财产 ③重在提高股份制经济在公有制经济中的比重 ④有利于促进公有制经济和非公有制经济的共同发展 A.①③B.②③C.②④D.①④ 8.右图是某市2009年各类经济成分在GDP中所占比重, 说明该市所有制结构是:() A.以按劳分配为主体,多种分配方式并存 B.以公有制为主体,多种所有制经济共同发展 C.以按生产要素分配为主体,多种分配方式并存 D.以非公有制为主体,多种所有制经济共同发展
江苏省泰兴市2019-2020学年上学期初中七年级期末考试数学试卷 (时间120分钟 满分100分) 一、选择题:(本大题共6小题,每小题2分,共12分) 1.-3的相反数是( ) A .-3 B .3 C .31- D .3 1 2.下列各式计算正确的是( ) A.() 72 5 a a = B.2 2212x x = - C. 62382·4a a a = D. 628a a a =÷ 3.一个几何体的三视图如图,则该几何体是( ) A . B . C . D . 4.将长方形ABCD 沿AE 折叠,得到如图所示的图形,已知'50CED ∠=?,则AED ∠的大小是( ) A. 40° B. 50° C.65° D.75° 5.下列说法正确的是( ) A .单项式y x 2 2 3 π的系数是 2 3 B .若AB =B C ,则点B 是线段AC 的中点 C .3和5是同类项 D .同一平面内,过一点有且只有一条直线与已知直线平行 6.整式mx +n 的值随x 的取值不同而不同,下表是当x 取不同值时对应的整式的值, x -2 -1 1 2
mx +n -12 -8 -4 0 4 则关于x 的方程-mx -n =8的解为( ) A. -1 B.0 C. 1 D.2 二、填空题(本大题共10小题,每小题2分,共20分) 7.某种感冒病毒的直径是0.00000012米,用科学记数法表示为____米. 8.当x 时, 1)20 =-x (有意义. 9.若单项式14a x y --与322b x y 是同类项,则b a =_________. 10.如图,直线AB 、CD 相交于点O ,OE ⊥CD ,∠AOE =60°,则∠BOC =__ °. 11.计算:20172016 25 .0?=__________. 12.将一堆糖果分给幼儿园的小朋友,如果每人2颗,那么就多8颗;如果每人3颗,那么就少12颗.若设共有小朋友x 人,则可列方程为________________. 13.将如图所示的图形剪去一个小正方形,使余下的部分恰好能折成一个正方体,下列编号为1、2、3、6的小正方形中不能剪去的是____(填编号). 14.观察:22201+?=a ;212222+?=a ;323222+?=a ;4 34222+?=a ;……, 请根据你猜想的规律写出n a =_______ __.(n 为正整数,注意填最简结果) 15.如图,若开始输入的x 的值为正分数,最后输出的结果为13,则满足条件的x 的值为_________.
关于学校的各项综合指标所列出 1.南京外国语学校99.5 2.南师附中9 3.3 3.江苏省苏州中学92.7 4.江苏省扬州中学92.5 5.南京金陵中学92.1 6. 江苏省木渎中学91.4 7.江苏省天一中学90.9 8.江苏省泰兴中学90.8 9.盐城中学90.7 10.江苏省苏州实验中学90.5 11.江苏省南通中学90.45 12.南京市第一中学90.4 13.无锡市辅仁高级中学90.35 14.江苏省常州高级中学90.2 15.江苏省前黄高级中学90.1 16.江苏省启东中学90.0 90分以上十六所,为江苏顶级学校。 18.南通第一中学89.4 19.江苏省锡山高级中学89.1 20. 无锡市第一中学89.0 21.江苏省梅村高级中学88.5 22.江苏省梁丰高级中学88.1 23.江苏省南菁高级中学88.0 24.常州市第一中学87.7 25.江苏省溧水高级中学87.45 27.苏州市第一中学87.0 28.苏州市第十中学86.4 29.江苏省江阴高级中学86.15 30.南京市第十三中学85.5 31.镇江市第一中学85.2 32.徐州市第三中学85.0 33.南京市中华中学84.75 34.苏州中学园区83.7 35.苏州新区第一中学83.4 36.江苏教育学院附属中学83.1 37.江苏省淮阴中学82.7 38.南京市第九中学82.65 39.江苏省常熟中学82.6 40.江苏省姜堰中学82.6 41.江苏省海安高级中学82.5 42.徐州市第一中学82.5 43.江苏省通州高级中学82.4 45.江苏省昆山中学81.6
46.江苏省如皋中学80.8 47.江苏省宜兴高级中学80.7 48.江苏省镇江中学80.4 49.江苏省怀仁高级中学80.2 50.江苏省黄桥中学80.2 51.南通市第三中学80.1 52.南京市江宁高级中学80.05 53.江苏省泰州中学80.0 80分以上53所。 54.姜堰市第二中学79.9 55.江苏省滨海中学79.1 56.江苏省华罗庚中学78.4 57.苏大附中77.6 58.江苏省清江中学77.5 59.江苏省郑集高级中学77.4 60.江苏省丹阳高级中学77.2 61.江苏省邗江中学75.7 62.江苏省武进高级中学75.4 63.江苏省南通市如东栟茶中学75.4 64.盐城第一中学74.8 65.江苏省扬中高级中学74.1 66.江苏省太湖高级中学74.0 67.江苏省建湖高级中学72.2 68.江阴市长泾中学71.5 69.江苏省侯集中学71.4 70.张家港高级中学70.6 71.江苏省奔牛高级中学70.2 72.南京航空航天大学附属中学70.0 70分以上72所学校 73.江苏省羊尖高级中学69.4 74.包场中学67.1 75.江阴市第一中学67.0 76.震泽中学66.2 77.江苏省太仓高级中学65.2 78.苏州第三中学65.1 79.东山高级中学64.7 80.南京市第五中学64.4 81.苏州市第六中学64.3 82.江苏省东台中学63.2 83.苏州新区二中63.1 84.太仓市沙溪高级中学60.5 85.江阴市青阳中学60.1 86.通州市西亭中学60.0 87.江苏省沭阳高级中学60.0 60分以上级别87所,属于优秀级学校
2017-2018学年江苏省泰州市泰兴市五年级(上)期末数学试卷 一、智慧宝库:(20分,其中第1、6题每空0.5分,其余每空1分) 1.(3.00分) 0.65平方千米=公顷306克=千克2200平方米=公 顷 5吨22千克=吨4.08平方分米=平 方厘米 0.5平方分米平方 厘米. 2.(1.00分)在一次数学测验中,某班平均分是85分,把高于平均分的部分记作正数,小丽得98分,记作,小军得分记作﹣8分,他实际得分是. 3.(1.00分)17.08的计数单位是,它有个这样的计数单位. 4.(1.00分)50个细菌8小时可繁殖838860000个,把838860000个改写成用“亿”作单位是亿个,精确到十分位约是亿个. 5.(0.50分)4÷0.5转化成乘法算式,若使结果不变,这个乘法算式应该是.6.(2.50分)在横线里填上“>”、“<”或“=”. 12.6×0.9212.60.420.42÷0.67 1.3÷0.88 1.3×0.88 2.4÷1.25 2.4×0.8 7.(1.00分)一个三位小数用四舍五入法取近似值是1.80,这个数最大是,最小是. 8.(1.00分)我们爱数学我们爱数学…第60个字是,前58个字中有个“爱”.9.(1.00分)用18个边长1厘米的小正方形拼成一个大长方形,一共有种不同的拼法,其中周长最大是厘米. 10.(1.00分)的商保留两位小数约是,保留三位小数约是. 二、明辨是非:(正确的打“√”,错误的打“×”)(5分) 11.(3.00分)小数都比自然数小..(判断对错) 12.(3.00分)4.6除以0.7,当商是6时,余数是4..(判断对错) 13.(3.00分)因为0.9=0.900,所以近似数0.900可以写成0.9..(判断对错)
江苏省泰兴市西城中学2017-2018学年七年级下学期期末考 试语文试题 学校:___________姓名:___________班级:___________考号:___________ 一、字词书写 1.根据拼音在田字格内依次写出相应的汉字。 闲xiá之余,yōu然漫步于羌溪河畔,碧水潺潺,繁花bānlán,鸟鸣啾唧,令人心旷神怡。 二、选择题 2.下列句子中标点符号使用正确 ..的一项是() A.《木兰诗》选自《乐府诗集》(北宋郭茂倩编,中华书局1979年版)。 B.“我对这次考试充满了信心,”他对我说:“因为我准备得很充分。” C.仰之弥高,越高,攀得越起劲,钻之弥坚,越坚,钻得越锲而不舍。 D.屈原、李白、杜甫……等,像一颗颗宝石,镶嵌在中华民族的史册上。 3.下列成语运用正确 ..的一项是() A.他嘴上虽然没有说不对,心里却不以为意 ....。 B.5月14日,川航一客机出现机械故障,机长刘传建力挽狂澜 ....,将飞机成功降落机场。 C.由于今年多次遇到旱痨灾害,庄稼的收成不好,农民们只能过个兀兀穷年 ....。 D.人民生活安居乐业 ....,社会安定有序,国家长治久安,群众的幸福感才会越来越强。 4.下列句子中,没有语病 ....的一项是() A.走进美丽的银杏公园,我停下脚步驻足观赏。 B.各地中小学建立和完善了校园安全工作机制。 C.这次全市开展的环保征文活动,五个小学的学生获得了二等奖。 D.由于公共自行车站点比较密集,使泰兴城区市民“绿色出行”更加便利。 5.(题文)下列说法有误 ..的一项是() A.我和.母亲漫步西湖,空气清新 ....,繁花似锦,嗅着花香,闭了眼,树上仿佛满.是累累硕果。(上句中的“和”是连词,“满”是副词,“空气清新”是主谓短语) B.陈忠实老师看到出版社的条件很差,就自掏腰包两万元,为改善我们的工作条件尽 了一点绵薄之力 ....。(“绵薄之力”是谦词,使用错误,此处应该用敬词)
2020┄2021学年江苏省泰州市泰兴一中高二(上)期中化学 试卷(必修) 一.选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分) 1.(3分)(2015?姜堰市)化学与科学、技术、社会、环境密切相关.下列有关说法中正确的是() A.提倡使用一次性发泡塑料餐具和塑料袋 B.食用的蛋白质、淀粉和脂肪都是高分子化合物 C.大力开发和应用氢能源有利于实现“低碳经济” D.绿色化学的核心是应用化学原理治理环境污染 2.(3分)(2015?南京校级模拟)碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一.碳酸氢钠属于() A.酸B.碱C.盐D.混合物 3.(3分)(2015?姜堰市)下列化学用语表达正确的是() A.Cl﹣的结构示意图: B.乙酸的结构式:C2H4O2 C.氯化氢分子的电子式:H+[:Cl:]﹣ D.质量数为137的钡原子:Ba 4.(3分)(2015?南京校级模拟)下列关于物质性质的说法正确的是() A.通常状况下,NO2是无色的气体
B.SO2能漂白品红等物质,说明SO2有氧化性 C.氯化钙溶液和AgNO3溶液混合有白色沉淀产生 D.加热时,铁单质与浓硝酸不发生反应 5.(3分)(2015?姜堰市)能够将溶液和胶体区分开的方法是() A.过滤B.观察颜色、状态 C.利用丁达尔效应D.闻气味 6.(3分)(2015秋?泰兴市校级期中)下列溶液中的Cl﹣浓度与100mL 1mol?L﹣1 MgCl2溶液中的Cl﹣浓度相等的是() A.150 mL 1 mol?L﹣1 NaCl溶液 B.75 mL 0.5mol?L﹣1CaCl2溶液 C.150 mL 2 mol?L﹣1 KCl溶液 D.75 mL 1 mol?L﹣1AlCl3溶液 7.(3分)(2015?南京校级模拟)下列仪器中一般不用作反应容器的是()A.试管B.烧瓶C.烧杯D.容量瓶 8.(3分)(2015?姜堰市)下列气体中,既能用浓硫酸干燥,又能用氢氧化钠固体干燥的是() A.O2B.NO2C.SO2D.NH3 9.(3分)(2015?南京校级模拟)在无色酸性溶液中能大量共存的离子组是()A.NH4+、Fe3+、SO42﹣、Cl﹣B.Ba2+、K+、OH﹣、NO3﹣ C.Al3+、Cu2+、SO42﹣、Cl﹣D.Na+、Ca2+、Cl﹣、NO3﹣
圆锥曲线 [目地要求] 1、了解圆锥面的概念 2、了解用平面从不同角度截圆锥面所得到的曲线 3、理解椭圆、双曲线、抛物线的定义 [重点难点] 重点:椭圆、双曲线、抛物线的定义 难点:圆锥面的截面的规律性 [典例剖析] 例1、已知△ABC中,B(-3,0),C(3,0)且AB、BC、AC成等差数列 (1)证:点A在一个椭圆上运动; (2)写出这椭圆的焦点坐标 例2、已知动点P到两个定点A(-5,0)、B(5,0)的距离之差为8,求点P的轨迹
例3、若动点M 的坐标满足方程22 53412x y x y +=+-,试判断动点M 的轨迹 例4、如图,已知定圆1F 和定圆2F 的半径分别为121,2r r ==,动圆M 与定圆1F 、2F 都外切,试判断动圆M 的圆心M 的轨迹 [学习反思] 已知平面上定点1F ,2F (122F F c =) 动点P (1) 若12PF PF +=常数2a ,则2a>2c 时,P 的轨迹是___________________ 2a=2c 时,P 的轨迹是____________________ (2) 若12PF PF - =常数2a ,则2a<2c 时,P 的轨迹是__________________ 2a=2c 时,P 的轨迹是____________________
[巩固练习] 1、 已知在坐标轴上有两定点1F (-4,0)、2F (4,0),点P 是平面上一点,且1210PF PF +=, 则点P 的轨迹是______________________________________ 2、 已知△ABC ,其中B (0,1)C (0,-1),且1AB AC -=,则点A 的轨迹是 ______________________________________________ 3、 已知定点M (1,1),定直线:3l x =,有一动点N ,点N 到点M 的距离MN 始终等于点N 到 直线l 的距离,则点N 的轨迹是_____________________________________ 4、 已知椭圆的两个焦点为1F (2,-3)、2F (3,-2),则此椭圆的焦距是___________ 5、 已知椭圆的焦点是1F 、2F ,P 是椭圆上的一个动点,如果延长1F P 到点Q ,使得2PQ PF =, 那么动点Q 的轨迹是____________________ 江苏省泰兴中学高二数学课后作业(6) 班级: 姓名: 学号: 【A 组题】 1、 若动点P 到两点1F (-5,0)、2F (5,0)的距离和为10,则P 的轨迹为___________ 2、 已知定点1F (-2,0)、2F (2,0)在满足下列条件的平面内,则动点P 的轨迹中为双曲 线的是___________________ ①123PF PF -=±;②124PF PF -=±;③125PF PF -=±;④22124PF PF -=± 3、 设定点1F (-7,0)、2F (7,0),动点P(x,y)满足条件1214PF PF -=,则动点P 的轨 迹是_________________ 4、 平面上与定点A(1,1)和定直线l :x+2y-3=0距离相等的点的轨迹方程为____________ 5、 平面内有两个定点1F 、2F 和一动点M ,设命题甲:12MF MF -是定值;命题乙:点M 的轨迹是双曲线,则命题甲是命题乙的_________________条件 6、一个圆过点M (-4,0)且与圆N :()2 249x y -+=相切(注意相切的情形的判断),求动
期末语文试卷 一、选择题(本大题共3 小题,共6.0分) 1. 下列各句中标点符号使用有错.误..的一项是() A. 我一边让雨湿着我的头发,一边吟诵杜甫的“随风潜入夜,润物细无声”,甚至想去田野悠悠 地踏青呢。 B. 不久书桌上德文字典和日文字典都摆起来了,果戈里的死魂灵,又开始翻译了。 C. 惊涛澎湃,掀起万丈狂潮;浊流宛转,结成九曲连环。 D. 那里装的是什么仙露琼浆?我凑上去,想摘一朵。 2. 下列各句中加点的成语使用正确..的一项是() A. 2019年1月16日,我国“氢确之父”于敏在北京溘然长逝,马革裹.尸...。 B. 他年方十一,却已能绘出如此意境空灵的山水面,的确令人刮目相待....啊! C. 老师反复提醒他注意书写,可他的字依然如群蚁排.衙...,潦草不堪。 D. 日寇的铁蹄践踏着中华大地,人民过着颠沛流.离...的生活。 3. 下列各句中说法正确..的一项是() A. “把.书送去”“比.前天热”“在.读书”加点的词都是介词,它们都没有单独使用,而是跟 名词结合在一起组成短语。 B. 对于广大的关东原野,我心里怀着挚痛的热爱,我无时无刻听见她呼唤我的名字。 C. “桃李飘香”“鸟语花香”“桃花的香”“闻到桃香”分别是主谓短语、并列短语、偏正短 语、动宾短语。 D. 《资治通鉴》是北宋名臣司马迁主持编纂的一部编年体通史,记载了从战国到五代共1362 年 间的史事。 二、多选题(本大题共1 小题,共3.0分) 4. 下列关于文学名著内容及常识表述错误的.两.项...是() A. 《海底两万里》是法国著名科幻和探险小说家凡尔纳创作的科幻小说,其中的科学幻想如今已 变成现实。 B. 《海底两万里》的主人公尼摩船长是一个智慧超群的领导人,“鹦鹉螺号”在南极被困冰层 时,只有他想到了用开水去化冰。 C. 《骆驼祥子》以20 年代的北平为背景,通过人力车夫祥子一生几起几落最终沉沦的悲惨遭 遇,反映了一个有良知的作家对底层劳动人民生存状况的同情。 D. 《骆驼祥子》中刻画了很多像祥子一样的小人物,如横死街头的车夫二强子,为养活兄弟出卖 肉体最终吊死的小福子,他们的悲剧是整个时代的悲剧。 E. “小萝卜头”是罗广斌、杨益言合著的长篇小说《红岩》中的人物。 三、默写(本大题共1 小题,共8.0分) 5. 按课文内容填空。当窗理云鬓,。 斯是陋室, ________ 。 黄梅时节家家雨, _________ 。 ______ ,何人不起故园情。 哲理诗是诗人对人生、社会的深度关注与睿智思索的智慧结品,往往把发人深省的哲理寓于富有特色的生活情趣之中:杜甫在泰山的壮丽美景中触景生情,想象 “ _____ ,________ ”的豪迈,激励我们勇于攀登;陆游在山西村溪水潺潺、山路陡 转的茅舍前感慨“ ________ ,_______ ”,告诉我们在困境中坚持,终究会出现豁然开 朗的境界。 四、其他(本大题共2 小题,共9.0分) 6. 根据拼音在田字格中写出相应的汉字。
江苏省泰兴市第一高级中学2009届高三第一次月考 物理试卷 命题人:叶副权 2008、9、27 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。共120分,考试用时100分钟 第Ⅰ卷选择题(共31分) 一、单项选择题(本题共5小题,每题3分,共15分。在每小题给出的四个选项中,只有一个选项是正确的。) 1、下列说法正确的是 A.行星的运动和地球上物体的运动遵循不同的规律 B.物体在转弯时一定受到力的作用 C.月球绕地球运动时受到地球的引力和向心力的作用 D.物体沿光滑斜面下滑时受到重力、斜面的支持力和下滑力的作用 2、如图所示,在距地面h高处以初速度v0沿水平抛出一个物体, 不计空气阻力,物体在下落过程中,下列说法中正确的是: A、物体在c点比a具有的机械能大 B、物体在a点比c点具有的动能大 C、物体在a、b、c三点具有的动能一样大 D、物体在a、b、c三点具有的机械能相等 3、物体m从倾角为α的固定的光滑斜面由静止开始下滑,斜面高为h,当物体滑至斜面底端,重 力做功的瞬时功率为 4、如图,一轻绳的一端系在固定粗糙斜面上的O点,另一端系一小球.给小球一足够大的初速度, 使小球在斜面上做圆周运动.在此过程中, A.小球的机械能守恒 B.重力对小球不做功 C.绳的张力对小球不做功 D.在任何一段时间内,小球克服摩擦力所做的功总是等于小球动能的减少 5、如图所示,站在汽车上的人用手向前推车的力为F,脚对车向后的静摩擦力为f,下列说法正确 的是B A. 当车匀速运动时,F和f对车做功的代数和为正功 B. 当车加速运动时,F和f对车做功的代数和为负功 C. 当车减速运动时,F和f对车做功的代数和为负功 D. 不管车做何种运动,F和f对车做的总功和总功率都为零 F f O
九年级英语一模试卷 (满分:120分时间:120分钟) 注意事项: 1.本试卷共分两部分,第Ⅰ卷为选择题,第Ⅱ卷为非选择题。 2.所有试题的答案均填写在答题卡上,答案写在试卷上无效。 第Ⅰ卷选择题(共60分) 一、单项选择(15分) 1. ---What do you think of ________ film “ The Avengers 2《复仇者联盟2》”? ---Wonderful. I’ve never seen ________ more exciting one. A. a; the B. a; a C. the, / D. the; a 2. ---What’s the most important morning news on CCTV-1 today? ---The Prime Minister(总理)of India, Modi visited the Terra-Cotta Warriors(兵马俑) in Xi’an and said the wonderful works of art ___________ him a lot. A. expressed B. impressed C. explained D. complained 3.---How was your May Day holiday? ---Just so so. We drove to Hangzhou and tried to find a place for parking, but they were all ___. A. given up B. stayed up C. put up D. taken up 4. Since the terrible earthquake happened in Nepal last month, __________ people there have become homeless and helpless. A. a great deal of B. more than eight thousands C. thousand of D. plenty of 5. Last month, we went to Li Zongsheng’s concert. The beautiful songs about his
江苏省泰兴中学2017-2018学年高二语文阶段性检测 一、语言运用题(15分) 二、1.在下面一段话空缺处依次填人词语,最恰当的一组是(3分) 场内遗留了不少造船厂房及机器设备,作为文物,它们都被认为;作为废铁,它们论吨计价;作为景观,他们往往与现代普通人的审美期望相去甚远,大多。但是我们从中仍感悟到工业“设计”的力量。可以肯定,在当年的机器制造行业中,甚至连“在可能的条件下美观”这样的指导条例肯定也。 A.毫无价值不堪入目不会存在 B.不名一文惨不忍睹不会存在 C.不名一文不堪入目不复存在 D.毫无价值惨不忍睹不复存在 2.下列各句中,没有语病的一项是(3分) A.2013年国庆节,全国各旅游景区游客人数和旅游总收入同比增长至5.2%和4%;但集中出游人满为患,引发了人们对假期安排的讨论。 B.“世界读书日”前夕,中国新闻出版研究院的调查结果显示,国民人均阅读量明显不足,图书行业的出版和消费呈现出不对称发展的态势。 C.专家指出,针对“山西地震谣言”事件,国家必须加快相关立法进程和打击力度,来有效遏制网络散播流言这一现象。 D.因不符合券商上市的新规定,目前,这家证券公司的上市申报材料已经被退回,其多年来上市的夙愿变得遥遥无期。 3.下列四个选项中,前后加点实词解释相同的一项是(3分) A.生孩九月,慈父见.背思垂空文以自见. B. 至激于义理者不然.然.自后余多在外,不长居 C. 一日,大母过.余曰于是乘其车,揭其剑,过.其友 D. 而用.流俗人之言用.之所趋异也 4.下列四个选项中,前后加点字用法相同的一项是(3分) A.且勇者不必死.节思垂.空文以自见 B. 太史公牛马 ..走再拜言吾妻死之年所手.植也 C. 客逾庖而宴.猥以微贱 ..,当侍东宫 D. 无以终.余年韩非囚.秦,《说难》《孤愤》 5.在下面一段文字横线处填人语句,衔接最恰当的一项是(3分) 红星小学门卫王然被区教育局评为“十大感动校园人物”,他的事迹中最突出的一条是认识全
2018-2019学年江苏省泰州市泰兴市八年级(上) 期末语文试卷 一、积累运用(24分) 1.(4分)根据拼音在田字格内写出相应的汉字。 走进古银杏森林公园,迎面是一座wéi妙wéi 肖的银杏仙子像,放眼望去,几 百棵银杏树俯仰生zī,抬头,只见枝条旁yì斜出,似在交头jiē耳。【注:wéi只写一个字】 2.(2分)下列句子标点符号使用不正确 ...的一项是() A.缅桂花即白兰花,北京叫作“把儿兰”(这个名字真不好听)。 B.做隧道的时候,泥土搬到哪里去了呢?为什么墙壁不会塌下来呢? C.牛肝菌色如牛肝,滑,嫩,鲜,香,很好吃。 D.《孟子二章》选自《孟子?公孙丑下》。 3.(2分)下列加点的成语使用没有错误 ....的一项是() A.快节奏的歌曲固然可以让人身心愉快,但时间一久,听众就觉得眼花缭乱....。 B.前几天天降大雾,走在马路上,几米外的电线杆也杳无消息....。 C.《舌尖上的中国》将中国饮食文化讲述得栩栩如生 ....。 D.泰兴市政府决定将政策、资源精准到户到人,因地制宜....、对症下药,力争消除贫困。4.(2分)下列说法错误..的一项是() A.“他从不和别人吵一句嘴。”这个句子的主干应为:他不吵嘴。 B.意思相同的句子即使语气不同,但产生的表达效果相同。 C.律诗是近体诗的一种,要求诗句字数整齐划一,有四联。一般说来,颔联、颈联的上下 句应是对仗句。偶句押韵,首句可押可不押。 D.“他酒没沾唇,心早就热了。”这句话运用了夸张的修辞手法。 5.(8分)默写 (1)所以动心忍性,。 (2),烟波江上使人愁。 (3),悠然见南山。 (4)它没有婆娑的姿态,。 (5)《春望》这首诗中表达了诗人于连绵战火中期待家人消息的焦急心情的诗句是,。 (6)晏殊在《浣溪沙》中,用“,”两句抒发了惋惜与欣慰的情感,更蕴 含着某种生活哲理。
泰兴的民间习俗 摘要:我的家乡泰兴,地处长江三角洲,位于江苏省苏中平原南部,是国务院最早批准的沿江开放城市之一、长江走廊上一座新兴的滨江工贸城市,自然也就有一些自己特有的习俗和风情。 关键词:泰兴,银杏之乡,黄桥烧饼,斋孤,泰兴花鼓 正文: 我的家乡泰兴有很多民间习俗,每个习俗都充分体现了泰兴人的质朴、乐观以及风土人情,下面就选几个泰兴特有的风俗介绍给大家,和大家分享一下。 一、银杏之乡 泰兴土壤肥沃,雨量充沛,四季分明,物产丰富,是银杏生产的最佳地带,素有“银杏之乡”的美称,1996年国务院发展研究中心授予泰兴市“中国银杏之乡”称号,2000年被国家林业局命名为首批“中国名特优经济林银杏之乡”。泰兴银杏以产量高,品质好而闻名中外,全市共定植银杏451.2万株,其中挂果树29.81万株,银杏常年产量在3000吨左右,占全国总产量的三分之一以上。而且泰兴的白果在昆明世博会上唯一被指定为无公害白果,享有永久冠名权。 历史:在中国,有文字记载的栽培、食用历史已有3000 多年了。因其果实为核果状,外皮剥净后呈白色,故名“白果”;宋代,白果
曾被列为贡品,皇帝尝后备加赞扬,赐它美名:银杏;银杏树生长缓慢,寿命极长,有“公植树孙得食”的说法,故又有“公孙果”之称。 品种:泰兴银杏的主要品种是“大佛指”。 成份:据测定,100克银杏核仁中含:淀粉62.4克,蛋白质11.56克,脂肪2.6克,糖粉6.3克,纤维素1.2克,矿物质3克。 特点:银杏,属于银杏科,落叶乔木,叶扇形,雌雄异株,果核为椭圆形或倒卵形,是一种子遗植物。外果皮为黄色肉质,有浆汁;中果皮为光滑的白色硬核;内果皮为杏黄色薄膜紧裹的绿色核仁,核皮薄而坚硬。 功效:中医常以银杏核仁入药,有止咳平喘、滋养补肾的功能,用于肺病咳嗽,老人体虚哮喘。《本草纲目》中说,银杏“熟食温肺益气,定喘嗽,缩小便,止白虫;生食降痰,消毒杀虫。” 另外值得一提的是,银杏核仁中含有一种白色结晶体,有小毒。《本草纲目》中提到:“然食多则收令太过,令人气壅胪胀昏顿”。《三元延寿书》中也有记载,有些人饿了,以白果代饭饱食,第二天便中毒死去,所以,银杏不可多吃,尤其不可生食过多。 二、黄桥烧饼 江苏泰兴黄桥镇有一种烧饼,叫作黄桥烧饼。这种烧饼是用油酥和面,而且还有馅,馅是用火腿或猪油等做成。烧饼在缸炉里一烤,酥脆焦黄,香喷喷,非常可口,这种烧饼只有这一个地方有,那就是泰兴。 黄桥烧饼,或咸或甜,咸的以肉丁、肉松、火腿、虾米、香料等
江苏省泰兴中学高二化学(选修)阶段性检测 (考试时间:100分钟总分:120分) 可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 第Ⅰ卷(选择题共40分) 选项符合题单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个 .... 意。 1.下列物质均可用作燃料,其中最环保的是 A.甲醇 B.天然气 C.液化石油气 D.氢气 2.合成氨反应:3H2+N2=2NH3其反应速率可以分别用v(H2)、v(N2)、v(NH3)[单位均为mol/(L·s)]表示,则正确的关系是 A.v(H2)=v(N2)=v(NH3)B.v(H2)=错误!未找到引用源。v (NH3) C.v(N2)=2v(NH3)D.v(N2)=3v(H2) 3.25℃时,将0.1mol·L—1氨水溶液加水稀释,下列数值变大的是 A.c(OH—)B.pH C.c(NH4+)/c(NH3·H2O)D.c (H+)·c(OH—) 4.在一定条件下发生反应:A(g)+B(g)xC(g)+D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V D=0.2mol/(L·min),下列说法正确的是 A.A和B的转化率均是20% B.x = 4 C.平衡时A的物质的量为3.2mol D.平衡时气体压强比原来减小 5.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢
板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不.正确的是() A.水既是氧化剂又是溶剂B.放电时OH—向正极移动 C.放电时正极上有氢气生成D.总反应为:2Li+2H2O===2LiOH+H2↑6.向0.1 mol·L?1 CH3COOH溶液中加入少量CH3COONa晶体或加水稀释时,都会引起A.溶液的pH增大B.CH3COOH的电离程度增大 C.溶液的导电能力减小 D.溶液中n(H+)减小 7.反应3Fe(s)+4H 2O(g)Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是 A.容器内压强不再改变B.v(H2O)=v(H2) C.气体的密度不再改变D.反应不再进行 8.下列反应均为吸热反应,其中一定不能自发进行的是 A.2CO(g)=2C(s)+O2(g)B.2N2O5(g)=4NO2(g)+O2(g)C.MgCO3(s)=MgO(s)+CO2(g)D.(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) 9.水的电离过程为H2O H++OH—,在不同温度下其平衡常数为K(25℃)=1.0×10—14, K(35℃)=2.1×10—14。则下列叙述正确的是 A.C(H+)随着温度升高而降低B.35℃时,c(H+)>c(OH—) C.25℃时,PH=3的盐酸中由水电离产生的H+浓度为1.0×10—3mol·L-1 D.35℃时,向溶液中加入稀氨水,平衡逆向移动,c(OH―)增大,K w不变10.下列关于热化学反应的描述中正确的是
2020年江苏省泰州市泰兴市事业单位招聘考试《行政能力测试》真题及答 案 一、选择题(在下列每题四个选项中选择符合题意的,将其选出并把它的标号写在题后的括号内。错选、多选或未选均不得分。) 1、经济基础对上层建筑的决定作用表现在()。 A、经济基础决定上层建筑的产生 B、经济基础可以独立存在 C、经济基础决定上层建筑的性质 D、经济基础决定上层建筑的变化 【答案】ACD 【解析】经济基础对上层建筑的决定作用主要表现在以下几个方面:(1)经济基础决定上层建筑的产生和上层建筑的性质。经济基础的性质决定上层建筑的性质,有什么样的经济基础,就必然有什么样的上层建筑与之相适应。(2)经济基础的变化决定上层建筑的变化。当某一社会的经济基础发生某些局部变化时,被其决定的上层建筑也要相应地发生局部变化;而当经济基础发生根本变革,即旧经济基础被新经济基础代替时,旧的上层建筑也必然被新的上层建筑所代替。 2、“大鹏之动,非一羽之轻也;骐骥之速,非一足之力也。”这句话体现的哲理是()。 A、共性与个性的关系 B、整体与部分关系原理 C、对立与统一的原理 D、内外因关系原理 【答案】B 【解析】“大鹏之动,非一羽之轻也;骐骥之速,非一足之力也。”说明要正确处理整体和部分的辩证关系,要着眼于整体。故选B。 3、公文的真实性指的是()。 A、事实上的真实与方针政策上的真实 B、事实上的真实与语言上的虚构 C、方针政策上的真实与格式上的约定俗成 D、语言上的虚构与格式上的约定俗成 【答案】A 【解析】公文的真实性要求的是事实上的真实与方针政策上的真实,这是公文写作的一大特点。故选A。 4、市水利局向市财政局请求增拨水利建设经费应用的文种是()。 A、请示
2019届江苏泰兴市九年级第二次模拟考试语文试卷 【含答案及解析】 姓名___________ 班级____________ 分数__________ 一、书写 1. 根据下面语段中的拼音写出相应的汉字。 三月时节,落英缤纷,fēi红色的花瓣飘落在轻轻晕开的波纹上,敲击出美妙的乐音,只有清风听到。不远处,在熙来rǎng往的人潮里,形形色色的陌生人接zhǒng而来,擦肩 而过。 请写出“熙”的第七笔的笔画名称________________________ 二、选择题 2. 下列标点使用有错误的一项是(___________ ) A.祖父栽花,我就栽花;祖父拔草,我就拔草。 B.中国睡眠研究会把今年“3 .21”世界睡眠日中国主题确定为“健康心理良好睡眠”。 C.茅盾是当之无愧的大家,该书以《子夜》为题也是别有深意的。 D.好久之后,父亲又像问自己又像是问我:这人是怎么了? 3. 下列成语使用有错误的一项是(_________ ) A.周末来到泰兴鼓楼商业区,虽只是浮光掠影地看看,但那里的变化,却给我留下了 极深刻的印象。 B.治理雾霾,政府当务之急是迅速采取节能减排措施,引导公众养成低碳生活习惯。 C.近期,微信朋友圈中流行的一篇文章《素颜泰兴》,言简意赅地介绍了泰兴的众多 美食。 D.你怎么能对老师苦口婆心的劝导充耳不闻呢?
三、名句名篇 4. 根据提示补写名句或填写课文原句。 ( 1 )安不忘危,____________________ (2) ____________________ ,多易必多难。 ( 3 ) ____________________,见端以知末。 (4)此中有真意,____________________。 ( 5 ) ________________,不求闻达于诸侯。 ( 6 )春天像健壮的青年,___________________________________ ,领着我们上前去。 (7)《茅屋为秋风所破歌》中,表达了诗人舍己为人、至死不渝的句子 是:, 。 四、文学作品阅读 5. 名著阅读: 1. 上边是两幅名著的插图,请认真 读图,按要求填空。 a.插图A是《水浒传》中的一幕场景,图中_________________________________ (人名)正踏着雪,迎着北风,飞也似的向______________________________ 奔去。 b.插图B中手持铁锹的人是名著《》中的主人公 ______________________________ (人名)。 2. 下列关于文学名著内容及常识的表述,不完全正确的一项是() A.《格列佛游记》是江奈生· 斯威夫特的一部杰出的游记体讽刺小说,以格列佛的 口气叙述周游四国的经历。通过格列佛在利立浦特、布罗卜丁奈格、飞岛国、慧骃国的奇遇,反映了18世纪前半期英国统治阶级的腐败和罪恶。 B.《朝花夕拾》中提到,《二十四孝图》中最使鲁迅先生不解甚至反感的是“老莱娱亲”
江苏省泰兴中学高一数学教学案(134) 必修 2 空间几何体的表面积(一) 班级 姓名 目标要求 1、 了解多面体的平面展开图; 2、 理解并掌握直棱柱、正棱柱的概念和侧面积公式; 3、 理解并掌握正棱锥、正棱台的概念和侧面积公式; 4、 领悟正棱柱、正棱锥、正棱台的侧面积公式之间的关系. 重点难点 重点:正棱柱、正棱锥、正棱台的概念和侧面积公式; 难点:正棱柱、正棱锥、正棱台的概念和侧面展开图. 典例剖析 例1、(1) 判断下列命题是否正确: ①侧棱长相等的三棱锥是正三棱锥 ( ) ②有两个侧面垂直于底面的棱柱是直棱柱 ( ) ③底面是正三角形,且侧棱长相等的三棱锥是正三棱锥 ( ) ④有两个相邻侧面垂直于底面的棱柱是直棱柱 ( ) (2)设集合{},{},{}A B C ===直四棱柱正四棱柱长方体, 则,,A B C 之间的包含关系是 . (3)侧面为直角三角形的正三棱锥, 侧面与底面所成角为θ, 则cos θ= . 例2、(1)正四棱柱1111ABCD A B C D -的底面边长为对角线1AC 长为13,则此正四棱柱的侧面积为 . (2)正三棱台上、下底面面积之比为1:9, 上底边长为a , 侧棱与底面成0 60, 它的全面积是 . 例3、如图,长方体交于点A 的三条棱长分别为 D C B A
A B C P N M 14,3,5AD AA AB ===, 则从点A 沿表面到1C 的最短距离为多少? 例4、已知正三棱锥P —ABC 的侧棱长为1,∠APB=40°,N 、N 分别是棱PB 、PC 上的点,求ΔAMN 的周长的最小值。 学习反思 1、简单的多面体可以沿多面体的某些棱将它剪开而成平面图形,这个平面图形叫做该多面体的 . 2、侧棱与底面垂直的棱柱叫做 ,直棱柱的侧面展开图是 ,S 直棱柱侧= . 3、如果一个棱锥的底面是 ,并且顶点在底面内的正投影是 ,这样的棱锥为 ,正棱锥的侧棱长都 , S 正棱锥侧= . 4、正棱锥被 于底面的平面所截, 之间的部分叫做正棱台,S 正棱台侧= . 5、正棱柱、正棱锥、正棱台的侧面积公式之间的关系可以图示为 6、长方体的长、宽、高分别为 ,,a b c ,则其对角线长为 . 课堂练习 1、底面边长为10,高为5的正四棱锥的侧面积是 . 2、一个正三棱锥的侧面展开图的顶角为平角,侧面积为