
常见缩略语集
1、药物临床试验英文缩写 (2)
2、血尿检查英文缩写 (7)
3、实验室英文缩写 (10)
更新日期:2017年1月20日
1 / 13
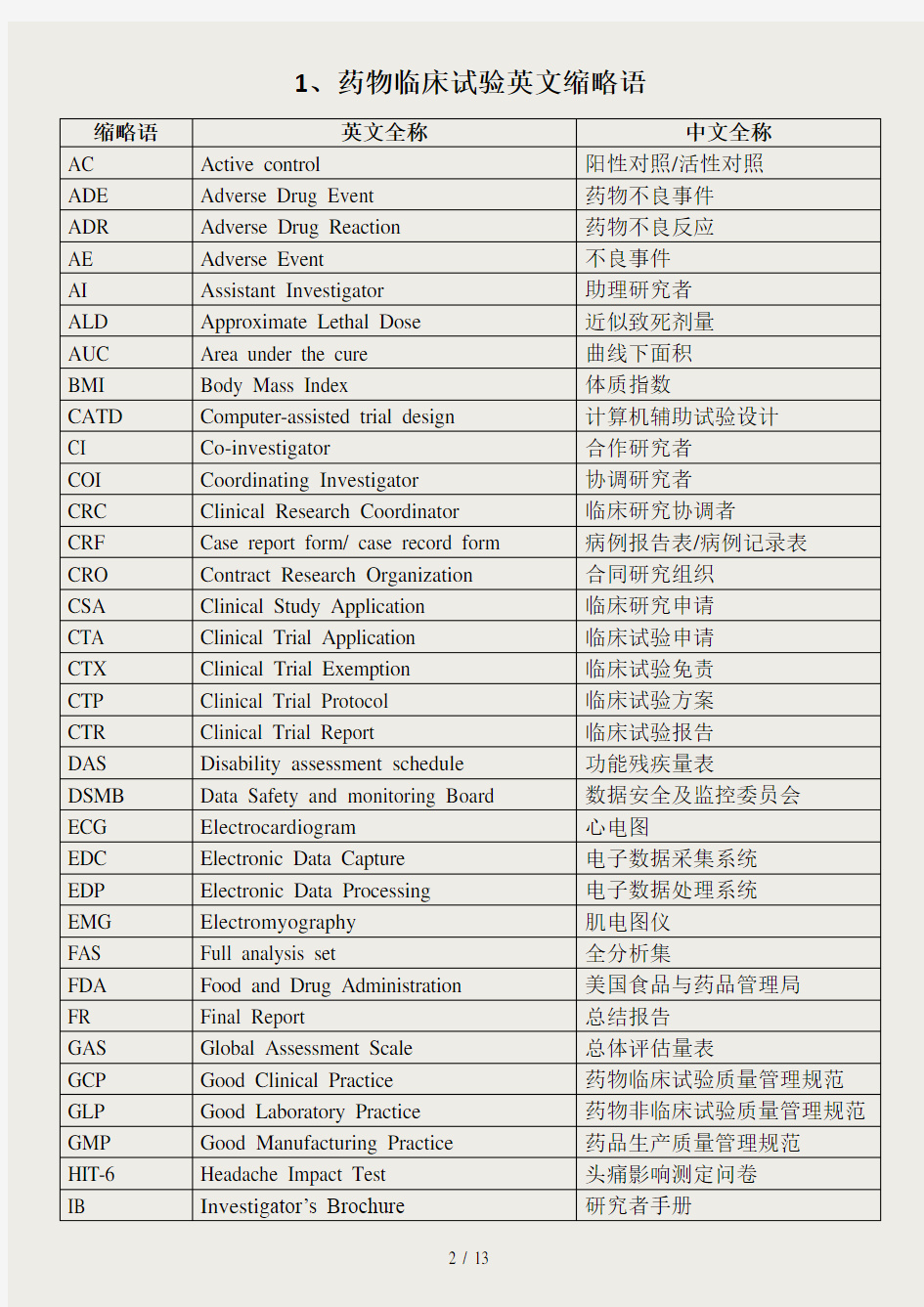
1、药物临床试验英文缩略语
缩略语英文全称中文全称
AC Active control 阳性对照/活性对照
ADE Adverse Drug Event 药物不良事件
ADR Adverse Drug Reaction 药物不良反应
AE Adverse Event 不良事件
AI Assistant Investigator 助理研究者
ALD Approximate Lethal Dose 近似致死剂量
AUC Area under the cure 曲线下面积
BMI Body Mass Index 体质指数
CATD Computer-assisted trial design 计算机辅助试验设计
CI Co-investigator 合作研究者
COI Coordinating Investigator 协调研究者
CRC Clinical Research Coordinator 临床研究协调者
CRF Case report form/ case record form 病例报告表/病例记录表CRO Contract Research Organization 合同研究组织
CSA Clinical Study Application 临床研究申请
CTA Clinical Trial Application 临床试验申请
CTX Clinical Trial Exemption 临床试验免责
CTP Clinical Trial Protocol 临床试验方案
CTR Clinical Trial Report 临床试验报告
DAS Disability assessment schedule 功能残疾量表
DSMB Data Safety and monitoring Board 数据安全及监控委员会
ECG Electrocardiogram 心电图
EDC Electronic Data Capture 电子数据采集系统
EDP Electronic Data Processing 电子数据处理系统
EMG Electromyography 肌电图仪
FAS Full analysis set 全分析集
FDA Food and Drug Administration 美国食品与药品管理局
FR Final Report 总结报告
GAS Global Assessment Scale 总体评估量表
GCP Good Clinical Practice 药物临床试验质量管理规范GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范
HIT-6 Headache Impact Test 头痛影响测定问卷
IB Investi gator’s Brochure研究者手册
2 / 13
IBR Institution review board 机构审查委员会
IC Informed Consent 知情同意
ICF Informed Consent Form 知情同意书
ICH International Conference on Harmonization 国际协调会议
IDM Independent Data Monitoring 独立数据监察
IDMC Independent Data Monitoring Committee 独立数据监察委员会
IEC Independent Ethics Committee 独立伦理委员会
IND Investigational New Drug 新药临床研究
IRB Institutional Review Board 机构审查委员会
ITT Intention-to-treat 意向性分析(统计学)
IVD In Vitro Diagnostic 体外诊断
IVRS Interactive V oice Response System 互动语音应答系统
IWRS interactive web response system 交互式网络响应系统
MA Marketing Approval/Authorization 上市许可证
MCA Medicines Control Agency 英国药品监督局
MHW Ministry of Health and Welfare 日本卫生福利部
MIDAS Migraine Disability Assessment 偏头痛残疾程度评估问卷MSQ Migraine-Specific Quality of Life questionnaire 偏头痛特异性生活质量问卷NDA New Drug Application 新药申请
NEC New Drug Entity 新化学实体
NIH National Institutes of Health 国家卫生研究所(美国)PI Principal Investigator 主要研究者
PL Product License 产品许可证
PMA Pre-market Approval (Application) 上市前许可(申请)
PP Per Protocol 符合方案集
PSI Statisticians in the Pharmaceutical Industry 制药业统计学家协会
QA Quality Assurance 质量保证
QC Quality Control 质量控制
RA Regulatory Authorities 监督管理部门
SA Site Assessment 现场评估
SAE Serious Adverse Event 严重不良事件
SAP Statistical Analysis Plan 统计分析计划
SAR Serious Adverse Reaction 严重不良反应
SD Source Data/Document 原始数据/文件
SD Subject Diary 受试者日记
SFDA State Food and Drug Administration 国家食品药品监督管理局
3 / 13
SDV Source Data Verification 原始数据核准
SEL Subject Enrollment Log 受试者入选表
SI Sub-investigator 助理研究者
SI Sponsor-Investigator 申办研究者
SIC Subject Identification Code 受试者识别代码
SIGN Scottish Intercollegiate Guidelines Network 苏格兰会际指南网络标准SOP Standard Operating Procedure 标准操作规程
SPL Study Personnel List 研究人员名单
SS Safety Analysis Set 安全分析集
SSL Subject Screening Log 受试者筛选表
T&R Test and Reference Product 受试和参比试剂
UAE Unexpected Adverse Event 预料外不良事件
ULN Upper Limit Normal 正常值上限
WHO World Health Organization 世界卫生组织
WHO-ICDRA WHO International Conference of
Drug Regulatory Authorities
WHO国际药品管理当局会议
无缩略语
A Approval 批准
Audit or inspection 稽查/视察Audit report 稽查报告Auditor 稽查员
B Bias 偏性/偏倚Bioequivalence 生物等效应Blank control 空白对照Blind codes 编制盲底Blind review 盲态审核Blind review 盲态检查Blinding method 盲法Blinding/masking 盲法/设盲
C Case history 病历Clinical equivalence 临床等效应Clinical study 临床研究Clinical trial 临床试验Co-investigator 合作研究者Comparison 对照Compliance 依从性
4 / 13
Composite variable 复合变量Consistency test 一致性检验Contract/ agreement 协议/合同Control group 对照组Coordinating committee 协调委员会
D Data management 数据管理Documentation 记录/文件Drop out 脱落
E Effectiveness 疗效
End point 终点Endpoint Criteria 终点指标Endpoint criteria/ measurement 终点指标Equivalence 等效性Essential Documentation 必需文件Ethics committee 伦理委员会Excellent 显效Exclusion criteria 排除标准
F Failure 无效/失败
Final point 终点
I Inclusion Criteria 入选表准Inclusion criteria 入选标准Information Gathering 信息收集Initial meeting 启动会议Inspection 检察/视察Institution inspection 机构检查Interim analysis 期中分析Investigational Product 试验药物Investigator 研究者
L Lost of follow up 失访
M Monitor 监察员Monitoring 监查Monitoring Plan 监察计划Monitoring Report 监察报告Multi-center Trial 多中心试验
N Non-clinical Study 非临床研究Non-inferiority 非劣效性
5 / 13
O Obedience 依从性Open-label 非盲Original medical record 原始医疗记录Outcome 结果Outcome Assessment 结果评价Outcome assessment 结果指标评价Outcome measurement 结果指标
P Patient file 病人档案Patient history 病历Placebo 安慰剂Placebo control 安慰剂对照Preclinical study 临床前研究Primary endpoint 主要终点Primary variable 主要变量Protocol 试验方案Protocol Amendments 修正案
Q Query list query form 应用疑问表R Randomization 随机
Reference Product 参比制剂
S Safety evaluation 安全性评价
Safety set 安全性评价的数据集Sample size 样本量样本大小Scale of ordered categorical ratings 有序分类指标Secondary variable 次要变量Sequence 试验次序
Simple Randomization 简单随机
Single blinding 单盲
Site audit 试验机构稽查Standard operating procedure 标准操作规程Sponsor 申办者
Sponsor-investigator 申办研究者
Study Audit 研究稽查
Study audit 研究稽查
Study Site 研究中心Subgroup 亚组
Sub-investigator 助理研究者
6 / 13
Subject 受试者
Subject 受试者
Subject diary 受试者日记Subject Enrollment 受试者入选Subject enrollment log 受试者入选表Subject Identification Code List 受试者识别代码表Subject Recruitment 受试者招募Subject screening log 受试者筛选表System audit 系统稽查System Audit 系统稽查
T Test Product 受试制剂Treatment group 试验组
Trial error 试验误差Trial Initial Meeting 试验启动会议Trial Master File 试验总档案Trial objective 试验目的Trial site 试验场所Triple blinding 三盲
Two one-side test 双单侧检验
U Un-blinding 揭盲
2、血尿检查英文缩略语
缩略语英文全称中文全称
血常规
AL allergy lymphocyte 变异淋巴细胞
BASO basophilic granulocyte 嗜碱性粒细胞
EOS eosimophil 嗜酸性粒细胞
GR granulocyte 粒性白细胞
HCT hematocrit 红细胞比积
HGB hemoglobin 血红蛋白
LYM lymphocyte 淋巴细胞
MCH mean corpusular hemoglobin 平均红细胞血红蛋白含量MCHC mean corpusular hemoglobin concerntration 平均红细胞血红蛋白浓度MCV mean corpusular volume 平均红细胞体积
MID mid-value 中值细胞
MONO monocytes 单核细胞总数
7 / 13
MPV mean platelet volume 平均血小板体积NEU neutrophilic granulocyte 中性粒细胞
PCT plateletocrit 血小板比积
PDW platelet distribution width 血小板分布宽度PLT/BPC platelet count/blood platelet count 血小板计数
RBC red blood cell 红细胞计数
RDW red blood cell volume distribution width 红细胞分布宽度WBC white blood cell 白细胞
血生化
α-HBD α-hydroxybutyric dehydrogenase α-羟丁酸脱氢酶a-AG a-acid glycoprotein a-酸性糖蛋白ALB albumin 白蛋白
ALP/AKP alkaline phosphatase 碱性磷酸酶
ALT alanine amiotransferase 丙氨酸氨基转移酶/谷丙转氨酶
AMY serum amylase 淀粉酶
ASO antistreptolysin 抗链球菌溶血素O
AST aspartate aminotransferase 门冬氨酸氨基转移酶/谷草转氨酶
BUN usea nitrogen 尿素氮
C3 complement C3 补体C3
C4 complement C4 补体C4
Ca serum calcium 钙
CHE cholinesterase 胆碱酯酶
CHOL cholesterol 胆固醇
CK creatine kinase 肌酸激酶
CK-MB creatine kinase-MB 肌酸激酶同工酶CRE、Cr creatinine 肌酐
CRP C- reactive protein C反应性蛋白
cTNT troponin T 肌钙蛋白T
DB/DBIL direct bilirubin 直接胆红素
γ-GT γ-glutamyl transpeptadase 谷氨酰转肽酶/转肽酶GLOB/GLO globulin 球蛋白
GLU glucose 血糖
GSP glycated serum prot 糖化血清蛋白
HDL-C high-density lipoprotein cholesterol 高密度脂蛋白
IBIL indirect bilirubin 游离胆红素
LDH lactate dehydrogenase 乳酸脱氢酶
LDL-C low-density lipoprotein cholesterol 低密度脂蛋白
8 / 13
IgA immunoglobin A 免疫球蛋白A IgG immunoglobin G 免疫球蛋白G IgM immunoglobin M 免疫球蛋白M IP inorganic phosphate 无机磷
Lp(a) lipoprotein(a)脂蛋白(a)Mg serum magnesium 镁
MTP mili-total protein 微量蛋白MYOG myoglobin 肌红蛋白
RF rheumatoid factor 类风湿因子
TB/TBIL total bilirubin 总胆红素
TBA total biliary acid 总胆汁酸
TG triglyceride 甘油三脂
TP total protein 总蛋白
UA/URIC uric acid 尿酸
UREA urea 尿素
VLDL very low-density lipoprotein 极低密度脂蛋白
尿常规
Addis count addis count 艾迪氏计数
BIL bilirubin 尿胆红素
BLD blood 隐血/潜血
BUN 尿素氮
GLU glucose 尿葡萄糖
HP high power objective 每高倍视野KET ketone 尿酮体
LEU leucocyte 尿白细胞
LP low power objective 每低倍视野NIT nitrite 亚硝酸盐
PH acidity 尿酸碱度
PRO protein 尿蛋白
OB occult blood test 大便隐血试验SG specific gravity 尿比重
URO/UBG urobilinogen 尿胆原
WBC white blood cell 白细胞
电解质
Na Sodium 钠
K kalium 钾
Cl chloride 氯
Ga calcium 钙
9 / 13
Mg magnesium 镁
体液常规
CSF cerebrospinal 脑积夜
Pandy pandy 庞氏试验
乙肝标志物
HBV hepatitis B virus 乙肝病毒
HBsAg hepatitis B surface antigen 乙肝表面抗原
HBsAb antibody to hepatitis surface antigen 乙肝表面抗体
HBcAg hepatitis B core antigen 乙肝核心抗原
HBcAb antibody to hepatitis B core antigen 乙肝核心抗体
HBeAg hepatitis B e-antigen 乙肝e抗原
HBeAb antibody to hepatitis B e-antigen 乙肝e抗体
ELISA enzymelinked immunosorbentassy 酶联免疫吸附试验HAV hepatitis A virus 甲肝病毒
HCV hepatitis C virus 丙肝病毒
输血免疫全套
HBV hepatitis B virus 乙型肝炎病毒
HCV hepatitis C virus 丙型肝炎病毒
TP treponema pallidum 梅毒螺旋体
HIV human immunodeficiency virus 人类免疫缺陷病毒
3、实验室英文缩略语
英文全称缩略语中文全称Accuracy 准确度
Alb 白蛋白
Alpha spending function 消耗函数
Analysis sets 统计分析的数据集
Attenuated Total Reflection ATR 衰减全反射法
AUCss 稳态血药浓度-时间曲线下面积Block 层
Block size 每段的长度
Carryover effect 延滞效应
Categorical variable 分类变量
Cav 平均浓度
circular dichroism CD 圆二色谱
10 / 13
clearance CL 清除率
Cmax 峰浓度
Confidence interval 可信区间
Confidence level 置信水平
Crossover design 交叉设计
Cross-over Study 交叉研究
Css 稳浓度
Cure 痊愈
Database 建立数据库
Descriptive statistical analysis 描述性统计分析
DF 波动系统
Dichotomies 二分类
Diviation 偏差
Dose-reaction relation 剂量-反应关系
Double dummy 双模拟
Double dummy technique 双盲双模拟技术Differential Scanning Calorimeter DSC 差示扫描热量计Emergency envelope 应急信件
Factorial design 析因设计
Fixed-dose procedure 固定剂量法
Forced titration 强制滴定
Full analysis set 全分析集
GC-FTIR 气相色谱-傅利叶红外联用GC-MS 气相色谱-质谱联用Generic drug 通用名药
Global assessment variable 全局评价变量
Group sequential design 成组序贯设计
Health economic evaluation HEV 健康经济学评价Hypothesis test 假设检验
Hypothesis testing 假设检验
Improvement 好转
Last observation carry forward LOCF 最接近一次观察的结转
LC-MS 液相色谱-质谱联用
Last observation carry forward LOCF 最近一次观察的结转
Logic check 逻辑检查
11 / 13
Limit of Quantization LOQ 定量限
Marketing approval/ authorization 上市许可证
Mass spectrum MS 质谱
Matched pair 匹配配对
Maximum Tolerated Dose MTD 最大耐受剂量
Mean residence time MRT 平均滞留时间Median lethal dose LD50 半数致死剂量Missing value 缺失值
Mixed effect model 混合效应模式
MS-MS 质谱-质谱联用
New chemical entity NCE 新化学实体
New drug application NDA 新药申请
Nuclear Magnetic Resonance Spectroscopy NMR 核磁共振谱
Non-parametric statistics 非参数统计方法Optical rotatory dispersion ORD 旋光光谱
Optional titration 随意滴定
Outlier 离群值
Parallel group design 平行组设计Parameter estimation 参数估计
Parametric statistics 参数统计方法Polytomies 多分类
Power 检验效能
Precision 精密度
Range check 范围检查
Rating scale 量表
Replication 可重复
Relative stadard deviation, RSD 日内和日间相对标准差Run in 准备期
Seriousness 严重性
Severity 严重程度
Severity 严重程度
Significant level 检验水准
Specificity 特异性
Standard curve 标准曲线
Statistic 统计量
12 / 13
Statistical analysis plan 统计分析计划Statistical model 统计模型Statistical tables 统计分析表Stratified 分层
Superiority 检验
Survival analysis 生存分析
SXRD 单晶X-射线衍射T1/2消除半衰期
Target variable 目标变量
TG 热重分析
TLC、HPLC 制备色谱
Tmax 峰时间
TP 总蛋白Transformation 变量变换
UV-VIS 紫外-可见吸收光谱Variability 变异
Variable 变量
Visual analogy scale 直观类比打分法Visual check 人工检查Vulnerable subject 弱势受试者
Wash-out 洗脱
Washout period 洗脱期
13 / 13
专业术语 缩略语英文全称中文全称 DCF data clarification form 数据澄清表,用于纸质query SDV source data verification 原始数据核对 ADE Adverse Drug Event药物不良事件 ADR Adverse Drug Reaction药物不良反应 AE Adverse Event不良事件 AI Assistant Investigator助理研究者 ? BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRAClinical Research Associate 临床监查员(临床监察员)CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表
CRO Contract Research Organization 合同研究组织CSAClinical Study Application 临床研究申请 CTAClinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMBData Safety and monitoring Board数据安全及监控委员会EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCPGood Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMPGood Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization国际协调会议
临床试验常见英文缩写 ADR(Adverse drug reaction)不良反应 AE(Adverse event)不良事件 SAE(Serious Adverse Event)严重不良事件 CRF(Case report form/case record form)病例报告表 CRO(Contract research organization)合同研究组织 EC(Ethics Committee)伦理委员会 GCP(Good clinical practice)药品临床试验管理规范 EDC(Electronic data capture)电子数据采集 IB(Investigator's Brochure)研究者手册 ND (Not Done) 未做 NA (Not Applicable) 不适用 UK (Unknown) 未知 PI(Principal investigator )主要研究者 Sub-I(Sub-investigator) 助理研究者 QA(Quality assurance) 质量保证 QC(Quality control) 质量控制 SDV(Source data verification)原始资料核对 SD(Source data)原始数据 SD(Source document ) 原始文件 SFDA 国家食品药品监督管理局 SOP(Standard operating procedure) 标准操作规程 IRB 机构审查委员会 ICF(Informed Consent Form) 知情同意书 TMF(trial master file)研究管理文件夹 临床试验常见英文单词 A ?Active control ,AC 阳性对照,活性对照阳性对照,活性对照?Adverse drug reaction ,ADR 药物不良反应药物不良反应?Adverse event ,AE 不良事件 ?Approval 批准 ?Assistant investigator 助理研究者 ?Audit 稽查 ?Audit report 稽查报告 ?Auditor 稽查员 B ?Bias 偏性,偏倚 ?Blank control 空白对照 ?Blinding/masking 盲法,设盲 ?Block 层 C ?Case history 病历 ?Case report form/case record form ,CRF 病例报告表,病例记录表?Clinical study 临床研究
药物临床试验英文缩写汇编
药物临床试验英文缩写号 1 ADE 药物不良事件Adverse Drug Event 2 ADR 药物不良反应Adverse Drug Reaction 3 AE 不良事件Adverse Event 4 AI 助理研究者Assistant Investigator 5 BMI 体质指数Body Mass Index 6 CI 合作研究者Co-investigato r 7 COI 协调研究者Coordinating Investigator
Research Organization 11 CSA 临床研究申请Clinical Study Application 12 CTA 临床试验申请Clinical Trial Application 13 CTX 临床试验免责Clinical Trial Exemption 14 CTP 临床试验方案Clinical Trial Protocol 15 CTR 临床试验报告Clinical Trial Report 16 DSM 数据安全及监控 Data Safety and
18 EDP 电子数据处理系 统Electronic Data Processing 19 FDA 美国食品与药品 管理局Food and Drug Administration 20 FR 总结报告Final Report 21 GCP药物临床试验质 量管理规范Good Clinical Practice 22 GLP 药物非临床试验 质量管理规范Good Laboratory Practice 23 GMP 药品生产质量管 理规范Good Manufacturing Practice
临床监查员专业术语、缩略语中英对照表 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员)CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization 国际协调会议 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统
专业术语 缩略语 英文全称 中文全称 数据澄清表,用于纸质 query 原始数据核对 DCF SDV data clarification form source data verification ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范 GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator's Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization 国际协调会议
药物临床试验英文缩写 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范GCP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on 国际协调会议 Harmonization IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统 MA Marketing Approval/Authorization 上市许可证 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请 NEC New Drug Entity 新化学实体
专业术语 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 ECRF 电子化病历报告表 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规 GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator's Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ECG Electrocardiogram 心电图 ICH International Conference on Harmonization 国际协调会 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 MA Marketing Approval/Authorization 上市许可证 IVRS Interactive Voice Response System 互动语音应答系统 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请 NEC New Drug Entity 新化学实体 NIH National Institutes of Health 国家卫生研究所(美国) PI Principal Investigator 主要研究者 PL Product License 产品许可证 PMA Pre-market Approval (Application ) 上市前许可(申请) PSI Statisticians in the Pharmaceutical Industry 制药业统计学家协会 QA Quality Assurance 质量保证 QC Quality Control 质量控制 RA Regulatory Authorities 监督管理部门 SA Site Assessment 现场评估 SAE Serious Adverse Event 严重不良事件 SAP Statistical Analysis Plan 统计分析计划 SAR Serious Adverse Reaction 严重不良反应 SD Source Data/Document 原始数据 /文件 SD Subject Diary 受试者日记 Subject identification code (SIC )受试者识别代码 SFDA State Food and Drug Administration 国家食品药品监督管理局 SDV Source Data Verification 原始数据核准 SEL Subject Enrollment Log 受试者入选表 SI Sub-investigator 助理研究者 SI Sponsor-Investigator 申办研究者 SIC Subject Identification Code 受试者识别代码 pd pharmacodynamics 药物效应动力学 SOP Standard 缩略语 英文全称 中文全称 ADE Adverse Drug Event 药物不良事件 AE Adverse Event 不良事件 BMI Body Mass Index 体质指数 COI Coordinating Investigator 协调研究者 ADR Adverse Drug Reaction 药物不良反应 AI Assistant Investigator 助理研究者 CI Co-investigator 合作研究者
专业术语 缩略语英文全称中文全称ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案CTR Clinical Trial Report 临床试验报告DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书
专业术语缩略语?英文全称?????????????????????????中文全称 DCFdataclarificationform数据澄清表,用于纸质query SDVsourcedataverification原始数据核对 ADE AdverseDrugEvent 药物不良事件 ADR AdverseDrugReaction 药物不良反应 AE AdverseEvent 不良事件 AI AssistantInvestigator 助理研究者 BMI BodyMassIndex 体质指数 CI Co-investigator 合作研究者 COI CoordinatingInvestigator 协调研究者 CRA ClinicalResearchAssociate 临床监查员(临床监察员) CRC ClinicalResearchCoordinator 临床研究协调者 CRF CaseReportForm 病历报告表 CRO ContractResearchOrganization 合同研究组织 CSA ClinicalStudyApplication 临床研究申请
CTA ClinicalTrialApplication 临床试验申请 CTX ClinicalTrialExemption 临床试验免责 CTP ClinicalTrialProtocol 临床试验方案 CTR ClinicalTrialReport 临床试验报告 DSMB DataSafetyandmonitoringBoard 数据安全及监控委员会EDC ElectronicDataCapture 电子数据采集系统 EDP ElectronicDataProcessing 电子数据处理系统 FDA FoodandDrugAdministration 美国食品与药品管理局 FR FinalReport 总结报告 GCP GoodClinicalPractice 药物临床试验质量管理规范GLP GoodLaboratoryPractice 药物非临床试验质量管理规范GMP GoodManufacturingPractice 药品生产质量管理规范 IB Investigator’sBroch ure 研究者手册 IC InformedConsent 知情同意 ICF InformedConsentForm 知情同意书 ICH InternationalConferenceonHarmonization 国际协调会议 IDM IndependentDataMonitoring 独立数据监察 IDMC IndependentDataMonitoringCommittee 独立数据监察委员会IEC IndependentEthicsCommittee 独立伦理委员会 IND InvestigationalNewDrug 新药临床研究
FDA Glossary: GCP,GLP,TRIAL Accuracy 准确度 Active control, AC 阳性对照,活性对照Adverse drug reaction, ADR 药物不良反应Adverse event, AE 不良事件 Adverse medical events 不良医学事件Adverse reaction 药物不良反应 Alb 白蛋白 ALD(Approximate Lethal Dose近似致死剂量ALP 碱性磷酸酶 Alpha spending function 消耗函数 ALT 丙氨酸氨基转换酶 Analysis sets 统计分析的数据集 Approval 批准 Assistant investigator 助理研究者 AST 天门冬酸氨基转换酶 ATR 衰减全反射法 AUCss 稳态血药浓度-时间曲线下面积 Audit 稽查 Audit or inspection 稽查/视察 Audit report 稽查报告 Auditor 稽查员
Bias 偏性,偏倚 Bioequivalence 生物等效应 Blank control 空白对照 Blind codes 编制盲底 Blind review 盲态审核 Blind review 盲态检查 Blinding method 盲法 Blinding/ masking 盲法,设盲 Block 分段 Block 层 Block size 每段的长度 BUN 尿素氮 Carryover effect 延滞效应 Case history 病历 Case report form 病例报告表 Case report form/ case record form, CRF 病例报告表,病例记录表Categorical variable 分类变量 Cav 平均浓度 CD 圆二色谱
专业术语缩略语?英文全称?????????????????????中文全称 DCFdataclarificationform 数据澄清表,用于纸质query SDVsourcedataverification 原始数据核对 ADE AdverseDrugEve nt 药物不良事件 ADR AdverseDrugReaction 药物不良反应 AE AdverseEve nt 不良事件 AI Assista ntl nvestigator 助理研究者 BMI BodyMassI ndex 体质指数 CI Co-i nvestigator 合作研究者 COI Coordi nat in gI nv estigator 协调研究者 CRA Cli ni calResearchAssociate 临床监查员(临床监察员) CRC Cli ni calResearchCoordi nator 临床研究协调者 CRF CaseReportForm 病历报告表 CRO Con tractResearchOrga nization 合同研究组织 CSA Cli ni calStudyApplicatio n 临床研究申请
CTX Cli ni calTrialExemption 临床试验免责 CTP Cli ni calTrialProtocol 临床试验方案 CTR Cli ni calTrialReport 临床试验报告 DSMB DataSafetya ndmo nitori ngBoard 数据安全及监控委员会EDC Electro nicDataCapture 电子数据采集系统 EDP Electro nicDataProcessi ng 电子数据处理系统 FDA Fooda ndDrugAdmi nistratio n 美国食品与药品管理局 FR Fin alReport 总结报告 GCP GoodCli ni calPractice 药物临床试验质量管理规范 GLP GoodLaboratoryPractice 药物非临床试验质量管理规范GMP GoodMa nufactur in gPractice 药品生产质量管理规范 IB Investigator ' sB r och 研究者手册 IC In formedCo nse nt 知情同意 ICF In formedCo nse ntForm 知情同意书 ICH In ternatio nalC onferenceonH arm on izatio n 国际协调会议IDM In depe nden tDataMo nitori ng 独立数据监察 IDMC In depe nde ntDataMo ni tori ngCommittee 独立数据监察委员会 IEC In depe nde ntEthicsCommittee 独立伦理委员会
GMP常见英文缩写 AQAI(Automated Quality Assurance Inspection Equipment):在线自动质量保证检查设备API(Active Pharmaceutical Ingredient):活性药物物质,即原料药 ANDA (Abbreviated New Drug Application):简化新药申请 ADR(Adverse Drug Reaction):不良反应 BSE(Bovine Spongiform Encephalopathy):疯牛病 BPCS(Business Planning and Control System):业务计划及控制系统 BIA(Business impact assessment): 商业影响评估 cGMP(current Good Manufacturing Practice):现行药品生产质量管理规范 CCCD(China Certification Committee for Drugs):中国药品认证委员会 CIP(Cleaning In Place):在线清洁 CV(Concurrent Validation):同步验证 CDER( Center for Drug Evaluation and Research): 药品研究与评价中心 COA(Certificate Of Analysis):分析报告单 CFR(Code of Federal Regulation):(美国)联邦法规 CDC(Centers for Disease Control and Prevention):疾病预防控制中心 COS/ CEP( Certificate of Suitability for European Pharmacopeia ):欧洲药典适用性证书CCD (Certification Committee for Drugs):药品认证管理中心 CPMP(Committee for Proprietary Medicinal Products): 欧洲专利药品委员会 CTD(Common Technical Document):通用技术文件 CDC( Centers for Disease Control and Prevention): 疾病预防控制中心 GMP(Good Manufacturing Practice):药品生产质量管理规范 ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use):人用药品注册技术要求国际协调会
临床试验常用的英文缩 写 Document number:NOCG-YUNOO-BUYTT-UU986-1986UT
专业术语 缩略语英文全称中文全称 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator助理研究者 ? BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRAClinical Research Associate 临床监查员(临床监察员)CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织CSAClinical Study Application 临床研究申请 CTAClinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责
CTP Clinical Trial Protocol 临床试验方案 CTR Clinical Trial Report 临床试验报告 DSMBData Safety and monitoring Board数据安全及监控委员会EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局 FR Final Report 总结报告 GCPGood Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMPGood Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure 研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书 ICH International Conference on Harmonization国际协调会议 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee独立数据监察委员会IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究
FDA Glossary: GCP,GLP,TRIAL Accuracy 准确度 Active control, AC 阳性对照,活性对照Adverse drug reaction, ADR 药物不良反应Adverse event, AE 不良事件 Adverse medical events 不良医学事件Adverse reaction 药物不良反应 Alb 白蛋白 ALD(Approximate Lethal Dose)近似致死剂量ALP 碱性磷酸酶 Alpha spending function 消耗函数 ALT 丙氨酸氨基转换酶 Analysis sets 统计分析的数据集 Approval 批准 Assistant investigator 助理研究者 AST 天门冬酸氨基转换酶 ATR 衰减全反射法 AUCss 稳态血药浓度-时间曲线下面积 Audit 稽查 Audit or inspection 稽查/视察 Audit report 稽查报告
Auditor 稽查员 Bias 偏性,偏倚 Bioequivalence 生物等效应 Blank control 空白对照 Blind codes 编制盲底 Blind review 盲态审核 Blind review 盲态检查 Blinding method 盲法 Blinding/ masking 盲法,设盲 Block 分段 Block 层 Block size 每段的长度 BUN 尿素氮 Carryover effect 延滞效应 Case history 病历 Case report form 病例报告表 Case report form/ case record form, CRF 病例报告表,病例记录表Categorical variable 分类变量 Cav 平均浓度 CD 圆二色谱
临床研究常用术语缩写表
SOP 类型缩写表 OP 操作规程Operating Procedures WI 工作指南Work Instructions TP 模板Template FM 批准的标准表格Approved Standard Forms OD 其他文件Other Documents 业务部门缩写表/ Functional Area Abbreviation Table: BS 生物统计Biostatistics BD 业务拓展Business Development CM 临床监查/运营Clinical Monitoring/Operation DM 数据管理Data Management IT 信息技术Information Technology MS 医学科学服务Medical Science Service PM 项目管理Project Management QA 质量保证Quality Assurance RM 记录管理Records Management RA 注册事务Regulatory Affairs SM SOP 管理SOP Management ST 研究中心管理服务Site Management Service TR 培训Training 试验主文档:(TMF)Trial Master File PMF 项目管理文件夹Project Management File CCF 申办方临床研究文件夹Central Clinical File CIF 申办方-研究者文件夹Central Investigator File ISF 研究者文件夹Investigator Site File BSF 生物统计学文件夹Biostatistics Study File DMSF 数据管理研究文件夹Data Management Study File
专业术语 缩略语英文全称中文全称DCF data clarification form 数据澄清表,用于纸质query SDV source data verification 原始数据核对 ADE Adverse Drug Event 药物不良事件 ADR Adverse Drug Reaction 药物不良反应 AE Adverse Event 不良事件 AI Assistant Investigator 助理研究者 BMI Body Mass Index 体质指数 CI Co-investigator 合作研究者 COI Coordinating Investigator 协调研究者 CRA Clinical Research Associate 临床监查员(临床监察员) CRC Clinical Research Coordinator 临床研究协调者 CRF Case Report Form 病历报告表 CRO Contract Research Organization 合同研究组织 CSA Clinical Study Application 临床研究申请 CTA Clinical Trial Application 临床试验申请 CTX Clinical Trial Exemption 临床试验免责 CTP Clinical Trial Protocol 临床试验方案CTR Clinical Trial Report 临床试验报告
DSMB Data Safety and monitoring Board 数据安全及监控委员会 EDC Electronic Data Capture 电子数据采集系统 EDP Electronic Data Processing 电子数据处理系统 FDA Food and Drug Administration 美国食品与药品管理局FR Final Report 总结报告 GCP Good Clinical Practice 药物临床试验质量管理规范 GLP Good Laboratory Practice 药物非临床试验质量管理规范GMP Good Manufacturing Practice 药品生产质量管理规范 IB Investigator’s Brochure研究者手册 IC Informed Consent 知情同意 ICF Informed Consent Form 知情同意书ICH International Conference on Harmonization 国际协调会议 IDM Independent Data Monitoring 独立数据监察 IDMC Independent Data Monitoring Committee 独立数据监察委员会 IEC Independent Ethics Committee 独立伦理委员会 IND Investigational New Drug 新药临床研究 IRB Institutional Review Board 机构审查委员会 IVD In Vitro Diagnostic 体外诊断 IVRS Interactive Voice Response System 互动语音应答系统 MA Marketing Approval/Authorization 上市许可证 MCA Medicines Control Agency 英国药品监督局 MHW Ministry of Health and Welfare 日本卫生福利部 NDA New Drug Application 新药申请