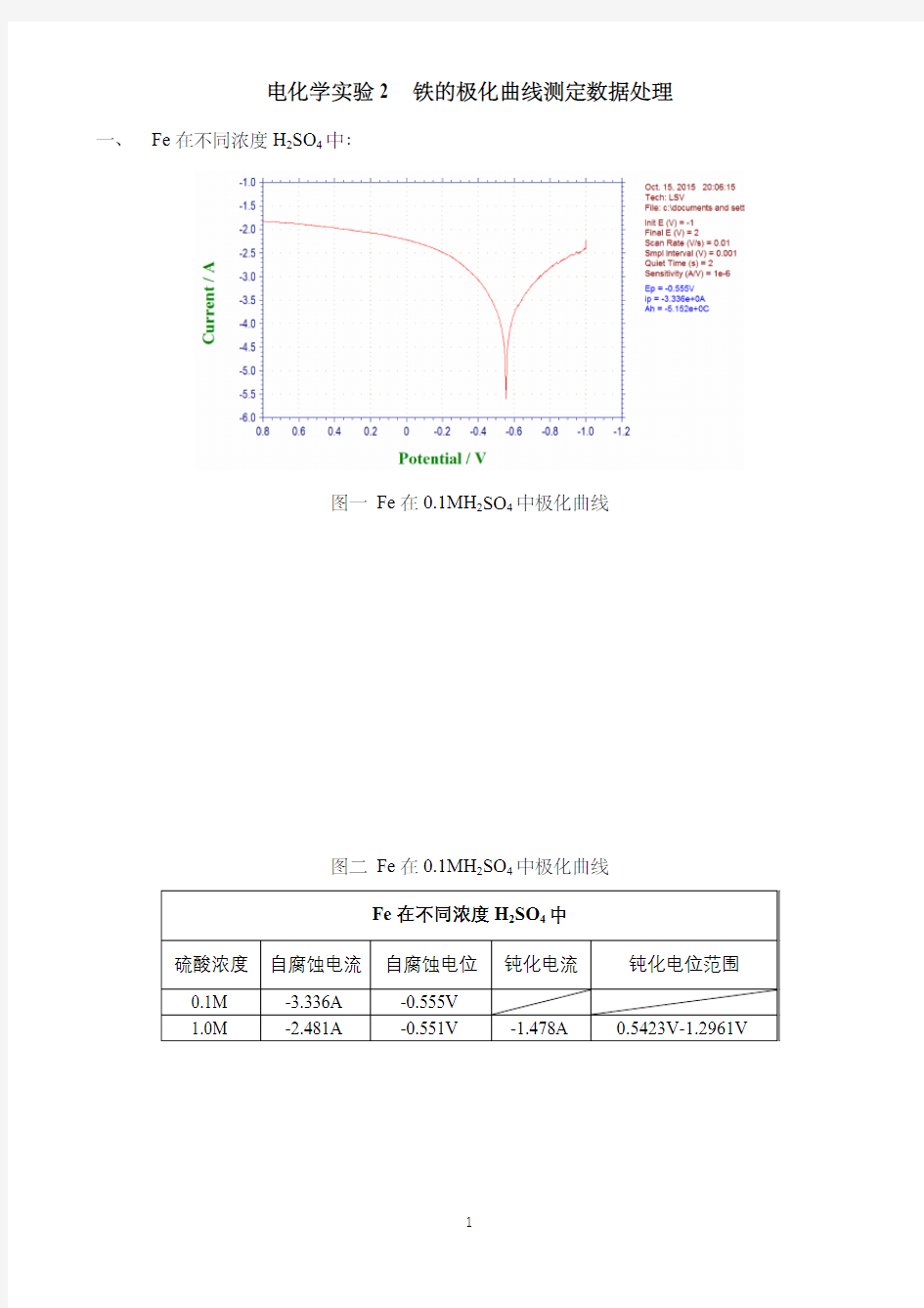

电化学实验2 铁的极化曲线测定数据处理?、Fe在不同浓度H2SO4中:
图?Fe在0.1MH2SO4中极化曲线
图?Fe在0.1MH2SO4中极化曲线
?、Fe在HCl及缓蚀剂中:
图三Fe在1M的HCl中极化曲线
图四Fe在1M的HCl中+1%乌洛托品极化曲线
已知:υ="#$$%&
'(
(*)
由图知:Fe在1M的HCl中,?腐蚀电流i1=-3.016A;
Fe在1M的HCl中+1%乌洛托品中,?腐蚀电流i2=-2.805A
所以:将i1、i2代?公式(*)得:
υ)=3600×/#×".$)#
1×2#34/=3.139g?m:1?h:);υ1=3600×/#×1.3$/
1×2#34/
=2.920g?m:1?h:)
结论:Fe在低浓度(0.1M )H2SO4中未钝化,在较?浓度(1M )H2SO4中钝化;腐蚀速率加?乌洛托品后下降,说明乌洛托品有缓释作?。
极化曲线 原理 1.在研究可逆电池的电动势和电池反应时电极上几乎没有电流通过,每个电极或电池反应都是在无限接近于平衡下进行的,因此电极反应是可逆的。当有电流通过电池时,则电极的平衡状态被破坏,此时电极反应处于不可逆状态,随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。在有电流通过电极时,由于电极反应的不可逆而使电极电位偏离平衡值的现象称作电极的极化。根据实验测出的数据来描述电流密度与电极电位之间关系的曲线称作极化曲线如图1所示。 金属的阳极过程是指金属作为阳极时,在一定的外电势下发生的阳极溶解过程,如下式所示: M→M n++ne - 此过程只有在电极电位大于其热力学电位时才能发生。阳极的溶解速度随电位变正而逐渐增大。这是正常的阳极溶出,但当阳极电位正到某一数值时,其溶解速度达到一最大值。此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。 曲线表明,电位从a 点开始上升(即电位向正方向移动),电流密度也随之增加,电位超过b 点以后,电流密度迅速减至很小,这是因为在金属表面上生成了一层电阻高、耐腐蚀的钝化膜。到达c 点以后,电位再继续上升,电流仍保图1金属极化曲线 ab 活性溶解区;b.临界钝化点;bc.过渡钝化区;cd.稳定钝化区;de.超(过)钝化区
持在一个基本不变的很小的数值上,电位升到d点时,电流又随电位的上升而增大。 2.影响金属钝化过程的几个因素 金属钝化现象已进行了大量的研究工作。影响金属钝化过程及钝化性质的因素,可归纳为以下几点: (1)溶液的组成。在中性溶液中,金属一般比较容易钝化,而在酸性或某些碱性的溶液中,则不易钝化;溶液中卤素离子(特别是Cl-)的存在,能明显地阻止金属的钝化;溶液中存在某些具有氧化性的阴离子(如CrO2-4)则可以促进金属的钝化。 (2)金属的化学组成和结构。各种纯金属的钝化能力不尽相同,例如铁、镍、铬三种金属的钝化能力为铬>镍>铁。因此,添加铬、镍可以提高钢铁的钝化能力及钝化的稳定性。 (3)外界因素(如温度、搅拌等)。一般来说,温度升高以及搅拌加剧,可以推迟或防止钝化过程的发生,这与离子扩散有关。 实验方法: 测量极化曲线有两种方法:控制电流法与控制电势法(也称恒电流法与恒电势法)。控制电势法是通过改变研究电极的电极电势,然后测量一系列对应于某一电势下的电流值。由于电极表面状态在未建立稳定状态前,电流会随时间改变,故一般测出的曲线为“暂态”极化曲线。 恒电位法:将研究电极上的电位维持在某一数值上,然后测量对应于该电位下的电流。由于电极表面状态在未建立稳定状态之前,电流会随时间而改变,故一般测出来的曲线为“暂态”极化曲线。在实际测量中,常采用的控制电位测量方法有下列两种。 (1)静态法:将电极电位较长时间地维持在某一恒定值,同时测量电流随时间的变化,直到电流值基本上达到某一稳定值。如此每隔20~50mV逐点地测量各个电极电位下的稳定电流值,即可获得完整的极化曲线。 (2)动态法:控制电极电位以较慢的速度连续地改变(扫描),并测量对应电位下的瞬时电流值,并以瞬时电流与对应的电极电位作图,获得整个的极化曲线。
《燃料电池电堆测试与分析》实验报告 一.实验目的: 1.掌握PEMFC电堆测试台的基本结构和操作方法; 2.通过实测,掌握电堆极化曲线的测试方法,学会绘制极化曲线、功率曲线等图谱; 3.能将燃料电池电堆的实测性能应用于燃料电池系统的构建上;锻炼运用理论分析、解决实际问题的能力和方法。 二.实验原理: 将所需测量的PEMFC电堆与NBT燃料电池测试系统连接,通过控制平台调节燃料电池的氢气和空气流量,设置负载的电流值(也就是燃料电池电堆的电流值),观察记录电压值和功率值得变化,利用所记录的数据画出燃料电池的i-V和i-P曲线。 三.实验仪器设备和器材 四.测试平台开机顺序测试 1.打开气源,检查氢气、空气(外部供应时)的压力是否正常、去离子水的液位是否正常;室内氢气泄露报警系统是否正常;氢气、空气与水的排放口是否连接妥当,氢气管路的出口必须接于室外。注意测试时的人员与设备的安全。 2.给测试平台上电,380V AC。 3.开启电脑,与设备联机。 4.手动设置适当的氢、空、冷却水温度(注意不应超过80℃)、各流体最低流量、电堆片数、活性面积等参数。 5.设定数据保存路径和文件名,开始记录数据。
6.测试极化曲线。根据电堆所需要氢空流量,手动设置电流,测试极化曲线。 7.实验结束。 五.提前制作电堆运行所需氢气和空气的流量表,如下表所示。 已知条件:电堆片数:19片,单电池活性面积250cm2; 阴/阳极化学计量比:3.5/1.5; 常压 六.绘制电堆的极化曲线和功率密度曲线,需要标明必要的测试条件。
七.绘制上述极化曲线上最大功率时的单片电池电压柱状图,并计算电压的 标准偏差。 学生(签名): 实验日期:2015.5.25
实验数据处理的基本方法 数据处理是物理实验报告的重要组成部分,其包含的容十分丰富,例如数据的记录、函数图线的描绘,从实验数据中提取测量结果的不确定度信息,验证和寻找物理规律等。本节介绍物理实验中一些常用的数据处理方法。 1列表法 将实验数据按一定规律用列表方式表达出来是记录和处理实验数据最常用的方法。表格的设计要求对应关系清楚、简单明了、有利于发现相关量之间的物理关系;此外还要求在标题栏中注明物理量名称、符号、数量级和单位等;根据需要还可以列出除原始数据以外的计算栏目和统计栏目等。最后还要求写明表格名称、主要测量仪器的型号、量程和准确度等级、有关环境条件参数如温度、湿度等。 本课程中的许多实验已列出数据表格可供参考,有一些实验的数据表格需要自己设计,表1.7—1是一个数据表格的实例,供参考。 表1.7—1数据表格实例 氏模量实验增减砝码时,相应的镜尺读数
2作图法 作图法可以最醒目地表达物理量间的变化关系。从图线上还可以简便求出实验需要的某些结果(如直线的斜率和截距值等),读出没有进行观测的对应点(插法),或在一定条件下从图线的延伸部分读到测量围以外的对应点(外推法)。此外,还可以把某些复杂的函数关系,通过一定的变换用直线图表示出来。例如半导体热敏电阻的电阻与温度关系为,取对数后得到 ,若用半对数坐标纸,以lgR为纵轴,以1/T为横轴画图,则为一条直线。 要特别注意的是,实验作图不是示意图,而是用图来表达实验中得到的物理量间的关系,同 时还要反映出测量的准确程度,所以必须满足一定的作图要求。 1)作图要求 (1)作图必须用坐标纸。按需要可以选用毫米方格纸、半对数坐标纸、对数坐标纸或极坐标纸等。
常用的数据处理方法 实验数据及其处理方法是分析和讨论实验结果的依据。常用的数据处理方法有列表法、作图法、逐差法和最小二乘法(直线拟合)等。 列表法 在记录和处理数据时,常常将所得数据列成表。数据列表后,可以简单明确、形式紧凑地表示出有关物理量之间的对应关系;便于随时检查结果是否合理,及时发现问题,减少和避免错误;有助于找出有关物理量之间规律性的联系,进而求出经验公式等。 列表的要求是: (1)要写出所列表的名称,列表要简单明了,便于看出有关量之间的关系,便于处理数据。 (2)列表要标明符号所代表物理量的意义(特别是自定的符号),并写明单位。单位及量值的数量级写在该符号的标题栏中,不要重复记在各个数值上。 (3)列表的形式不限,根据具体情况,决定列出哪些项目。有些个别的或与其他项目联系不大的数据可以不列入表内。列入表中的除原始数据外,计算过程中的一些中间结果和最后结果也可以列入表中。 (4)表中所列数据要正确反映测量结果的有效数字。 列表举例如表1-2所示。 表1-2铜丝电阻与温度关系 铜丝电阻R / 作图法 作图法是将两列数据之间的关系用图线表示出来。用作图法处理实验数据是数据处理的常用方法之一,它能直观地显示物理量之间的对应关系,揭示物理量之间的联系。 1.作图规则 为了使图线能够清楚地反映出物理现象的变化规律,并能比较准确地确定有关物理量的量值或求出有关常数,在作图时必须遵守以下规则。 (1)作图必须用坐标纸。当决定了作图的参量以后,根据情况选用直角坐标纸、极坐标纸或其他坐标纸。 (2)坐标纸的大小及坐标轴的比例,要根据测得值的有效数字和结果的需要来定。原则上讲,数据中的可靠数字在图中应为可靠的。我们常以坐标纸中小格对应可靠数字最后一位的一个单位,有时对应比例也适当放大些,但对应比例的选择要有利于标实验点和读数。最小坐标值不必都从零开始,以便做出的图线大体上能充满全图,使布局美观、合理。 (3)标明坐标轴。对于直角坐标系,要以自变量为横轴,以因变量为纵轴。用粗实线在坐标纸上描出坐标轴,标明其所代表的物理量(或符号)及单位,在轴上每隔一定间距标明
碳钢在碳酸铵溶液中的极化曲线 【目的要求】 1. 掌握准稳态恒电位法测定金属极化曲线的基本原理和测试方法。 2. 了解极化曲线的意义和应用。 3. 掌握恒电位仪的使用方法。 【实验原理】 1. 极化现象与极化曲线 为了探索电极过程机理及影响电极过程的各种因素,必须对电极过程进行研究,其中极化曲线的测定是重要方法之一。我们知道在研究可逆电池的电动势和电池反应时,电极上几乎没有电流通过,每个电极反应都是在接近于平衡状态下进行的,因此电极反应是可逆的。但当有电流明显地通过电池时,电极的平衡状态被破坏,电极电势偏离平衡值,电极反应处于不可逆状态,而且随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。由于电流通过电极而导致电极电势偏离平衡值的现象称为电极的极化,描述电流密度与电极电势之间关系的曲线称作极化曲线,如图2-19-1 所示。 图2-19-1 极化曲线 A-B:活性溶解区;B:临界钝化点;B-C:过渡钝化区; C-D:稳定钝化区;D-E:超(过)钝化区 金属的阳极过程是指金属作为阳极时在一定的外电势下发生的阳极溶解过程,如下式所示: M→M n++n e 此过程只有在电极电势正于其热力学平衡电势时才能发生。阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,但当阳极电势正到某一数值时,其溶解速度达到最大值,此后阳极溶解速度随电势变正反而大幅度降低,这种现象称为金属的钝化现象。图2-19-1中曲线表明,从A点开始,随着电位向正方向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减至最小,这是因为在金属表面生产了一层电阻高,耐腐蚀的钝化膜。B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流。电势到达C 点以后,随着电势的继续增加,电流却保持在一个基本不变的很小的数值上,该电流称为维钝电流,直到电势升到D点,电流才又随着电势的上升而增大,表示阳极又发生了氧化过程,可能是高价金属离子产生,也可能是水分子放电析出氧气,DE段称为过钝化区。 2. 极化曲线的测定 (1) 恒电位法 恒电位法就是将研究电极的电极电势依次恒定在不同的数值上,然后测量对应于各电位下的电流。极化曲线的测量应尽可能接近体系稳态。稳态体系指被研究体系的极化电流、电极电势、电极表面状态等基本上不随时间而改变。在实际测量中,常用的控制电位测量方法有以下两种: 阶跃法将电极电势恒定在某一数值,测定相应的稳定电流值,如此逐点地测量一系列各个电极电势下的稳定电流值,以获得完整的极化曲线。对某些体系,达到稳态可能需要很长时间,为节省时间,提高测量重现性,往往人们自行规定每次电势恒定的时间。 慢扫描法控制电极电势以较慢的速度连续地改变(扫描),并测量对应电势下的瞬时电流值,以瞬时电流与对应的电极电势作图,获得整个的极化曲线。一般来说,电极表面建立稳态的速度愈慢,则电位扫描速度也应愈慢。因此对不同的电极体系,扫描速度也不相同。为测得稳态极化曲线,人们通常依次减小扫描速度测定若干条极化曲线,当测至极化曲线不
实验数据处理基本方法 实验必须采集大量数据,数据处理是指从获得数据开始到得出最后结 论的整个加工过程,它包括数据记录、整理、计算与分析等,从而寻找出 测量对象的内在规律,正确地给出实验结果。因此,数据处理是实验工作 不可缺少的一部分。数据处理涉及的内容很多,这里只介绍常用的四种方 法。 1列表法 对一个物理量进行多次测量,或者测量几个量之间的函数关系,往往 借助于列表法把实验数据列成表格。其优点是,使大量数据表达清晰醒目, 条理化,易于检查数据和发现问题,避免差错,同时有助于反映出物理量 之间的对应关系。所以,设计一个简明醒目、合理美观的数据表格,是每 一个同学都要掌握的基本技能。 列表没有统一的格式,但所设计的表格要能充分反映上述优点,应注意以下几点:1.各栏目均应注明所记录的物理量的名称(符号 )和单位; 2.栏目的顺序应充分注意数据间的联系和计算顺序,力求简明、齐全、有条理; 3.表中的原始测量数据应正确反映有效数字,数据不应随便涂改,确实要修改数据时, 应将原来数据画条杠以备随时查验; 4.对于函数关系的数据表格,应按自变量由小到大或由大到小的顺序排列,以便于判 断和处理。 2图解法 图线能够明显地表示出实验数据间的关系,并且通过它可以找出两个 量之间的数学关系,因此图解法是实验数据处理的重要方法之一。图解法 处理数据,首先要画出合乎规范的图线,其要点如下: 1.选择图纸作图纸有直角坐标纸 ( 即毫米方格纸 ) 、对数坐标纸和 极坐标纸等,根据 作图需要选择。在物理实验中比较常用的是毫米方格纸,其规格多为17 25 cm 。 2.曲线改直由于直线最易描绘 , 且直线方程的两个参数 ( 斜率和截距 ) 也较易算得。所以对于两个变量之间的函数关系是非线性的情形,在用图解法时 应尽可能通过变量代换 将非线性的函数曲线转变为线性函数的直线。下面为几种常用的变换方法。 ( 1) xy c ( c 为常数 ) 。 令 z 1,则 y cz,即 y 与 z 为线性关系。 x ( 2) x c y ( c 为常x2,y 1 z ,即 y 与为线性关系。
实验九极化曲线的测定 【目的要求】 1. 掌握稳态恒电位法测定金属极化曲线的基本原理和测试方法. 2. 了解极化曲线的意义和应用. 3. 掌握恒电位仪的使用方法. 【实验原理】 1. 极化现象与极化曲线 为了探索电极过程机理及影响电极过程的各种因素,必须对电极过程进行研究,其中极化曲线的测定是重要方法之一.我们知道在研究可逆电池的电动势和电池反应时,电极上几乎没有电流通过,每个电极反应都是在接近于平衡状态下进行的,因此电极反应是可逆的.但当有电流明显地通过电池时,电极的平衡状态被破坏,电极电势偏离平衡值,电极反应处于不可逆状态,而且随着电极上电流密度的增加,电极反应的不可逆程度也随之增大.由于电流通过电极而导致电极电势偏离平衡值的现象称为电极的极化,描述电流密度与电极电势之间关系的曲线称作极化曲线,如图2-19-1所示. 图2-19-1 极化曲线 A-B:活性溶解区;B:临界钝化点B-C:过渡钝化区;C-D:稳定钝化区D-E:超(过)钝化区 金属的阳极过程是指金属作为阳极时在一定的外电势下发生的阳极溶解过程,如下式所示: M→Mn++ne 此过程只有在电极电势正于其热力学电势时才能发生.阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,但当阳极电势正到某一数值时,其溶解速度达到最大值,此后阳极溶解速度随电势变正反而大幅度降低,这种现象称为金属的钝化现象.图2-19-1 中曲线表明,从A点开始,随着电位向正方向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减至最小,这是因为在金属表面生产了一层电阻高,耐腐蚀的钝化膜.B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流.电势到达C点以后,随着电势的继续增加,电流却保持在一个基本不变的很小的数值上,该电流称为维钝电流,直到电势升到D点,电流才有随着电势的上升而增大,表示阳极又发生了氧化过程,可能是高价金属离子产生也可能是水分子放电析出氧气,DE段称为过钝化区. 2. 极化曲线的测定 (1) 恒电位法 恒电位法就是将研究电极依次恒定在不同的数值上,然后测量对应于各电位下的电流.极化曲线的测量应尽可能接近体系稳态.稳态体系指被研究体系的极化电流,电极电势,电极表面状态等基本上不随时间而改变.在实际测量中,常用的控制电位测量方法有以下两种: 静态法:将电极电势恒定在某一数值,测定相应的稳定电流值,如此逐点地测量一系列各个电极电势下的稳定电流值,以获得完整的极化曲线.对某些体系,达到稳态可能需要很长时间,为节省时间,提高测量重现性,往往人们自行规定每次电势恒定的时间. 动态法:控制电极电势以较慢的速度连续地改变(扫描),并测量对应电位下的瞬时电流值,以瞬时电流与对应的电极电势作图,获得整个的极化曲线.一般来说,电极表面建立稳态的速度愈慢,则电位扫描速度也应愈慢.因此对不同的电极体系,扫描速度也不相同.为测得稳态极化曲线,人们通常依次减小扫描速度测定若干条极化曲线,当测至极化曲线不再明显变化时,可确定此扫描速度下测得的极化曲线即为稳态极化曲线.同样,为节省时间,对于那些只是为了比较不同因素对电极过程影响的极化曲线,则选取适当的扫描速度绘
北京理工大学能源与化学工程实验预习报告 姓名班级学号 实验日期2016年 4 月 27 日指导教师____________________ 同组姓名成绩_______________ 实验名称阴极极化曲线的测量 一、实验目的 1.掌握测量极化曲线的基本原理和测量方法 2.测定铁电极在碱性溶液中的阴极极化曲线 3.学会根据极化曲线分析溶液中添加剂作用的方法 二、实验内容和原理 在电化学研究中,很多电化学反应表现在电极的计划上,因此测量电极的极化曲线是很重要的研究方法。在电流通过电极与电解液界面时,电极电位将偏离平衡电极电位,当电位向负向偏离时,称之为阴极极化,向正向偏离时,称之为阳极极化。在电镀工艺中,用测定阴极极化的方法研究电镀液各组分及工艺条件对阴极极化的影响,而阳极极化可用来研究阳极行为或腐蚀现象。 所谓极化曲线就是电位与电流密度之间的关系曲线。测量极化曲线的方法分为恒电流法和恒电位法,而每种方法又可分为稳流法和暂态法。本实验是测量在碱性镀锌溶液中,香草醛光亮对阴极极化的影响。 三、主要仪器设备 1.实验仪器 CHI电化学工作站1台,电解池1个。 2.试剂及材料 ZnO,NaOH,香草醛,低碳钢电极(表面积为1cm2),铂片电极1块,硫酸亚汞电极1个。
四、操作方法与步骤 本实验采用CHI电化学工作站中的线性电位扫描法分别测量以下两种电解液中的阴极极化曲线: (1)ZnO 12g/L+NaOH 120g/L (2)ZnO 12g/L+NaOH 120g/L+香草醛 0.2g/L 扫描速度:2mV/s;电位扫描范围:-1.18~ -2.18V。 1.接好线路。 2.测量阴极极化曲线 (1)研究电极为低碳钢电极,表面积为1cm2(注意测试面积一定要准确,不测部分要用绝缘漆涂好)。将待测的电极用金相砂纸打磨,除去氧化膜,用丙酮洗涤涂油。再用脱脂棉蘸酒精擦洗,用蒸馏水冲洗干净,再用滤纸吸干,放进电解池中。 (2)电解池中的辅助电极为铂电极,参比电极为硫酸亚汞电极。 (3)启动CHI电化学工作站,运行测试软件。在Setup菜单中点击“Technique”选项。在弹出菜单中选择“Linear Sweep Voltammetry”测试方法,然后点击OK按钮。 (4)在S额突破菜单中点击“Parameters”选项。在弹出菜单中输入测试条件:Init E为-1.18V,Final E为-2.18V,Scan Race为0.002V/S,Sample Interval为0.001V,Quiet Time为2s,Sensitivity为6- 1 ,选择 10 Auto-sensitivity。然后点击OK按钮。 (5)在Control菜单中点击“Run Experiment”选项,进行极化曲线的测量。 (6)改变溶液组成,测试电极在第二种溶液中的阴极极化曲线,测试条件同上。 3.实验完毕,关闭仪器,将研究电极清洗干净待用。 五、实验结果与分析
实验数据处理的几种方法 物理实验中测量得到的许多数据需要处理后才能表示测量的最终结果。对实验数据进行记录、整理、计算、分析、拟合等,从中获得实验结果和寻找物理量变化规律或经验公式的过程就是数据处理。它是实验方法的一个重要组成部分,是实验课的基本训练内容。本章主要介绍列表法、作图法、图解法、逐差法和最小二乘法。 1.4.1 列表法 列表法就是将一组实验数据和计算的中间数据依据一定的形式和顺序列成表格。列表法可以简单明确地表示出物理量之间的对应关系,便于分析和发现资料的规律性,也有助于检查和发现实验中的问题,这就是列表法的优点。设计记录表格时要做到:(1)表格设计要合理,以利于记录、检查、运算和分析。 (2)表格中涉及的各物理量,其符号、单位及量值的数量级均要表示清楚。但不要把单位写在数字后。 (3)表中数据要正确反映测量结果的有效数字和不确定度。列入表中的除原始数据外,计算过程中的一些中间结果和最后结果也可以列入表中。 (4)表格要加上必要的说明。实验室所给的数据或查得的单项数据应列在表格的上部,说明写在表格的下部。 1.4.2 作图法 作图法是在坐标纸上用图线表示物理量之间的关系,揭示物理量之间的联系。作图法既有简明、形象、直观、便于比较研究实验结果等优点,它是一种最常用的数据处理方法。 作图法的基本规则是: (1)根据函数关系选择适当的坐标纸(如直角坐标纸,单对数坐标纸,双对数坐标纸,极坐标纸等)和比例,画出坐标轴,标明物理量符号、单位和刻度值,并写明测试条件。 (2)坐标的原点不一定是变量的零点,可根据测试范围加以选择。,坐标分格最好使最低数字的一个单位可靠数与坐标最小分度相当。纵横坐标比例要恰当,以使图线居中。 (3)描点和连线。根据测量数据,用直尺和笔尖使其函数对应的实验点准确地落在相应的位置。一张图纸上画上几条实验曲线时,每条图线应用不同的标记如“+”、“×”、“·”、“Δ”等符号标出,以免混淆。连线时,要顾及到数据点,使曲线呈光滑曲线(含直线),并使数据点均匀分布在曲线(直线)的两侧,且尽量贴近曲线。个别偏离过大的点要重新审核,属过失误差的应剔去。 (4)标明图名,即做好实验图线后,应在图纸下方或空白的明显位置处,写上图的名称、作者和作图日期,有时还要附上简单的说明,如实验条件等,使读者一目了然。作图时,一般将纵轴代表的物理量写在前面,横轴代表的物理量写在后面,中间用“~”
极化曲线的测定 一、实验目的 掌握恒电位测定极化曲线的方法,测定碳钢(圆型钢筋)在碱性溶液中的恒电位阳极极化曲线及其极化电位。 二、实验原理 实际的电化学过程并不是在热力学可逆条件下进行的。在电流通过电极时,电极电位会偏离其平衡值,这种现象称为极化。在外电流的作用下,阴极电位会偏离其平衡位置向负的方向移动,称为阴极极化;而阳极电位会偏离其平衡位置向正的方向移动,称为阳极极化。在电化学研究中,常常测定极化曲线,即电极电位与电流密度的关系。铁在硫酸溶液中典型的阳极极化曲线如图23.1所示,该曲线分为四个区域: 电 流 密 度 i 阳极电位φ + 图23.1 阳极极化曲线 1.从点a 到点b 的电位范围称金属活化区。此区域内的ab 线段是金属的正常阳极溶解,以铁电极为例,此时铁以二价形式进入溶液,即Fe → Fe 2+ + 2e-。a 点即为金属的自然腐蚀电位。 2.从b 点到c 点称为钝化过渡区。bc 线是由活化态到钝化态的转变过程,b 点所对应的电位称为致钝电位,其对应的电流密度ib 称为致钝电流密度,此时Fe 2+离子与溶液中的-24 SO 离子形成4FeSO 沉淀层, 阻碍了阳极反应进行,导致电流密度开始下降。由于+H 不容易到达4FeSO 沉淀层的内部,因此铁表面的pH 逐步增大。 3.从c 点到d 点的电位范围称为钝化区。由于金属表面状态发生变化,阳极溶解过程的过
电位升高,金属的溶解速率急剧下降。在此区域内的电流密度很小,基本上不随电位的变化而改变。此时的电流密度称为维持钝化电流密度i m 。对铁电极而言,此时32O Fe 在铁表面生成,形成致密的氧化膜,极大地阻碍了铁的溶解,出现钝化现象。 4.de 段的电位范围称为过钝化区。在此区阳极电流密度又重新随电位增大而增大,金属的溶解速度又开始增大,这种在一定电位下使钝化了的金属又重新溶解的现象叫做过钝化。电流密度增大的原因可能是产生了高价离子(如,铁以高价转入溶液),或者达到了氧的析出电位,析出氧气。 测定极化曲线实际上是测定有电流流过电极时电极电位与电流的关系,极化曲线的测定可以用恒电流和恒电位两种方法。恒电流法是控制通过电极的电流(或电流密度),测定各电流密度时的电极电位,从而得到极化曲线。恒电位法是将研究电极的电位恒定地维持在所需的数值,然后测定相应的电流密度,从而得到极化曲线。由于在同一电流密度下可能对应多个不同的电极电位,因此用恒电流法不能完整的描述出电流密度与电位间的全部复杂关系。 本实验采用控制电极电位的恒电位法测定碳钢在碱性溶液中的阳极极化曲线。碳钢常用作建筑钢筋,是大量使用的建筑材料。混凝土凝结过程中会析出氢氧化钙等碱性物质,并在钢筋表面形成保护膜,阻止钢筋的腐蚀。同时,渗入混凝土内部的雨水等外来物质会带入2CO 、 Cl 等,改变钢筋表面的pH 值和腐蚀电位。本实验模拟钢筋在混凝土中所处的碱性环境,通过恒电位法测定其极化曲线,了解影响钢筋腐蚀的各种因素。 三、仪器与试剂 HDY-I 型恒电位仪(南京桑力电子设备厂),三电极池及支架,碳钢电极,铂电极,饱和甘汞电极,34HCO NH 饱和溶液,浓3NH 水,1%(体积比)硫酸溶液,丙酮,金相砂纸。烧杯(100ml )2只,量筒(50或100ml )1只。 恒电位仪前面板如图23.2所示,以功能作用划分为14个区: 图23.2 前面板示意图
实验数据的处理 在做完实验后,我们需要对实验中测量的数据进行计算、分析和整理,进行去粗取精,去伪存真的工作,从中得到最终的结论和找出实验的规律,这一过程称为数据处理。实验数据处理是实验工作中一个不可缺少的部分,下面介绍实验数据处理常用的几种方法。 一、列表法 列表法就是将实验中测量的数据、计算过程数据和最终结果等以一定的形式和顺序列成表格。列表法的优点是结构紧凑、条目清晰,可以简明地表示出有关物理量之间的对应关系,便于分析比较、便于随时检查错误,易于寻找物理量之间的相互关系和变化规律。同时数据列表也是图示法、解析法的数值基础。 列表的要求: 1、简单明了,便于看出有关量之间的关系,便于处理数据。 2、必须注明表中各符号所代表的物理量、单位。 3、表中记录的数据必须忠实于原始测量结果、符合有关的标准和规则。应正确地反映测量值的有效位数,尤其不允许忘记未位为“0”的有效数字。 4、在表的上方应当写出表的内容(即表名) 二、图示法 图示法就是在专用的坐标纸上将实验数据之间的对应关系描绘成图线。通过图线可直观、形象地将物理量之间的对应关系清楚地表示出来,它最能反映这些物理量之间的变化规律。而且图线具有完整连续性,通过内插、外延等方法可以找出它们之间对应的函数关系,求得经验公式,探求物理量之间的变化规律;通过作图还可以帮助我们发现测量中的失误、不足与“坏值”,指导进一步的实验和测量。定量的图线一般都是工程师和科学工作者最感兴趣的实验结果表达形式之一。 函数图像可以直接由函数(图示)记录仪或示波器(加上摄影记录)或计算机屏幕(打印机)画出。但在物理教学实验中,更多的是由列表所得的数值在坐标纸上画成。为了保证实验的图线达到“直观、简明、清晰、方便”,而且准确度符合原始数据,由列表转而画成图线时,应遵从如下的步骤及要求: 1、图纸选择 依据物理量变化的特点和参数,先确定选用合适的坐标纸,如直角坐标纸、双对数坐标纸、单对数坐标纸、极坐标纸或其他坐标纸等。原则上数据中的可靠数字在图中也应可靠,数据中的可疑位在图中应是估计的,使从图中读到的有效数字位数与测量的读数相当。例如:作电阻R(Ω)与温度T(?C)的图时,可以选用直角坐标纸或单对数坐标纸作图。选择何种坐标纸要看需要,若
1.极化曲线:表示电极电位与极化电流或极化电流密度之间的关系曲线。如电极分别是阳极或阴极,所得曲线分别称之为阳极极化曲线(anodic polarization curve)或阴极极化曲线(cathodic polarization curve)。 2.极化曲线分为四个区,活性溶解区、过渡钝化区、稳定钝化区、过钝化区。极化曲线可用实验方法测得。分析研究极化曲线,是解释金属腐蚀的基本规律、揭示金属腐蚀机理和探讨控制腐蚀途径的基本方法之一。 极化曲线以电极电位为横坐标,以电极上通过的电流为纵坐标,获得的曲线称为极化曲线。它表征腐蚀原电池反应的推动力电位与反应速度电流之间的函数关系。直接从实验测得的是实验极化曲线。而构成腐蚀过程的局部阳极或者局部阴极上单独电极反应之电位与电流关系称为真实极化曲线,即理想极化曲线。 3.此过程只有在电极电势正于其热力学电势时才能发生。阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,但当阳极电势正到某一数值时,其溶解速度达到最大值,此后阳极溶解速度随电势变正反而大幅度降低,这种现象称为金属的钝化现象。图1中曲线表明,从A点开始,随着电位向正方向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减至最小,这是因为在金属表面生产了一层电阻高,耐腐蚀的钝化膜。B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流。电势到达C点以后,随着电势的继续增加,电流却保持在一个基本不变的很小的数值上,该电流称为维钝电流,直到电势升到D点,电流才有随着电势的上升而增大,表示阳极又发生了氧化过程,可能是高价金属离子产生也可能是水分子放电析出氢气,DE段称为过钝化区。
阳极极化曲线的测定与分析 了解自腐蚀电位、致钝电位和维钝电位、过钝解自腐蚀电位、致钝电位和维钝电位、过钝化电位以及致钝电流密度和维钝电流密度等概化电位以及致钝电流密度和维钝电流密度等概念;念; 2. 2. 掌握恒电位法测定阳极极化曲线的原理和方掌握恒电位法测定阳极极化曲线的原理和方法;法; 3. 3. 通过阳极极化曲线的测定,判定实施阳极保护通过阳极极化曲线的测定,判定实施阳极保护的可能性,初步选取阳极保护的技术参数;的可能性,初步选取阳极保护的技术参数; 4. 4. 掌握掌握IM6ex IM6ex电化学工作站的使用方法。 电化学工作站的使用方法。 将一种金属将一种金属((电极电极))浸在电解液中,在金属与溶液之间就会浸在电解液中,在金属与溶液之间就会形成电位,这种电位称为该金属在该溶液中的电极电位。 形成电位,这种电位称为该金属在该溶液中的电极电位。 当有外加电流通过此电极时,其电极电位会发生变化,这当有外加电流通过此电极时,其电极电位会发生变化,这种现象称为电极的极化。如果电极为阳极,则电极电位将种现象称为电极的极化。如果电极为阳极,则电极电位将向正方向偏移,称为阳极极化;对于阴极,电极电位将向向正方向偏移,称为阳极极化;对于阴极,电极电位将向负方向偏移,称为阴极极化。 负方向偏移,称为阴极极化。电极电位随电流密度变化的电极电位随电流密度变化的关系曲线称为极化曲线关系曲线称为极化曲线。为了判定金属在电解质溶液中采。为了判定金属在电解质溶液中采取阳极保护的可能性,选择阳极保护的取阳极保护的可能性,选择阳极保护的33个主要技术参个主要技术参数数——致钝电流密度致钝电流密度、、维钝电流密度维钝电流密度和和钝化区的电位范围钝化区的电位范围,,需要测定阳极极化曲线。 需要测定阳极极化曲线。 阳极极化曲线可以用阳极极化曲线可以用恒电位法恒电位法和和恒电流法恒电流法测定。 测定。图图11是一是一条较典型的阳极极化曲线。曲线条较典型的阳极极化曲线。曲线ABCDE ABCDE是恒电位法(即维是恒电位法(即维持电位恒定,测定相对应的电流值)测得的阳极极化曲线。 持电位恒定,测定相对应的电流值)测得的阳极极化曲线。 当电位从当电位从AA逐渐正向移动到逐渐正向移动到BB点时,电流也随之增加到点时,电流也随之增加到BB点,点,当电位过当电位过BB点以后,电流反面急剧减小,这是因为在金属点以后,电流反面急剧减小,这是因为在金属表面上生成了一层高电阻耐腐蚀的钝化膜,钝化开始表面上生成了一层高电阻耐腐蚀的钝化膜,钝化开始发生。人为控制电位的增高,电流逐渐衰减到发生。人为控制电位的增高,电流逐渐衰减到CC。。 在在CC点之后,电位若继续增高,由于金属完全进入点之后,电位若继续增高,由于金属完全进入图 1 可钝化金属的阳极极化曲线钝态,电流维持在一个基本不变的很小的值钝态,电流维持在一个基本不变的很小的值————维钝电流维钝电流ii pp 。当电位增高到。当电位增高到DD点以后,金属进入了点以后,金属进入了过钝化状态,电流又重新增大。从过钝化状态,电流又重新增大。从AA点到点到BB点的范点的范围叫活化区,从围叫活化区,
课程 实 验 者 名 称 页数( ) 专业 年级、班 同组者姓名 级别 姓 名 实验 日 期 年 月 日 一、目的和要求 1、 掌握恒电位法测定电极极化曲线的原理和实验技术。通过测定Fe 在NaCl 溶液中的极化曲线,求算Fe 的自腐蚀电位,自腐蚀电流 2、论极化曲线在金属腐蚀与防护中的应用 二、基本原理 当金属浸于腐蚀介质时,如果金属的平衡电极电位低于介质中去极化剂(如H +或氧分子)的平衡电极电位,则金属和介质构成一个腐蚀体系,称为共轭体系。此时,金属发生阳极溶解,去极化剂发生还原。在本实验中,镁合金和钢分别与0.5mol/L 的NaCl 溶液构成腐蚀体系。 镁合金与NaCl 溶液构成腐蚀体系的电化学反应式为: 阳极: Mg= Mg 2++2e 阴极: 2H 2O+2e=H 2+2OH - 钢与NaCl 溶液构成腐蚀体系的电化学反应式为: 阳极: Fe= Fe 2++2e 阴极: 2H 2O+2e=H 2+2OH - 腐蚀体系进行电化学反应时的阳极反应的电流密度以 i a 表示, 阴极反应的速度以 i k 表示, 当体系达到稳定时,即金属处于自腐蚀状态时,i a =i k =i corr (i corr 为腐蚀电流),体系不会有净的电流积累,体系处于一稳定电位c ?。根据法拉第定律,即在电解过程中,阴极上还原物质析出的量与所通过的电流强度和通电时间成正比,故可阴阳极反应的电流密度代表阴阳极反应的腐蚀速度。金属自腐蚀状态的腐蚀电流密度即代表了金属的腐蚀速度。因此求得金属腐蚀电流即代表了金属的腐蚀速度。金属处于自腐蚀状态时,外测电流为零。 极化电位与极化电流或极化电流密度之间的关系曲线称为极化曲线。测量腐蚀体系的阴阳极极化曲线可以揭示腐蚀的控制因素及缓蚀剂的作用机理。在腐蚀点位附近积弱极化区的举行集会测量可以可以快速求得腐蚀速度。在活化极化控制下,金属腐蚀速度的一般方程式为: 其中 I 为外测电流密度,i a 为金属阳极溶解的速度,i k 为去极化剂还原的速度,βa 、βk 分别 为金属阳极溶解的自然对数塔菲尔斜率和去极化剂还原的自然对数塔菲尔斜率。 令?E 称为腐蚀金属电极的极化值,?E =0时,I =0;?E>0时,是阳极极化,I>0,体系通过阳极电流。?E<0时,I<0, 体系通过的是阴极电流,此时是对腐蚀金属电极进行阴极极化。因此外测电流密度也称为极化电流密度 测定腐蚀速度的塔菲尔直线外推法:当对电极进行阳极极化,在强极化区,阴极分支电流i k =0, )]ex p()[ex p(k c a c corr k a i i i I β??β??---=-=c E ??-=?)]ex p()[ex p(k a corr E E i I ββ?--?=)ex p(a corr a E i i I β?==
铁的极化曲线 实验结果的记录与处理: 1、Fe在0.1mol/L的硫酸溶液中铁的极化钝化曲线 联立两直线方程得:log Icorr= ?4.25A , Icorr=5.58×10?5A ;Ecorr= ?0.56V。 因为实验所用电极直径为2mm,面积为Πmm2, 故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10?5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10?2A, 钝化电流密度=1.14×10?2/(Π×0.0012)=3.63×103(A/ m2) 钝化电位范围:1.318?1.602V 2、Fe在1.0mol/L的硫酸溶液中铁的极化钝化曲线
联立两直线方程得:log Icorr= ?4.25A , Icorr=5.58×10?5A ;Ecorr= ?0.56V。 因为实验所用电极直径为2mm,面积为Πmm2, 故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10?5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10?2A, 钝化电流密度=1.14×10?2/(Π×0.0012)=3.63×103(A/ m2) 钝化电位范围:1.318?1.602V 3、Fe在1.0mol/L的HCl溶液中铁的极化钝化曲线
联立两直线方程得:log Icorr= ?4.25A , Icorr=5.58×10?5A ;Ecorr= ?0.56V。 因为实验所用电极直径为2mm,面积为Πmm2, 故自腐蚀电流密度=自腐蚀电流/电极面积=5.58×10?5 /(Π×0.0012)=17.8(A/ m2)由图知,钝化电流Ip=1.14×10?2A, 钝化电流密度=1.14×10?2/(Π×0.0012)=3.63×103(A/ m2) 钝化电位范围:1.318?1.602V 4、Fe在含1%的乌洛托品的1.0mol/L的HCl溶液中铁的极化钝化曲线
1.4 实验数据处理的几种方法 物理实验中测量得到的许多数据需要处理后才能表示测量的最终结果。对实验数据进行记录、整理、计算、分析、拟合等,从中获得实验结果和寻找物理量变化规律或经验公式的过程就是数据处理。它是实验方法的一个重要组成部分,是实验课的基本训练内容。本章主要介绍列表法、作图法、图解法、逐差法和最小二乘法。 1.4.1 列表法 列表法就是将一组实验数据和计算的中间数据依据一定的形式和顺序列成表格。列表法可以简单明确地表示出物理量之间的对应关系,便于分析和发现资料的规律性,也有助于检查和发现实验中的问题,这就是列表法的优点。设计记录表格时要做到:(1)表格设计要合理,以利于记录、检查、运算和分析。 (2)表格中涉及的各物理量,其符号、单位及量值的数量级均要表示清楚。但不要把单位写在数字后。 (3)表中数据要正确反映测量结果的有效数字和不确定度。列入表中的除原始数据外,计算过程中的一些中间结果和最后结果也可以列入表中。 (4)表格要加上必要的说明。实验室所给的数据或查得的单项数据应列在表格的上部,说明写在表格的下部。 1.4.2 作图法 作图法是在坐标纸上用图线表示物理量之间的关系,揭示物理量之间的联系。作图法既有简明、形象、直观、便于比较研究实验结果等优点,它是一种最常用的数据处理方法。 作图法的基本规则是: (1)根据函数关系选择适当的坐标纸(如直角坐标纸,单对数坐标纸,双对数坐标纸,极坐标纸等)和比例,画出坐标轴,标明物理量符号、单位和刻度值,并写明测试条件。 (2)坐标的原点不一定是变量的零点,可根据测试范围加以选择。,坐标分格最好使最低数字的一个单位可靠数与坐标最小分度相当。纵横坐标比例要恰当,以使图线居中。 (3)描点和连线。根据测量数据,用直尺和笔尖使其函数对应的实验点准确地落在相应的位置。一张图纸上画上几条实验曲线时,每条图线应用不同的标记如“+”、“×”、“·”、“Δ”等符号标出,以免混淆。连线时,要顾及到数据点,使曲线呈光滑曲线(含直线),并使数据点均匀分布在曲线(直线)的两侧,且尽量贴近曲线。个别偏离过大的点要重新审核,属过失误差的应剔去。 (4)标明图名,即做好实验图线后,应在图纸下方或空白的明显位置处,写上图的名称、作者和作图日期,有时还要附上简单的说明,如实验条件等,使读者一目了然。
讲座 实验误差及数据处理 教学要求 1、了解实验误差及其表示方法; 2、掌握了解有效数字的概念,熟悉其运算规则; 3、初步掌握实验数据处理的方法。 重点及难点 重点:实验误差及其表示方法;有效数字;实验数据处理。 难点:有效数字运算规则;实验数据的作图法处理。 教学方法与手段 讲授,ppt演示。 教学时数 4学时 教学内容 引言 化学实验中经常使用仪器对一些物理量进行测量,从而对系统中的某些化学性质和物理性质作出定量描述,以发现事物的客观规律。但实践证明,任何测量的结果都只能是相对准确,或者说是存在某种程度上的不可靠性,这种不可靠性被称为实验误差。产生这种误差的原因,是因为测量仪器、方法、实验条件以及实验者本人不可避免地存在一定局限性。 对于不可避免的实验误差,实验者必须了解其产生的原因、性质及有关规律,从而在实验中设法控制和减小误差,并对测量的结果进行适当处理,以达到可以接受的程度。 一、误差及其表示方法 1.准确度和误差 ⑴准确度和误差的定义 准确度是指某一测定值与“真实值”接近的程度。一般以误差E表示, E=测定值-真实值 当测定值大于真实值,E为正值,说明测定结果偏高;反之,E为负值,说明测定结果偏低。误差愈大,准确度就愈差。 实际上绝对准确的实验结果是无法得到的。化学研究中所谓真实值是指由有经验的研究人员同可靠的测定方法进行多次平行测定得到的平均值。以此作为真实值,或者以公认的手册上的数据作为真实值。 ⑵绝对误差和相对误差 误差可以用绝对误差和相对误差来表示。 绝对误差表示实验测定值与真实值之差。它具有与测定值相同的量纲。如克、毫升、百分数等。例如,对于质量为0.1000g的某一物体。在分析天平上称得其质量为0.1001g,则称量的绝对误差为+0.0001g。 只用绝对误差不能说明测量结果与真实值接近的程度。分析误差时,除要去
一、实验目的 1.掌握阳极极化曲线测试的基本原理和方法; 溶液中的阳极极化曲线; 2.测定Zn电极在1M KOH溶液和1M ZnCl 2 3. 通过实验理解金属电极钝化与活化过程。 二、实验原理 线性电位扫描法是指控制电极电位在一定的电位范围内,以一定的速度均匀连续的变化,同时记录下各电位下反应的电流密度,从而得到电位-电流密度曲线,即稳态电流密度与电位之间的函数关系:i= f(ψ)。 特别适用于测量电极表面状态有特殊变化的极化曲线。如下:如阳极钝化行为的阳极极化曲线。 阳极极化:金属作为阳极时在一定的外电势下发生的阳极溶解过程叫做阳极极化,如下式所示:M = Mn+ + ne 【金属的钝化现象:阳极的溶解速度随电位变正而逐渐增大。这是正常的阳极溶出。但当阳极电位正到某一数值时,其溶解速度达到一最大值。此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。】线性电位扫描法不但可以测定阴极极化曲线,也可以测定阳极极化曲线,特别适用于测定电极表面状态有特殊变化的极化曲线,如测定具有阳极钝化行为的阳极极化曲线,用线性电位扫描法测得的阳极极化曲线,如下图所示 ?AB段-----称为活性溶解区;此时金属进行正常的阳极溶解,阳极电流随电位改变服从Tafel公式的半对数关系。 ?BC段-----称为钝化过渡区;此时是由于金属开始发生钝化,随着电极电位的正移,金
属的溶解速度反而减小了。 ?CD段-----称为钝化稳定区;在该区域中金属的溶解速度基本上不随电位二改变; ?DE段-----称为过度钝化区;此时金属溶解速度重新随电位的正移而增大,为氧的析出 或者高价金属离子的生成。 从阳极极化曲线上可以得到下列参数:c点对应的电位---临界钝化电位;c点对应的电 流—临界钝化电流密度;而这些参数恒电流法是测不出来的。 影响金属钝化的因素很多,包括溶液的组成、金属的组成和结构以及外界条件。 金属Zn是中性锌锰电池、碱性锌锰电池和锌-空气电池等的负极材料,其电化学行为受 到广泛的研究。本实验应用线性电位扫描法测量金属Zn电极在1M KOH和1M ZnCl2 中阳极 极化曲线。实验中控制电极电位以较慢的速度连续地改变(扫描),并测量对应电位下的瞬 时电流值,并以瞬时电流与对应的电极电位作图,获得整个的极化曲线,故称为动电位法。 三、实验器材 CHI电化学工作站、锌电极、Hg/HgO电极、甘汞电极、铂电极、三口电解槽、1M KOH 溶液250ml、1M ZnCl2溶液250ml。 左:仪器施加的电压信号; 右:测量到的电流-电压关系曲线(极化曲线)