
质量管理工作程序(框图)目录
质量管理工作程序(框图)
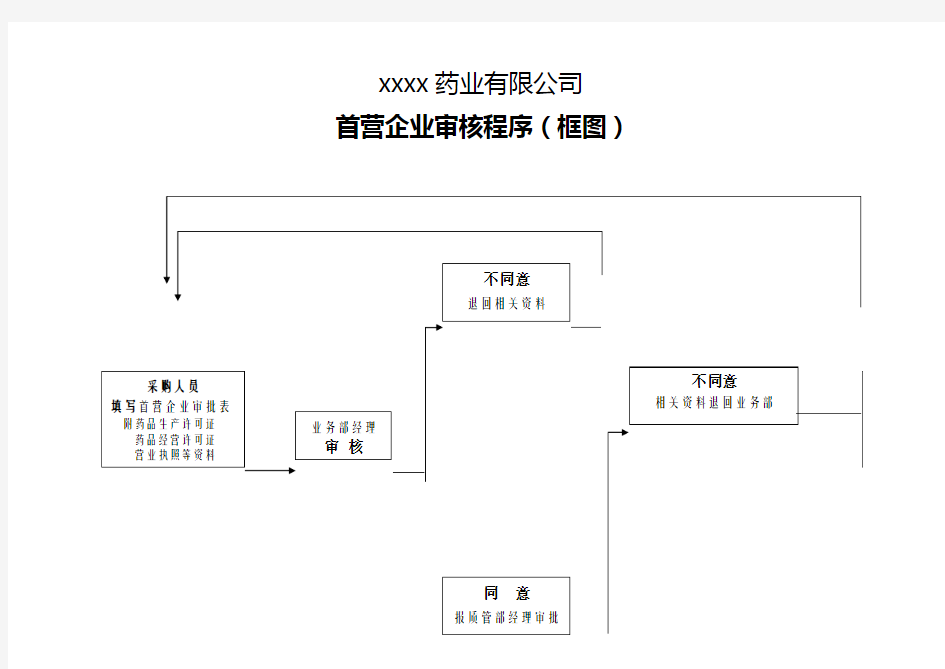
首营企业审核程序(框图)
首营品种审核程序(框图)
药品购进程序(框图)
药品验收入库程序(框图)
药品在库养护程序(框图)
药品开票、配货、复核、发货运输程序(框图)购进药品退出程序(框图)
不合格药品的确定及处理程序(框图)(一)
不合格药品的确定及处理程序(框图)(二)
不合格药品的确定及处理程序(框图)(三)
药品销后退回程序(框图)
首营企业审核程序(框图)
首营品种审核程序(框图)
药品验收入库程序(框图)
药品在库养护程序(框图)
药品开票、配货、复核、发货运输程序(框图)
购进药品退出程序(框图)
不合格药品的确定及处理程序(框图)(一)
不合格药品的确定及处理程序(框图)(二)
不合格药品的确定及处理程序(框图)(三)
药品销后退回程序(框图)
质量管理工作程序(框图)
药品购进程序(框图)
车间质量控制流程图 质检检验自检质控抽检/工序互检
质控流程 一、原材料(辅料)到我司,库管应及时通知质检, 检验外观质量和辅料性能实验;合格后方可接货入库;库管负责人如不通知质检,外观质量不合格、辅料性能实验不合格,由库管负责人承担责任;如原片外观质量、铝条外观、铝条与二次胶 的粘接度、分子筛温升实验(必须让客户带备份分子筛);注:质检按照原材料检验标准进行检验; 二、切割工序:质控员按照公司内控标准、客户要求 及操作规范进行检验和监督;1.质控员要及时对 该工序半成品进行检验,有质量异常及时通知该工段负责人找出原因及时改善,如负责人不及时改善可以直接上报、上级领导给予解决;质检发现质量异常没有及时通知该工序负责人或出现 重大质量事故,对质控部领导和当班质控员进行处罚;2.在切割时发现原片有质量异常,该工序 负责人应及时通知质控员到现场确认,质控员要填写质量异常单,做好投诉原材料供应商的第一首资料;如该工序负责人没有及时通知质控员,
出现质量事故由该工序承担;3.切割LOW-E原 片时,该工序负责人要把箱卡保存好,质控员不 定时的进行抽捡。如果不按规定操作,后果由工 序负责人承担;4.质控员要及时监督操作员是否 按操作规范进行操作。(切割LOW-E玻璃时:是 否检验切割刀头油量大小、气孔通畅、台面清洁 度、戴口罩、戴手套、落架、贴软木垫);如不 按操作规范进行操作,质控员要及时处理并通知 该工序负责人;5.该工序补片前要通知质控员到 现场确认玻璃次破原因,方可补片; 三、磨边工序:质控员按照公司内控标准、客户要求 及操作规范进行检验和监督;注:该工序负责人 一定要检验上段工序交接的产品质量,如有异常 处理不了,及时通知质控员进行处理。不知会质 控员,出现质量事故由该工序负责人承担;1.质 控员要第一时间检测离子水,是否在标准内,有 异常及时通知该工序负责人,如不改善出现质量 事故由该工序负责人承担;2.在生产过程中质控 员要抽捡清洗过来的半成品(清洁度、边部质量、尺寸及对角线偏差)。有异常要及时通知该工序 负责人,要及时改善,如不改善出现质量事故由 该工序负责人承担;3、打孔前一定要核对好图
浙江永达工贸有限公司 质量管理体系策划流程图(关键流程) 共2 页第1 页 流程顾客营销部研发部工艺部品质部计划部采购部生产部协作厂 新品开发需求营销情报 资料接收 开发能力评估产 开发进度、技术能力、品质保证、作业环境、材料供应、生产能力、生产/检测设备、成本之可行性 品 NG 总经理例会决定 策 NG OK 签订协议、确定进度、报价划 OK 设计方案 阶 段开发计划书 确定--设计目标、可靠性和质量目标、初始材料清单、 初始过程流程图、初始特性清单、产品保证计划 策划评价会(成立项目小组) NG OK OK 产品设计品质策划 DFMEA 、可制造性和装配设计 设计评审 设计验证 产 图样定稿试制组装夹具 品 部件清单加工单位确定 试 部件开发协议 专用部件确定 开发协议 制 试制品控制计划、产品/过程特殊特性确定( 段 发出试制订单下零件试制订单 确 试验基准交换 试验基准交换试验基准制定零件加工制作 ) 试验方法决定 阶 段 初物品送验 初物品检验初物品检验 试制品组装试制品检验 试制品输出、反馈不良内容研讨会 试制(段确)评审会NG OK
浙江永达工贸有限公司 质量管理体系策划流程图(关键流程) 关键流程图 共2 页第2 页 流程顾客营销部研发部工艺部品质部计划部采购部生产部协作厂 制订过程流程图、 制订过程流程图、车间平面布置图、特性矩阵图、PFMEA、试生产控制计划、MSA 计划、Ppk 计划 设备、工装试验设备、 承认样品取得试制品修正 设计制作专用量具提出量 包装设计 重要工序指定检验基准产 量产图样承认图样修订 改进标准化作业标准制订制订准 量产样品制作指示 备 量产组织 发出生产指示零部件加工 确 检验基准交换 认(受入检验入 库 量 组装、检查 过程检验 确 MSA SPC ) 阶 样品提供交货检验 试验报告提供确认试验 段 量产承认批准量产控制计划、包装评价 NG 量确评审会 OK 量产订单量产批准书 量 订单评审生产/采购计划 零部件加工产 受入检验入库 销 售组装/包装/检查 过程检验 阶 成品检验入库 段 出货检查 制品交付 外部设计变更设计变更 交 变更协调会 付 变更信息联系 变更通知单变更安排变更日期指示 服 组装、检查 变更确认初物管理 初物管理 务 进料、过 程、 品质不良信息 最终检验 阶 不良信息 段 不良处理、查明原因、防止再发生、内部质量检查、改进内容标准化
流程叙述负责人记录/参考 进料:收到仓库的送检通知单,准备验收; 查看产品的检验报告:要求供应商提供产品检验报告;判定:检查产品检验报告上的各指标是否符合要求; 合格:报告合格再抽样检验; 不合格:通知品管主管; 知会仓库,退货:在送检通知单填写不合格;交予仓库,退货处理; 知会采购部:与采购部沟通该供应商提供该批次产品的问题; 抽检合格:抽检合格,填写送检单,交予仓库;仓管员/ 检验员 检验员 检验员 检验员 品管主 管 检验员 仓管员 品管主 管 采购员 检验员/ 仓管员 仓管员 检验员 《送检通知 单》 《产品检验 报告》 《产品检验 报告》 《原材料内 控标准》 《送检通知 单》 《质量内部 联络单》 《供应商每 批供应记录 表》 《送检通知 书》
入仓:仓库接到送检单,安排入仓; 存档:所有文件检验记录存档《原材料检验报告》《每月原材料质量统计》 质量管理部:生产过程工作流程表 流程叙述负责人记录/参考 原料投产:原料投入生产; 巡检:生产过程中,现场QC对各个车间进行巡查,抽检 检验合格:继续一生产部 现场QC 现场QC 品管主 管 品管主 《原料投产 单》 《车间清洗 消毒记录》 《车间品质 控制检查记 录》 进料 查看产品检验报告 判定 合格 抽检 合格 入仓 存档 通知主管知会仓库,退货 知会采购部NO 质量管理部:进料工作流程图
道工序; 检验不合格:通知主管, 通知有关人员:品管主管和生产主管决定不合格半成品返工还是报废; 报废:对有问题的成品进行销毁,并对该次事件提出合理的整改建议; 整改意见:相关人员对该次事件进行原因分析,提出整改意见; 成品:半成品经过合格工序生产完成; 检验:对成品抽样检验各指标; 入仓:检验合格产品在放行单上签字,入仓保存;存档:把各项检验记录,检查记录,整改意见书等保存起来。管/生产 主管 品管主 管/生产 主管 生产部 检验员 检验员/ 仓管员 检验员 《生产过程 杂物记录》 《质量异常 报告》 《整改报 告》 《纠正预防 措施》 《理化指标 检验原始记 录》 《微生物检 验原始记 录》 《产品检验 报告》 《每月产品 质量小结》 《放行单》 《入仓单》 所有相关文 件
兽药GMP 验收程序及注意事项 1、首次会议参会人员:检查组全体人员,观察员,被检查企业负责人、与检查范围有关的企业中层技术和管理人员。检查组长主持会议。 会议流程: 1)检查组长介绍检查组成员,宣读检查范围、检查路线、日程安排、工作纪律; 2)企业负责人介绍参加会议的企业人员,汇报GMp 筹备、建设情况,确定联络人。 2、现场检查检查路线:厂区周边环境和厂区环境——生产车间——辅助设施——仓库——质检室。 检查重点:按照检查要点,重点查看现场环境、布局和卫生状况;设施配置、运行状况;人员操作熟练规范程度;核实批生产、批检验、批包装纪律及物料检验等各项纪律在案的真实性、准确性;物料流转制度执行情况等。 3、核实软件及记录重点检查各类制度、规程、标准项目内容是否符合要求,核对各项记录、凭证,是否与制度规定一致。 4、人员考核对企业负责人、企业中层技术和管理人员、关键岗位(如质检、称量、配液、混合、灌装、分装、仓库、制水、空调等)的操作人员进行法规、管理知识和操作技能等方面的考核。根据考核结果和现场操作综合判定人员整体素质状况。 5、组织评议 结合实际,对照“标准”,逐条做出综合评价,并形成检查报告、缺陷项目表。 一个条款的结果判定: Y 基本符合要求(75 分以上); Y- 存在一定缺陷(50-75 分); N 严重缺陷(50 分一下)。 通过要求:关键项N 为0 一般项化药N《=22% 中药N《=25% 折算: 1、只计算一般项的缺陷。 2、三个丫-折成一个N。 3、将一般项的N和丫-折算成N,以N数除以一般项检查条款数,即为不符合率。
4、用100%减不符合率为得分。 6、末次会议参会人员为首次会议人员。 征得检查组同意后,也可企业全体人员参加。 工作流程: 1)交换意见。检查组长宣读检查报告,缺陷项内容。必要时,其他检查人员进行补充。检查组应针对缺陷项目表,提出具体的和尽可能详细的整改内容,并告知报告基本要求;企业就检查报告及缺陷项目内容提出交换意见。 2)企业对检查报告、缺陷项目表进行确认; 3)双方在检查报告、缺陷项目表上签字; 4)缺陷项目表、检查报告和评定标准打分表一式两份报农业部,交省兽药管理部门一份。5)检查组长讲话,企业负责人讲话,观察员讲话。 6)合影留念(做广告也要用) 检查结束后,组长将检查报告、缺陷项目表、现场检查方案、企业有关信息(厂名和地址)中英文名称等材料一并上报农业部。
ZJQC-OD01:质量管理体系认证实施程序认证实施程序如下图所示: ZJQC 企业
一、认证的申请与受理 1. 申请质量管理体系认证的基本条件: ●具有独立的法人地位; ●产品生产/服务符合国家法规的规定; ●申请方正在/拟建立文件化的质量管理体系。 2. 申请方应填写《管理体系认证申请表》,ZJQC在收到申请之后,做出受理与否的书面答复。 3. 在接受申请后,双方签定认证合同,同时,由申请方签署《受审核方反馈信息单》。 二、审核准备 1. 在安排审核前,申请方应确保: ●建立了文件化的质量管理体系; ●质量管理体系运行三个月以上; ●至少进行过一次内部质量管理体系审核与管理评审,且内审已覆盖所有的场所和标准条款。 2. 申请方应向ZJQC提供 ●质量手册及程序文件一套; 3. ZJQC将对上报文件进行审查,并将文件审查报告反馈给企业。需要时,申请方对质量手册作适当修改后,再次报送ZJQC复审。文件审查合格后,才能安排现场审核。 三、预审核(委托方需要时) 预审核的目的在于: ●确定受审核方的质量管理体系是否就位,能够迎接认证审核; ●使受审核方取得对ZJQC审核程序与方法及审核气氛的感性认识; ZJQC对预审核做以下控制: ●对同一受审核方的预审核次数不超过一次; ●预审核的现场审核人日数不超过正式审核现场人日数的50%; ●不因预审核而减少正式审核的人日数。
ZJQC将根据预审核的情况,考虑安排正式审核的时间与审核组人选。 四、现场审核 1. ZJQC至少在审核开始的一周前将审核计划(包括审核员名单、审核日期和日程安排)书面通知受审核方,经受审核方确认后,按计划实施现场审核。 2. 审核范围涉及质量管理体系运行有关的部门、岗位、人员、活动及相关的文件与记录。 3. 审核采用抽样的方法,审核组通过交谈、调阅文件与记录以及查看现场的方式,寻找受审核方质量管理体系符合认证标准及相关职能文件的证据。对于未能提供符合标准及质量管理体系文件证据的部门/岗位/人员/活动,审核组将开具不合格报告。 4.在现场审核末次会议前,审核组要与企业负责人沟通情况,在末次会议上要报告审核结论(推荐认证、推迟推荐认证注册和不推荐认证),并明确对不合格纠正措施的要求。 ●推荐认证:通过现场审核,没有或仅有少量一般不符合项; ●推迟推荐认证注册:存在三个以下严重不符合项和若干个一般不符合项,并在90个工作日内内采取有效纠正措施,个别或少数条款和部门需要重新审核; ●不推荐认证:存在三个以上(含三个)严重不符合项,造成系统失效,并在90个工作日内不能采取有效纠正措施,全部条款需要重新审核。 5. 对审核中发现的不合格项,受审核方要采取纠正措施,并经审核组验证,验证的方式有书面验证和现场验证两种。验证合格后,审核组方能将审核报告及相关资料报ZJQC,提交认证决定。 五、决定与发证注册 1.ZJQC对审核报告和相关资料进行审查后,做出是否准予认证注册的决定,并书面通知受审核方。 2. 凡通过注册的获证方由ZJQC颁发证书,并在公司网站(https://www.doczj.com/doc/9517755118.html,)和内部出版物《认证与管理》上予以公告。 3. 未被批准的受审核方要在通知中说明原因。如申请方再次提出申请,至少6
为保证产品的质量,满足客户的要求,规范公司产品生产制造的运作和管理,保障产品的产能和质量。 二、范围
按照公司的技术、质量、成本要求组织生产的产品,其生产制造采购过程的管理。 三、定义术语 ODM:制造商负责设计生产,在产品成型后,被委托商买去以自己的名义出售的合作生产方式。 四、职责和权限(包括但不限于) 4.1、采购部负责0DM管理 4.1.1、ODM项目立项。 4.1.2、ODM厂家选点;起草和签订ODM有关协议、合同,组织对所选的工厂考核和评价;与工厂沟通双方协作部门、人员的职责及权限;工厂成品交货期评审;ODM产品的成本控制;ODM产品生产过程控制。 4.1.3、ODM产品成本、利润分析、综合报价核算。 4.1.4、ODM工厂评审、合格供方的管理。 4.2、开发设计 4.2.1、ODM产品的研发、编制、确认ODM有关的技术文件,产品认证。 4.2.2、确认ODM成品检验关键指标、型式试验及相关试验和不合格的处理,负责质量改善。 4.3、财务 4.3.1、ODM项目立项审核,产品价格审核和有关盈利测算。
6.1、?ODM工厂的开发? 6.1.1、在对ODM工厂的开发中,采购部负责和ODM工厂签订合同协议,包括但不限于《ODM合作框架协议》、《质量协议》、《商标许可协议》、《价格协议》。? 6.1.2、在对ODM工厂的开发中,采购部负责收集与产品的生产制造相关联的资料:包含《供应商注册申请表》、工艺流程、重点生产设备清单、关键的监视和测量设备清单、关键岗位及检验岗位清单、重要原材料的清单与合格供应商清单。? 6.1.3、开发与质量负责ODM产品技术工艺准备:确认产品零部件明细表、产品规格书、关键零部件清单、零部件检验标准、出厂检验标准、生产用图纸,并负责部品考核,编制考核报告,即部品(样品、性确、量确)报验兼结果报告。 6.1.4、质量按照《产品出厂标准》负责ODM的产品质量的监督检验,并出具监督检验报告。 6.1.5采购部负责ODM工厂的供应商名单的维护。?? 6.2?、ODM工厂的评价与再评价? 6.2.1、ODM工厂的评价与再评价流程参照采购控制程序进行,同时也必须满足6.3)?ODM工厂的管理及生产过程控制及6.4)?ODM监督抽查的要求。 6.2.2、采购部组织开发、质量、财务对ODM工厂自少每年评审一次并出具供应商评审报告。 6.3?、ODM工厂的管理及生产过程控制 6.3.1、月度生产计划的编制和管理? 6.3.1.1、采购部根据市场部的需求、生产计划完成情况、成品库存、ODM工厂生产能力及生产状况等编制ODM成品的月度生产计划,与ODM工厂确认后实施。? 6.3.1.2?、ODM工厂应严格按生产计划的要求按时、按质、按量供货,当生产计划因实际情况需要修改时,由采购部负责组织与ODM工厂进行协商,下达新的生产计划确认后实施。?? 6.3.2、?ODM运行控制及生产过程控制? 6.3.2.1?、采购部负责对ODM工厂合同、协议的履行情况进行监督。?
建立质量管理体系的流程 建立管理体系,无论是 ISO9001质量管理体系、ISO14000环境管理体系,还是HACCP 食品安全管理体系,或者是其他管理体系,一般来说,流程相似,但不同的管理体系还是略有区别。下面仅以建立ISO9001质量管理体系为例,说明建立管理体系的流程。 1 总体流程划分 建立ISO9001质量管理体系的流程,依据PDCA原理(PLAN:策划;DO:实施;CHECK:检查;ACTION:改进),通常包括四个阶段。通俗一点,也就是包括人们通常所说的“写我所做,做我所写,记我所做,持续改进”的内容。这四个阶段为:准备阶段、策划质量管理体系阶段、体系运行阶段和认证审核阶段。总体完成时间大约需要四个月左右。不同的管理体系时间要求上略有差别。下图所示为质量管理体系流程图: 1.1 准备阶段 : 体系策划时间:一周左右。 企业成立贯标小组,通常由企业最高管理者担任组长,组员包括由最高管理者任命的管理者代表、各级管理人员和技术骨干。贯标小组与咨询顾问讨论、拟定建立质量管理体系的计划草案。 1.2 体系策划阶段 时间:一个月左右。 本阶段包括企业调研、诊断,标准培训,体系文件的编写、修订,文件发布等过程。 1.3 体系运行阶段 时间:一般管理体系标准都要求运行三个月以上。 本阶段包括:文件培训,质量管理体系运行指导,内部审核培训、指导,管理评审培训、指导等过程。 1.4 认证审核阶段 时间:半个月左右
本阶段包括:符合性审核(模拟审核),认证前准备,认证机构现场审核,指导关闭不符合项,获得证书等过程。 现场审核由独立的第三方认证机构实施,评价企业的质量管理体系与标准的符合程度,以确定是否颁发认证证书。 2 各阶段工作重点 2.1 成立贯标小组 贯标小组最好由公司总经理担任组长,最大限度地发挥体系建立所需的领导作用,实现“运筹帷幄、决胜千里”。 管理者代表的主要作用是代表总经理全权负责 ISO9001相关事宜,最好由主管业务的副总经理担任,一方面,其对组织内各个部门的运作较为熟悉,另一方面,在进行管理决策时,有足够的权力和影响力。 2.2 调研 时间: 1~2天,部门多、流程复杂的企业需要的时间会相应多一些。 调研是建立质量管理体系的基础。其目的在于:了解企业的管理现状,并与标准对照,找出差距,修订建立质量管理体系计划草案,形成最终的实施计划。 调研前企业应收集与以上内容有关的资料,包括企业的组织机构说明(图)、工作制度、操作规程、检验规程、在用的工作记录种类清单及记录表格样式、技术手册、设备台帐、计量仪器清单、适用的法律法规及国标等。 调研工作由咨询顾问小组全面细致地调查了解企业的组织结构、职责权限、管理过程、生产过程、质量管理现状、设备管理现状、员工素质现状等,在充分了解公司的基本情况后,与公司高层管理人员进行沟通,明确公司发展的方向和思路、组织机构的设置、管理体系的策划结构等。 调研工作根据企业的情况,一般需要 1~2天的时间,部门多、流程复杂的企业需要的时间会多一些。 2.3 培训 培训分三次进行: A、标准培训 B、文件培训 C、内审及管理评审培训 2.3.1 标准培训 时间:大约需要二到三天。
精心整理
为保证产品的质量,满足客户的要求,规范公司产品生产制造的运作和管理,保障产品的产能和质量。 二、范围 按照公司的技术、质量、成本要求组织生产的产品,其生产制造采购过程的管理。 三、定义术语 ODM:制造商负责设计生产,在产品成型后,被委托商买去以自己的名义出售的合作生产方式。 四、职责和权限(包括但不限于) 4.1、采购部负责0DM管理 4.1.1、ODM项目立项。 4.1.2、ODM厂家选点;起草和签订ODM有关协议、合同,组织对所选的工厂考核和评价;与工厂沟通双
6.2?、ODM工厂的评价与再评价? 6.2.1、ODM工厂的评价与再评价流程参照采购控制程序进行,同时也必须满足6.3)?ODM工厂的管理及生产过程控制及6.4)?ODM监督抽查的要求。 6.2.2、采购部组织开发、质量、财务对ODM工厂自少每年评审一次并出具供应商评审报告。 6.3?、ODM工厂的管理及生产过程控制 6.3.1、月度生产计划的编制和管理? 6.3.1.1、采购部根据市场部的需求、生产计划完成情况、成品库存、ODM工厂生产能力及生产状况等编制ODM成品的月度生产计划,与ODM工厂确认后实施。?
6.3.1.2?、ODM工厂应严格按生产计划的要求按时、按质、按量供货,当生产计划因实际情况需要修改时,由采购部负责组织与ODM工厂进行协商,下达新的生产计划确认后实施。?? 6.3.2、?ODM运行控制及生产过程控制? 6.3.2.1?、采购部负责对ODM工厂合同、协议的履行情况进行监督。? 6.3.2.2、为保证生产计划的完成,质量负责对ODM工厂生产过程进行监控并出具?“ODM生产过程监控记录”。监控内容主要包括:?产品一致性、关键岗位人员的确认、监视和测量设备的确认、产品工序流转与检查卡、不合格品处理情况、成品一次交验合格率情况、成品的出厂检验报告、成品的入库单等。?? 6.3.2.3、过程的确认管理?:当产品结构或生产工艺需要变更时,?采购部协调开发和质量确认其效果后,提供确认报告,方可投入批量生产。?ODM产品的重要原材料、零部件(技术要求、参数、供应商等)发生 6.3.3、? 和ODM 6.3.4?、 6.3.4.1 视需要对 6.3.4.2 6.3.4.3 6.3.5 6.3.5.1 6.3.5.2、 6.3.6 6.3.6.1 6.3.6.2 6.4?、 6.4?.1、对已经批量生产的ODM产品,质量部对ODM工厂应确保每年至少进行一次质量管理体系审核、ODM产品年度检验试验,并出具相关报告给公司。对于质量部审核、检验中发现的问题,采购部和ODM 工厂应“限期整改”。? 6.4?.2、公司每年在对ODM产品进行监督抽查不通过时(发生质量事故、虽未构成质量事故,但市场投诉较多、产品抽检发现致命性不合格),应复审,决定“限期整改”或“停产整顿”。? 6.5、?其他? 6.5.1、当公司新增产品型号时,采购部按照要求进行管理与控制,并签订新增供货产品补充协议。? 6.5.2、产品超过1年未生产时,采购部应组织公司相关部门对ODM产品进行检验测试,检验合格方可进行。?
酒店质量管理标准体系(QC)推行方案 为提高酒店确保酒店质量管理标准体系得到有效运行和实施,确保酒店质量管理体系的持续适宜,特制定此推行方案,主要从学习培训、执行文件、监督检查、适宜性修改、考评考核等方面加以控制。 一、机构设置: 来自资料搜索网(https://www.doczj.com/doc/9517755118.html,) 海量资料下载 为了保证酒店质量管理标准体系的有效运行,建立酒店质量管理体系推行小组(质检小组),成员(质检员)来自酒店各部门的管理人员;酒店质量管理标准体系推行成员主要负责协助和监督各部门的运行,每周定期召开例会,向酒店总经理汇报体系文件的执行情况及存在的问题,具体人员及分工如下表: 二、执行方式: 质检小组在组长的领导下,有权对酒店各部门进行全面服务质量监督和检查。部门级在部门经理领导下,
由部门质检小组对本部门各环节工作进行监督检查,主管级负责对本管区的工作进行监督和检查。组成:质检小组—部门—主管三级督导制度,以及周报、月报等“二报”制度,最后汇总到质检小组(人力资源部)统一上报,部门内部主管督导人员由各部门自选决定,名单上报质检小组(人力资源部)。 1. 每日例行检查工作: 1)部门内部:由部门经理安排人员按《酒店QC检查标准》进行内部检查,填写《每日检查情况报表》; 2)酒店质检小组:由人力资源部质检成员对酒店的各个部门进行检查并要填写《酒店QC自查报告》; 3)总值经理: 对各部门酒店质量管理标准体系执行情况进行抽查,在交班本上填写具体抽查内容及情况; 2.每周例行检查工作: 1)部门内部:部门经理(质检成员)要全面进行自身部门的检查,填写《周质量检查报告表》,周六将《周质量检查报告表》交人力资源部复查; 2)酒店质检小组:周一由人力资源部综合各部门的质检情况发文《周质检报告情况》抄送酒店各部门,呈报总经办,; 3.每月例行检查工作: 1)酒店质检小组:每月16号由质检小组组长(总经理)组织带队(酒店质量检查成员)到各部门对酒店质量管理标准体系执行情况进行检查,并现场讲评。 2) 每月5号人力资源部综合各部门的质检情况发文《月质检报告情况》抄送酒店各部门,呈报总经办。3.执行和监督检查: 酒店质量管理标准体系文件下发后,按规定日期投入运行,要求员工严格按文件的标准执行,养成良好的工作习惯,执行的要求和措施如下: 1.严格按照文件要求作业,严禁随意操作; 2.严格依照实际工作情况进行记录,严禁弄虚作假; 3.反映问题通过正确渠道向质检小组反映,严禁诋毁文件和抵制推行工作。 4.根据酒店质量管理标准体系执行要求制定严厉的惩罚措施,对推行不力的部门和个人进行处罚,处罚措施包括:警告、通报批评、降级、解聘处理等。 四、监察督导制度 (一)建立三级质量联保责任制 部门经理对主任负责,主任对领班(部长)负责,领班(部长)对员工负责。一旦发现服务质量问题,将追究责任,除对当事人进行淘汰、处分、扣资等处理外,也将对其主管、经理进行处分和扣罚。 1.客人投诉率超过2‰,当事人按酒店的规章制度进行处理,同时也处理部门经理、主管、领班(部长)。 2.部门发生违纪: 受到最后警告:扣当事人50元的工资,部门经理、主管、领班(部长)扣罚50元至100元。(不含50元)
操作规程目录
1、质量文件管理程序 2、药品采购操作规程 3、药品收货操作规程 4、药品验收操作规程 5、药品销售操作程序 6、处方审核、调配、核对操作规程 7、药品拆零销售操作规定 8、含特殊药品的复方制剂销售操作规程 9、营业场所药品陈列操作规程 10、营业场所药品陈列检查操作规程 11、营业场所冷藏药品的存放操作规程 12、计算机系统的操作和管理操作规程制度1:
质量文件管理程序 一、目的: 对质量活动进行预防、控制和改进,确保企业所经营药品安全有效和质量管理体系正常有效地运行,规范质量管理文件的起草、审核、批准、执行、存档等操作程序。 二、适用范围: 适用于企业经营质量管理过程中的质量管理制度、工作程序等文件。责任:质量负责人、质量管理员对本程序的实施负责。 三、内容: (一)文件的起草 1、文件应由门店质量负责人依据有关规定和实际工作的需要,提出起草申请,报公司质量负责人。 2、公司质量负责人接到申请后,应对文件的题目进行审核,并确定文件编号,然后指定有关人员起草。 3、文件一般应由门店质量负责人起草,如有特殊情况可指定熟悉法律法规、药品经营质量管理和企业实际情况的人员起草。 4、如有特殊情况可指定熟悉法律法规、药品经营质量管理和企业实际情况的人员起草。起草人、起草日期、审
核人、审核日期、批准人、批准日期、执行日期、分发人员、目的、依据、适用范围和内容。 5、岗位职责还应有质量责任、主要考核指标和任职资格。 6、文件编号规则: (1)形式:企业代码-文件类别代码-顺序号 (2)企业代码:由本企业名称前两个字的第一个拼 音大写代表。 (3)文件类别代码:质量管理制度(代码为ZD ); 岗位职责(代码为GZ );操作程序(代码为CX )。 (4)顺序号按文件类别分别用2位阿拉伯数字,从“01”开始顺序编 号。 7、文件起草时应依据文件的合法性、实用性、合理性、指令性、可操作性、可检查考核性等六个方面进行制定。 (二)文件的审核和批准: 1、公行审核。 2、审核的要点: (1)是否与现行的法律法规相矛盾。 (2)是否与企业实际相符合。 (3)是否与企业的现行的文件相矛盾。 (4)文件的意思是否表达完整。
管理体系认证实施程序 认证实施程序如下图所示: 认证机构 企业申请方要求时否 是 是 否 是否 介绍认证信息询问 受理申请 签定合同文件审查 符合?提交质量管理体系文件提出申请 现场审核准备现场审核 推荐认证认证决定与发证注册 采取纠正措施所有不合格 关闭?发现不合 格? 监督审核 复评 预审核申请方确认
一、认证的申请与受理 1.申请质量管理体系认证的基本条件: ●具有独立的法人地位; ●产品生产/服务符合国家法规的规定; ●申请方正在/拟建立文件化的质量管理体系。 2.申请方应填写《管理体系认证申请表》,认证机构在收到申请之后,做出受理与否的书面答复。 3.在接受申请后,双方签定认证合同,同时,由申请方签署《受审核方反馈信息单》。 二、审核准备 1.在安排审核前,申请方应确保: ●建立了文件化的质量管理体系; ●质量管理体系运行三个月以上; ●至少进行过一次内部质量管理体系审核与管理评审,且内审已覆盖所有的场所和标准条款。 2.申请方应向认证机构提供 ●质量手册及程序文件一套; 3.认证机构将对上报文件进行审查,并将文件审查报告反馈给企业。需要时,申请方对质量手册作适当修改后,再次报送认证机构复审。文件审查合格后,才能安排现场审核。 三、预审核(委托方需要时) 预审核的目的在于: ●确定受审核方的质量管理体系是否就位,能够迎接认证审核; ●使受审核方取得对认证机构审核程序与方法及审核气氛的感性认识; 认证机构对预审核做以下控制: ●对同一受审核方的预审核次数不超过一次; ●预审核的现场审核人日数不超过正式审核现场人日数的50%; ●不因预审核而减少正式审核的人日数。
产品验收流程 关键字:_________________________________________ 主送:丿___________________________________________________________ 报送:总__________________________________________ 抄送:____________________________________________________________ 印数:_______ 拟稿:吴霞核对:______
1.流程目的 1.1对产品的质量和达到的效果有一个考核和评价;该流程为项目管理工作的重要节点,产品经理对产品 的形式上验收预示着产品的主要开发工作已完成,产品已经基本可以投入运营。 2.适用范围: 2.1预发布或系统测试验证通过的项目程序。 3.流程主导人:产品经理 4.关键指标及目标值: 4.1关键指标:质量;时间 4.2目标值: 1)产品验收通过质量标准: A类错误B类错误C类错误D类错误E类建议 无无W 5%或少于5个 < 50% 暂不作要求 错误评定类别如下,包括但不限于如下类别。 A类一严重错误,包括以下各种错误:由于程序所引起的死机,非法退出死循环 数据库发生死锁 因错误操作导致的程序中断 功能错误 与数据库连接错误 数据通讯错误 B类一较严重错误,包括以下各种错误: 程序错误 程序接口错误 数据库的表、业务规则、缺省值未加完整性等约束条件 C类一一般性错误,包括以下各种错误:操作界面错误(包括数据窗口内列名定义、含义是 否一致) 打印内容、格式错误 简单的输入限制未放在前台进行控制 删除操作未给出提示数据库表中有过多的空字段D类一较小错误,包括以下各种错误: 界面不规范 辅助说明描述不清楚 输入输出不规范 长操作未给用户提示 提示窗口文字未采用行业术语 可输入区域和只读区域没有明显的区分标志 E类一测试建议 2)流程工期偏差率不超过原项目计划的50%
兽药验收程序及注意事项 1、首次会议 参会人员:检查组全体人员,观察员,被检查企业负责人、与检查范围有关的企业中层技术和管理人员。检查组长主持会议。 会议流程: 1)检查组长介绍检查组成员,宣读检查范围、检查路线、日程安排、工作纪律;2)企业负责人介绍参加会议的企业人员,汇报筹备、建设情况,确定联络人。 2、现场检查 检查路线:厂区周边环境和厂区环境——生产车间——辅助设施——仓库——质检室。 检查重点:按照检查要点,重点查看现场环境、布局和卫生状况;设施配置、运行状况;人员操作熟练规范程度;核实批生产、批检验、批包装纪律及物料检验等各项纪律在案的真实性、准确性;物料流转制度执行情况等。 3、核实软件及记录 重点检查各类制度、规程、标准项目内容是否符合要求,核对各项记录、凭证,是否与制度规定一致。 4、人员考核 对企业负责人、企业中层技术和管理人员、关键岗位(如质检、称量、配液、混合、灌装、分装、仓库、制水、空调等)的操作人员进行法规、管理知识和操作技能等方面的考核。根据考核结果和现场操作综合判定人员整体素质状况。 5、组织评议 结合实际,对照“标准”,逐条做出综合评价,并形成检查报告、缺陷项目表。 一个条款的结果判定: Y 基本符合要求(75分以上); 存在一定缺陷(50-75分); N 严重缺陷(50分一下)。 通过要求:关键项N为0
一般项化药N《=22% 中药N《=25% 折算: 1、只计算一般项的缺陷。 2、三个折成一个N。 3、将一般项的N和折算成N,以N数除以一般项检查条款数,即为不符合率。 4、用100%减不符合率为得分。 6、末次会议 参会人员为首次会议人员。 征得检查组同意后,也可企业全体人员参加。 工作流程: 1)交换意见。检查组长宣读检查报告,缺陷项内容。必要时,其他检查人员进行补充。检查组应针对缺陷项目表,提出具体的和尽可能详细的整改内容,并告知报告基本要求;企业就检查报告及缺陷项目内容提出交换意见。 2)企业对检查报告、缺陷项目表进行确认; 3)双方在检查报告、缺陷项目表上签字; 4)缺陷项目表、检查报告和评定标准打分表一式两份报农业部,交省兽药管理部门一份。 5)检查组长讲话,企业负责人讲话,观察员讲话。 6)合影留念(做广告也要用) 检查结束后,组长将检查报告、缺陷项目表、现场检查方案、企业有关信息(厂名和地址)中英文名称等材料一并上报农业部。 验收注意事项 1、接待安排
药房各项工作流程 一、交班 每日当班人员进入药房后依次打开电源,翻看交班本,整理处方检视未完成的具体药房事务。值夜班人员晚上整理室卫生,保证所有上架药品,药架,室(包括门前三包)干净,整洁,不得有灰尘。 二、验收药品流程 每日检查药房药品库存情况,便于计划进药并登记库存不足的药品。采购药品由专人负责,供货商将药品送至药房后货到存放于待验区,清点件数。对照实物、随货同行单(票)确认相关信息无误,做到票、帐、货相符;无随货同行单(票)或者随货同行单(票)中所列容与采购记录以药品实际情况不符的,不得收货,验收进口药品应当有加盖供货单位质量管理专用章原印章的相关证明文件,如《进口药品注册证》或《医药产品注册证》。确认无误后药品按照分类上架,随行票据签字并通知入库员将药品入电脑中。 三、药品养护检查列药品摆放并每月一次对药品做好养护记录。 重点药品养护品种包括: 1)、首营品种; 2)、主营品种; 3)、药品监督管理部门重点监控品种; 4)、近期发生过质量问题的品种; 5)、储存时间达两年或近效期的品种或有效期短的品种;6)、由于异常原因可能出现问题的药品; 7)、易变质药品; 8)、特殊储存要求的品种(如生物制品等)。
药品养护程序: 1、养护员对柜台列药品按月循环检查养护。 2、养护员做好详细检查养护记录。 3、检查养护合格的继续销售。 4、养护过程中发现有问题药品应停止销售,对于近效期药品移至近效期药品专柜,对于过期药品应立即下架并登记做报损处理。 四、每天上午9:00,下午3:00两次对各库温湿度进行记录;包括药房室温度、湿度及冰箱冷藏药品温度。如不在正常围及时采取相应措施。 常温库:温度 0~30℃相对湿度45%~75% 阴凉库:温度不高于20℃相对湿度45%~75% 冷库:温度2~10℃ 五、负责处方发药包括门诊处方和住院医嘱治疗单,遵照医嘱发放药品,严格遵守“四查十对”。 四查十对: 1)、查处方:对科别、、年龄 2)、查药品:对药名、剂型、规格、数量; 3)、查配伍禁忌:对药品性状、用法用量; 4)、查合理用药:对临床诊断。 发药程序: 接到处方时,首先要认真的审查处方,查姓史(包括编号、诊断)、药名、规格、剂量、用法、配伍禁忌、用药是否合理,如有疑问应及时与医生联系。处方检查合格后接方人将处方交调配员。调配人员接到合格处方后再次核对、药品、规格、剂量等情况。最后叫病人发药,并向病人交待清楚用药方法及注意事项,比如生物制品须冷藏,冷冻则失效,以保证药品安全有效地使用;外用制剂如洗剂的稀释,PP粉
质量管理体系流程图 顾客customer 顾客对产品的要求 Customer’s requests 已 定 新开发产品 与顾客沟通 Communication with customer 确定顾客对产品的要求 Confirmation the product 新开发产品立项 New project approval 小批量试产trial produce 产品设计计划 Product design 检验和试验区 test 设计开发 design&exploitation NO 设计评审 Design review 产品服务product service 型产品的设计开发 产 Design & exploitation 品 产品认证 product certification 样机制作sample making 顾客订购产品信息 Product information 顾客要求的评审 review 签订合同sign contract 产品定型与技术文件完成product approval & technical document done 生产准备(进入ERP 系统)prepare produce(in ERP system) 采购计划purchase plan生产计划produce plan 采购实施purchasing 生产计划实施producing 装配、产品包装 packing 产品入仓 products warehousing 客户验货 Customer inspection 检验和测量子力学test & measure 物料进仓materials warehousing NO NO 配送dispatching OK 检验和测试 Checking&test 产品交付 Products delivery
建立和实施质量管理体系工作流程: 第一阶段:策划与准备 一、体系策划准备 1、顾客需求和期望分析 2、质量管理体系/业务流程诊断 3、推行工作准备 二、体系策划 4、质量方针和目标的策划 5、业务流程/过程的设计策划 6、职能分配/职责/组织结构的策划 7、体系文件的策划 第二阶段:体系建立 三、基础培训 8、ISO9000族标准理解与实施培训 9、体系文件编写培训 10、内审员培训 四、文件编写 11、体系文件编写 12、体系文件审批和发布 第三阶段:体系运行 五、体系运行 13、体系运行动员与宣布实施 14、确定和提供必需的资源 15、体系实施运行 第四阶段:体系评价和完善 六体系评价和完善 16、内部质量审核 17、管理评审 18、体系纠正及改进
建立质量管理体系的流程 建立管理体系,无论是 ISO9001质量管理体系、ISO14000环境管理体系,还是HACCP食品安全管理体系,或者是其他管理体系,一般来说,流程相似,但不同的管理体系还是略有区别。下面仅以建立ISO9001质量管理体系为例,说明建立管理体系的流程。 1 总体流程划分 建立ISO9001质量管理体系的流程,依据PDCA原理(PLAN:策划;DO:实施;CHECK:检查;ACTION:改进),通常包括四个阶段。通俗一点,也就是包括人们通常所说的“写我所做,做我所写,记我所做,持续改进”的内容。这四个阶段为:准备阶段、策划质量管理体系阶段、体系运行阶段和认证审核阶段。总体完成时间大约需要四个月左右。不同的管理体系时间要求上略有差别。下图所示为质量管理体系流程图: 1.1 准备阶段 : 体系策划时间:一周左右。 企业成立贯标小组,通常由企业最高管理者担任组长,组员包括由最高管理者任命的管理者代表、各级管理人员和技术骨干。贯标小组与咨询顾问讨论、拟定建立质量管理体系的计划草案。 1.2 体系策划阶段 时间:一个月左右。 本阶段包括企业调研、诊断,标准培训,体系文件的编写、修订,文件发布等过程。 1.3 体系运行阶段 时间:一般管理体系标准都要求运行三个月以上。 本阶段包括:文件培训,质量管理体系运行指导,内部审核培训、指导,管理评审培训、指导等过程。 1.4 认证审核阶段 时间:半个月左右 本阶段包括:符合性审核(模拟审核),认证前准备,认证机构现场审核,指导关闭不符合项,获得证书等过程。
1基因工程药物的概念:将分离提取的可表达有免疫原性或治疗性物质的目的基因插入适宜的质粒载体中,而后导入选定的受体细胞中进行增殖,由培养分泌物或细胞破碎物中提取精制目的基因产物,制成用于预防,治疗或诊断的生物制品,称重组DNA制品。 2药品微生物总数检查的概念?:是检测药物在单位质量或体积内所含有的活菌数量,用以判断药品被污染的程度和标志。 3药品细菌数测定的概念:是微生物的定量检查,对非规定灭菌药品中污染的活菌数量进行测定,以每克或每毫升供试药品作为剂量单位 4生物检定的概念:是一种运用适当的方法和技术判断合成药物,天然药物,中成药和生化药物的原料药,及其制剂的质量是否符合有关质量标准规定的方法。 5对比检定:是以生物统计为工具,利用药物效价(浓度)在一定范围内的药理作用随浓度的增加而增加,且在一定的条件下存在直线关系,通过设计特定的实验,选择适当的反应指标,把供试品和标准品在同等条件下进行比较,计算出供试品的效价。 6量反应:当一定剂量的药物作用于生物体时,所引起的反应是可用量来表示大小的。 7质反应:当一定剂量的药物作用于动物体后,观察某一反应或反应的某一程度出现与否所引起的反应只有质的变化,只能用一组动物中出现正(或负)反应的百分率来表示。 8限度实验的概念:是指通过药品对实验动物的作用来测定出药品中测试物的最低含量或浓度的方法。 9异常毒性检查法:一定量的供试品注入小鼠体内或口服给药,在48h内观察小鼠死亡情况,以判断供试品是否符合规定的一种方法。 10药品的异常毒性试验:用稳定剂量按指定的操作方法和给药途径给予规定体重的某种动物观察其急性毒性反应,反应的判断以实验动物死亡与否为终点。 11药品检验的基本程序:取样,鉴别,检查,含量测定,写出检验报告。 12药典的内容:凡例,正文,附录,索引。 13对药品质量控制的全过程起指导作用的法令文件有:GMP,GLP,GSP,GCP. 14药品的特殊性:质量重要性,两重性,时限性,专属性。 15生物检定特点:1生物差异性大,2实验误差大,3实验周期长 16生物检定的标准品:国际标准品,国家标准品,工作标准品 17供试液制备的机械分散法通常有哪几种方法?1电动匀质装置2研磨法3振荡器法 18药品微生物限度检验对象的特殊性:1不确定性2分布的不均匀性3活体特征 19核酸类药物包括哪几种?反义核酸类药物,非反义的寡核苷酸,基因疫苗和基因药物 20药品细菌数测定防止菌落蔓延的方法? 答:1加TTC溶液:倾注培养基前,在每1000ml营养琼脂内加入灭菌1%TTC溶液1ml。 2开盖干燥:将已凝固的琼脂平板开盖,倒置斜放于净化工作台上,开机后合盖。 3换盖:将已凝固的琼脂平板盖换上新近干热灭菌的。 21微生物总数检查的抽样:一般供试品的检验量为10g或10ml;膜剂为100平方厘米,检查沙门菌的供试品,其检验量应增加20g或20ml。检验量为每次最少应分取2瓶以上的样品共10g或10ml,中药蜜丸至少应分取4丸以上共10g,片剂不少于4片,一般应随机抽取不少于检验用量的3倍量供试品。 22供试液准备及供试液制备的基本要求: 答:*一般将供试品制备成供试溶液或悬浮液 *供试液制备应适应供试品的理化性质,不得改变污染微生物的数量和种类 *(1)一批供试品需做多项检验:微生物,化学,药理学 首先取出规定量供试品供微生物学校验,其余部分做其他检验。 (2)供试品在检验之前,应保持包装状态,严禁开启。