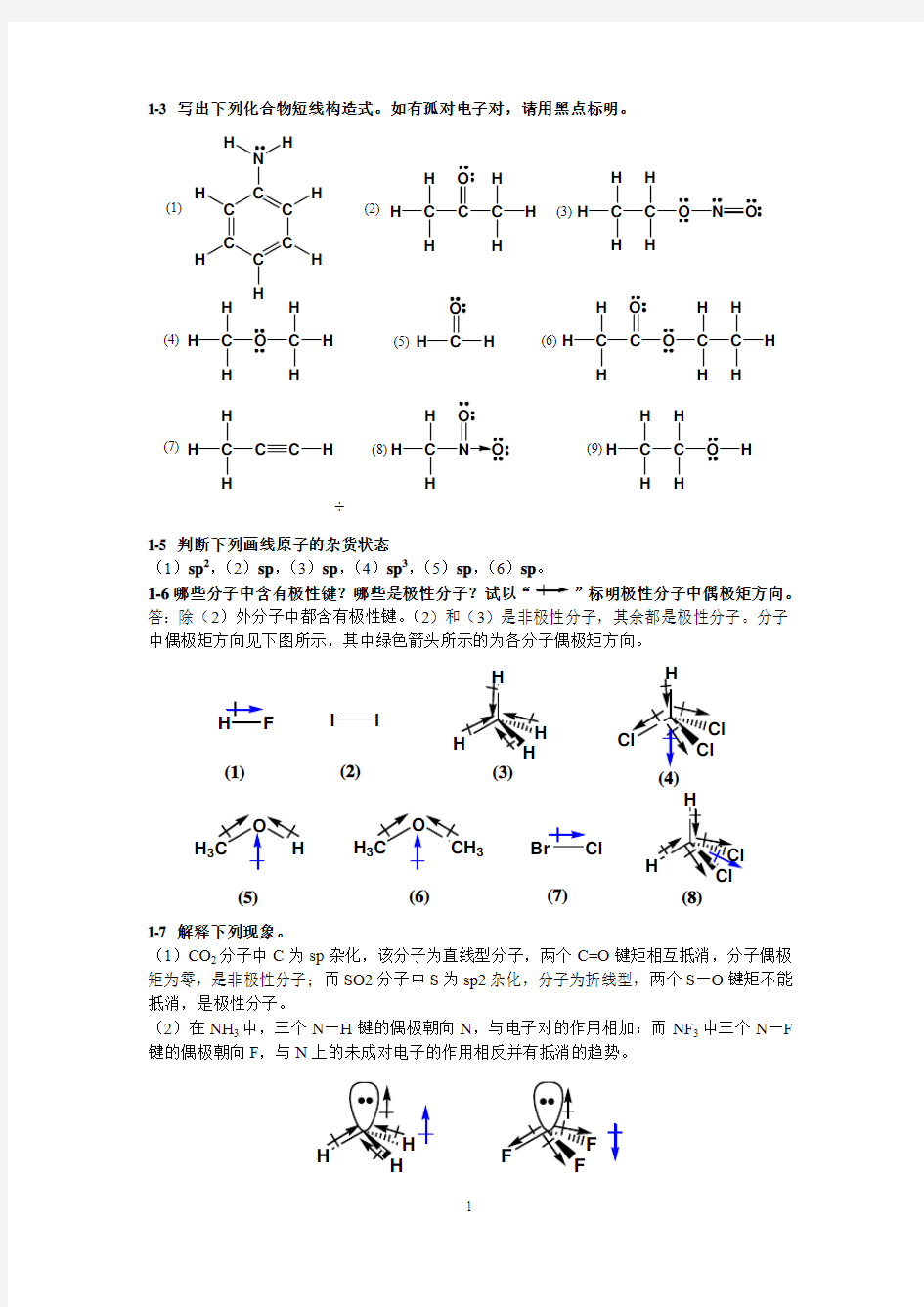

1-3 写出下列化合物短线构造式。如有孤对电子对,请用黑点标明。
÷
C C C
C C C
N
H
H
H H H
C C
H H
H
C O H H
H
H
C H C H O
N
O
H C H
O
C H H
H
H
O
H
C H
C
O O
C
C H H H
H
C H
C
C
H
H C H
N
O
O
H
C H C H
O
H
(1)
(2)(3)(4)(5)(6)(7)(8)(9)
1-5 判断下列画线原子的杂货状态 (1)sp 2,(2)sp ,(3)sp ,(4)sp 3,(5)sp ,(6)sp 。 1-6哪些分子中含有极性键?哪些是极性分子?试以“”标明极性分子中偶极矩方向。 答:除(
2)外分子中都含有极性键。(2)和(3)是非极性分子,其余都是极性分子。分子中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
H
H 33
H 3
I I
(1)
(2)
(3)
(5)
(6)
(7)
(8)
1-7 解释下列现象。
(1)CO 2分子中C 为sp 杂化,该分子为直线型分子,两个C=O 键矩相互抵消,分子偶极矩为零,是非极性分子;而SO2分子中S 为sp2杂化,分子为折线型,两个S —O 键矩不能抵消,是极性分子。
(2)在NH 3中,三个N —H 键的偶极朝向N ,与电子对的作用相加;而NF 3中三个N —F 键的偶极朝向F ,与N 上的未成对电子的作用相反并有抵消的趋势。
(3)Cl和F为一同主族元素,原子共价半径是Cl比F大,而电负性是F比Cl大。键的偶极矩等于μ=qd,q为正电荷中心或负电荷中心上的电荷量,d为正负电荷中心的距离。HCl 键长虽比HF的长,但F-中心上的电荷量大大于Cl-上的电荷量,总的结果导致HF的偶极矩大于HCl。所以键长是H—Cl较长,偶极矩是H—F较大。
1-8 将下列各组化合物中指定键的键长由长到短排列并说明理由。
答:(1)从乙烷,乙烯到乙炔,碳原子杂化态由sp3到sp2至sp,s成份提高,拉电子能力增强,虽同属于碳氢键但键长缩短。
(2)键长顺序为C—I>C—Br>C—Cl>C—F。因为卤素原子核外电子层数为I>Br>Cl >F,即其范德华半径为I>Br>Cl>F,则其原子共价半径I>Br>Cl>F。
(3)碳碳键键长为乙烷>乙烯>乙炔。因为碳原子杂化态由sp3到sp2至sp,其共价键分别为单键、双键和叁键,碳碳原子间的作用力是乙烷<乙烯<乙炔,作用力越强,则两原子被拉得越紧,键长越短。
1-9 将下列各组化合物按酸性由强到弱排列。
(1)D>A>C>B;(2)A>B>D>C
1-10 下列物种哪些是:(1)亲核试剂,(2)亲电试剂,(3)既是亲核试剂又是亲电试剂?答;(1)亲核试剂:Cl-,H2O,CH3OH,CH2=CH2,HCHO,CH3CN,-CH3;
(2)亲电试剂:H+,AlCl3,Br+,Fe3+,+NO2,HCHO,CH3CN,+CH3,ZnCl2,Ag+,BF3;(3)既是亲核试剂又是亲电试剂:HCHO,CH3CN;
(4)两者都不是的:CH4。
1-11 按质子酸碱理论,下列化合物哪些是酸?哪些是碱?哪些既是酸又是碱?
答:酸:NH3,HS-,HBr,H2O,NH4+,HCO3-;
碱:NH3,CN-,HS-,H2O,HCO3-;
既是酸又是碱:NH3,HS-,H2O,HCO3-。
1-12 按Lewis酸碱理论,在下列反应中,哪个反应物为酸?哪个反应物为碱?
答:(1)H2O 为酸,CN-为碱;(2)BF3为酸,HCHO为碱;(3)H2O 为酸,CH3NH2为碱;(4)Cu2+为酸,NH3为碱;(5)AlCl3为酸,COCl2为碱;(6)I2为酸,I-为碱。
1-13 指出下列哪些属于极性质子溶剂?哪些属于极性非质子溶剂?哪些属于非极性溶剂?答:极性质子溶剂:(5)(6);极性非质子溶剂:(1)(4)(7)(8);非极性溶剂:(2)(3)。1-14 矿物油(相对分子质量较大饱和烃的混合物)不溶于水或乙醇中,但可以溶于正已烷。答:矿物油为非极性分子,根据“相似相溶”原则,它可溶于非极性的正已烷,而不能溶于有极性的水或乙醇(水或乙醇醇间能形成氢键,分子间的引力非常强,故矿物油分子不能克服这种氢键与乙醇或水相互渗透而溶解)。
1-18 下列物质是否含有共轭酸和共轭碱?如有,请分别写出。
答:(1)即有共轭酸也有共轭碱,共轭酸是CH3NH3+,共轭碱是CH3NH2-;
(2)共轭酸是CH3OH;
(3)即有共轭酸也有共轭碱,共轭酸是CH3CH2OH2+,共轭碱是CH3CH2O-;
(4)共轭酸是H2;
(5)共轭酸是CH4;
(6)共轭碱酸是CH3CH2+,共轭碱是CH2=CH-。
1-19 将下列物种按碱性,由强至弱排列成序。
答:参照书中表1-9排出,CH3CH2->H2N->HC≡C->CH3O->OH-。
1-20 下列极限式中,哪个式子是错误的,为什么?
答:(1)中C是错的,因为此式中原子核的相对位置改变了;
(2)中C是错的,因为此式中的单电子数改变了(A、B式中单电子数为1,C中为3);
(3)中C和D是错的,因为C式2个N原子外层价电子数不是8(而是6和10),D式中间N原子外层价电子数也不符合八隅体要求。
2-1 用系统命名法命名下列烷烃。
(1)2,2,5-三甲基已烷;(2)3,6-二甲基-4-正丙基辛烷;(3)4-甲基-5-异丙基辛烷;(4)2-甲基-3-异丙基庚烷;(5)5-正丙基-6-异丙基十二烷;
(6)3,3-二甲基-4-乙基-5-(1,2-二甲基丙基)壬烷;(7)4-异丙基-5-正丁基癸烷;(8)3,6,6-三甲基-4-正丙基壬烷。
2-2 用系统命名法命名下列不饱和烃。
(1)4-甲基-2-戊炔;(2)2,3-二甲基-1-戊烯-4-炔;(3)1-已烯-5-炔;
(4)3-异丁基-4-己烯-1-炔;(5)3-甲基-2,4-庚二烯;(6)2,3-已二烯;
(7)2-甲基-2,4,6-辛三烯;(8)4-甲基-1-已烯-5-炔;(9)亚甲基环戊烷;
(10)2,4-二甲基-1-戊烯;(11)3-甲基-4-(2-甲基环已基)-1-丁烯。
2-3 用系统命名法命名下列化合物。
(1)3-甲基环戊烯;(2)环丙基乙烯;(3)4,4-二氯-1,1-二溴螺[2.4]庚烷;
(4)3-烯丙基环戊烯;(5)1-甲基-3-环丙基环戊烷;(6)3,5-二甲基环已烯;(7)螺[4.5]-1,6-癸二烯;(8)1-甲基螺[3.5]-5-壬烯;(9)2-甲基-1-环丁基戊烷;(10)2,2-二甲基-1-环丁基二环[2.2.2]辛烷;(11)5,7,7-三甲基二环[2.2.1]-2-庚烯;(12)二环[4.2.0]-7-辛烯;(13)1-甲基-4-乙基二环[3.1.0]已烷。
2-4 写出下列化合物的构造式。
(1) 3-甲基环己烯(2) 3,5,5-三甲基环己烯(3) 二环[2.2.1]庚烷(4) 二环[4.1.0]庚烷(5) 二环[2.2.1]-2-庚烯(6)二环[3.2.0]-2-庚烯(7) 螺[3.4]辛烷
(8) 螺[4.5]-6癸烯(9) 2-甲基二环[3.2.1]-6-辛烯(10) 7,7-二甲基二环[2.2.1]-2,5-庚二烯
3
3 H3
3
H3
H3
(1)
(2)(3)
(4)(5)(6)(7)
(8)(9)(10)
2-5 用系统命名法命名下列化合物。
(1)3,3-二甲基-2-苯基戊烷;(2)1,3,5-三甲基-2-异丙基苯(或2,4,6-三甲基异丙苯);(3)1-苯(基)丙烯;(4)二苯(基)乙炔;(5)1-甲基蒽;(6)2-环丙基萘(7)1,2-二苯基苯;(8)1,4-二甲基萘。
(1)3-甲基-1-溴丁烷; (2)2-甲基-3-氯丁烷; (3)1,1,3,3-四氟-1-氯丙烷; (4)二氟一氯甲烷;(5)氯甲基苯(或苯甲基氯,或氯化苄,或苄基氯,或苯一氯甲烷); (6)2-甲基-1,2-二碘丁烷; (7)(2-氯苯基)乙烯 ;
(8)1-溴-1-丁烯-3炔; (9)3-甲基-6-溴环已烯; (10)4-甲基-5-氯 -2-戊炔。 2-7 写出下列化合物的构造式。
(1) 2,4-二硝基氟苯 (2) 六氯化苯 (3) 六溴代苯 (4) 氯化苄 (5) 2-甲基-2,3-二碘丁烷 (6) 2-氯-2-丁烯 (7)3-苯基-1-溴-2-丁烯 (8) 叔氯丁烷 (9) 仲丁基溴
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
F
NO 2
NO 2
Cl
Cl
Cl
Cl
Cl
Cl Br Br
Br
Br
Br
Br CH 2Cl CH 3CCHCH
3
I 3
I
H 3CC
CHCH 3
CH 2CH
CCH 3
Br (CH 3)3C
Cl
CH 3CH 2CHCH 3
2-8用系统命名法命名下列化合物。
(1)4-甲基-2-戊醇; (2)3-甲氧-2-戊醇; (3)5-溴-1-已炔-3-醇; (4)3-苯基-1,2-戊二醇; (5)1-甲基环已醇; (6)5-甲基-1,3-苯二酚; (7)2-丁硫醇; (8)4-甲基-2-戊硫醇; (9)1-苯基-2-丙烯-1-醇; (10)4-甲基-4’-乙基二苯甲醇; (11)4-环戊烯-1,3-二醇; (12)4-(3,3-二甲基丁基)-6-苯基-5-已烯-3-醇 (13)1,4-丁二醇。 2-9 写出下列化合物的构造式。
(1) 仲丁醇 (2) 2,3-二甲基-2,3-丁二醇 (3) 二苯甲醇 (4) 新戊醇 (5) 1,3-丙二醇甲乙醚 (6) 乙硫醇 (7) 1-苯基-2-丙醇 (8 ) 间溴苯酚 (9) 异丁醇 (10) 叔丁醇 (11)对苯二酚 (12) 丙三醇 (13) β,β′-二甲氧基乙醚
(1)
(2)
(3)(4)
(5)
(6)
(7)
(8)
(9)
(10)
CH 3CHCH 2CH 3
OH
H 3C
C
C
CH 3
3OH 3
OH
CH OH
CH 32OH
CH 3
CH 3
CH 2CH 2CH 23
2H 5
CH 3CH 2SH
CH 23
OH
OH
Br
(CH 3)2CHCH 2OH
(CH 3)3COH
OH
HO
(11)
(12)
(13)
CH 2CHCH 2(CH 3OCH 2CH 2)2O
(1)4-戊烯-2-酮; (2)3-甲基-2-丁烯醛; (3)3-羟基丁醛; (4)1,3-二苯基-2-丙烯酮; (5)3-苯基-2-丙烯醛(或β-苯基丙烯醛); (6)4-甲基环己基甲醛; (7)3-甲酰基己二醛; (8)3,3-二甲基-5-乙基-6-庚烯-2,4-二酮; (9)2,4-戊二酮; (10)3-甲酰基环戊酮(3-环戊酮甲醛); (11)螺[2.4]-5-庚酮; (12)4-溴已醛; (13)3-甲基-2,6-萘醌。 2-11写出下列化合物的构造式。 (1)
(2)
(3)
(4)
(5)
(6)
(7)
O
COOH CHO
HOOC
HOOCCH 2CHCH 2CH 2CH 3
NO 2
COOH
HOOC
C C
CH 3
COOH
CH 3
HCOOCHCH 3
CH 3
CH 32CH 22CH 2CHCH 3
3
Cl
O
2-12 命名下列化合物。
(1)3-甲基-戊二酸单乙酯; (2)丁酸对甲氧基苯酯;
(3)3-甲基-4-丁内酯(或β-甲基-γ-丁内酯); (4)环已基甲酸(或环已烷羧酸); (5)N-溴代丁二酰亚胺; (6)4-硝基乙酰苯胺; (7)丙烯酰氯; (8)2-甲基-N-苯基丙酰胺; (9)4-硝基-1,2-苯二甲酸酐; (10)戊二酸酐; (11)3-苯(基)丙烯酰胺; (12)乙酸(正)丁酯; (13)对甲(基)苯磺酸。 2-13 写出下列化合物的构造式。(1.3.5.7.8.)
(1)
(2)
(3)
(4)(6)
(7)
(8)
C CH 2COCH 2CH 2CHCH 3Cl
O
CH 3
CH 322H 5
O
O
O O
C
O Cl C O
CH 2CH 2CH 2CH 2CH 3
CH 3C O N
CH 3CH 3
O C O C O
O
O O
H 3C
SO 2NH 2
2-14命名下列化合物。
(1)三乙胺; (2)环丙胺; (3)甲基乙基环丁基胺; (4)N,N-二甲基仲丁胺; (5)N,N-二甲基苯胺; (6)2-硝基丙烷; (7)2,4-二硝基氯苯; (8)4-硝基-2-氯苯酚; (9)丁晴; (10)丙烯腈; (11)乙二胺; (12)丙亚氨基环戊烷; (13)1,6-已二腈;(14)对苯二胺;(15)5-甲氧基-3-氨基已烷。
2-15 写出下列化合物的构造式。(1.2.3.5.6.)
(1)
(2)
(3)
(4)
(5)
(6)
H 2C
CHCH 3
O
CH 3CH 2CHCH 2CH 3
3
CH 2
C COCH 3
O
CH 3
NHCH 2CH 2Cl
NH 2
NHCH 3H 2N
CH 3CHCN
CH 3
(7)
(8)
2
CH 2COOH
O
(9)
(10)
(11)
(12)
(13)
CH 3(CH 2)7CH CH (CH 2)6CH 23
O
NH 2
O
CH 3SCH 2CH 3
Cl
NH 2H 2N
Cl
CH 2
Cl
H 2
N
NH 2
Cl
(14)
HOOCCHCCHCH 3
3O
3
C O C O O
H 3C
SO 2Cl
(15)
(16)
2-16写出下列基的构造式。
(1)
(2)
(3)
(4)
(5)
(6)
(11)
(12)
CH 3CH 2
C 6H 5
(CH 3)2CH
CH 3CH 2CHCH 3
(CH 3)3CCH 2
CH 3CH 2CHCH 2CH 2
CH 3
CH 3CH 2O
ClCH 2
NO 2
(CH 3)2NCH 2
3
或(7)
(9)
(8)
(10)
(H 3C)2HC
3-1 下列化合物是否有顺反异构体?若有,试写出它们的顺反异构体。 (1)没有顺反异构体; (2)、(3)、(4)均有顺反异构体。
3
3
3
3
(2)
(3)
(4)
顺式
反式3
3
3
(顺式)
顺式
反式
γ-1反-2顺-2反-4
顺-2反-4
γ-1γ-1反-4
γ-1顺-2顺-4
顺式
反式顺式顺式
反式
反式
反-2γ-1顺-4反-2γ-1顺-4
3-2 下列化合物中有无手性碳原子?若有,请用“*”标记。 (1)、(4)、(5)、(6)、(8)、(9)、(10)、(11)均有手性碳原子; 而(2)、(3)、(7)、(12)无手性碳原子。
C C 2H 5
H
C H CH
3
C
H C
H C 2H 5
(1)
(9)
(10)
(4)
(5)
(6)
(8)
CH 3C HDC 2H 5
*CH 3C HCH 2CH
2CH 3
*CH 3C HClCHCl C HClCH 3
*
CH 2CH 3*
OH Br
**
3
COOH
CH 3
OH
****
(11)
3-3 下列化合物中有无手性碳原子?若有,请用“*”标记。 (1)、(4)、(5)、(6)、(8)、(9)、(10)、(11)均有手性碳原子; 而(2)、(3)、(7)、(12)无手性碳原子。
C C 2H 5
H
C H CH
CH 3
C
H C
H C 2H 5
(1)
(9)
(10)
(4)
(5)
(6)
(8)
CH 3C HDC 2H 5
*CH 3C HCH 2CH
2CH 3
*CH 3C HClCHCl C HClCH 3
*
2CH 3*
OH Br
**
3
COOH
CH 3
OH
****
(11)
3-4 指出下列化合物是否有旋光活性? (2)、(5)有旋光活性;(1)中有一个甲基和羟基所在平面的对称面;(3)含甲酰基和氯所在的苯平面是分子的对称面;(4)为平面型分子,同时也含有对称中心;(6)、(7)和(8)三个分子都有对称面[(6)和(7)为内消旋体,其中(7)中3号碳原子上三个原子或基团
旋转后即可看出;(8)取代的乙烯有平面型分子,即二个双键碳原子、与双键碳相连的H、Cl、Br、C共六个原子在同一平面]。
OH
2
OH
CH2OH
Br H
HO H
2
OH
Br H
对称面
内消旋体
*
*
3-5 下列分子是否有手性?
(1)是平面型分子,无手性;(2)有手性;(3)有手性;
(4)分子有对称中心,无手性。
3-6 标明下列分子中手性碳原子的构型,并指出它们之间的关系。
(1)(3)(4)
(2)
CH3
Cl H
2
H
5
H3C OH
OH
H3C
C2H5
Cl
H
CH
3
3
3
C2H
H32H5
3
R
R
R
S
(1)与(3)为对映体;(2)与(4)为同一化合物;
(1)与(2)或(4)为非对称映体,(3)与(2)或(4)也是非对映体。
3-7 下列化合物有几个立体异构体?写出化合物(1)和(2)的立体异构体,并标明其不对称碳原子的构型。
必须将顺反异构、对映异构、对称因素进行综合分析。
(1)(3)
(6)
(4)
(5)
(2)
(8)
(7)
Cl Cl
CH3
O2N
OH
Cl
Cl
CHCH3
CH3
H3C C
H
CHCH3
OH O
*
*
*
*
**
*
*
**
*
*
*
*
*
(1)和(8)有两个不同手性碳,它们各有4个立体异构体;(2)(4)有两个相同手性碳,有3个立体异体;(4)有两个相同手性碳,有4个立体异构体;(3)有三个不同手性碳,有8个立体异构体;(5)有一个手性碳,所以有2个立体异构体;(6)有顺反异构体[类似于3-1中的(2))];(7)二个不同手性碳,有4个立体异构体;(8)有2个相互制约的桥头手性碳原子,相当于一个不对称碳原子,所以有2个立体异构体。
(1)
(2)
a
b
a b
3-8写出下列化合物的立体结构式。
(1)
(3)
(6)
(4)
(5)
(2)
C H
CH 32CH 3
CH CH 3CH 2CH H 2C
CH
CH 2
C C H H 3C
H C
H
C
H CH 3
(CH 3)2CH
C C
C CH
CH 2CH 3
CH 3
I CH 3
H
6H 13
CH 3OH C C
CH 3H
H
(8)
(7)
H
3
H 3CO
H H 3CO CH 3
OH 2CH 3
H
CH 3H CHO
3-9 用系统命名法命名下列化合物(立体异构体用R-S 或Z-E 标明其构型)。 (1) (3S )-3-乙基-5-己烯-1-炔; (2) (Z )-3-叔丁基-2-己烯-4-炔; (3) (3Z ,7E )-3,8-二甲基-3,7-癸二烯; (4) (S )-3-氧代环已烷羧酸; (5) (2Z ,4R )-4-甲基-2-已烯; (6) (3Z ,5S ,6S )-5-氯-6-溴-3-庚烯; (7) (R )-4-甲基-3-溴-1-戊烯; (8 ) (2S ,5S )-5-氯-2-溴庚烷;
(9) (2R ,3E )-4-甲基-2-羟基-3-己烯酸; (10)(2S ,3R )-2,3-二甲基-2,3-二羟基丁二酸。 3-10指出下列构象是否有对映体?如果有,写出其对映体。
(1)没有构象对映体(有对称面); (2)有构象对映体;(3)和(4)有对映体。
(3)
(4)
(2)
3
H 3
3
3
3-11用Newman 式画出下列分子的优势构象式。
(1)
(3)
(2)
3-13 请画出(2R ,3R )-2-氯-3-溴戊烷的Fischer 投影式与其优势构象的锯架式和Newman 式。
CH 3Cl H CH 2CH 3
H
Br 25
Cl H
CH 3
H Br
C 2H 5
Fischer 投影式 Newman 式 锯架式 3-14 试画出下列化合物的最稳定的构象式。(1.2.3.4.)
C 2H 5
C 2H 5
H 3C
OH
HO C(CH 3)3
CH 3
CH
3
(1)
(2)
(3)
(4)
(5)
(6)
(7)(8)
H
3-15 某化合物的分子式是C 5H 10O ,无光学活性,分子中有环丙烷环,在环上有两个甲基和一个羟基,请写出它的可能的构型式。
3
3
3-16解释下列术语。
(1)手性分子——不能和它的镜像完全重叠的分子。
(2)对映体——互为实物和镜像关系,相对映而不重合的两种构型分子。 非对映体——不存在实物与镜像关系的构型异构体。
(3)构象——由于绕σ键轴旋转而使分子中原子或基团在空间的不同排列方式。 (4)外消旋体——两个对映体的等量混合而形成不具有旋光性的混合物。
内消旋体——分子内存在两个以上不对称碳原子,但分子内部存在对称因素(旋光相互抵消),该物质无旋光性,它是一种纯物质。
(5)几何异构体——由于双键或环的存在,某些原子或基团在空间的排列方式不同而产生的异构现象。
(6)构造异构——指分子式相同而分子中原子或基团的连接次序不同的化合物。 (7)构型异构——指构造式相同而原子或基团在空间的排布方式不同的异构体。
(8)构象异构——由于单键的内旋转而产生的分子结构中原子或基团在空间的不同排列形象。 (9)消旋化——旋光性化合物在物理因素或化学试剂作用下变成两个对映体的平衡混合物,失去旋光性的过程。
4-1 如何用IR 光谱区别下列各组化合物。
(1)异戊烷分子中有异丙基,在1370—1380cm -1 的吸收峰分裂成两峰,强度接近; (2)在3000cm -1以上无吸收峰者为丁烷; (3)在3000—3100cm -1无吸收者为环已烷; (4)在3010cm -1附近有吸收峰者为甲叉基环已烷(亚甲基环已烷); (5)在3025cm -1附近和2720cm -1处有强吸收峰者为4-已烯醛; (6)在1060cm -1附近有强吸收峰者为正戊醇;
(7)在1750—1860cm-1出现两个峰,其中高频峰强于低频峰者为乙酐。 4-2 如何用1H-NMR 谱区分下列各组化合物?
(1)环丁烷只有一个单峰,而甲基环丙烷有四组吸收峰; (2)新戊烷只有一个单峰,而正戊烷有三组吸收峰;
(3)前者(1-氯-2-溴乙烷)有两组峰,而后者(1,2-二溴乙烷)只有一个单峰。
4-3 比较下面两化合物中所标出的质子在1H-NMR 谱中化学位移大小,并从低场到高场的
顺序排列。
(1)B →A →C →D ; (2)A →B →C 。
4-4 请将下列各化合物中画线的质子的化学位移按由低场至高场的顺序排列。 (2)→(1)→(3)。
4-6 请将下列各组化合物按紫外吸收波长由大到小的顺序排列。 (1) B →D →A →C ; (2) D →C →B →A 。 4-7根据NMR 谱推测下列化合物可能的构造式。
C CH 3
CH 3
H 3C
Br
CH 2OH
CH 3CH Br
CH 3
(1)
(2)
(3)(4)
CH 2CH 2CHCH 3Br
4-8某化合物的分子式为C 4H 8O,它的红外光谱在1715cm -1有强吸收峰,它的核磁共振谱有
一单峰,相当于三个H ,有一四重峰相当于二个H ,有一三重峰相当于三个H.。试写出该化合物的构造式。
CH 3CCH 2CH 3O
该化合物为丁酮,其构造式为
4-9根据光谱分析,分别推断下列各芳香族化合物可能的构造式。
(1)(2)(3)
CH 2CH 2CH 2Br CH 2CCH 3
O
C CH 3
CH 3
CH 3
4-11某化合物的分子式为C 4H 6O ,其光谱性质为:
UV 谱:在230nm 附近有吸收峰,κ>5000;
1
H-NMR 谱:δ=2.03(3H )双峰,δ=6.13(1H )多重峰,δ=6.87(1H )多重峰;
δ=9.48(1H )双峰;
IR 谱:在1720 cm -1 2720cm -1处有强吸收。 试推该化合物的构造式。
δ2.03
δ6.13
δ6.87δ9.48该化合物构造式为CH 3CH C H CHO
4-12根据光谱分析,分别推测下列各脂肪族化合物的构造式:
(1)分子式为C 3H 6O
UV 谱:210nm 以上无极大值;IR 谱:1080cm -1; 1
H-NMR 谱:δ=4.75(4H )三重峰,δ=2.75(2H )五重峰,J=7.1Hz 。 (2) 分子式为C 3H 7NO UV 谱:219nm(κ=60);IR 谱:3413cm -1,3236cm -1,1667cm -1; 1
H-NMR 谱:δ=6.50(2H )宽单峰,δ=2.25(2H )四重峰,δ=1.10(3H )三重峰,J=7.5Hz 。 (3) 分子式为C 4H 7N
UV 谱:219nm 以上无极大值;IR 谱:2273cm -1;
1H-NMR 谱:δ=2.82(1H )七重峰,δ=1.33(6H )双峰,J=6.7Hz 。 (4)分子式为C 8H 8O 2
UV 谱:270nm(κ=420);IR 谱:1725cm-1;
1H-NMR 谱:δ=11.95(1H )单峰;δ=7.21(5H )多重峰,δ=3.53(2H )单峰。
(2)(3)(4)
H 2C O H 2C CH 2
CH 3CH 2CONH 2
(CH 3)2CHCN
CH 2C O
OH
(1)
4-13化合
物分子式为C 4H 6O 2,其13C-NMR 谱如下图所示,推断其可能的构造。
H 2C
C H
C O
CH 312
3
4该化合物构造式为:O 4-14化合物A ,mp :21℃;元素分析:C :79.97%,H :6.71%,O :13.32%;MS 、IR 、NMR
谱如图所示,提出A 的结构式并解释三谱的归属。 答:A 为苯乙酮。结构式如下示。
CH 3
O
MS 图中m /z =120,是A 的分子离子峰,m /z =105是A 去甲基后离子峰,m /z =77是苯基离子峰。
IR 谱图中1750cm -1处的强吸收峰是羰基的伸缩振动峰,在1300cm -1附近分别为甲基中C —H 的弯曲振动和C —C 的弯曲振动峰。指纹区二个吸收峰(760cm -1、690cm -1)是C —H 的面外弯曲振动峰。
1
H-NMR 较高场的单重峰,对应的是CH 3—中3个H ,较低场对应的是苯环中的5个
H 。
第五章饱和烃
5-1 写出符合下列条件的C7H16的构造式,并各以系统命名法命名。
(1)庚烷(3)3-甲基已烷
(4)2,2-二甲基戊烷(5)2,3-二甲基戊烷(6)2,4-二甲基戊烷
(7)3,3-二甲基戊烷(8)3-乙基戊烷
5-2 写出下列烷基的名称及常用缩写符号。
(1)甲基(Me—);(2)乙基(Et—);(3)正丙基(n-Pr—);(4)异丙基(i-Pr—);(5)正丁基(n-Bu—);(6)异丁基(i-Bu—);(7)仲丁基(s-Bu—);
(8)叔丁基(t-Bu—)。
5-3 比较下列化合物沸点的高低,并说明原因。
(1) CH3(CH2)4CH3(2) (CH3)2CH(CH2)2CH3
(3)CH3CH2C(CH3)3(4) CH3CH2CH(CH3)CH2CH3
(1)>(4) >(2)>(3)同碳数的烷烃异构体,含支链越多,分子间作用力越弱,沸点越低。
5-4 完成下列反应式:
OSO3
H
Br
Br
(1)
HO2C(CH2)4CO2H
HNO3
+
(2)
Br
Br
-60℃
Br 2
+(3)
CH(CH 3)
2
CO 2H 2O
Cl
+Cl
Cl
Cl
碳正离子重排导致的产物
++
CH(CH 3)2Br
C(CH 3)2Br
+
(4)Br
HBr
(5)
5-5 比较下列化合物构象的稳定性大小。
1,4-二甲基环已烷的构象稳定性(1)<(2)。原因是(1)中的二个甲基均处于a 键上,而(2)中的二个甲基则皆处于e 键上,后者构象能量较低,较稳定。
3
H 3
3
CH 3
CH 3
H 3C
CH 3
(1)
(2)
5-6 下列异构体中哪个最稳定?
题目所示二甲基环已酮三个异构体对应的构象式如下,从中可看出(3)最稳定,因为其两个甲基均处于e 键上,体系能量较低。 O
O
O
(1)
(2)(3)
5-7 环丙烷内能高是由哪些因素造成的?
环丙烷分子中碳原子为不等性sp 3杂化,轨道重叠比开链烷烃的小,形成的碳碳共价键键能小(即有角张力),容易断裂,不如开链烷烃牢固;其次是环丙烷的三个碳原子共平面,
相邻两个碳原子上的C —H 键是重叠式构象,存在扭转张力。基于上述原因,导致环丙烷的内能较高。
5-8 用费歇尔(Fischer )投影式表示下列化合物的构型,并用R / S 标记手性碳的构型。
3H
CH 3
Br
H
CH 3
Br
D
2Cl
H 3
C
(1)(2)
(3)
三个化合物费歇尔投影式如下
CH 2Cl
D
H
3CH 3
H
Cl 2CH 3CH 3H Br CH 3
H
Br (1)
(2)(3)
S
S R
S
5-9 下列四个纽曼投影式表示的化合物,哪些是对映体?哪些是非对映体?哪些是同一化合
物的不同构象?
CH 3
H Cl 2H 5H
Br
H 32H 5
C 2H 5Br
H
H
3C Cl H
(1)
(4)(2)
(3)
32H 5C 2H H 332H 52H 5Br
H
CH 3Cl H
C 2H 5Br
H H Cl CH 3
2H 5Br H
CH 3H
Cl
CH 3
Cl H C 2H 5
H
Br C 2H 5
Br H CH 3
Cl
H H Cl H 3C C 2H 5H
Br
3H Cl
C 2H 5H
Br
CH 3
H Cl C 2H 5Br
H C 2H 5
H
Br Cl
H
CH 32H 5
H Br
CH 3Cl
H
(1)(2S ,3R )-2-氯-3-溴戊烷; (2)(2R ,3R )-2-氯-3-溴戊烷; (3)(2S ,3R )-2-氯-3-溴戊烷; (4)(2S ,3S )-2-氯-3-溴戊烷。
∴(2)和(4)是对映体;(2)和(1)或(3)、(4)和(1)或是非对映体;(1)和(3)
是同一化合物的不同构象。
5-10 写出环戊烷生成氯代戊烷的反应机理并画出链增长阶段的反应势能变化草图。在图上标明反应物、中间体、过渡态和生成物的结构。并指出哪一步是反应的控制步骤。 反应机理如下三式所示:
(1)(2)(3)Cl 2h υ或△Cl
2C 5H 10HCl C 5H 9+Cl
++C 5H 9Cl C 5H 9++Cl 2C 5H 9C 5H
9C 5H 9
Cl
+C 5H 9Cl
链引发
链增长
链终止
反应势能变化草图:
从反应势能草图中可看出,反应机理(2)中第一步即环戊基自由基生成步的活化能较大,所以是整个反应的速率控制步骤。
5-11 2,2,4-三甲基戊烷可以生成哪些碳自由基?按稳定性由大到小的顺序排列这些自由基。 可生成下列自由基。
CH 3
(CH 3)2CH
(CH 3)3C
(CH 3)2CHCH 2
(CH 3)3CCH 2H 2C
C H 2
C CH 3
CH 3
H
CH 3
CH 3
H 3C
C H C
CH 3CH 3
H
CH 3CH 3H 3C
C H 2
C CH 3CH 3
H
CH 3CH 2
H 3C
C H 2
C CH 3CH 3
C
CH 3
CH 3CH 3CHCH 2C(CH 3)3
其稳定性为:3°R ·>2°R ·>1°R ·>CH 3·
C 5H 10+Cl ?
C 5H 9Cl+Cl ?
C 5H 9?+HCl
中间体(自由基)
过渡态1
过渡态2
能量
5-12 下列反应 t -BuOCl + RH → RCl + t -BuOH 如果链引发反应为:
t -BuOCl → t -BuO·+ Cl· ,写出链增长反应。
(2)
+(1)RH
+t -BuOH
R
+t -BuOCl
R
RCl +t -BuO t -BuO
5-13甲烷在用光照进行氯代反应时,可以观察到如下现象,试用烷烃的氯代反应机理解释这些现象。
(1) 将氯先经用光照,然后立即在黑暗中与甲烷混合,可以获得氯代产物。
(2) 将氯气先经光照,,然后在黑暗中放置一段时间再与甲烷混合,则不发生氯代反应。 (3) 将氯气先经光照,,然后在黑暗中与氯气混合,也不发生氯代反应。
(1) Cl 2先用光照,产生氯自由基·Cl ,迅速在黑暗中与CH 4混合,Cl·来不及相互结合,可与甲烷产生连锁反应得到氯化产物。
(2) Cl 2通过光照射虽产生自由基·Cl.,但在黑暗中经过一段时间后,又重新结合成Cl 2,Cl 2再与甲烷混合时,由于无自由基存在,也无产生自由基条件,故不发生反应。
(3) 甲烷解离能较大,光照不足以产生自由基,黑暗中Cl 2也不产生自由基,故不发生反应。 5-14 回答下列问题。(1)为什么烷烃不活泼?(2)为什么在烷烃高温热解过程中,断裂的主要是C —C 键而不是C —H 键?(3)烷烃的燃烧是一个强烈的放热反应,但该反应并不在室温下发生。
(1)烷烃分子中只有C —C 键和C —H 键两种非极性σ键,σ键键能较大,化学性质稳定。 (2)经查表知C —C 键能347.3kJ·mol -1,而C —H 键能414.2kJ·mol -1,即前者键能较小,所以断裂的主要是C —C 键而不是C —H 键。
(3)由于其反应的活化能非常高,所以在室温下不易反应。
5-15 下列哪些化合物物可以用烷烃的卤代反应制备?哪些不适合?请说明理由。 (2)、(4)、(5)和(6)可用烷烃的卤代反应制备,而(1)和(3)不适合用烷烃的卤代反应制备。原因是(2)、(5)和(6)对应的烷烃各只有一种H ,它们发生卤代反应时,仅生成一种一卤代产物;(4)中氢虽然有两种H ,但其叔H 和伯H 被溴取代的活性相差1600倍,所以,它发生溴代时仍然可得到高产率的目标产物。而(1)对应的烷烃有5种H ,(3)对应的烷烃有11种H ,也即(1)和(3)对应的烷烃发生卤代反应会生成多种一卤代产物。 5-16 下列反应可以得到几种一溴代物(包括立体异构体)?如果伯氢和仲氢的反应速率比为1 :82,请估算各种产物的相对含量。
2
h υ
戊烷发生一溴代反应可得到3种构造异构产物。
(3)
(2)
(1)
H 3C
H 2
C
C H 2H 2C
2Br H 3C
H 2C
C H 2CH
CH 3Br H 3C
H 2C
CH H 2C
CH 3
*
其中(2)有一个手性碳,存在对映异构体。所以共有4种一溴代物。
1-溴戊烷
2-溴戊烷+3-溴戊烷
伯氢的总数
仲氢的总数
伯氢的相对活性
仲氢的相对活性
×
=6
6
1
82
×
=
1
82 =
1-溴戊烷的含量
=
=
1
1+82
×100% 1.2%
2-溴戊烷的含量=82
1+82×100%65.9% 2
3
=
3-溴戊烷的含量=82
1+82×100%32.9% 1
3
=
2-溴戊烷中R型和S型是等量的(消旋化),即各为32.9%。
目录lin 湛
第一章绪论 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。 答案: NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么? 答案: NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。因为两者溶液中均为Na+,K+,Br-, Cl-离子各1mol。由于CH4与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。 答案: 写出下列化合物的Lewis电子式。 答案: 下列各化合物哪个有偶极矩?画出其方向。 答案: 根据S与O的电负性差别,H2O与H2S相比,哪个有较强的偶极-偶极作用力或氢键? 答案: 电负性O>S,H2O与H2S相比,H2O有较强的偶极作用及氢键。 下列分子中那些可以形成氢键? b. CH3CH3 c. SiH4 d. CH3NH2 e. CH3CH2OH f. CH3OCH3 答案: d. CH3NH2 e. CH3CH2OH 醋酸分子式为CH3COOH,它是否能溶于水?为什么? 答案:能溶于水,因为含有C=O和OH两种极性基团,根据相似相容原理,可以溶于极性水。 第二章饱和烃 卷心菜叶表面的蜡质中含有29个碳的直链烷烃,写出其分子式。 答案:C29H60 用系统命名法(如果可能的话,同时用普通命名法)命名下列化合物,并指出(c)和(d)中各碳原子的级数。答案: a. 2,4,4-三甲基-5-正丁基壬烷5-butyl-2,4,4-trimethylnonane b. 正己烷 hexane ,3-二乙基戊烷 3,3-diethylpentane -甲基-5-异丙基辛烷5-isopropyl-3-methyloctane e.2-甲基丙烷(异丁烷)2-methylpropane(iso-butane) ,2-二甲基丙烷(新戊烷) 2,2-dimethylpropane(neopentane)
有机化学总结 一.有机化合物的命名 1. 能够用系统命名法命名各种类型化合物: 包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。 2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。 立体结构的表示方法: 1 )伞形式:COOH OH 3 2)锯架式:CH 3 OH H H OH C 2H 5 3) 纽曼投影式: 4)菲舍尔投影式:COOH 3 OH H 5)构象(conformation) (1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠 式。 (2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象 是全重叠式。
(3)环己烷构象:最稳定构象是椅式构象。一取代环己烷最 稳定构象是e取代的椅式构象。多取代环己烷最稳定构象是e 取代最多或大基团处于e键上的椅式构象。 立体结构的标记方法 1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个 优先的基团在同一侧,为Z构型,在相反侧,为E构型。 CH3 C C H C2H5CH3 C C H 2 H5 Cl (Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯 2、顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。 CH3 C C H CH3 H CH3 C C H H CH3 顺-2-丁烯反-2-丁烯 33 3 顺-1,4-二甲基环己烷反-1,4-二甲基环己烷 3、R/S标记法:在标记手性分子时,先把及手性碳相连的四个 基团按次序规则排序。然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R构型,如果是逆时针,则为S构型。 a R型S型 注:将伞状透视式及菲舍尔投影式互换的方法是:先按要求书写其透视式或投影式,然后分别标出其R/S构型,如果两者构型相同,则为
高等有机化学习题 第一章 化学键 一、用共振轮说明下列问题 1) 联本中的C 1-C 2键长为什么比乙烷中的键长短?联苯的硝化反应为什么主要发生在2-位 和4-位? 联苯的共振结构式可表是如下: (1) 由共振结构式可以看出C 1-C 2键有双键结构的贡献,故比乙烷的C 1-C 2键短。 (2) 由共振结构式可以看出邻对位负电荷相对集中,故有利于发生硝化反应。 2) 方酸为什么是强酸?(强于硫酸) 方酸的共振结构式可表是如下:对吗? 由方酸的共振结构式可以看出方酸的电子离域效果更好。 二、试推测6,6-二苯基富烯的亲电取代发生于哪个环,哪个位置?亲核取代发生于哪个环, 哪个位置? 6,6-二苯基富烯的共振式如下: 由6,6-二苯基富烯的共振式可以看出,亲电取代发生在五元环的2位上,而亲核取代 发生在苯环的2位上。 三、计算烯丙基正离子和环丙烯正离子π分子轨道的总能量,并比较两者的稳定性。 烯丙基正离子有两个电子在成键轨道上其总能量为 E 烯丙基正离子=2E 1=2(α+1.414β)=2α+2.828β 11' O HO O O O OH O O O OH O O O HO O O O S O O HO O S O O OH O S O O O S O O OH
环丙烯正离子有两个电子在成键轨道上其总能量为 E 环丙烯正离子=2E 1=2(α+2β)=2α+2β 能量差值为 E 烯丙基正离子- E 环丙烯正离子=(2α+2.828β)- (2α+2β)=0.828β 因此,环丙烯正离子比烯丙基正离子稳定。 四、用HMO 法分别说明烯丙基负离子和环丙烯负离子的电子排布和成键情况,并比较两者 稳定性。 五、简要说明 1)吡咯和吡啶分子的极性方向相反,为什么? 吡咯分子中氮原子给出一对为共用电子参与了共轭分子的大π键,也就是电子从氮原子流向五员环,而吡啶分子中氮原子只拿出一个电子参与共轭,并且氮原子的电负性大于碳原子使电子流向氮原子的方向。因此,两个分子的极性正好相反。 2)富烯分子为什么具有极性?其极性方向与环庚富烯的相反,为什么? 富烯分子中环外双键的流向五员环形成稳定的6π体系的去向,从而环外双键中的末端碳原子带有部分正电荷,五员环接受电子后变成负电荷的中心,因此分子具有极性。 N N H 能级 烯丙基负离子 环丙基负离子 α+1.414β α+2β E=2(α+1.414β)+2α-2(α+2β)-2(α-β) = 2α+2.828β+2α-2α-4β-2α+2β =1.172β
(十三) 将下列的自由基按稳定性大小排列成序。 ⑴ 3 ⑵ CH 3CHCH 223 ⑶ CH 3CCH 2CH 33 ⑷ CH 3CHCHCH 33 解:自由基的稳定性顺序为:⑶>⑷>⑵>⑴ (一) 完成下列反应式: (3) (CH 3)2C=CH 2 + Br 2 (CH 3)2C CH 2Br Br (CH 3)2C CH 2Cl Br (CH 3)2C CH 2OH Br + + (4) CH 3CH 2C CH CH 3CH 2CH 2 CHO CH 3CH 2C CH OH H 3222- (5) CH 3+ Cl 2 + H 2O CH 3 OH Cl CH 3 Cl OH + (6) 33 CH 3CH 3 (1) 1/2(BH )22 (7) CH 3 CH 2 Cl 500 C o (A) (B) CH 3 CH 2 Cl HBr ROOR CH 3 CH 2Br Cl (9) CH 3CH 2C CH + H 2O 4 H 2SO 4 CH 3CH 2 CH 3 O (10) COOH + CH 3COOH 4 CH=CHCH 3 (12) Br + Br 2o (13) Br + NaC CH (14) C=C C 6H 5 C 6H 5 H H 33 C O H 6H 5 H C 6
(六) 在下列各组化合物中,哪一个比较稳定?为什么? (1) (A) H H CH(CH 3)2 CH 3 , (B) C=C H CH(CH 3)2 H CH 3 (2) (A) CH 3 , (B) CH 3 (3) (A) , (B) , (C) (4) (A) , (B) (5) (A) , (B) , (C) 。 (6) (A) CH 3 , (B) CH 2 (七) 将下列各组活性中间体按到稳定性由大小排列成序: (1) CH 3CHCH 3 Cl 3CCHCH 3 (CH 3)3C (A)(B)(C) (2) (CH 3)2CHCH 22(CH 3)22CH 3(CH 3)23(A)(B)(C) 解:(1)C >A >B (2)B >C >A (八) 下列第一个碳正离子均倾向于重排成更稳定的碳正离子,试写出其重排后碳正离子的结构。 (1) CH 3CH 2CH 2 (2) (CH 3)2CHCHCH 3 (3) (CH 3)3CCHCH 3 (4) CH 3 (1) CH 3CHCH 3 (2) (CH 3)2CCH 2CH 3 (3) (CH 3)2CCH(CH 3)2 (4) CH 3 (4) (CH 3)2C=CHCH 2CHCH=CH 2 CH 3 + CH 3 CH 3 CH 3 解: (CH 3)222CHCH=CH 23 + (CH 3)2C=CHCH 2CHCH=CH 2 CH 3
烷烃 1.用系统命名法命名下列化合物: 1.(CH 3)2CHC(CH 3)2 CHCH 3 CH 32. CH 3CH 2CH CHCH 2CH 2CH 3 CH 3CH(CH 3)2 2,3,3,4-四甲基戊烷 2,4-二甲基-3-乙基己烷 3. CH 3CH 2C(CH 3)2CH 2CH 3 4.CH 3CH 3CH 2CHCH 2CH 2CCH 2CH 3 CHCH 3CH 3 CH 2CH 3 1 2 3 4 5 6 7 8 3,3-二甲基戊烷 2,6-二甲基-3,6-二乙基辛烷 5.1 2 3 4 5 6 7 6 . 2,5-二甲基庚烷 2-甲基-3-乙基己烷 7 . 8. 1 2 3 4 5 67 2,4,4-三甲基戊烷 2-甲基-3-乙基庚烷 2.写出下列各化合物的结构式: 1.2,2,3,3-四甲基戊烷 2,2,3-二甲基庚烷 CH 3 C C CH 2CH 3 CH 3 CH 3CH 3 CH 3CH 3 CH 3CHCHCH 2CH 2CH 2CH 3 CH 3 3、 2,2,4-三甲基戊烷 4、2,4-二甲基-4-乙基庚烷 CH 3 C CHCH 3CH 3CH 3 CH 3 CH 3CHCH 2CCH 2CH 2CH 3 3 CH 3CH 3 5、 2-甲基-3-乙基己烷 6、三乙基甲烷 CH 3 CH 3CHCHCH 2CH 2CH 3 2CH 3 CH 3CH 2CHCH 2CH 3 2CH 3 7、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷
CH 3CHCH(CH 3)2 2CH 3 CH 3CH 2CH C(CH 3)3 CH 2CHCH 3 CH 3 3.用不同符号表示下列化合物中伯、仲、叔、季碳原子 3 CH 2 C CH 3 2CH 3C CH 3CH 3 1. 1 1 1 1 1 1 2CH 3 4 02. 4 03 1 1 323)33 4. 2. 3. 4. 5. 6. 1. 5.不要查表试将下列烃类化合物按沸点降低的次序排列: (1) 2,3-二甲基戊烷 (2) 正庚烷 (3) 2-甲基庚烷 (4) 正戊烷 (5) 2-甲基己烷 解:2-甲基庚烷>正庚烷> 2-甲基己烷>2,3-二甲基戊烷> 正戊烷 (注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。)
化学专业函授本科 《高等有机化学》试卷 A 题号 一 二 总分 统分人 复核人 得分 一. 回答下列问题(每题4分,15题,共60 分): 1. 下列分子哪些能形成分子内氢键?哪些能形成分子内氢键? A 、 NO 2COOH B 、 N H C 、F OH D 、 F OH 2. 举例说明由sp 2杂化方式组成的碳—碳三键。 3. 写出下列化合物的最稳定构象: a. OH CH(CH 3)2 H 3C H H H b. FCH 2 CH 2OH 4. 利用空间效应,比较下列物质消除反应的速率大小。 得分 阅卷人 系 专业 层次 姓名 学号 ┉┉┉┉┉┉┉┉┉密┉┉┉┉┉┉┉┉┉┉封┉┉┉┉┉┉┉┉┉┉线┉┉┉┉┉┉┉┉┉┉
A、OH B、 OH C、 OH D、 OH 5. 比较下列各组化合物的酸性大小。(1) A、COOH NO2B、 COOH OCH3C、 COOH OCH3D、 COOH NO2 (2) A、OH NO2B、 OH OCH3C、 OH OCH3D、 OH NO2 (3)
A 、NH 2NO 2 B 、 NH 2 OCH 3 C 、NH 2 OCH 3D 、NH 2 NO 2 (4) A 、 CH 3 NO 2 B 、 CH 3 OCH 3 C 、CH 3 OCH 3 D 、CH 3 NO 2 6. 下列化合物酸性最弱的是? OH NO 2 OH NO 2 OH NO 2 OH A B C D 7. 下列醇与卢卡斯试剂反应活性最高的是? A CH 3CH 2CH 2CH 2OH B CH 3CH(OH)CH 2CH 3 C (CH 3)2CHCH 2OH D (CH 3)3COH 8. 下列物种中的亲电试剂是: ;亲核试剂 是 。
高等有机化学习题及期末复习 一、回答下列问题:(22小题,1-14每题1分,15-22,每题2分,共30分) 1. 亲核反应、亲电反应最主要的区别是( ) A. 反应的立体化学不同 B. 反应的动力学不同 C. 反应要进攻的活性中心的电荷不同 D. 反应的热力学不同 2. 下列四个试剂不与 3-戊酮反应的是( ) A. RMgX B. NaHSO3饱和水溶液 C. PCl3 D. LiAlH4 3.指出下列哪一个化合物(不)具有旋光性? 4. 区别安息香和水杨酸可用下列哪种方法 A. NaOH(aq) B. Na2CO3(aq) C. FeCl3(aq) D. I2/OH-(aq) 5. 比较下列化合物的沸点,其中最高的是 6. 指出下列哪一个化合物的紫外吸收光谱波长最短( ) 7.下列化合物在常温平衡状态下,最不可能有芳香性特征的是( ) 8.下列含氧化合物最难被稀酸水解的是( ) 9. 二环乙基碳亚胺(DCC)在多肽合成中的作用是( )
A. 活化氨基 B. 活化羧基 C. 保护氨基 D. 保护羧基 10. 比较下列化合物在 H2SO4中的溶解度( ) 11. 下列关于α-螺旋的叙述,错误的是( ) A. 分子内的氢键使α-螺旋稳定 B. 减少 R 基团间的不同的互相作用使α-螺旋稳定 C. 疏水作用使α-螺旋稳定 D. 在某些蛋白质中α-螺旋是二级结构的一种类型 12. 比较苯酚(I)、环己醇(II)、碳酸(III)的酸性大小 A. II>I>III B. III>I>II C. I>II>III D. II>III>I 13.1HNMR 化学位移一般在 0.5-11ppm,请归属以下氢原子的大致位置: A. -CHO B. -CH=CH C. -OCH3 D. 苯上 H 14. 按沸点由高到低排列的顺序是:()>()>()>()>()。 a. 3–己醇; b. 正己烷; c. 2–甲基–2–戊醇; d. 正辛醇; e. 正己醇。 15. 指出下列化合物中标记的质子的酸性从大到小的顺序: 16. 指出小列化合物的碱性大小的顺序: 17. 下面几种酒石酸的立体异构体熔点相同的是: 18. 用箭头标出下列化合物进行硝化反应时的优先反应位置: 19. 下列化合物那些有手性?
《有机化学》习 题 解 答 ——陈宏博主编. 大连理工大学出版社. 2005.1第二版 第一章 1-1 有机化合物一般具有什么特点? 答:(1)有机化合物分子中,原子之间是以共价键相连; (2)在有机化合物中,碳原子之间以及碳原子和其他非金属原子之间可形成不同类型共价键;两碳原子间可以单键、双键或叁键相连,碳原子间可以是链状,也可以是环状,且分子骨架中可以掺杂其他元素的原子; (3)大多数有机物不易溶于水,易燃烧;液体易挥发;固体熔点低; (4)有机化合物的化学反应速率一般较小;有机反应常伴有副反应。 1-2 根据键能数据,判断乙烷分子CH 3CH 3在受热裂解时,哪种共价键易发生平均断裂? 答:在乙烷分子中,C –C 间键能为347.3 kJ /mol, 而C –H 间键能为414.2 kJ /mol. 由于C –C 间键能小于C –H 间键能,所以乙烷受热裂解时,C -C 键易发生平均断裂。 1-3根据电负性数据,以δ+或δ-标注形成下列极性共价键的原子上所带的部分正电荷或负电荷。 O -H , N -H , H 3C -Br , O ═C ═O ,C ─O , H 2C ═O 答: + - -δδH O + --δδH N - + -δδBr C H 3 - +-==δδδO C O - +=δδO C H 2 1-4 指出下列化合物的偶极矩大小次序。 CH 3CH 2Cl, CH 3CH 2Br, CH 3CH 2CH 3, CH 3C ≡N, CH 3CH ≡CH 2 答: CH 3 C ≡N > CH 3CH 2Cl > CH 3CH 2Br > CH 3CH=CH 2 > CH 3CH 2CH 3 1-5 解释下列术语。 键能,键的离解能, 共价键,σ键,π键,键长,键角,电负性,极性共价键,诱导效应,路易斯酸(碱), 共价键均裂,共价键异裂,碳正离子,碳负离子,碳自由基,离子型反应,自由基型反应 答案略,见教材相关内容 1-6 下列各物种,哪个是路易斯酸?哪个是路易斯碱? (C 2H 5)2O ,NO 2 ,+CH 3CH 2 ,NH 3BF 3 ,,..CH 3CH 2 +AlCl 3 , I - ,H 2O .. .. : CH 3CH 2OH .. .. H 3+O , , NH 4+,, NC -HC C -Br + , Br - HO - , SO 3 ,CH 3SCH 3.... , C 6H 5NH 2 ,..(C 6H 5)3P . . 答: 路易斯酸: BF 3 ,NO 2 ,CH 3CH 2 ,AlCl 3 , H 3O , NH 4 , SO 3 , Br ++ + + +
ProblemⅠ Write the IUPAC name for the following structures 1.4-Ethyl-5-methyl octane 2.5-(3-Pentenyl)-3,6,8-decatriene-1-yne 3.Bicyclo[12,2,2]octadeca-14,16(1)diene 4.5-methyl spiro[2,4]heptane 5.4-Phenyl-2-naphthol 6.1-methyl-1,2-ethanediol 7.Magnesium di(1-propanolate) 8.2-Hexen-4-ynedioic acid 9.2,4,5-trioctanetriane 10.Methyl 3-ethyl-5-phenyl heptanoate 11.5,9,12,15,21-pentaoxaheptacosane-1,27-diol 12.1,2-Cyclohexane dicarboxylic anhydride 13.azocine 14.6H-1,2,5-Thidiazine 15.N-Methyl-N-propylpentylamine OR Methyl penthyl propyl ammonium 16.1H-pyrazolo[4,3-d]oxazole 17.4H-[1,3] oxathiolo[4,5-b]pyrrole Write the systematic name for the following structures 18.azine Hexahydrozine azole azolidone 1,2-Diazine 1,3-Diazine 1,3-Diazole 1,2-oxazole oxin Thiole ProblemⅡ Write the systematic name for the following structures 1.3-bromo-2-(propenyl)-2,4-hexadienoic acid 2.1-Ethoxy-6-octen-1-yne-3,5-dione 3.4-chloro-2-methyl-2-cyclohexenol 4.(2-methyl)butyl 3-bromo-2-hydroxy-2-methyl 3-butenate 5.1,3,5-Naphthalene triacetic acid 6.5-(4-Hydroxy-1-butynyl)-2-nonen-6-yne 7.2-Amino-5-bromo diphenylamine 8.4,5-Dichloro-2-(4-chloro-2-hydroxy methyl-5-oxo-3-hexenyl)-1-cyclohexane carboxylic acid 9.N-(2,3-Dimethybutyl)-3,5-dihydroxy-3-ethyl pentanamide 10.2-Ethyl-4-ethyl amino-2-methyl-3-oxobutanal 11.2-hydroxy-1-(2-hydroxy-5methyl-1-phenylazo) Naphthalene-4-sulfonic acid 12.Methyl 3-{4-[2-hydroxy-3-(1-methyl ethyl)amino propoxy]}benzenepropanoate
第一章 绪 论 问题一参考答案 H 2N C NH 2 O C 6H 6Cl 6 C 14H 30 CS 2 C 5H 10O 5 NaHCO 3 CaC 2 有机物质: 无机物质: 1-1 1-2 醋酸能溶于水,1-庚烯和硬脂酸能溶于苯。 CH 2C CH 2 CH 3CH 2CH CH C CH CH 3CH CH 3 CH CH 2 sp 2 sp sp 2 sp 3 sp 3 sp 2 sp 2 sp sp sp 3 sp 3sp 3 sp 2 sp 2 1-3 1-4 CO 2分子中,虽然碳-氧键为极性键,但由于分子几何形状为线型,单个键矩相互抵消:O C O ,所以μ=0。 1-5 价线式 简化式 缩写式 H C C C C H H H CH 3CH 2 CH CH 2CH 3CH 2CH CH 2H C C C C H H H H H H H CH 3 CH CH CH 3 CH 3CH CHCH 3 C C C C H H H H H H H H H 2C H 2C 2 CH 2C C C H H H H C H H C H 2C CH 2 H 2 1-6 酸性次序为:H 3O + >NH 4+ >CH 3OH >CH 3NH 2 习题一参考答案 1. (1) sp 3 (2) sp (3) sp 2 (4) sp (5) sp 3 (6)sp 2 2. (1),(3),(6)互为同分异构体;(2),(4),(5),(7)互为同分异构体。 3. (1)醇类 (2)酚类 (3)环烷烃 (4)醛类 (5)醚类 (6)胺类 4.π键的成键方式:成键两原子的p 轨道沿着与连接两个原子的轴垂直的方向“肩并肩”重叠而形成。π键特点:①电子云平面对称;②与σ键相比,其轨道重叠程度小,对外暴露的态势大,因而π键的可极化度大,在化学反应中易受到亲电试剂的进攻而发生共价键的异裂;③由于总是与σ键一起形成双键或叁键,所以其成键方式必然限制σ键单键的相对旋转。 5. (1) (2) (5)易溶于水;(5) (4) (6)难溶于水。 6.C 6H 6 7.C 3H 6F 2 8. (1) (2) (3)(4) H 3C O CH 3 (5)(6) Cl C Br H C H 3C H O C 2H 5
第二章 烷烃作业参考答案 1、 共有九种: CH 3-CH 2-CH 2-CH 2-CH 2-CH 2-CH 3 CH 3-CH-CH 2-CH 2-CH 2-CH 3 2CH 3-CH 2-CH-CH 2-CH 2-CH 3 3CH 3-CH-CH-CH 2-CH 3 3CH 3CH 3-CH-CH 2-CH-CH 3 CH 3 CH 3 CH 3-C-CH 2-CH 2-CH 3 CH 3 CH 3 CH 3-CH 2-C-CH 2-CH 3 CH 3 CH 3-CH 2-CH-CH 2-CH 2 CH 2-CH 3 CH 3-C 3 CH 3CH-CH 3 CH 3 2、(1)3-甲基戊烷 (2)2,5-二甲基-3,4-二乙基己烷 (3)2,2,3,4-四甲基戊烷 (4)2-甲基-5-乙基庚烷 (5)2-甲基-3-环丁基丁烷 (6)顺-1-甲基-3-乙基环戊烷(7)反-1-甲基-4-乙基环己烷 (8)1-甲基-4-乙基-3-叔丁基环己烷 3、(1) (2) CH 3-CH-CH 2-CH 2-CH 3 3 CH 3-C-CH 2CH 3H 3 C H 3 (3) (4) CH 3-CH-CH-CH-CH-CH 3 3CH 3CH 2 CH 3 2CH 3 3)3 4、(1) (2) CH 3CH 2-C CH 3 CH-CH 3 CH 3 CH 3-C-CH-CH-CH 33CH 3 3 CH 3-CH-C-CH 2-CH 3CH 3CH 3CH 3 CH 3-C-CH 2-CH-CH 3 CH 3CH 3 CH 3 5、(1)错。改为:2,2-二甲基丁烷 (2)错。改为:2,2,5-三甲基-4-乙基己烷 (3)正确 (4)错。改为:2,2-二甲基丁烷
有机化学总结 一.有机化合物的命名 1. 能够用系统命名法命名各种类型化合物: 包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COO H>-S O3H>-CO OR>-C OX>-CN>-C HO>>C =O>-OH(醇)>-OH(酚)>-SH >-N H2>-OR >C=C >-C ≡C->(-R >-X >-NO 2),并能够判断出Z/E构型和R/S 构型。 2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fis ch er 投影式)。 立体结构的表示方法: 1 )伞形式:COOH OH 3 2)锯架式:CH 3 H H OH 2H 5 3) 纽曼投影式 : 4)菲舍尔投影 式:COOH 3 OH H 5)构象(c onforma tion)
(1)乙烷构象:最稳定构象是交叉式,最不稳定构象 是重叠式。 (2)正丁烷构象:最稳定构象是对位交叉式,最不稳 定构象是全重叠式。 (3)环己烷构象:最稳定构象是椅式构象。一取代环 己烷最稳定构象是e取代的椅式构象。多取代环己烷最稳定构象是e取代最多或大基团处于e键上的椅式构象。立体结构的标记方法 1.Z/E标记法:在表示烯烃的构型时,如果在次序规则 中两个优先的基团在同一侧,为Z构型,在相反侧, 为E构型。 CH3 C C H C2H5CH3 C C H 2 H5 Cl (Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯 2、顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。 CH3 C C H CH3 H CH3 C C H H CH3 顺-2-丁烯反-2-丁烯 33 3 顺-1,4-二甲基环己烷反-1,4-二甲基环己烷 3、R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R构型,如果是逆时针,则为S构型。
有机反应机理的研究 3.1解释下列化合物的酸碱性大侠 (1) N N N(CH 3)2 PKa 10.58 7.79 5.06 A. B. C. (2)CO 2H OH A. 酸性 CO 2H B. > 3.2 CH 2 C N 3 Ph △ H 2CPh N C O 在上式所示的Curtius 重排中。PhCH 2—基从C 上前与至N ,试设计一个实验考察P —是完全从C 上断裂形成了两个碎片,然后再结合起来,还是PhCH 2—总保持键合状态。 3.3 硝基甲烷在醋酸根离子存在时很容易与溴生成α—溴硝基甲烷,而用完全氘代的化合物CD3NO2反应时,反应速率比原来慢6.6倍,你认为该反应的速率决定步骤是哪一步?试写出反应机理。 3.4对反应:PhCH 2Cl+OH -→PhCH 2OH+Cl - 可提出下列两种机理,请至少设计两种不同的实验帮助确定实际上采用的是哪种机理。 C H PhCH 2OH Cl- + SN 2第一步: SN 1:第二步:PhCH 2慢 PhCH 2 + OH- PhCH 2OH 注意:由一个烃基或芳基取代CH 2中一个或两个H 是难以接受的,因为这样可能使机理完全改变。 3.5 X COCH 3 + Br 2 H + HBr X COCH 2Br + (1) σ=-0.45;(2)反应数与[Br 2]无关;(3)取代基X 的+I 效应加速反应 (4)反应不受光火有机过氧化物的影响。
试按以上给出的条件设计合理的反应历程。 3.6 α—醋酸—对硝基乙烯的水解是酸催化反应 OCOCH 3 NO 2 C CH 2 O NO 2 C CH 3 H 2O + CH 3CO 2H 在6%的硫酸中,动力学同位素效应k (H2O )/k (D2O )是0.75,多少69%的硫酸中,动力学同位素效应改变为3.25,试推测此反应的机理。 3.7 下列反应: H 3C SO 2OCH 3 LiX + CH 3X DMF 3C SO 3Li 相对反应速率分别为:Cl-(7.8)>Br-(3.2)>I-(1.0),若分别在上述反应中加入9%的水,在与LiCl 反应,反应速率比不加水时慢24倍,而与KI 反应,反应速率只慢2倍,试解释之。 3.8 2,2—二甲基—4—苯基—3—丁烯酸进行热脱羧反应,得到2—甲基—4—苯基—2—丁烯和二氧化碳。 CH CMe 2CO H HCPh H 2CPh CH CMe 2 + CO 2 a b c 在a 位上用D 取代H ,观察到同位素效应k H /k D =2.87,同样,在b 位上碳的同位素效应k 12/k 14=1.035(对碳而言,这是大值),这些现象如何说明脱羧反应是协同机理,试拟定一个可能的过渡态。 答案: 3.1(1)A 中氮上的孤电子对,使其具有碱性。 B 中氮上孤电子对,可与苯环共轭,碱性变小。 C 中氮上孤电子对,与苯环共轭的同时和氮相连的两个甲基使氮上孤电子对不裸露, 碱性比B 稍小。 (2) 因为A 中COOH 与OH 形成分子内氢键,酸性较大。即: O C O OH 3.2使用一个光活性的迁移基团,如在PhCH (CH 3)CON 3中,若消旋化意味着该基团完全 断裂离去。构型保持则意味着不是这样(后者是真实的结果)。 3.3重氢化合物反应更慢,因为C —D 键比C —H 键更强,这时决定速率的步骤应是硝基甲烷的电离,醋酸根负离子可以作为催化这步反应的碱,然后是硝基甲烷负离子与溴的快速反应。 CH 3NO 2+CH 3COO--CH 2NO 2+CH 3COOH -CH 2NO 2 + Br 2快 CH 2BrNO 2 + Br-
华东理工大学有机化学 课后答案 Pleasure Group Office【T985AB-B866SYT-B182C-BS682T-STT18】
部分习题参考答案 2-1 (5) 顺-1,2-二溴环己烷 (6) (7) 5-甲基螺[]辛烷 2-4 (3)>(2)>(5)>(1)>(4) 2-6 (1) 正丙基(n-Pr-) (2)异丙基(i-Pr-) (3) 异丁基(i-Bu-) (4)叔丁基(t-Bu-) (5)甲基(Me-) (6) 乙基(Et-) 2-7 (3) CH3CH2CH(CH3) 2 (4) (CH3)4C 2-8(3)、(6)等同;(2)、(5)构造异构;(1)、(4) 构象异构 2-9(1) 用Br2。因氢原子活性有差异,溴原子活性适中,反应选择性强,主要得到 CH3 Br。 (2) 用Cl2。只有一种氢,氯原子反应活性高。 2-10 CH3CH2·的稳定性大于CH3·,易于生成。 2-112,3-二甲基丁烷有四个典型构象式,2,2,3,3-四甲基丁烷有二个;前者最稳定的构象 式为 3 H3 。 2-16(4)>(2)>(3)>(1) 4-4 4-5(1) (2) 2,3-二甲基-2-丁烯>2-甲基-2-戊烯>反-3-己烯>顺-3-己烯>1-己烯 (3)2-甲基-1-丙烯快(形成叔碳正离子) 4-6(1)亲电加成反应,中间体为碳正离子,有重排 (2)甲醇与碳正离子结合;直接失去质子而形成醚 5-9 (1)Br2/CCl4;Ag(NH3)2NO3,(2)顺丁稀二酸酐; Ag(NH3)2NO3, 5-11 5-12 6-1 (a) C3H7NO (b) C2H3OCl
部分习题参考答案 2-1 (5) 顺-1,2-二溴环己烷 (6) 1,7,7-三甲基二环[2、2、1]庚烷 (7) 5-甲基螺[3、4] 辛烷 (8) (9) C C C C CH 3CH 3CH 3 CH 3 H 3H 3 (10) (CH 3)2CHCH 2CH 2CH 3 (11) 2-4 (3)>(2)>(5)>(1)>(4) 2-6 (1) 正丙基(n -Pr-) (2) 异丙基(i -Pr-) (3) 异丁基(i -Bu-) (4) 叔丁基(t -Bu-) (5)甲基(Me-) (6) 乙基(Et-) 2-7 (3) CH 3CH 2CH(CH 3) 2 (4) (CH 3)4C 2-8 (3)、(6)等同;(2)、(5)构造异构;(1)、(4) 构象异构 2-9 (1) 用Br 2。因氢原子活性有差异,溴原子活性适中,反应选择性强,主要得到 CH 3 Br 。 (2) 用Cl 2。只有一种氢,氯原子反应活性高。 2-10 CH 3CH 2·的稳定性大于CH 3·,易于生成。 2-11 2,3-二甲基丁烷有四个典型构象式,2,2,3,3-四甲基丁烷有二个;前者最稳定的构象式为 3H 3。 CH(CH 3)2 CH 3 33)2 ( 顺 ) > ( 反 ) (2) 2-13 3)2 3 3)2 CH 3 (1) H 3 H 3(2) < >2-15 2-16 (4)>(2)>(3)>(1) 4-4 (7) H OH CH 3 OH CH 3 C 2H 5 HO H HO CH 3 CH 3 C 2H 5 (8) (CH 3)2CHC O H 3C O O CHCH 3 (CH 3)2CHC O CH 3 O CHCH 3
《高等有机化学》模拟考试题(二) 一.填空 1、几种重要的有机反应活性中间体有------、 ----------、---------、--------、--------和---------。 2、萘磺化时,得到α-萘磺酸是-------控制产物,得到β-萘磺酸是------控制产物。 3、写出下列化合物最稳定的构象式: (1) HOCH 2CH 2F 用Newman 投影式表示为:------------; (2)反式十氢化萘 用构象式表示为:--------; (3)(S)-2-丁醇 用Fischer 投影式表示为:-----------; 4、α-蒎烯1H 3C CH 32 中1和2两个甲基上的亲核化学位移δ值较小者为 --------;这是由于----------所致。 5、 下列烷氧基负离子:(a ) C 6H 5O -,(b )CH 3CH 2CH 2CH 2O -,(c )(CH 3)3CO -,其中碱性最强的是---------,亲核性最强的是---------。 6、有机光化学反应中,分子的激发态常有-------和----------两种。但大多数光化学反应是按-----------进行的。在二苯甲酮与异丙醇的光化学反应中,当加入萘时,该反应中止,反应中的二苯甲酮是---------剂,而萘是二苯甲酮激发态的一种-------剂。 二.写出写列反应的主要产物 C C Ph H 3C CH 3 Ph H + 1 N(CH 2 )OH CH 3 2. C N CH 3OH H 2SO 4 3. OH H 3CO 2SO C O H 3C 4. 3 5. COCHN 2 1)Ag 2O 2) H 2O 6. CH 3 H 3C OCH 2CH=CHCH 3 7. C C 3 OTs H 3C CH 3CH 2ONa 328.
高等有机化学习题(2) Problem Ⅲ 1. Calculate △H θ for the reaction CH 3 +Cl F CH3Cl + F △ H θf (Cl-F) = - 51.1 KJmol -1 2. The following reaction was described as a first-order reaction .Suggest a reaction mechanism. C 6H 5 C 6H 5 C C NC NC CN CN +C 6H 5 6H 5 CN CN CN CN 3. The following reaction was described as a second-order reaction. Suggest a reaction mechanism. C 6H 5N NH C 6H 6 N 2 + 4. Suggest a reaction mechanism for the reaction. NH 2 2 NH 2 CH 3 Cl CH 3 + CH 3 5. The κH and κD of following reaction was determined. (CH 3)2CHBr (CD 3)2CHBr C 2H 5ONa 25℃ Alkene κH =1.76 sec -1κD =0.26 sec -1 (1) Calculate the isotopic effect. (2) Suggest a reaction mechanism. 6. Compare the each of the following pairs of reaction. Which reaction was more negative entropy of activation? (1) A + COOH COOH COOH COOH B C CH 2 H 3C H 3C 2 C CHC(CH 3)3 H 3C H 3C
第一章 绪论习题参考答案 1. 某化合物的分子量为60,含碳%、含氮%、含氧%,确定该化合物的分子式。 解:① 由各元素的百分含量,根据下列计算求得实验式 1:2:133.3:7.6:34.3162 .53:17.6:121.40== 该化合物实验式为:CH 2O ② 由分子量计算出该化合物的分子式 216 121260 =+?+ 该化合物的分子式应为实验式的2倍,即:C 2H 4O 2 2. 在C —H 、C —O 、O —H 、C —Br 、C —N 等共价键中,极性最强的是哪一个? 解:由表1-4可以查得上述共价键极性最强的是O —H 键。 3. 将共价键⑴ C —H ⑵ N —H ⑶ F —H ⑷ O —H 按极性由大到小的顺序进行排列。 解:根据电负性顺序F > O > N > C ,可推知共价键的极性顺序为: F —H > O —H > N —H > C —H 4. 化合物CH 3Cl 、CH 4、CHBr 3、HCl 、CH 3OCH 3中,哪个是非极性分子? 解:CH 4分子为高度对称的正四面体空间结构,4个C —H 的向量之和为零,因此是非极性分子。 5. 指出下列化合物所含官能团的名称和该化合物所属类型。 CH 3 OH (2) 碳碳三键,炔烃 羟基 ,酚 (4) COOH 酮基 ,酮 羧基 ,羧酸 (6) CH 3CH 2CHCH 3 OH 醛基 ,醛 羟基 ,醇 (1) CH 3CH 2C CH (3) CH 3COCH 3 (5) CH 3CH 2CHO
(7) CH3CH2NH2 氨基,胺 6. 甲醚(CH3OCH3)分子中,两个O—C键的夹角为°。甲醚是否为极性分子?若是,用 表示偶极矩的方向。 解:氧原子的电负性大于碳原子的电负性,因此O—C键的偶极矩的方向是由碳原子指向氧原子。甲醚分子的偶极矩是其分子中各个共价键偶极矩的向量之和,甲醚分子中的两个O—C键的夹角为°,显然分子是具有极性的,其偶极矩的方向如下图所示。 3 7. 什么叫诱导效应?什么叫共轭效应?各举一例说明之。(研读教材第11~12页有关内容) 8. 有机化学中的离子型反应与无机化学中的离子反应有何区别? 解:无机化学中的离子反应是指有离子参加的反应,反应物中必须有离子。而有机化学中的离子型反应是指反应物结构中的共价键在反应过程中发生异裂,反应物本身并非一定是离子。