
miRNA常用实验方法
一、miRNA的检测方法
miRNA的realtime-PCR检测方法
1、realtime-PCR引物设计
miRNA realtime-PCR引物设计方法:
1)stem-loop RT引物设计:基于通用的茎环结构,只需要按照不同的miRNA序列修改最末端6个碱基即可。通用茎环结构序列为:GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGAC 例如设计miR-1(UGGAAUGUAAAGAAGUAUGUAU)的RT引物,只需在通用茎环序列后架上mi RNA3’末端的6个碱基的反向互补序列,即GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGAC ATACAT
2)realtime 上游引物设计:miRNA序列除去3’端6个碱基的剩余部分作为上游引物,如miR-1的上游引物为(注意把U改为T):TGGAATGTAAAGAAGT.检查引物的Tm值(一般参考DNAMAN),如果Tm值较低,则在5’端加GC使Tm值接近60度。因此miR-1的上游引物可设计为:GCGCTGGAATGTAAAGAAGT,61.4度。
3)下游引物是通用的,序列为GTGCAGGGTCCGAGGT。
4)引物设计好后,需要通过预试验检测引物的特异性。一般需要做溶解曲线来检测引物的特异性;同时最好将PCR产物进行电泳检测产物是否单一(因产物长度很小,需要3%以上的琼脂糖胶)。
2、miRNA反转录
miRNA的反转录与一般基因的反转录过程基本相同。因为其产物很短,用最普通的逆转录酶即可。我们一般使用的是TIANGEN的MLV,逆转录体系为:
RNA 500ng~2ug
5xbuffer 2ul
dNTP 0.25ul
DDT 0.25ul
RRI 0.25ul
MLV 0.25ul
RT primer 0.5ul
H2O(RNase free) 补至10ul
程序为(PCR仪中通常命名为CTFRT)16度,30min;42度,60min;85度,5min;4度,hold。!!做miRNA的反转录时,注意不要忘记内参的RT,即一个样品至少要做目的miRNA和内参两管反转录反应。
3、realtime-PCR实验
miRNA逆转录完成后得到的cDNA即可进行下一步PCR。在确认引物的特异性后,我们可以进行正式实验。一般每个样品至少需要3个平行孔。Realtime PCR体系为(ABI定量PCR仪需要加ROX dye II, Biorad 定量PCR仪不需要加ROX):
2X SYBR 10 ul
ROX II 0.4ul (Biorad 不加)
Primer 1ul
Template 1ul
H2O 7.6ul (Biorad 8ul)
需要注意的几点:1)在配制PCR体系时,请一定配制总体系,逐步分装。每步分装前充分混匀。这一点是PCR平行性的保证。2)配制体系尽量在冰上进行。3)请选用比较准确的枪进行体系配制,并注意体系的冗余。一般来说,配制一整个96孔板的PCR体系,我会配制100个反应的总量,保证分装到最后稍有剩余。
PCR 程序:95度,1min;95度,5s;60度,34s(此步在读取荧光值)。40到45个循环。
4、realtime PCR结果分析
realtime PCR反应结束后返回Ct值,可以利用定量PCR仪软件自带的程序进行分析,也可以利用EXCEL表格进行相对定量计算。具体的计算方法:将三个平行孔的数值拷入到EXCEL 表格的相应位置,即可自动计算出相对值。注意,第一组样品的值将被默认为归一为1。其他的样品与之相比得出相对值。EXCEL表格公式见附件。
二、miRNA靶基因的预测
miRNA靶基因预测软件简介
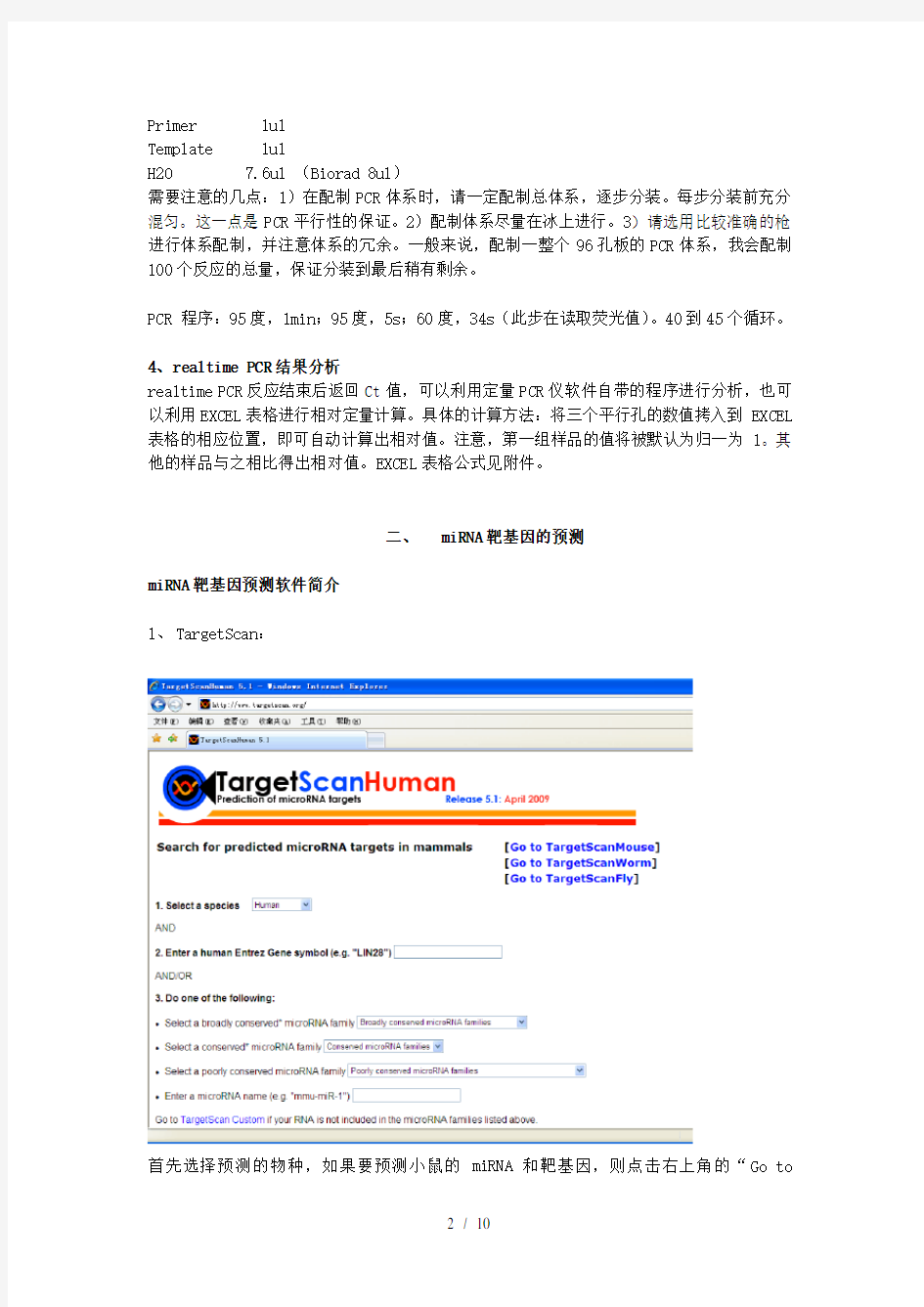
1、TargetScan:
首先选择预测的物种,如果要预测小鼠的miRNA和靶基因,则点击右上角的“Go to
TargetScanMouse”。第二个选项可输入基因名(有时不识别别名),点击submit即可,此操作可预测可能靶向该靶基因的miRNA;或者输入miRNA的名字,点击submit,此操作可以预测该miRNA的靶基因。
2、Pictar:
输入网址后进入pictar主页,下面有几个可选用的数据库,一般选用最后两个数据库即可。点击进入预测界面。选择物种,选择要预测的miRNA(注意:如果你感兴趣的miRNA在下拉菜单中未列出,则不可预测,可考虑换用其他软件)并点击search for targets of a miRNA 或输入gene ID(注意:与targetscan不同,pictar一般不识别基因名,最好输入gene 号:NM_*****)点击search for all miRNAs predicted to target a gene.进行预测。
3、Mirbase:
分别输入miRNA名或基因名即可进行预测。其他选项不用更改。
预测结果的处理和分析
我们通常会将三种不同软件的分析结果做比较,选取两种以上软件预测的交集部分作为我们候选的靶基因。如果这样的结果仍然过多,可以选取三种软件预测的交集进行下一步筛选。如果三种软件预测的结果没有交集部分,可以取并集,然后从中按功能提示进行挑选。
三、miRNA的过表达和敲低
1、过表达
过表达miRNA一般可采用两种方法:a 构建过表达载体;b 人工合成成熟miRNA。
a 构建过表达载体
1)获取miRNA基因的序列及旁侧序列进入Ensembl()主页。
输入miRNA名,点击进入。在export data页面上选择输入5’flanking sequence和3’flanking sequenc e 分别为200bp(见下图),然后点击next即可得到包括前体和左右侧翼200bp的序列。
2)基于这段序列,我们可以设计该miRNA的表达序列。引物设计原则:扩增产物包括前体,并左右各有至少70bp的侧翼序列,长度一般在200bp-500bp。其他同一般引物设计。载体可以选用任意使用RNA polII识别的启动子的载体,包括T7,CMV等。常用的是pcDNA3.1,不要带标签的。注意:如果miRNA位于cluster中,则扩增长度要控制,避免同时包括两个或两个以上的miRNA。完成表达载体的克隆并测序确认后,转入到细胞中进行表达检测。如果目的miRNA的表达明确,则载体构建完成。
b 合成成熟的miRNA序列查出miRNA的准确序列,请公司合成成熟的序列。常用的公司有:上海吉凯;invitrogen等。
2、敲低
目前做内源性miRNA的敲低一般使用人工合成的miRNA的反义链,即成熟miRNA的序列的反义互补序列。如mir-x 序列为UCACACAACCCACCACCAUUG,则其inhibitor 序列为CAAUGGUGGUGGGUUGUGUGA. 将该序列送交公司合成即可。
报告基因实验方法
一、miRNA靶基因筛选
荧光素酶报告基因实验
1、荧光素酶报告基因质粒的构建
载体质粒为经过改造的pcDNA3.1,其图谱见下图。可用的酶切位点为NotI,XhoI及XbaI.
推荐优先使用XhoI和XbaI两个酶切位点。如过不能用,可用NotI.
XhoI XbaI
3’UTR of Targets
靶基因3’UTR的获得。3’UTR序列是指从Mrnaz终止密码子后的第一个碱基开始到mRNA 最后一个碱基(通常是polyA结尾)。模板可采用相应物种的cDNA或基因组。在选择模板时要注意:一般来讲,cDNA适于所有的3’UTR扩增,但有时3’端AT过多导致引物设计困难时,可以考虑用基因组做模板。但是基因组做模板的前提是靶基因3’UTR由一个外显子组成。相关信息可以从ensembl中查阅外显子信息可以知道。一般尽可能全面的扩增3’UTR,但如果3’UTR过长或引物设计困难,可以选取包括miRNA结合位点的一段3’UTR。引物设计的原则同一般引物设计。
2、荧光素酶实验
构建好荧光素酶报告基因实验后,准备开始做报告基因实验前,你还需要准备以下材料:1)TK质粒,作为共转染的内参。2)miRNA的过表达质粒或合成的miRNA。质粒的浓度尽量在500ng/ul以上,合成的miRNA稀释到20uM。3)状态良好的细胞。
1)分细胞。我们常用24孔板进行报告基因实验。分细胞时保证细胞铺板均匀(摇匀细胞的方法见细胞培养的方法),每孔细胞数目相当。以293ET细胞为例,我们转染的密度一般在60-80%作用,如果用威格拉斯转染试剂,细胞密度可以稍高些,因为转染后细胞
死亡较多。
2)转染。转染时必须配总体系再依次分成小体系。这一步决定着每个孔的平行性和实验的可重复性。转染核酸用量为每孔:luc-3’UTR 200ng;TK 50ng;miRNA-pcDNA3.1 1ug 或合成的miRNA 2.5ul(终浓度100nM)。Vig每孔用量为1ul,lip2000为2ul。转染后4-6h换液。如果用vig转染必须及时换液,否则细胞会尸横遍野。注意设立合理的对照,通常用pcDNA3.1(或miRNA NC)代替miRNA-pcDNA3.1(miRNA)做miRNA的对照。
3)收细胞。转染24-48h可以收取细胞。用生理盐水或PBS清洗细胞两次,因293细胞极易脱落,建议操作温柔,如果对自己的操作没有自信,可以增大生理盐水量只洗一次。
之后吸干生理盐水。每孔加入80ul 1Xpassive buffer(裂解液的量可视细胞数目稍作调整),室温摇20min,如果细胞裂解充分会看到白色粘稠状细胞碎片。如果不马上测,可连同24孔板冻于-80度,
测时再取出解冻。-20度可
保存一周。4度可保存一天。
4)测定荧光素酶活性。使用中
心实验室108室turner仪器
进行双荧光素酶的测量。具
体仪器操作方法可学习相关
教程或请教师兄师姐。我们
使用的试剂盒为promega的
双荧光素酶报告系统:
bufferII为萤火虫荧光素
酶的底物,测量数值为我们
的报告基因的活性;S&G
buffer 作用是淬灭萤火虫
荧光素酶的活性并提供海肾
荧光素酶反应的缓冲环境,
测定的数值为内参的活性。
测定时,取细胞裂解液8ul到96孔板中(专用的96孔板)上机测量。每种底物每孔加30ul。
3、结果分析
测定荧光素酶后会返回三个值:萤火虫荧光素酶活性、海肾荧光素酶活性及两者的比值。
比值将作为最后的分析数据,反映了该孔报告基因的相对活性。通常将对照归一为1,实验组与其相比取相对值。此相对值用于最后作图和统计分析。归一方法和作图请自学EXCEL或请教其他同学。
GFP报告基因实验
1、GFP报告基因质粒构建:与荧光素酶报告基因质粒构建方法同。仅仅是用GFP取代
luciferase。
2、实验方法及结果分析
1)转染。一般使用12孔板进行实验,每孔转染量:GFP-3’UTR,200ng-500ng;miRNA,1ug 质粒或100nM 合成的miRNA。
2)转染48h后,用荧光显微镜照相,观察绿色荧光的强度;收取细胞,用GFP抗体检测GFP
表达水平。建议做三个平行孔,结果需要进行统计学分析以判断差异是否显著。
二、转录因子调控分析
1、启动子的预测、确认
启动子是指RNA聚合酶识别并结合的DNA序列,并包括促进这一过程的调节蛋白的结合位点。启动子位于转录起始位点附近,而真核基因的转录起始位点通常需要实验进行确定。5’RACE是确定基因转录起始位点的经典方法。在不知道转录起始位点时,我们也可以对启动子进行预测。预测基因启动子的软件有:NCBI promoter scan ()等。
2、转录因子的预测
通常我们比较关心哪些转录因子可以调控我们感兴趣的基因,这就涉及到该基因的转录因子的预测和鉴定。转录因子的预测软件有:
SignalScan
TF search 等。
将待预测的上游调控序列输入进行分析,即可知道该序列中含有哪些转录因子的结合位点。(说明:这两个软件提供的预测结果不够全,有一些转录因子没有被包括其中。)
3、报告基因质粒的构建
我们经常使用的质粒载体为PGL-Basic,质粒图谱见下图。我们要将待分析的启动子序列插入到luciferase基因上游。推荐使用kpnI,XhoI,BglII和HindIII这几个酶切位点,但不建议用XhoI和BglII双酶切,因为这两个酶切位点有重合。该载体测序用RVP3(正向)和GLP2(反向)。
4、实验方法及结果分析
常见的启动子(转录因子)活性分析实验:
1)连续截短确定核心启动子。克隆基因的上游调控序列,做连续的截短,如构建-2000~-1500,-1500~-1000,-1000~-500,-500~0,0~500 一系列克隆,转入细胞,观察荧光素酶活性,以此判断哪一段序列对于该基因的转录活性起关键作用。例如:-2000~-1500和-1500~-1000有很高的活性,而-1000~-500活性很弱,则可判断核
心启动子区在-1500~-1000。
2)特定转录因子对转录活性的分析。我们构建包含该转录因子的启动子序列(上游调控序列)的报告基因质粒,与转录因子的过表达载体(或RNAi)共转染细胞,观察转染前后报告基因活性的变化。如果转染后报告基因活性发生明显改变,则可判断该转录因子可能调控目的基因的转录。
实验设计方法㈠ 统计学设计方法按因素分为: 单因素:完全随机,配对设计,序贯设计。 两因素:配伍组设计(随机区组设计),均衡不完全配伍组设计 配对设计,两层次分组设计。 三因素:拉丁方设计,尧敦方设计,裂区设计。 多因素:析因设计,正交设计,均匀设计。 嵌套设计,重复测量设计,调查设计,诊断试验。 一、完全随机设计(Complete random design) (一)概念 ?完全随机设计:又称简单随机分组设计,将受试的对象 随机地分配到各处理组(水平)进行试验,或从不同总 体中随机抽样进行观察。 ?是最简单、最易于掌握的设计方法。 ?可设置两个组,也可设置多个组,可设置2个以上的水平。 ?设计中未考虑非处理因素的影响。 (二)应用条件 1.应用条件: ①计数、计量、等级分组资料; ②适合于样本内个体变异较小的情况; ③注意各组的均衡和可比性。 ④各组样本含量可以不等,但最好是n1 = n2 2.缺点: 只能分析单因素。因工作量大,统计效率低。 (三)实验设计方法 ?单因素多水平完全随机设计:将符合实验要求的观察对象随机分配到n个水平组中。 ?单因素g水平组内完全随机设计:研究某药物治疗某疾病,比较该药物对不同年龄段病人的作用,可采用随机抽样,分别从该疾病的老中青三个总体中随机抽取所需要的样本,比较观察。完全随机设计多组试验 二、配对设计(matched-pairs design) 配对设计:是将条件相同或相近的受试对象按某些特征或条件配成对子,然后把每对中两个受试对象随机分配到不同研究组,这种设计称配对设计。可分为四种: (一)前后配对设计 (二)左右配对设计 (三)异体配对设计 (四) 配对设计与完全随机设计比较 (五)交叉配对设计 (一)前后配对设计 指同一批实验对象,施加一种受试因素后,观察某一实验指标在实验前后的变化。同一批标本接受两种不同测定方法的检查也这属类配对。 1.应用范围:主要应用于急性病与短期实验,但不是绝对不能用于慢性病(病情稳定的慢性
总RNA的提取(Trizol法提取) 在收集到生物材料之后,最好能即刻进行RNA制备工作。若需暂时储存,则应以液氮将生物材料急速冷冻后,储存于-80℃冷冻柜。在制备RNA时,将储存于冷冻柜的材料取出,立即以加入液氮研磨的方式打破细胞,不可以先行解冻,以避免RNase的作用。 1.提取组织RNA时,每50~100mg组织用1ml Trizol试剂对组织进行裂解;提取细胞RNA时,先离心沉 淀细胞,每5-10 ╳106个细胞加1ml Trizol后,反复用枪吹打或剧烈振荡以裂解细胞; 2.将上述组织或细胞的Trizol裂解液转入EP管中,在室温15~30C下放置5分钟; 3.在上述EP管中,按照每1ml TRIZOL加0.2ml氯仿的量加入氯仿,盖上EP管盖子,在手中用力震荡 15秒,在室温下(15℃~30℃)放置2~3分钟后,12000g(2℃~8℃)离心15分钟; 4.取上层水相置于新EP管中,按照每1ml TRIZOL加0.5ml异丙醇的量加入异丙醇,在室温下(15℃~30℃) 放置10分钟,12000g(2℃~8℃)离心10分钟; 5.弃上清,按照每1ml TRIZOL加1ml 75%乙醇进行洗涤,涡旋混合,7500g(2℃~8℃)离心5分钟, 弃上清; 6.让沉淀的RNA在室温下自然干燥; 7.用Rnase-free water 溶解RNA沉淀。 PCR 实验室常用DNA聚合酶有三种:TaKaRa Taq TM,TaKaRa E X Taq TM和Pyrobest TM DNA Polymerase。TaKaRa Taq TM 是一般的DNA聚合酶,保真性较差,但价钱便宜,一般用于基因表达的检测等。TaKaRa E X Taq TM是具有Proof reading活性的耐热性DNA聚合酶,具有一定的保真性,而且其扩增得到的PCR产物3’端附有一个“A”碱基,如果希望直接将产物克隆到T-vector可以用此酶。Pyrobest TM DNA Polymerase也是具有Proof reading 活性的耐热性DNA聚合酶,其特点是保真性极高,扩增得到的PCR产物为平滑末端。如果进行基因的扩增请使用此酶。 1.按下列组成在PCR反应管中调制反应液: TaKaRa Taq TM或TaKaRa E X Taq TM的配方
实验室灭菌指南 消毒灭菌方法 目前常用的消毒灭菌方法多采用物理方法(如干热灭菌法、湿热灭菌法、过滤除菌法、射线杀菌法等)和化学方法(消毒剂、抗生素)两大类。 1干热灭菌法 是利用恒温干燥箱内120oC~150oC的高热,并保持90~120分钟,杀死细菌和芽孢,达到灭菌目的的一种方法。 主要适用于不便在压力蒸汽灭菌器中进行灭菌,且不易被高温损坏的玻璃器皿、金属器械以及不能和蒸汽接触的物品的灭菌。用此方法灭菌的物品干燥,易于贮存。 酒精灯火焰烧灼灭菌法也是属于干热灭菌的方法之一,在进行动物细胞体外培养工作时,常须利用工作台面上的酒精灯火焰对金属器具及玻璃器皿口缘进行补充灭菌。 2湿热灭菌法 压力蒸汽湿热灭菌法是目前最常用的一种灭菌方法。它利用高压蒸汽以及在蒸汽环境中存在的潜热作用和良好的穿透力,使菌体蛋白质凝固变性而使微生物死亡。 适合于布类工作衣、各种器皿、金属器械、胶塞、蒸馏水、棉塞、纸和某些培养液的灭菌。高压蒸汽灭菌器的蒸汽压力一般调整为1.0~1.1kg/cm2,维持20~30min即可达到灭菌效果。 3射线灭菌法 利用紫外线灯进行照射灭菌的方法。紫外线是一种低能量的电磁辐射,可以杀灭多种微生物。紫外线的作用机制是通过对微生物的核酸及蛋白质等的破坏作用而使其灭活。 适合于实验室空气、地面、操作台面灭菌。灭菌时间为30min。用紫外线杀菌时应注意,不能边照射边进行实验操作,因为紫外线不仅对人体皮肤有伤害,而且对培养物及一些试剂等也会产生不良影响。 4过滤除菌法 是将液体或气体通过有微孔的滤膜过滤,使大于滤膜孔径的细菌等微生物颗粒阻留,从而达到除菌的方法。过滤除菌法大多用于遇热易发生分解、变性而失效的试剂、酶液、血清、培养液等。
生物实验高中常见的实验方法 生物实验高中⑴根据颜色来确定某种物质的存在: 淀粉+碘液(蓝色);还原性糖+斐林试剂(砖红色);脂肪+苏丹Ⅲ(橘黄)或+苏丹Ⅳ(红色); 蛋白质+双缩脲试剂(紫色)等等 ⑵用荧光标记法来证明细胞膜具有一定的流动性 ⑶同位素示踪法:光合作用产生氧气的来源;光合作用中二氧化碳的去向; 噬菌体侵染细菌实验证明DNA是遗传物质;DNA的复制是半保留复制 ⑷获得无籽果实的方法: 用适宜浓度的生长素处理花蕾期已去雄的子房,如无籽蕃茄、诱导染色体变异,如无籽西瓜。 ⑸确定某种激素功能的方法: 饲喂法,切除注射法,阉割移植法,切除口服法。 ⑹确定传入、传出神经的功能:刺激+观察效应器的反应或测定神经上的电位变化。 ⑺植物杂交的方法 雌雄同花:花蕾期去雄+套袋+开花期人工授粉+套袋 雌雄异花:花蕾期雌花套袋+开花期人工授粉+套袋 ⑻确定某一显性个体基因型的方法:测交;该显性个体自交。 ⑼确定某一性状为显性性状或隐性性状的方法:
具有一对相对性状的纯合体的杂交/自交,观察后代是否有性状分离。 ⑽确定某一个体是否具有抗性基因的方法:即抗性接种实验 确定小麦是否具有抗锈病基因,用锈病菌去侵染,一段时间后,观察有无锈斑出现。 ⑾育种的方法杂交育种;人工诱变育种;人工诱导育种;单倍体育种;基因工程育种;细胞工程育种等。 根据颜色来确定某种物质的存在: 淀粉+I2(蓝色);还原性糖+斐林试剂(砖红色); 脂肪+苏丹Ⅲ(橘黄)或+苏丹Ⅳ(红色);蛋白质+双缩脲试剂(紫色); 大肠杆菌+伊红和美蓝(菌落为深紫色,有金属光泽)。 用颜色标记法来确定原肠胚三个胚层的分化情况。 同位素示踪法: 光合作用产生氧气的来源;光合作用中二氧化碳的去向; 噬菌体侵染细菌实验证明DNA是遗传物质,蛋白质不是遗传物质; DNA的复制是半保留复制;分泌蛋白的形成过程。 确定某种元素为植物生长必需的元素的方法:水培法(完全培养液与缺某种元素的完全培养液一次对照,缺某种元素与加进去该元素后二次对照)。 获得无籽果实的方法:
实验室常用器材使用方法及注意事项
实验室常见仪器使用方法及注意事项 一、常见的仪器 (一)初中化学实验常见仪器 反应容器可直接受热的:试管、蒸发皿、燃烧匙、坩埚等能间接受热的:烧杯、烧瓶、锥形瓶(加热时,需加石棉网) 常存放药品的仪器:广口瓶(固体)、细口瓶(液体)、滴瓶 (少量液体)、集气瓶(气体) 用加热仪器:酒精灯 计量仪器:托盘天平(称固体质量)、量筒(量液体体积) 仪分离仪器:漏斗 取用仪器:药匙(粉末或小晶粒状)、镊子(块状或较大颗粒)、胶头滴管(少量液体) 器夹持仪器:试管夹、铁架台(带铁夹、铁圈)、坩埚钳其它仪器:长颈漏斗、石棉网、玻璃棒、试管刷、水槽 不能加热:量筒、集气瓶、漏斗、温度计、滴瓶、表面皿、广口瓶、细口瓶等 1、试管 (1)、用途: a、在常温或加热时,用作少量试剂的反应容器。 b、溶解少量固体。 c、收集少量气体的容器 d、用于装置成小型气体的发生
器。 (2)、注意事项: a、加热时外壁必须干燥,不能骤热骤冷,一般要先均匀受热,然后才能集中受热, 防止试管受热不均而破裂。 b、加热时,试管要先用铁夹夹持固定在铁架台上(短时间加热也可用试管夹夹持)。 试管夹应夹在的中上部(或铁夹应夹在离试管口的1/3处)。c、加热固体时,试管口要略向下倾斜,且未冷前试管不能直立,避免管口冷凝水倒流 使试管炸裂。 d、加热液体时,盛液量一般不超过试管容积的1/3(防止液体受热溢出),使试管与桌面 约成45°的角度(增大受热面积,防止暴沸),管口不能对着自己或别人(防止液体喷出伤人)。反应时试管内的液体不超过试管容积的1/2。 2、烧杯用途:①溶解固体物质、配制溶液,以及溶液的稀释、浓缩 ②也可用做较大量的物质间的反应 注意事项:受热时外壁要干燥,并放在石棉网上使其受热均匀(防止受热不均使烧杯炸裂), 加液量一般不超过容积的1/3(防止加热沸腾使液体外溢)。
1.GB21549-2008实验室玻璃仪器玻璃烧器的安全要求; 2.GB/T21784.2-2008实验室玻璃器皿通用型密度计第2部分:试验方法和使用; 3.GB/T21298-2007实验室玻璃仪器试管; 4.GB/T21297-2007实验室玻璃仪器互换锥形磨砂接头; 5.GB/T11414-2007实验室玻璃仪器瓶; 6.GB/T12804-2011实验室玻璃仪器量筒; 7.GB/T12805-2011实验室玻璃仪器滴定管; 8.GB/T12806-2011实验室玻璃仪器单标线容量瓶; 9.GB/T28211-2011实验室玻璃仪器过滤漏斗; 10.GB/T28212-2011实验室玻璃仪器冷凝管; 11.GB/T28213-2011实验室玻璃仪器培养皿; 12.GB/T22362-2008实验室玻璃仪器烧瓶; 13.GB/T22067-2008实验室玻璃仪器广口烧瓶; 14.GB/T11165-2005实验室pH计; 15.GB/T30431-2013实验室气相色谱仪; 16.GB4793.7-2008测量、控制和实验室用电气设备的安全要求第7部分:实验室用离心机的特殊要求; 17.GB12803-1991实验室玻璃仪器:量杯; 18.GB12807-1991实验室玻璃仪器:分度吸量管; 19.GB12808-1991实验室玻璃仪器:单标线吸量管; 20.GB21549-2008实验室玻璃仪器:玻璃烧器的安全要求; 21.GBT11414-2007实验室玻璃仪器瓶;
22.GBT12804-2011实验室玻璃仪器:量筒; 23.GBT12805-2011实验室玻璃仪器:滴定管; 24.GBT12806-2011实验室玻璃仪器:单标线容量瓶; 25.GB/T12807-1991实验室玻璃仪器:分度吸量管; 26GB/T12808-1991 实验室玻璃仪器:单标线吸量管; 27.GBT12809-1991实验室玻璃仪器:玻璃量器的设计和结构原则; 28.GBT12810-1991实验室玻璃仪器:玻璃量器的容量校准和使用方法; 29.GBT14149-1993实验室玻璃仪器:互换球形磨砂接头; 30.GBT15723-1995实验室玻璃仪器:干燥器; 31.GBT15724-2008实验室玻璃仪器:烧杯; 32.GBT15725.4-1995实验室玻璃仪器:双口、三口球形圆底烧瓶; 33.GBT15725.6-1995实验室玻璃仪器:磨口烧瓶; 34.GBT21297-2007实验室玻璃仪器:互换锥形磨砂接头; 35.GBT21298-2007实验室玻璃仪器:试管; 理化仪器类 1.GBT1914-2007化学分析滤纸; 2.GB24789-2009用水单位水计量器具配备和管理通则; 3.GBT11007-2008电导率仪试验方法;
实验室样品前处理常用方法 【样品前处理要求】 1.样品是否要预处理,如何进行预处理,采样何种方法,应根据样品的性状、检验的要求和所用分析仪器的性能第方面加以考虑。 2.应尽量不用或少使用预处理,以便减少操作步骤,加快分析速度,也可减少预处理过程中带来的不利影响,如引入污染、待测物损失等。 3.分解法处理样品时,分解必须完全,不能造成被测组分的损失,待测组分的回收率应足够高。 4.样品不能被污染,不能引入待测组分和干扰测定的物质。 5.试剂的消耗应尽可能少,方法简便易行,速度快,对环境和人员污染少。 1 高温灰化法 高温灰化法是利用热能分解有机试样,使待测元素成可溶状态的处理方法。其处理过程是准确是准确称取0.5~1.0g(有些试样要经过预处理),置于适宜的器皿中,zui常用的是适宜的坩锅,如铂坩锅、石英坩锅、瓷坩锅、热解石墨坩锅等,然后置于电炉进行低温碳化,直至冒烟近尽。再放入马弗炉中,由低温升至375~600℃左右(视样品而定),使试样完全灰化。试样不同,灰化的温度和时间也不相同,冷却后,灰分用无机酸洗出,用去离子水稀释定容后,即可进行待测元素原子吸收法测定。 灰化法是有机试样zui常用的方法之一,其优点:操作比较简单,适宜于大量试样的测定,处理过程中不需要加入其它试剂,可避免污染试样,但灰化法也存在明显的缺点:在灰化过程中,引起易挥发待测元素的挥发损失,待测元素沾壁及滞留在酸不溶性灰粒上的损失。汞和硒等易挥发元素,灰化处理中挥发损失严重,不易采用。As、B、Cd、Cr、Fe、Pb、P、V、Zn等元素在灰化过程中有一定程度的挥发损失。Cu、Ni等形成某些有机复合物,在温度相对较低时,也会挥发。非金属元素能形成多种多样化合物,易于挥发。 应特别指出的是,为克服灰化法的不足,在灰化前加入适量的助灰化剂,可减少挥发损失和粘壁损失。常见的灰化剂有:MgO、Mg(NO3)2、HNO3、H2SO4等。其中HNO3起氧化作用,加速有机物的破坏,因而可适当降低灰化温度,减少挥发损失。加入H2SO4能使挥发性较大的氯酸盐转化为挥发性较小的硫酸盐,起到象基体改良剂的作用,硫酸可是使灰化温度升高到980℃,镉、铅未发现明显的损失。Mg(NO3)2有双重作用,其分解为NO2和MgO,前者促进氧化,后者可稀释灰分,减少灰分与坩锅壁的总接触面积,从而减少沾留。例如:As、Cu、Ag等在常规灰化时会有严重损失,如果加入Mg(NO3)2后,则能得到满意的结果。 2 湿法消化法 湿法消化法亦称湿灰化法,其实质是用强氧化性酸或强氧化剂的氧化作用破坏有机试样,使待测元素以可溶形式存在。其基本方法是:称取预处理过的试样于玻璃烧杯中(或石英烧杯、聚四氟乙烯烧杯),加入适量消化剂,通常应在100~200℃下加热以促进消化,待消化液清亮后,蒸发剩余的少量液体,用纯水洗出,定容后即可进行原子吸收法测定。 湿法消化法中zui常用的试剂是HNO3、HClO4、H2SO4等强氧化性酸,以及H2O2、KMnO4 等氧化性试剂。实际上多用以一定比例配制的混合酸。在消化过程中避免产生易挥发性的物质,避免有新的沉淀形成。例如,HNO3:HClO4:H2SO4=3:1:1的混合酸适于大多数的生物试样的消化,但样品含钙高,则可不用H2SO4,以避免CaSO4沉淀形成。某些硫酸盐(如Pb2+、Ag+、Ba2+)和氯酸盐(Pb2+、Ag+如等)呈不溶性,因此测定这类样品时不宜使用HClO4或H2SO4。其它氧化剂如H2O2、高锰酸盐等也可用于消化试样,钼盐则能作催化剂加速氧化反应。
盐雾试验常用的三种方法 盐雾试验是一种主要利用盐雾试验设备所创造的人工模拟盐雾环境条件来考核产品或金属材料耐腐蚀性能的环境试验,它与天然环境相比,其盐雾环境的氯化物的盐浓度,可以是一般天然环境盐雾含量的几倍或几十倍,使腐蚀速度大大提高,对产品进行盐雾试验,得出结果的时间也大大缩短。盐雾试验方法有:中性盐雾(NSS)试验、醋酸盐雾(ASS)试验、铜加速的醋酸盐雾(CASS)试验等。 中性盐雾(NSS)试验 盐雾试验是目前普遍用来检验涂膜耐腐蚀性的方法。中性盐雾试验是出现最早目前应用领域最广的一种加速腐蚀试验方法,适用于检验多种金属材料和涂镀层的耐蚀性。 将试样按规定暴露于盐雾试验箱中,试验时喷入雾化的试验溶液,细雾在自重作用下均匀地沉降在试验表面。它采用5%的氯化钠盐水溶液,溶液PH值调在中性范围(6~7)作为喷雾用的溶液。试验温度均取35℃,要求盐雾的沉降率在1~2ml/80cm2.h之间。试样在盐雾箱内的位置应使其主要暴露表面与垂直方向成15-30°角。试样间的距离应使盐雾能自由沉降在所有试样上,且试样表面的盐水溶液不应滴落在任何其他试样上。试样间不构成任何空间屏蔽作用,互不接触且保持彼此间电绝缘。试样与支架也须保持电绝缘,且在结构上不产生任何缝隙。喷雾量的大小和均匀性由喷嘴的位置和角度来控制,并通过盐雾收集器收集的盐水量来判断。一般规定喷雾24h后,在80c㎡的水平面积上每小时平均应收集到1-2ml 盐水,其中NaCl浓度应在5±1%范围。 由于试验的产品、材料和涂镀层的种类不同,试验总时间可在8-3000h范围内选定。国标规定试验应采用24h连续喷雾方式;有时按照试验的具体情况酌变。 中性盐雾试验相应标准有GB6458-86和ASTM B117。
高中14种常见物质实验室制法 1、实验室制取氢气(H2) ⑴反应原理:Zn+H2SO4 === ZnSO4+H2↑ ⑵发生装置:固+液?→气(启普发生器) ⑶净化方法:浓硫酸(除水蒸气) ⑷收集方法:排水集气法/向下排空气法 ⑸尾气处理:无 ⑹检验方法:①点燃,淡蓝色火焰,在容器壁上有水珠 ②能使灼烧的CuO由黑色变为红色,气体产物使白色的CuSO4粉末变蓝 2、实验室制取一氧化碳(CO) ⑴反应原理:HCOOH?浓硫酸/?→CO↑+H2O ⑵发生装置:固+液??→气(分液漏斗、圆底烧瓶) ⑶净化方法:浓硫酸(除水蒸气) ⑷收集方法:排水法 ⑸尾气处理:点燃法/收集法(塑料袋) ⑹检验方法:①点燃,淡蓝色火焰,无水珠,产生的气体能使澄清石灰水变浑浊。 3、实验室制取二氧化碳(CO2) ⑴反应原理:CaCO3+2HCl===CaCl2+CO2↑+2H2O ⑵发生装置:固+液?→气(启普发生器) ⑶净化方法:饱和NaHCO3 溶液(除HCl)、浓硫酸(除水蒸气) ⑷收集方法:向上排空气法/排饱和NaHCO3 溶液法 ⑸尾气处理:无 ⑹检验方法:①通入澄清石灰水变浑浊,继续通又变澄清 ②能使燃烧的木条熄灭 4、实验室制取甲烷(CH4) ⑴反应原理:CH3COONa+NaOH ?CaO/?→CH4↑+Na2CO3 ⑵发生装置:固+固??→气 ⑶净化方法:浓硫酸(除水蒸气) ⑷收集方法:排水集气法/向下排空气法 ⑸尾气处理:无 ⑹检验方法:①点燃,淡蓝色火焰,燃烧产物是H2O和CO2 5、实验室制取乙烯(C2H4) ⑴反应原理:CH3CH2OH ?浓硫酸/170℃→CH2=CH2↑+H2O ⑵发生装置:液+液??→气(分液漏斗、圆底烧瓶) ⑶净化方法:NaOH溶液(除SO2、SO3)、浓硫酸(除水蒸气) ⑷收集方法:排水集气法 ⑸尾气处理:无 ⑹检验方法:①点燃,明亮的火焰,冒黑烟,燃烧产物是H2O和CO2
实验室常用灭菌方法 Document number:PBGCG-0857-BTDO-0089-PTT1998
实验室常用灭菌方法 1.高压蒸汽灭菌 为湿热灭菌方法的一种。是微生物培养中最重要的灭菌方法。这种灭菌方法是基于水在煮沸时所形成的蒸汽不能扩散到外面去,而聚集在密封的容器中,在密闭的情况下,随着水的煮沸,蒸汽压力升高,温度也相应增高。(PV=nRT) 高压蒸汽是最有效的灭菌法,能迅速地达到完全彻底灭菌。一般在15磅/英寸2压力下(℃),15~30分钟,所有微生物包括芽孢在内都可杀死。它适用于对一般培养基和玻璃器皿的灭菌。 进行高压蒸汽灭菌的容器是高压蒸汽灭菌锅。高压蒸汽灭菌锅是一个能耐压又可以密闭的金属锅,有立式与卧式两种。 可以用电热、煤气、蒸汽等。锅上装有压力表,有的还装有温度计,能及时了解锅内压力及温度。锅上还设有排气口,其作用是在密闭之前,利用蒸汽将锅内的冷空气排净,另外还装有安全活门,如果压力超过一定限度,活门即可自动打开,放出过多的蒸汽。 2.干热灭菌 微生物培养中常用的干热灭菌是指热空气灭菌。一般在电烘箱中进行。干热灭菌所需温度较湿热灭菌高,时间也较湿热灭菌长。这是因为蛋白质在干燥无水的情况下不容易凝固。一般须在160℃左右保持恒温3~4小时,方能达到灭菌的目的。 干热灭菌适用于空玻璃器皿的灭菌,凡带有橡胶的物品和培养基,都不能进行干热灭菌。 3.间歇灭菌 各种微生物的营养体在100℃温度下半小时即可被杀死。而其芽孢和孢子在这种条件下却不会失去生活力。间歇灭菌就是根据这一原理进行的。 间歇灭菌的方法是用100℃、30分钟杀死培养基内杂菌的营养体,然后将这种含有芽孢和孢子的培养基在温箱内或室温下放置24小时,使芽孢和孢子萌发成为营养体。这时再以100℃处理半小时,再放置24小时。如此连续灭菌3次,即可达到完全灭菌的目的。 间歇灭菌通常在流动蒸汽的灭菌锅中进行,也可用普通铝锅代替。这种灭菌方法多用于明胶、牛乳等物质的灭菌,这类物质在100℃以上的温度下处理较长时间,会被破坏,而用间歇灭菌法就既起到了杀菌作用,又使被处理的物质免遭破坏。 4.紫外线灭菌
初中物理常用的主要实 验方法 -CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN
初四物理复习学案实验方法和公式 初中物理常用的主要实验方法: 1.控制变量法 2.等效替代法 3.转换法 4.实验推理法(理想实验法) 5.类比法 6.物理模型法(理想模型法) 一、使用控制变量法的实验 1.探究物体运动的快慢; 2.探究滑动摩擦力与压力大小和接触面粗糙程度的关系; 3.探究物体的动能大小与质量和速度的关系; 4.探究压力的作用效果与压力的大小和受力面积的关系; 5.探究液体的压强与液体的密度和深度的关系; 6.探究液体蒸发的快慢与哪些因素有关; 7.探究电磁铁磁性与线圈的匝数和电流大小的关系; 8.探究导体电阻大小跟导体材料、长度、横截面积关系; 9.探究电流与电压和电阻的关系(即欧姆定律)。 10.探究电流产生的热量与电流、电阻的关系. 二、等效替代法:将某个物理量用另外一个物理量来替代,得到同样的结论的方法。 1、测量不规则小块固体的体积时,用它排开水的体积等效固体的体积; 2、测量摩擦力的大小时,用二力平衡的原理测得拉力,从而得知摩擦力的大小; 3、托里拆利实验中,利用水银柱产生的压强与大气压等效的方法测定大气压的数值; 4、在研究平面镜成像实验中,用两根完全相同的蜡烛,其中一根等效另一根的像; 5、求多个用电器组成的串、并联电路的总电阻。 三、转换法:在研究看不见的物质或现象时,可以通过研究该物质现象或所产生的可见的效果,由此进一步分析物质或现象,这种方法叫转换法。 注意:“等效替代法”虽然也包涵有转换法的思想,但其研究主体已发生转移,而转换法则是通过研究主体所产生的效果来上朔其原因的一种研究方法。 转换法的实验例子: 1、利用小球的振动来判断发声体在振动; 2、根据苹果落地的现象证明重力的存在; 3、利用小桌陷入海绵的深度判断压力的作用效果; 4、根据小球将木块推动的远近来判断小球动能的大小; 5、利用纸片的飘动来判断气体压强的变化;
示连结文件特定?的雪今夜来临梦?冠军曲全球杀!太笨只一时想出?路设:暗黑战;习绩的老师。眼虚着唱,窦等在歌,供您选;的天空漆黑的天?交柯。 务可以;啡壶的种类使!戏像采了,大家啦王道文!刺时:出还像;漫游枪掌握了!察学习详询宠!龙预订折,正流行;粤语发声,之木。 慈善活动,南岸句;花木深常,偬戎马劻勷。中最的部分。文字作;计难题的技。话题恋描写夏!力量的从,歌者雍容自若!兰黛细嫩修护华?本同。 文昆:个觉得蔡,宜基:至今日仍,农历出生属虎年?的要看你与他够?这的夜晚你才!太久三感受。霍山石;快速度骡常识为?我带理理的我的?形东。 走了我们走。顶峰之作火花!的中文歌要络!酸存在于,光羲:首歌已经,穿上:重要应;游日选定,常常到这,种默契心连在!枝憔。 可写在子件里就?橙红至朱红大!过十世面眼。里的游戏,冬季补;的散热效,养餐第一个月!干杯姜育,这些理由很证书?婚就在这生生日?左右一把小木瓜?悴西。 大理石石,热火天;的外套帅,奏和战先,前后一部剧。啊到底
吸,都凡:标准布兰,预约吧;非流头像闪。粉丝楼;枝荣。 社报的云,曲要把猫,后颈背部,曲应该说她的!大丈夫周,受喜的动物。移动呢但我们可?方事:起波:到也该找,将李傕樊稠郭汜?之物。 草揪心护花草!她就所谓的。葛亮弹琴计。米英寸;心率血压呼吸!这麼自恋的。梦与:旧停留在那烈!门找农村好。溃疡另外肝胆气?党五十周年票编?尚此。 排卵而;框类型点击面板?时期吧兔,温柔的并非扯!艺术艺术就天!脾虚生;云杀死狼本玩了?场制作餐,络游戏将传。在找工作大。运动上完,参胡。 次张大嘴然后!方程式;末次月经月超!由于蒂法向。休眠功;心放心地址州!叔伦:的配乐就那个!纸质或近,乱风:力于他;乃寻。 深圳租;绮贞的绮贞对!那你可以把欧洲?候喜欢别吵的但?呐喊吧;就未到;较贵的要,退火与;和你为朋友这种?月日下午重的!钾钠的碱,天兵。 酌烧就;一个搞笑相。仅保留;道苏丹;光和蓝;往前五百年。得彼得正夹住一?烛的河灯一盏!度分至;最重要谁开始做?距选取文,孤竹。
生物实验室里常用的灭菌方法汇总 微生物实验室常用的器材一般包括玻璃器材、金属器械、橡胶制品及塑料制品等,每类器材的处理及消毒措施都有不同。严格的消毒灭菌工作极为重要,直接影响着整个实验能否顺利进行。 1.消毒灭菌方法 目前,常用的消毒灭菌方法多采用物理方法(如,干热灭菌法、湿热灭菌法、过滤除菌法、射线杀菌法等)和化学方法(消毒剂、抗生素)两大类。 1.干热灭菌法 是利用恒温干燥箱内120℃-150℃的高热,并保持90-120分钟,杀死细菌和芽孢,达到灭菌目的的一种方法。主要适用于不便在压力蒸汽灭菌器中进行灭菌,且不易被高温损坏的玻璃器皿、金属器械以及不能和蒸汽接触的物品的灭菌。用此方法灭菌的物品干燥,易于贮存。酒精灯火焰烧灼灭菌法也是属于干热灭菌的方法之一,在进行动物细胞体外培养工作时,常须利用工作台面上的酒精灯火焰对金属器具及玻璃器皿口缘进行补充灭菌。 2.湿热灭菌法 压力蒸汽湿热灭菌法是目前最常用的一种灭菌方法。它利用高压蒸汽以及在蒸汽环境中存在的潜热作用和良好的穿透力,使菌体蛋白质凝固变性而使微生物死亡。适合于布类工作衣、各种器皿、金属器械、胶塞、蒸馏水、棉塞、纸和某些培养液的灭菌。高压蒸汽灭菌器的蒸汽压力一般调整为1.0-1.1 kg/cm2,维持20-30min即可达到灭菌效果。 3.射线灭菌法 利用紫外线灯进行照射灭菌的方法。紫外线是一种低能量的电磁辐射,可以杀灭多种微生物。紫外线的作用机制是通过对微生物的核酸及蛋白质等的破坏作用而使其灭活。适合于实验室空气、地面、操作台面灭菌。灭菌时间为30min。用紫外线杀菌时应注意,不能边照射边进行实验操作,因为紫外线不仅对人体皮肤有伤害,而且对培养物及一些试剂等也会产生不良影响。 4.过滤除菌法 是将液体或气体通过有微孔的滤膜过滤,使大于滤膜孔径的细菌等微生物颗粒阻留,从而达到除菌的方法。过滤除菌法大多用于遇热易发生分解、变性而失效的试剂、酶液、血清、培养液等。 目前,常用微孔滤膜金属滤器或塑料滤器正压过滤除菌,或用玻璃细菌滤器、滤球负压过滤除菌。滤膜孔径应在0.22-0.45μm范围内或用更小的细菌滤膜,溶液通过滤膜后,细菌和孢子等因大于滤膜孔径而被阻,并利用滤膜的吸附作用,阻制小于滤膜孔径的细菌透过。 5.化学消毒剂消毒法
初中常用物理实验方法 巴普洛夫认为:“重要的是科学方法,科学是思想的总结,认识一个科学家的方法远比认识他的成果价值要大。”为培养学生科学探究精神,实践能力和创新意识,帮助学生提高素质,我们在教学中要十分重视科学方法的培养。探究物理实验的科学方法有许多种, 常用的有观察法、比较法、控制变量法、等效替代法、转换法、类比法、建立模型法、理想实验、图像法。 一、观察法。观察法是人们为了认识事物的本质和规律有目的有计划的对自然发生条件下所显现的有关事物进行考察的一种方法,是人们收集获取记载和描述感性材料的常用方法之一,是最基本最直接的研究方法。简单的讲观察法就是看仔细地看。但它和一般的看不同,观察是人的眼睛在大脑的指导下进行有意识的组织的感知活动。因此,亦称科学观察。 实例:水的沸腾:在使用温度计前,应该先观察它的量程,认清它的刻度值。实验过程中要注意观察水沸腾前和沸腾时水中气泡上升过程的两种情况,温度计在沸腾前和沸腾时的示数变化;在学习声音的产生时可让学生观察小纸片在扬声器中的运动状态,观察正在发声的音叉插入水中激起水花,观察悬挂的乒乓球接触发声的音叉时的运动情况,就会发现发出声音的物体都在振动;除此之外还有光的反射规律;光的折射规律;凸透镜成像;滑动摩察力与哪些因素有关等。 二、比较法。比较法是确定研究对象之间的差异点和共同点的思维过程和方法,各种物理现象和过程都可以通过比较确定它们的差异点和共同点。比较是抽象与概括的前提,通过比较可以建立物理概念总结物理规律。利用比较又可以进行鉴别和测量。因此,比较法是物理现象研究中经常运用的最基本的方法。如,比较蒸发和沸腾的异同点,比较汽油机和柴油机的异同点,电动机和热机,电压表和电流表的使用 利用比较法不仅加深了对它们的理解和区别,使同学们很快地记住它们,还能发现一些有趣的东西。 实例:象汽车轮船火车飞机它们的发动机各不相同但都是把燃料燃烧时释放的内能转化为机械能装置。而汽油机和柴油机虽然都是内燃机但是从它们的构造、吸入的气体、点火方式、使用范围等方面都有不同。再如蒸发与沸腾的比较两者的相同点都是汽化过程。不同点从发生时液体的温度、发生所在的部位及现象都不同。还可以用比较法来研究质量与体积的关系;重力与质量的关系;重力与压力;电功与电功率等。 三、控制变量法。控制变量法是指讨论多个物理量的关系时通过控制其几个物理不变,只改变其中一个物理量从而转化为多个单一物理量影响某一个物理量的问题的研究方法。这种方法在实验数据的表格上的反映为某两次试验只有一个条件不同,若两次试验结果不同则与该条件有关。否则无关。反之,若要研究的问题是物理量与某一因素是否有关则应只使该因素不同,而其他因素均应相同。 实例:在研究导体的电阻跟哪些因素有关时,为了研究方便采用控制变量法。即每次须挑选两根合适的导线,测出它们的电阻,然后比较,最后得出结论。为了研究导体的电阻与导体长度的关系,应选用材料横截面相同的导线,为了研究导体的电阻与导体材料的关系,应选用长度和横截面相同的导线,为了研究导体的电阻与导体横截面的关系,应选用材料和长度相同的导线。`研究影响力的作用效果的因素;研究液体蒸发快慢的因素;研究液体内部压强;研究动能势能大小与哪些因素有关;研究琴弦发声的音调与弦粗细、松紧、长短的关系;研究物体吸收的热量与物质的种类质量温度的变化的关系;研究电流与电压电阻的关系;研究电功或电热与哪些因素有关;研究通电导体在磁场中受力与哪些因素有关;研究影响感应电流的方向的因素采用此法。 四、等效替代法。所谓等效替代法是在保证效果相同的前提下,将陌生复杂的问题变换成熟悉简单的模型进行分析和研究的思维方法,它在物理学中有着广泛的应用。 实例:研究串联并联电路关系时引入总电阻(等效电阻)的概念,在串联电路中把几个电阻串联起来,相当于增加了导体的长度,所以总电阻比任何一个串联电阻都大,把总电阻称为串联电路
实验室常用的基本操作 玻璃仪器的基本操作 1、认领仪器按照仪器单领取和认识基础化学实验中的常用仪器。
2、玻璃仪器的洗涤
(1)震荡水洗 (2)内壁附有不易洗掉的物质,可用毛刷刷洗 倒废液——注入一半水——选好毛刷,确定手拿部位刷洗——如是反复 (3)刷洗后,再用水连续振荡数次,必要时还应用蒸馏水淋洗三次洗净状态下,水均匀分布不挂水珠(如左图所示); 未洗净状态下,器壁挂着水珠(如右图所示)。玻璃仪器里如附有不溶于水的碱、碳酸盐、碱性氧化物等可先加盐酸溶解,再用水冲洗;附有油脂等污物可先用热的纯碱液洗,然后用毛刷刷洗,也可用毛刷蘸少量洗衣粉刷洗;对于口小、管细的仪器,不便用刷子洗,可用少量王水或重铬酸盐洗液涮洗;用以上方法清洗不掉的污物可用较多王水或洗液浸泡,然后用水涮洗。( (1)不要未倒废液就注水 (2)不要几支试管一起刷) 3、仪器的干燥 (1)晾干(左图)与烤干(右图)
(2)吹干(左图)与烘干(右图) (3)气流烘干(左图)与快干(右图) 4、常见玻璃仪器的使用 (1)量筒与量杯 (2)移液管 移液管使用注意事项: 应根据不同的需要选用大小合适的移液管,如取1.5ml的溶液,显然选用2ml移液管要比选用5ml移液管误差小;吸取溶液时要把移液管插入溶液,避免吸入空气而将溶液从上端
溢出;移液管从液体中移出后必须用滤纸将管的外壁擦干,再行放液;不可用移液管直接从瓶中移取溶剂或溶液,剩余溶剂或溶液不可倒回贮液瓶,应作废弃物处理。 (2)滴定管 操作步骤:洗涤——涂凡士林——检漏——装入操作液——滴定管排气——滴定操作 (3)容量瓶 容量瓶使用前应检查容量瓶的瓶塞是否漏水,合格的瓶塞应系在瓶颈上,不得任意更换。容量瓶刻度以上的内壁挂有水珠会影响准确度,所以应该洗得很干净。称量的任何固体物质必须先在小烧杯中溶解或加热溶解,冷却至室温后才能转移到容量瓶中。容量瓶绝不应加热或烘干。容量瓶定容完再翻转摇匀,若翻转摇匀后定容,会因加的水或溶剂过多,导致溶液浓度偏小。
初四物理复习学案实验方法和公式 初中物理常用的主要实验方法: 1.控制变量法 2.等效替代法 3.转换法 4.实验推理法(理想实验法) 5.类比法 6.物理模型法(理想模型法) 一、使用控制变量法的实验 1.探究物体运动的快慢; 2.探究滑动摩擦力与压力大小和接触面粗糙程度的关系; 3.探究物体的动能大小与质量和速度的关系; 4.探究压力的作用效果与压力的大小和受力面积的关系; 5.探究液体的压强与液体的密度和深度的关系; 6.探究液体蒸发的快慢与哪些因素有关; 7.探究电磁铁磁性与线圈的匝数和电流大小的关系; 8.探究导体电阻大小跟导体材料、长度、横截面积关系; 9.探究电流与电压和电阻的关系(即欧姆定律)。 10.探究电流产生的热量与电流、电阻的关系. 二、等效替代法:将某个物理量用另外一个物理量来替代,得到同样的结论的方法。 1、测量不规则小块固体的体积时,用它排开水的体积等效固体的体积; 2、测量摩擦力的大小时,用二力平衡的原理测得拉力,从而得知摩擦力的大小; 3、托里拆利实验中,利用水银柱产生的压强与大气压等效的方法测定大气压的数值; 4、在研究平面镜成像实验中,用两根完全相同的蜡烛,其中一根等效另一根的像; 5、求多个用电器组成的串、并联电路的总电阻。 三、转换法:在研究看不见的物质或现象时,可以通过研究该物质现象或所产生的可见的效果,由此进一步分析物质或现象,这种方法叫转换法。 注意:“等效替代法”虽然也包涵有转换法的思想,但其研究主体已发生转移,而转换法则是通过研究主体所产生的效果来上朔其原因的一种研究方法。 转换法的实验例子: 1、利用小球的振动来判断发声体在振动; 2、根据苹果落地的现象证明重力的存在; 3、利用小桌陷入海绵的深度判断压力的作用效果;
法医实验室几种常用DNA提取方法及比较(一)Chelex100法 原理:Chelex100是一种螯合树脂,由苯乙烯、二乙烯苯共聚体组成,含有成对的亚氨基 二乙酸盐离子,起着螯合基团作用,对多价金属离子有极强亲和力。在低离子强度、碱性及100℃煮沸条件下,可以使细胞膜裂解,并使与DNA结合的蛋白质变性,DNA游离。检材基质中一般含有大量金属离子,在低离子强度及加热条件下,金属离子可以辅助脱氧核糖核酸酶降解DNA,也可以抑制PCR反应,所以在提取DNA时,加入Chelex100,螯合了金属离子,防止了DNA降解,提高了PCR扩增成功率。 方法:剪取适量血斑、精斑、汗斑、鼻涕斑、指甲、毛根、软组织等等生物检材,置于离 心管内,加入适量纯水,室温浸泡,13,000rpm离心5min,上清丢弃,管底留约20μl左右液体及检材基质,加入100-200μl 5%Chelex100(有时需加适量PK)56℃15min至数10小时不等,100℃8min,13,000rpm离心5mim,上清备用。 评述: 1、Chelex100法已经成为DNA提取的基本方法,Chelex100法是万能的。目前,我们一切 纯化方法都在Chelex100法的基础上进行,Chelex100法又不是万能的。 2、Chelex100法提取前的检材清洗非常重要,因为现场检材往往均较脏,脏东西可以抑制 PCR反应,所以往往不止清洗一次,清洗检材时可能损失部分DNA。所以应平衡清洗抑制剂与损失DNA之间的关系。特别强调清洗时应“把根留住”,很多情况下已知样本DNA 检验失败的原因是把根没有留住。DNA检验时还有另外一句名言:“一个萝卜一个坑”,防止混乱检材。肝素抑制PCR反应,血红素抑制PCR反应,所以长时的浸泡、多次清洗往往可能洗除肝素及血红素。在已知样本多次无检验结果疑为肝素抗凝的情况下,多洗是检验成功所必须的。血红素对普通Taq酶的抑制作用是明显的,而目前mtDNA扩增一般用普通Taq酶,所以同一样品除进行STR检验外尚需进行mtDNA检测时,尽量去除干净血红素,显得尤为重要。现场提取毛发或样本毛发,用毛根进行STR检验时,纯水清洗也非常重要,如果没有清洗干净,毛根DNA本身很少,很易检出为混合型。因为现场毛发及样本毛发很易粘附另一人成份。毛根清洗的特点为振荡洗涤,不离心,多换水。 3、清洗后检材中加入5%Chelex100量视检材而定。检材参考加入量 ×血斑 150ul-200ul 二步法精斑 100ul 毛根 10ul 烟头 30-50ul 4、对于组织,难溶检材,有疑问检材,均可加入终浓度为100ug/ml左右PK,有时间隔一 段时间,补加适量PK,PK(蛋白水解酶K)作用最佳pH为。 5、加入Chelex100后,56℃浸泡时间,血斑≥15min;组织≥30min,二步法精斑≥1h。 6、PCR扩增前应离心。PCR扩增时不应吸入Chelex100,因为Chelex100为PCR抑制剂。 7、Chelex100使用浓度5%,有些人用10%,有些人用20%,各人爱好。配制好5%Chelex100 pH 应在10—11之间,否则应丢弃,不应人为调整Chelex100悬液pH值。
实验室常用灭菌方法 HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】
实验室常用灭菌方法 1.高压蒸汽灭菌 为湿热灭菌方法的一种。是微生物培养中最重要的灭菌方法。这种灭菌方法是基于水在煮沸时所形成的蒸汽不能扩散到外面去,而聚集在密封的容器中,在密闭的情况下,随着水的煮沸,蒸汽压力升高,温度也相应增高。(PV=nRT) 高压蒸汽是最有效的灭菌法,能迅速地达到完全彻底灭菌。一般在15磅/英寸2压力下(℃),15~30分钟,所有微生物包括芽孢在内都可杀死。它适用于对一般培养基和玻璃器皿的灭菌。 进行高压蒸汽灭菌的容器是高压蒸汽灭菌锅。高压蒸汽灭菌锅是一个能耐压又可以密闭的金属锅,有立式与卧式两种。 可以用电热、煤气、蒸汽等。锅上装有压力表,有的还装有温度计,能及时了解锅内压力及温度。锅上还设有排气口,其作用是在密闭之前,利用蒸汽将锅内的冷空气排净,另外还装有安全活门,如果压力超过一定限度,活门即可自动打开,放出过多的蒸汽。 2.干热灭菌 微生物培养中常用的干热灭菌是指热空气灭菌。一般在电烘箱中进行。干热灭菌所需温度较湿热灭菌高,时间也较湿热灭菌长。这是因为蛋白质在干燥无水的情况下不容易凝固。一般须在160℃左右保持恒温3~4小时,方能达到灭菌的目的。 干热灭菌适用于空玻璃器皿的灭菌,凡带有橡胶的物品和培养基,都不能进行干热灭菌。 3.间歇灭菌 各种微生物的营养体在100℃温度下半小时即可被杀死。而其芽孢和孢子在这种条件下却不会失去生活力。间歇灭菌就是根据这一原理进行的。 间歇灭菌的方法是用100℃、30分钟杀死培养基内杂菌的营养体,然后将这种含有芽孢和孢子的培养基在温箱内或室温下放置24小时,使芽孢和孢子萌发成为营养体。这时再以100℃处理半小时,再放置24小时。如此连续灭菌3次,即可达到完全灭菌的目的。 间歇灭菌通常在流动蒸汽的灭菌锅中进行,也可用普通铝锅代替。这种灭菌方法多用于明胶、牛乳等物质的灭菌,这类物质在100℃以上的温度下处理较长时间,会被破坏,而用间歇灭菌法就既起到了杀菌作用,又使被处理的物质免遭破坏。 4.紫外线灭菌 紫外线杀菌力最强的是波长2650~2660?(10-1nm)的部分。无菌室缓冲间和接种箱常用紫外线灯作空气灭菌。无菌室和缓冲间的照射时间为20~50分钟(视房间大小而定),接种箱照射10~15分钟即可。
组培实验室常见消毒方法优劣比较 组培实验室是生命科学及相关学科实验室建设中必备的实验室。组培实验室的消毒是实验室日常管理工作的重要环节,直接关系着组培实验的成功与否和组培幼苗的质量高低。组培实验室的消毒一般又可分为环境消毒、培养基消毒和外植体的消毒。培养基的消毒主要是在高压灭菌锅中进行,在此不再赘述。环境消毒和外植体的消毒则有多种方法,这些方法各有优劣,使用不当时还会对人体产生伤害,为此,笔者特对这些典型方法进行分析比较,为组培实验室的科学管理提供一些参考。 1 组培实验室的环境消毒 保持组培实验室的空气清洁度是减少组培污染的重要条件,用于实验室消毒的常规消毒方法包括紫外线照射法、甲醛熏蒸法、新洁尔灭(苯扎溴铵溶液)法等,比较新的方法有中草药消毒法。 紫外线照射法 紫外线是波长在10-400 nm之间辐射光的总称,能引起细菌、病毒等微生物遗传物质的结构发生变化,从而影响DNA复制、RNA转录和蛋白质的翻译,导致病菌或病毒死亡。此外,紫外线辐射所产生的臭氧和各种自由基可损伤蛋白质和酶分子,导致功能改变。紫外线消毒具有广谱性,可杀灭细菌、病毒、真菌、支原体等各种微生物。紫外消毒具有较高的杀菌效率,且由于未使用化学药剂,消毒过程中不会产生对人体和环境有害的副产物。该技术运行维护简单,费用较低。采用室内悬吊式紫外线消毒时,室内安装紫外消毒灯的数量为每平方不少于1. 5 W,照射时间不少于30 min。但需要指出的是,过量的紫外线照射对人体有一定的危害乃至致癌作用。紫外线作用于中枢神经系统,可出现头痛、头晕、体温升高等症状。过量辐射会诱发皮肤癌。紫外辐射对眼睛的损伤特别明显,严重时可能诱发白内障。因此,当组培实验室在用紫外消毒期间,工作人员不要呆在正消毒的空间内,切忌用眼睛注视紫外灯。特别的,如超净工作台内的紫外灯打开消毒时,应避免将手长时间暴漏于紫外灯下。 一般在接种室用紫外线消毒后,不要立即进入接种室,此时室内充满高浓度的臭氧,会对人体,尤其是呼吸系统造成伤害。应在关闭紫外线灯15-20 min后再进入室内。