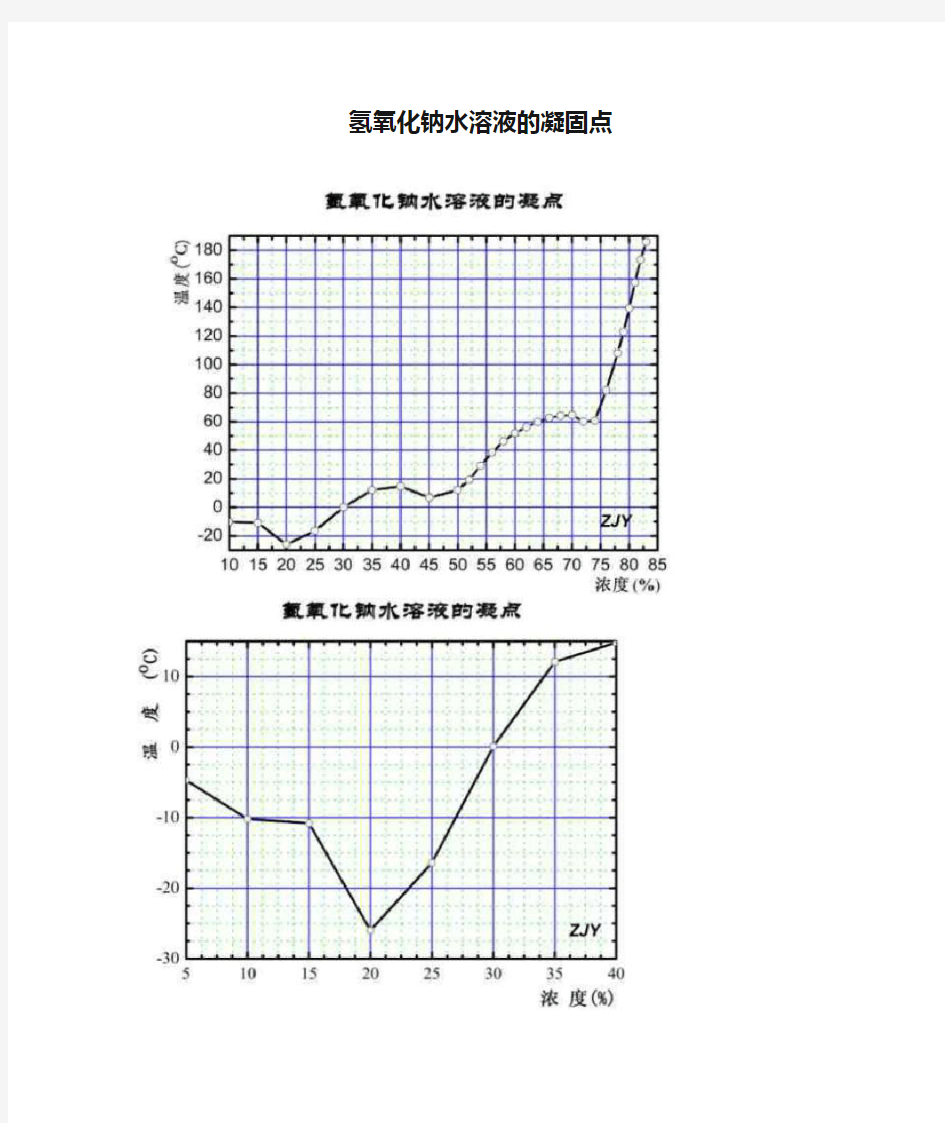

氢氧化钠水溶液的凝固点
氢氧化钠纯品为无色透明晶体,相对密度2.130。熔点318.4℃。沸点1390℃。市售烧碱有固态和液态两种:纯固体烧碱呈白色,有块装、片状、棒状、粒状,质脆;纯液体烧碱为无色
透明液体。固体烧碱有很强的吸湿性。易溶于水,溶解时放热,水溶液呈碱性,有滑腻感;溶于乙醇和甘油;不溶于丙酮、乙醚。腐蚀性极强,对纤维、皮肤、玻璃、陶瓷等有腐蚀作用。与金属铝和锌、非金属硼和硅等反应放出氢;与氯、溴、碘等卤素发生歧化反应;与酸类起中和作用而生成盐和水。
氢氧化钠标准溶液浓度测量不确定度评定报告 编制:付学飞 审核:王淑芳 批准:许百红 京博农化科技股份有限公司分析检测中心 2011-8-2
氢氧化钠标准溶液浓度测量不确定度评定报告 1目的 评定0.5mol/L 氢氧化钠标准溶液浓度测量的不确定度 2依据标准 《化学试剂标准滴定溶液的制备》GB /T 601-2002 3试验条件 1) 设备名称:分析天平 设备型号:AE-240 设备编号:CARC0007 测量范围:0-200g 准确度等级或示值误差:±0.0001g 分辨率或最小分度值:0.0001g 2) 玻璃仪器名称: 50ml 碱式滴定管 准确度等级:A 级 最大允许误差±0.05ml 最小分度值:0.01ml 3) 工作基准试剂名称名称:基准邻苯二甲酸氢钾 3.2 检测环境条件:温度——25℃ 湿度—— 50% 3.3标准溶液编号:20110712 4过程描述与数学模型 4.1配制过程 称取110g 氢氧化钠溶于100ml 无二氧化碳的水中,注入聚乙烯容器中,密闭放置至溶液清亮,用塑料管量取上层清液,用无二氧化碳的水稀释至1000ml 。 4.2标定过程 称取于105-110℃下用电烘箱箱至干燥的工作基准试剂邻苯二甲酸氢钾3.6g ,加无二氧化碳的水溶解,加入两滴酚酞指示液(10g/L ),用配制好的氢氧化钠滴定溶液滴定至浅粉色。并保持30s ,同时做空白试验。 氢氧化钠标准滴定溶液的浓度[])(NaOH c ,数值以mol/L 表示,按照下式计算 M V V m NaOH C ?-?=)(1000)(21 式中:m ——邻苯二甲酸氢钾的质量分数的准确值,g ; V 1——滴定消耗氢氧化钠滴定溶液的体积,ml ; V 2——空白试验耗用的氢氧化钠滴定溶液的体积,ml ;
氢氧化钠标准溶液的配 制 集团标准化办公室:[VV986T-J682P28-JP266L8-68PNN]
验四氢氧化钠标准溶液的配制和标定 一、目的 1、配制0.1mol/L 氢氧化钠溶液 2、氢氧化钠溶液的标定 二、材料 仪器:碱式滴定管(50ml )、容量瓶、锥形瓶、分析天平、台秤。 试剂:邻苯二甲酸氢钾(基准试剂)、氢氧化钠固体(A.R )酚酞指示剂:1g 酚酞溶于适量乙醇中,再稀释至100mL 。 三、实验原理 NaOH 有很强的吸水性和吸收空气中的CO 2,因而,市售NaOH 中常含有Na 2CO 3。 反应方程式:2NaOH+CO 2→Na 2CO 3+H 2O 由于碳酸钠的存在,对指示剂的使用影响较大,应设法除去。 除去Na 2CO 3最通常的方法是将NaOH 先配成饱和溶液(约52%,W/W ),由于Na 2CO 3在饱和NaOH 溶液中几乎不溶解,会慢慢沉淀出来,因此,可用饱和氢氧化钠溶液,配制不含Na 2CO 3的NaOH 溶液。待Na 2CO 3沉淀后,可吸取一定量的上清液,稀释至所需浓度即可。此外,用来配制NaOH 溶液的蒸馏水,也应加热煮沸放冷,除去其中的CO 2。 标定碱溶液的基准物质很多,常用的有草酸(H 2C 2O 42H 2O )、苯甲酸(C 6H 5COOH )和邻苯二甲酸氢钾(C 6H 4COOHCOOK )等。最常用的是邻苯二甲酸氢钾,滴定反应如下: C 6H 4COOHCOOK+NaOH →C 6H 4COONaCOOK+H 2O 计量点时由于弱酸盐的水解,溶液呈弱碱性,应采用酚酞作为指示剂。 四、操作步骤 1、0.1mol/LNaOH 标准溶液的配制 用小烧杯在台秤上称取120g 固体NaOH ,加100mL 水,振摇使之溶解成饱和溶液,冷却后注入聚乙烯塑料瓶中,密闭,放置数日,澄清后备用。准确吸取上述溶液的上层清液5.6mL 到1000毫升无二氧化碳的蒸馏水中(可以煮沸),摇匀,贴上标签。 2、0.1mol/LNaOH 标准溶液的标定 将基准邻苯二甲酸氢钾加入干燥的称量瓶内,于105-110℃烘至恒重,用减量法准确称取邻苯二甲酸氢钾约0.6000克,置于250mL 锥形瓶中,加50mL 无CO2蒸馏水,温热使之溶解,冷却,加酚酞指示剂2-3滴,用欲标定的0.1mol/LNaOH 溶液滴定,直到溶液呈粉红色,半分钟不褪色。平行滴定三次。同时做空白试验(滴定除了标定物——邻苯二甲酸氢钾以外的水)。 五、结果结算 NaOH 标准溶液浓度计算公式: m/M C NaOH = (V 2-V 1) 式中:m---邻苯二甲酸氢钾的质量,g V 1---氢氧化钠标准滴定溶液在滴定管中初读数,mL V 2---氢氧化钠标准滴定溶液在滴定管中末读数,mL 邻苯二甲酸氢钾的摩尔质量=204.2g/mol
NaOH密度,质量分数与摩尔浓度对应(一) 密度g/m3 质量分数%摩尔浓度mol/L密度g/m3质量分数,%摩尔浓度mol/L 1.005 0.602 0.151 1.095 8.74 2.391 1.01 1.045` 0.264 1.1 9.19 2.527 1.015 1.49 0.378 1.105 9.645 2.664 1.02 1.94 0.494 1.11 10.1 2.802 1.025 2.39 0.611 1.115 10.555 2.942 1.03 2.84 0.731 1.12 11.01 3.082 1.035 3.29 0.851 1.125 11.46 3.224 1.04 3.745 0.971 1.13 11.92 3.367 1.045 4.2 1.097 1.135 1 2.37 3.51 1.05 4.655 1.222 1.14 1 2.83 3.655 1.055 5.11 1.347 1.145 13.28 3.801 1.06 5.56 1.474 1.15 13.73 3.947 1.065 6.02 1.602 1.155 14.18 4.095 1.07 6.47 1.731 1.16 14.64 4.244 1.075 6.93 1.862 1.165 15.09 4.395 1.08 7.38 1.992 1.17 15.54 4.545 1.085 7.83 2.123 1.175 15.99 4.697 1.09 8.28 2.257 1.18 16.44 4.85 NaOH密度,质量分数与摩尔浓度对应(二) 密度g/m3 质量分数%摩尔浓度mol/L 密度g/m3 质量分数%摩尔浓度mol/L 1.185 16.89 5.004 1.37 34.03 11.65 1.19 17.345 5.16 1.375 34.52 11.86 1.195 17.8 5.317 1.38 35.01 1 2.08 1.2 18.255 5.476 1.385 35.5 1 2.29 1.275 25.1 8 1.39 36 1 2.51 1.28 25.56 8.178 1.395 36.495 1 2.73 1.285 26.02 8.357 1.4 36.99 1 2.95 1.29 26.488.0539 1.405 37.49 13.17 1.295 26.94 8.722 1.41 37.99 13.3 1.3 27.41 8.906 1.415 38.49 13.61 1.305 27.87 9.092 1.42 38.99 13.84 1.31 28.33 9.278 1.425 39.495 14.07 1.315 28.8 9.466 1.43 40 14.3 NaOH密度,质量分数与摩尔浓度对应(三)
第一部分化学品及企业标识 化学品中文名:30%氢氧化钠溶液 化学品俗名或商品名:30%液碱 化学品英文名:Sodium hydroxide;Caustic soda 第二部分成分/组分信息 纯品混合物 化学品名称:氢氧化钠溶液 有害成分浓度CAS No. 氢氧化钠30% 1310-73-2 第三部分危险性概述 危险性类别:第8.2类碱性腐蚀品 侵入途径:吸入、食入 健康危害:本品有强烈刺激和腐蚀性。腐蚀鼻中隔;直接接触皮肤和眼可引起灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克。环境危害:对水体可造成污染。 燃爆危险:本品不燃,具强腐蚀性、强刺激性,可致人体灼伤。 第四部分急救措施 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟就医。 眼睛接触:立即提起眼睑,用大量就动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,
给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:用水漱口,给饮牛奶或蛋清。就医。 第五部分消防措施 危险特性:与酸发生中和反应并放热。具有强腐蚀性。 有害燃烧产物:可能产生有害的毒性烟雾。 灭火方法及灭火剂:本品不燃,由其它物质引起火灾时,应注意该物质的腐蚀性。 灭火注意事项:消防人员应穿防酸碱消防服。 第六部分泄漏应急处理 应急处理:隔离泄漏污染区,限制出入。液碱泄漏:收集回收后用水冲洗,冲洗水经中和处理后排入废系统。 消除方法:加入大量水中,调节至中性,再放入废水系统。也可用大量水冲洗,经稀释的洗水放入废水系统。如大量泄漏,收集回收或无害处理后废弃。 第七部分操作处理与储存 操作注意事项:操作人员必须经过专门培训持证上岗,严格遵守工艺规程和岗位操作法。操作人员穿耐酸碱服,戴耐酸碱手套,戴防护眼镜。避免与酸类接触。搬运时要轻装轻卸,防止包装及容器损坏。配备泄漏应急处理设备。应当注意倒空容器内的残留物。稀释或制备溶液时,应把碱加入水中,避免沸腾和飞溅。储存注意事项:液碱贮槽应设围堤,并有明显标志。 第八部分暴露控制/个体防护
第一部分化学品及企业标识 化学品中文名:45%氢氧化钠溶液 化学品俗名或商品名:45%液碱 化学品英文名:Sodium hydroxide;Caustic soda 企业名称:沈阳化工股份有限公司 地址:沈阳市铁西区卫工北街46号 邮编:110026 传真号码:0086-024-******** 企业应急电话:0086-024-******** 技术说明书编号:SH/003 生效日期:2007年8月1日 国家应急电话: 第二部分成分/组分信息 纯品混合物 化学品名称:氢氧化钠溶液 有害成分浓度CAS No. 氢氧化钠45% 1310-73-2 第三部分危险性概述 危险性类别:第8.2类碱性腐蚀品 侵入途径:吸入、食入 健康危害:本品有强烈刺激和腐蚀性。腐蚀鼻中隔;直接接触皮肤和眼可引起灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克。
环境危害:对水体可造成污染。 燃爆危险:本品不燃,具强腐蚀性、强刺激性,可致人体灼伤。 第四部分急救措施 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟就医。 眼睛接触:立即提起眼睑,用大量就动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:用水漱口,给饮牛奶或蛋清。就医。 第五部分消防措施 危险特性:与酸发生中和反应并放热。具有强腐蚀性。 有害燃烧产物:可能产生有害的毒性烟雾。 灭火方法及灭火剂:本品不燃,由其它物质引起火灾时,应注意该物质的腐蚀性。 灭火注意事项:消防人员应穿防酸碱消防服。 第六部分泄漏应急处理 应急处理:隔离泄漏污染区,限制出入。液碱泄漏:收集回收后用水冲洗,冲洗水经中和处理后排入废系统。 消除方法:加入大量水中,调节至中性,再放入废水系统。也可用大量水冲洗,经稀释的洗水放入废水系统。如大量泄漏,收集回收或无害处理后废弃。
密度溶质的质量分数氢氧化钠溶液的浓度 密度(20℃ )g/cm3 NaOH的质量分数/(g/100g溶液) 物质的量浓度(mol/L) 1 0.159 0.0393 1.0050.6020.151 1.01 1.0450.264 1.015 1.490.378 1.02 1.940.494 1.025 2.390.611 1.03 2.840.731 1.035 3.290.851 1.04 3.7450.971 1.045 4.2 1.097 1.05 4.655 1.222 1.055 5.11 1.347 1.06 5.56 1.474 1.065 6.02 1.602 1.07 6.47 1.731 1.075 6.93 1.862 1.087.38 1.992 1.0857.83 2.123 1.098.28 2.257 1.0958.74 2.391 1.19.19 2.527 1.1059.645 2.664 1.1110.1 2.802 1.11510.555 2.942 1.1211.01 3.082 1.12511.46 3.224 1.1311.92 3.367 1.1351 2.37 3.51 1.141 2.83 3.655 1.14513.28 3.801 1.1513.73 3.947 1.15514.18 4.095 1.1614.64 4.244 1.16515.09 4.395 1.1715.54 4.545 1.17515.99 4.697 1.1816.44 4.85 1.18516.89 5.004 1.1917.345 5.16 1.19517.8 5.317 1.218.255 5.476 1.20518.71 5.636
实验七:氢氧化钠浓度的标定 一.实验目的 1练习分析天平的使用方法并掌握减量称量法 2 掌握滴定操作并学会正确判断终点; 3 学会配制和标定碱标准溶液的方法。 二.实验原理: 1、氢氧化钠标准溶液不能准确配制的原因; NaOH易吸湿,不是基准物质,故不能准确配制NaOH标准溶液,需用邻苯二甲酸氢钾标定,属于强碱滴定弱酸。 2、标定氢氧化钠溶液的工作基准试剂,滴定反应到达化学计量点时溶液的pH 值; 工作基准试剂是:邻苯二甲酸氢钾。 C 6H 4 COOHCOOK + NaOH → C 6 H 4 COONaCOOK + H 2 O 计量点时pH= 3、选用何种指示剂,终点时的颜色; 选用酚酞作指示剂,终点是溶液由无色变为淡红色,且内不退色。 如何选择指示剂 强碱滴定强酸时,随着NaOH溶液的加入,溶液pH值发生变化,以pH对NaOH 的加入量作图得滴定曲线,计量点前后NaOH溶液由不足到过量(%); 溶液pH的突然变化称滴定突跃,突跃的pH范围称滴定突跃范围; 酸碱指示剂、指示剂的变色范围酸碱指示剂本身是弱酸或弱碱:HIn = H+ + In-,HIn与In-有不同的颜色,pH=p K a(HIn)+lg[In-]/[HIn],当[In-] =[HIn],pH=p K a为理论变色点;[In-]/[HIn]≤ 看到酸色,≥10,看到碱色,变色范围的pH=p K a±1,但实际观测到的与理论计算有差,因人眼对各种颜色的敏感度不同,加上两种颜色互相掩盖,影响观察。如酚酞p K a=,变色pH范围为~。不同的人的观察结果也不同。
指示剂的选择使指示剂的理论变色点处于滴定突跃范围。 4、计算公式 C(NaOH)= m(KHC8H4O4) = m(KHC8H4O4) M(KHC8H4O4)V(NaOH) * V(NaOH) 三.主要仪器与试剂 主要仪器:电子天平,分析天平,250m烧杯(4个),表面皿(4个),滴定管,称量瓶,玻璃棒,干燥器,量筒。 主要试剂:NaOH(S)、邻苯二甲酸氢钾、酚酞 四.操作步骤:五.实验结果及分析 用到的计算公式: 1. C(NaOH)= m(KHC8H4O4) = m(KHC8H4O4) M(KHC8H4O4)V(NaOH) * V(NaOH) 2.平均值的计算: =(X1+X2+X3+……+X n)/n 3.标准偏差计算: 4:统计量计算式为:T n=(X n- ) /S 六.问题及思考题 ★思考题
氢氧化钠(溶液)安全技术说明书 第一部分化学品及企业标识 化学品中文名称:氢氧化钠。 化学品英文名称:sodiumhydroxide 化学品中文别名称:烧碱;火碱;苛性钠。 推荐用途:用于制药、造纸、炼铝、炼钨、人造丝、人造棉和肥皂制造业,用于生产染料、塑料、药剂及有机中间体,旧橡胶的再生,制金属钠、水的电解以及无机盐生产中,制取硼砂、铬盐、锰酸盐、磷酸盐等,实验室化学试剂,碱性干燥剂。 限制用途:严禁用于食品和饲料加工。 第二部分危险性概述 物理和化学危险性:腐蚀金属锌、铝、锡和铅,生成易燃易爆的氢气。与铵盐反应生成氨,有着火和爆炸的危险。 侵入途径:吸入、皮肤接触、眼睛接触、食入 健康危害:本品具有强烈腐蚀性和刺激性。粉尘刺激眼和呼吸道,腐蚀鼻中隔; 直接接触皮肤和眼可引起灼伤;误食可造成消化道灼伤,粘膜糜烂、出血和休克。 环境危害:对环境有害,对水体可造成污染。 次要危险 危险性类别 腐蚀性物质 危险标识 警示语警告 强烈腐蚀性和刺激性,误食可造成消化道 危险说明 灼伤。 ?应用贮槽储存 防范说明
第三部分成分/组成信息 物质混合物" 第四部分急救措施 皮肤接触:立即脱去污染的衣物,用大量流动清水充分冲洗,直至皂样物质彻底消失或创面的pH值成中性为止。就医。 眼睛接触:立即提起眼睑,用大量流动清水充分冲洗;用2%?3%的硼酸液冲 洗或湿敷。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难给输氧。如呼吸停止,即进行人工呼吸。就医。 食入:用水漱口,给饮牛奶或蛋青,禁止催吐。就医。 第五部分消防措施 危险特性:与酸发生中和反应并放热。腐蚀某些塑料、橡胶或涂层。在潮湿空气中,腐蚀金属铝、锌、锡和铅,生成易燃易爆的氢气。具有强腐蚀性。 有害燃烧产物:无意义。 灭火方法及灭火剂:本品不会燃烧,根据看火原因选择适当灭火剂灭火。用水、砂土扑救,应注意防止物品遇水产生飞溅,造成灼伤。 灭火注意事项及措施:消防人员必须穿全身耐酸碱消防服,佩戴过滤式防毒面具(全面罩)或隔离式呼吸器灭火。尽可能将容器从火场移至空旷处,喷水保持容器冷却,直至灭火结束。 第六部分泄漏应急处理 作业人员防护措施和防护装备:穿耐酸碱服,戴耐酸碱手套,戴防护手套。应急处置程序:疏散有关人员、隔离污染区;限制出入。阻隔和切断泄漏源。切断泄漏源,收集回收后用水冲洗残留物,冲洗水经过中和处理后排入废水处理系统。 防止发生次生危害的预防措施:应特别注意对水体的影响。 第七部分操作处置与储存 操作处理注意事项:操作人员应佩戴佩戴防护眼镜和胶皮手套。避免与酸类接触。搬运时轻装轻卸,防止包装及容器损坏。配备泄漏应急处理设备。应当注意倒空容器内本品残留物。稀释或配制溶液时应把碱倒入水中,避免沸腾和飞溅。
河南(05-12年)中考氢氧化钠的知识点汇总 1、称量:由于它易潮解,不能放在纸上称量,必须放在玻璃器皿里称量。 2、用途:氢氧化钠制肥皂利用了它的化学性质 3、化学性质:(1)与二氧化碳的反应。利用实验装置中气球的变化,U形管中 液面的变化等,如何检验氢氧化钠是否变质、部分变质还是全部变质考查。 (2)腐蚀性(可否选用浓氢氧化钠溶液等碱性物质来涂抹蚊虫叮咬处)(3)与酸的反应(反应前后溶液质量的变化) (4)与盐反应(与硫酸铜反应) 4、工业制法:写方程式 5、俗称:火碱、烧碱、苛性钠 6、除杂(氢氧化钠中混有碳酸钠) 7、氢氧化钠溶液与氢氧化钙溶液具有相似化学性质的原因 8、保存:密封保存 9、氢氧化钠溶液的酸碱度 10、氢氧化钠溶于水温度变化(U形管中液面的变化) 未考内容:1、氢氧化钠去除油污 2、氢氧化钠做干燥剂 3、氢氧化钠溶液与石灰水的鉴别 4、氢氧化钠和三氧化硫反应 1. 下列实验操作正确的是() 2、.下列物质的用途只与物质的物理性质有关的是() A. 干冰用于人工降雨 B. 用熟石灰中和土壤的酸性 C. 液氧用作火箭的助燃剂 D. 氢氧化钠可用于制肥皂 3、检验一瓶长期露置在空气中的NaOH溶液是否变质,下列不能作为检验用的试剂的是()
A澄清石灰水B氢氧化钡溶液C氯化钙溶液D酚酞试液 4.围绕一瓶NaOH固体是否变质的问题,通过如下问题和实验进行研究。(1)写出NaOH固体变质的化学方程式:。(2)能否用酚酞试液检验NaOH是否变质?,理由是 (3)取少量固体于试管中,滴加稀盐酸,有气泡产生,该现象能否证明NaOH 已经变质?请说明理由。。(可用文字说明也可用化学方程式表示) (4)为证明变质的固体中仍然存在NaOH,某同学按如下操作进行实验: ①取少量固体溶于水,向其中加入足量CaCl 溶液,现象 2 为,反应的化学方程式 为。 ②取①所得溶液于试管中,向其中滴加少量的,现象 为。其结论是变质的固体中仍然存在NaOH。 5、甲、乙两同学为了探究实验室中久置的氢氧化钠固体是否变质,进行了如下实验。请与他们一起完成探究活动。 【探究问题】氢氧化钠固体是否变质。 【实验探究】甲、乙两同学分别设计了不同的实验方案并加以实验。 ⑴乙同学认为甲同学的结论不科学,其理由是。 ⑵乙同学的试验中,观察到的现象A应为,该反应的化学方程式为;氢氧化钠固体变质的原因是 (用化学方程式表示)。 【拓展应用】 ⑶氢氧化钠溶液容易变质,必须密封保存。实验室必须密封保存的药品还有很多,试另举一例。 ⑷若要除去上述变质的氢氧化钠溶液中的杂质,应加入适量的(填化学式)溶液而除去。 【答案】⑴碳酸钠溶液也显碱性(碳酸钠溶液的pH>7)⑵有白色沉淀产生
氢氧化钠 英文名:sodium hydroxide分子式:NaOH CAS号:1310-73-2浓度:30%险 碱性腐蚀品,有强烈的刺激和腐蚀性。吸入、食入有害;引起皮肤灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克!对环境可能有害。 【预防措施】 ·包装应使用耐碱材质的容器,容器必须盖紧。 ·不可与酸类物质等混装,不可与酸、食品等混存。 ·戴防护手套、防护眼镜、防护面罩。 ·工作场所不得进食、饮水或吸烟,误食者应立即就医。 ·禁止排入环境。 ·工作完毕,淋浴更衣 【事故响应】 ·小量泄漏:避免扬尘,用洁净的铲子收集于干燥、洁净、有盖的容器中,也可以用大量水冲洗,洗水稀释后放入废水系统。 ·大量泄漏:收集回收或运至废物处理场所处置。 ·皮肤接触:立即脱去被污染的衣着。用大量清水冲洗20-30分钟。如有不适感,就医。 ·眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗10-15分钟。如有不适感,就医。 ·吸入:迅速脱离现场至空气新鲜处。保持通风。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。·食入:误服者用水漱口,给饮牛奶或蛋清。就医。 ·灭火方式:用水、砂土扑救,但须防止物品遇水产生飞溅,造成灼伤。 【安全储存】 ·储存:储存于干燥清洁的仓间内。注意防潮和雨淋。应与易燃或可燃物及酸类分开存放。分装和搬运作业要注意个人防护。搬运时要轻装轻卸,防止包装及容器损坏。雨天不宜运输。 【废弃处置】 ·中和、稀释后,排入下水道,高浓度对水生生物有害。 请参阅盐酸化学品安全技术说明书 供应商:xxxxxxxxxxxxxxxxxxxxxxxxxx 电话:xxxxxxxx 地址:xxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxx 邮编:xxxxxxxxx 化学事故应急咨询电话:xxxxxxxxx
氢氧化钠水溶液的密度和浓度对照表 密度ρ20 kg/m3 浓度密度ρ20 kg/m3 浓度 %(质量)kmol/m3%(质量)kmol/m3 1000 0.159 0.040 1270 24.65 7.824 1010 1.045 0.264 1280 25.56 8.178 1020 1.94 0.494 1290 26.48 8.539 1030 2.84 0.731 1300 27.41 8.906 1040 3.75 0.971 1310 28.33 9.278 1050 4.66 1.222 1320 29.26 9.656 1060 5.56 1.474 1330 30.20 10.04 1070 6.47 1.731 1340 31.14 10.43 1080 7.38 1.992 1350 32.10 10.83 1090 8.28 2.257 1360 33.06 11.24 1100 9.19 2.527 1370 34.03 11.65 1110 10.10 2.802 1380 35.01 12.08 1120 11.01 3.082 1390 36.00 12.51 1130 11.92 3.367 1400 36.99 12.95 1140 12.83 3.655 1410 37.99 13.39 1150 13.73 3.947 1420 38.99 13.84 1160 14.64 4.244 1430 40.00 14.30 1170 15.54 4.545 1440 41.03 14.77 1180 16.44 4.850 1450 42.07 15.25 1190 17.35 5.160 1460 43.12 15.74 1200 18.26 5.476 1470 44.17 16.23 1210 19.16 5.796 1480 45.22 16.73 1220 20.07 6.122 1490 46.27 17.23 1230 20.98 6.451 1500 47.33 17.75 1240 21.90 6.788 1510 48.38 18.26 1250 22.82 7.129 1520 49.44 18.78 1260 23.73 7.475 1530 50.50 19.31
氢氧化钠标准溶液的溶液配制与标定 一、实验目的 1.学会配制一定浓度的标准溶液的方法。 2.学会用滴定法测定酸碱溶液浓度的原理和操作方法。 3.进一步练习滴定管、移液管的使用。 4.初步掌握酸碱指示剂的选择方法。熟悉指示剂的使用和终点的判据。 二、实验原理 测定时,一般都使用浓度约为0.1mol/L NaOH标准溶液。由于NaOH固体试剂的纯度不高,并易吸收空气中的CO2和水分,因此,不能直接配制法配制NaO H标准溶液,而必须用标定法。 标定碱液的基准物质很多,经常使用的基准物,如草酸(H2C2O4·2H2O,相对分子质量为126.07)、邻苯二甲酸氢钾(HOOCC6H4COOK,简写KHP相对分子质量为204.44)等。其中最常用的是邻苯二甲酸氢钾,滴定反应的化学方程式如下: 滴定终点时由于弱酸盐的水解,溶液呈碱性,所以应采用酚酞为指示剂,当溶液呈现微红色,30s内不褪色即为终点。 计算公式: 三、实验步骤 1.NaOH标准溶液的配制 经计算配制500ml 0.1 mol/L NaOH标准溶液需4g NaOH固体。
用台秤称量4g NaOH于1000ml烧杯中,用100ml量筒加入500ml水,并用玻璃棒搅拌溶解。 2.NaOH溶液浓度的标定 用分析天平精确称量0.5g左右的KHP三份,分别于250ml锥形瓶中,用10 0ml量筒加入30ml水,充分振荡使其完全溶解,滴加2滴酚酞指示剂。 用50ml碱式滴定管盛装NaOH标准溶液滴定至终点,记录消耗NaOH标准溶液的体积。 四、数据记录与处理(利用表中数据,练习数据处理) 五、注意事项 1.称量邻苯二甲酸氢钾时,所用锥形瓶外壁要干燥并编号(以后称量同)。 2.NaOH饱和溶液侵蚀性很强,长期保存最好用聚乙烯塑料化学试剂瓶贮存(用一般的饮料瓶会因被腐蚀而瓶底脱落)。在一般情况下,可用玻璃瓶贮存,但必须用橡皮塞。 六、思考题 1.如果用H2C2O4·2H2O标定时,又如何操作? 2.标定时,三次滴定消耗标准溶液的体积之间,远超过容量分析允许的0.2 %相对误差,即0.04ml,如此分析测定的结果能准确吗?
氢氧化钠溶液安全技术说明书 第一部分化学品及企业标识 化学品中文名:30%氢氧化钠溶液 化学品俗名或商品名:30%液碱 化学品英文名:Sodium hydroxide;Caustic soda 技术说明书编码:TTSX003 第二部分成分/组分信息 纯品混合物 化学品名称:氢氧化钠溶液 有害成分浓度CAS No. 氢氧化钠30% 1310-73-2 第三部分危险性概述 危险性类别:第8.2类碱性腐蚀品 侵入途径:吸入、食入 健康危害:本品有强烈刺激和腐蚀性。腐蚀鼻中隔;直接接触皮肤和眼可引起灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克。环境危害:对水体可造成污染。 燃爆危险:本品不燃,具强腐蚀性、强刺激性,可致人体灼伤。 第四部分急救措施 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟就医。 眼睛接触:立即提起眼睑,用大量就动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:用水漱口,给饮牛奶或蛋清。就医。
第五部分消防措施 危险特性:与酸发生中和反应并放热。具有强腐蚀性。 有害燃烧产物:可能产生有害的毒性烟雾。 灭火方法及灭火剂:本品不燃,由其它物质引起火灾时,应注意该物质的腐蚀性。 灭火注意事项:消防人员应穿防酸碱消防服。 第六部分泄漏应急处理 应急处理:隔离泄漏污染区,限制出入。液碱泄漏:收集回收后用水冲洗,冲洗水经中和处理后排入废系统。 消除方法:加入大量水中,调节至中性,再放入废水系统。也可用大量水冲洗,经稀释的洗水放入废水系统。如大量泄漏,收集回收或无害处理后废弃。 第七部分操作处理与储存 操作注意事项:操作人员必须经过专门培训持证上岗,严格遵守 工艺规程和岗位操作法。操作人员穿耐酸碱服,戴耐酸碱手套, 戴防护眼镜。避免与酸类接触。搬运时要轻装轻卸,防止包装及 容器损坏。配备泄漏应急处理设备。应当注意倒空容器内的残留 物。稀释或制备溶液时,应把碱加入水中,避免沸腾和飞溅。 储存注意事项:液碱贮槽应设围堤,并有明显标志。 第八部分暴露控制/个体防护 最高容许浓度:中国MAC(mg/m3):0.5 前苏联MAC(mg/m3):0.5 美国TLV—TWA:OSHA 2 mg/m3 美国TLV—STEL:ACGIH 2mg/m3 监测方法:重量法 工程控制:密闭操作。提供安全淋浴和洗眼设备。 呼吸系统防护:穿耐酸碱服,戴耐酸碱手套,戴防护眼镜。必要时,佩戴空气(氧气)呼吸器。 眼睛防护:呼吸系统防护中已作防护或佩戴防护眼镜。 身体防护:穿耐酸碱服。
密度g/m3 质量分数%摩尔浓度mol/L密度g/m3质量分数,%摩尔浓度mol/L 1.005 0.602 0.151 1.095 8.74 2.391 1.01 1.045` 0.264 1.1 9.19 2.527 1.015 1.49 0.378 1.105 9.645 2.664 1.02 1.94 0.494 1.11 10.1 2.802 1.025 2.39 0.611 1.115 10.555 2.942 1.03 2.84 0.731 1.12 11.01 3.082 1.035 3.29 0.851 1.125 11.46 3.224 1.04 3.745 0.971 1.13 11.92 3.367 1.045 4.2 1.097 1.135 1 2.37 3.51 1.05 4.655 1.222 1.14 1 2.83 3.655 1.055 5.11 1.347 1.145 13.28 3.801 1.06 5.56 1.474 1.15 13.73 3.947 1.065 6.02 1.602 1.155 14.18 4.095 1.07 6.47 1.731 1.16 14.64 4.244 1.075 6.93 1.862 1.165 15.09 4.395 1.08 7.38 1.992 1.17 15.54 4.545 1.085 7.83 2.123 1.175 15.99 4.697 1.09 8.28 2.257 1.18 16.44 4.85 NaOH密度,质量分数与摩尔浓度对应(二) 密度g/m3 质量分数%摩尔浓度mol/L 密度g/m3 质量分数%摩尔浓度mol/L 1.185 16.89 5.004 1.37 34.03 11.65 1.19 17.345 5.16 1.375 34.52 11.86 1.195 17.8 5.317 1.38 35.01 1 2.08 1.2 18.255 5.476 1.385 35.5 1 2.29 1.275 25.1 8 1.39 36 1 2.51 1.28 25.56 8.178 1.395 36.495 1 2.73 1.285 26.02 8.357 1.4 36.99 1 2.95 1.29 26.48 8.0539 1.405 37.49 13.17 1.295 26.94 8.722 1.41 37.99 13.3 1.3 27.41 8.906 1.415 38.49 13.61 1.305 27.87 9.092 1.42 38.99 13.84 1.31 28.33 9.278 1.425 39.495 14.07 1.315 28.8 9.466 1.43 40 14.3
氢氧化钠安全技术说明书 第一部分:化学品名称 中文名称:氢氧化钠 英文名称:sodiun hydroxide 中文名称2:烧碱 英文名称2:Caustic soda 技术说明书编码:813 CAS No.:1310-73-2 分子式:NaOH 分子量:40.01 第二部分:成分/组成信息 有害物成分:氢氧化钠 含量:≥99.5% CAS No.:1310-73-2 第三部分:危险性概述 危险性类别:第8.2类碱性腐蚀品 侵入途径:吸入、食入、皮肤接触。 健康危害:本品有强烈刺激和腐蚀性。粉尘刺激眼和呼吸道,腐蚀鼻中隔;皮肤和眼直接接触可引起灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克。 环境危害:对水体可造成污染。 燃爆危险:本品不燃,具强腐蚀性、强刺激性,可致人体灼伤。 第四部分:急救措施 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。就医。 眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:用水漱口,给饮牛奶或蛋清。就医。 第五部分:消防措施 危险特性:与酸发生中和反应并放热。遇潮时对铝、锌和锡有腐蚀性,并放出易燃易爆的氢气。本品不会燃烧, 遇水和水蒸气大量放热, 形成腐蚀性溶液。具有强腐蚀性。 有害燃烧产物:可能产生有害的毒性烟雾。 灭火方法:用水、砂土扑救,但须防止物品遇水产生飞溅,造成灼伤。 第六部分:泄漏应急处理 隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具(全面罩),穿防酸碱工作服。不要直接接触泄漏物。小量泄漏:避免扬尘,用洁净的铲子收集于干燥、洁净、有盖的容器中。也可以用大量水冲洗,洗水稀释后放入废水系统。大量泄漏:收集回收或运至废物处理场所处臵。
氢氧化钠考点聚焦 氢氧化钠(NaOH),俗称烧碱、火碱、苛性钠,常温下为白色晶体,有强腐蚀性。易溶于水,其水溶液呈碱性,能使酚酞变红。 一、验证二氧化碳与氢氧化钠反应的发生 探究题1.有下列四种实验设计及操作,实验过程中其现象不足以说明C02与Na0H溶液发生了反应的是() 问题:如下装置能否证明CO2与氢氧化钠溶液发生了反应?如能,各自会出现什么样的实验现象? 练习.有下列四种实验设计及操作,实验过程中其现象可以说明C02与Na0H溶液确实发生了化学反应的是() A B C D 二、检验氢氧化钠是否变质 氢氧化钠久露于空气中,不仅会吸收空气中的水分而潮解,而且可以和空气中的二氧化碳气体发生化学反应生成碳酸钠,导致氢氧化钠变质。 检验NaOH溶液是否变质,大致有以下几种方案: 方案一、选择一种酸溶液,如盐酸。但是,所以如果用盐酸来检验时,一定要注意,所取的盐酸的量必须是过量,否则就不可以确定NaOH是否变质。 方案二、选择一种碱溶液,如Ca(OH)2溶液、Ba(OH)2溶液,此方案的灵敏度比较高。 但是要设计方案来验证CO2与NaOH溶液的是否确实发生了化学反应,而不是CO2溶解在NaOH溶液中时。我们就不可以选取此类碱溶液来验证。因为CO2本身就可以溶于水中,形成H2CO3,H2CO3遇到Ca(0H)2或Ba(OH)2时,会生成白色沉淀。而应该从CO2与NaOH反应产
物的角度来验证,可以取通入CO2后液体,向所取液体里加入足量的稀盐酸(或适量CaCl2溶液),充分振荡后,观察现象。 方案三、选择一种盐溶液,如BaCl2溶液。有时,同学们常用CaCl2溶液代替BaCl2溶液检验NaOH是否变质。这种方案存在缺陷。因为当加入的CaCl2溶液中的Ca2+与NaOH中的OH--的浓度比较大时,也会因为一定温度下Ca(OH)2的溶解度相对比较小,而有部分Ca(OH)2晶体析出,使得溶液中出现浑浊现象。所以关于盐的选择,最好选取BaCl2,不宜用CaCl2。 探究题2:四位同学分别用下列四种方法检验NaOH溶液是否已经变质(含有Na2CO3) ①加入少量稀盐酸,无气泡放出,则一定不含有Na2CO3; ②加少量澄清石灰水,有沉淀生成,则一定含有Na2CO3; ③加少量CaCl2溶液,有沉淀生成则一定含有Na2CO3; ④加少量BaCl2溶液,有沉淀生成,则一定含有Na2CO3。 其中探究方法和结论都正确的是() A、①② B、①②③ C、②④、①②③④ 探究题3.向Na2CO3溶液里滴加盐酸,开始时无气泡产生,后来才有气泡产生;向盐酸里滴加Na2CO3溶液时,立即就有气泡产生。这说明() A、Na2CO3过量时,主要发生的反应是 Na2CO3+HCl = NaHCO3+NaCl B、Na2CO3跟盐酸不反应 C、盐酸过量时,主要发生的反应是Na2CO3+2HCl = 2NaCl+H2O+CO2↑ D、产生的气泡是挥发出来的氯化氢气体 三、探究氢氧化钠的变质程度 探究题4:某化学兴趣小组甲、乙、丙三位同学对暴露在空气中的氢氧化钠是否全部变质进行了探究:甲同学,取样品加入盐酸,有气泡产生,完全反应后,蒸干得到的固体全部是氯化钠,认为样品全部变质。 乙同学,取样品加水溶解,滴加无色酚酞试液变红色,认为样品没有全部变质。 丙同学,取样品加水后溶解,先加入过量的A溶液,过滤后在滤液中加入B溶液,通过观察现象得出正确结论:A为 B为。 得出正确结论的理由为。 四、除去氢氧化钠变质后的碳酸钠杂质 变质后的NaOH溶液中会有较多的CO32-,可以加入含Ca2+或Ba2+的溶液,与CO32-结合成沉淀,通过过滤而除去。为了不再引入新的杂质,考虑到原来NaOH溶液中存在OH-,此时选用Ba(OH)2溶液的效果比较好。因为,一定温度下Ca(OH)2溶液的质量分数相对比较小,溶液相对比较稀,除去杂质的效果远远不如用Ba(OH)2溶液好。 答案探究题1:B 1:能,图1中U形管中的红墨水被倒吸进集气瓶中。2:能,图2是锥形瓶内气球胀大。3:能,图3盛氢氧化钠溶液的广口瓶内的长导管口有气泡产生,原因是锥形瓶内二氧化碳气体反应后,气压减少,使盛氢氧化钠溶液的广口瓶内气压也减小,空气沿导管被压入广口瓶内。D 探究题2: C 探究题3:A、C 探究4:甲不正确。乙不正确。丙同学的方案是: BaCl2,无色酚酞试液
氢氧化钠滴定液配制与标定 1误差要求 2 氢氧化钠滴定液(1mol/L、0.5mol/L、0.1mol/L、0.05mol/L、或0.02mol/L、0.01molL) 仪器:分析天平、托盘天平、烧杯、碱式滴定管(50mL)、玻棒、胶头滴管、量筒、容量瓶(1000 mL)、称量瓶、锥形瓶 3 配制:取氢氧化钠适量,加水振摇使溶解成饱和溶液,冷却后,置聚乙烯塑料瓶中,静置数日,澄清后备用。 氢氧化钠滴定液(1mol/L)取澄清的氢氧化钠饱和溶液56ml,加新沸过的冷水使成1000ml,摇匀。 氢氧化钠滴定液(0.5mol/L)取澄清的氢氧化钠饱和溶液28ml,加新沸过的冷水使成1000ml,摇匀。 氢氧化钠滴定液(0.1mol/L)取澄清的氢氧化钠饱和溶液 5.6ml,加新沸过的冷水使成1000ml,摇匀。 4 标定:氢氧化钠滴定液(1mol/L)取在105℃干燥至恒重的基准邻苯二甲酸氢钾约6g,精密称定,加新沸过的冷水50ml,振摇,使其尽量溶解;加酚酞指示液2滴,用本液滴定;在接这终点时,应使邻苯二甲酸氢钾完全溶解,滴定至溶液显粉红色。每1ml氢氧化钠滴定液(1mol/L)相当于204.2 mg 的邻苯二甲酸氢钾。根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度,即得。 氢氧化钠滴定液(0.5mol/L)取在105℃干燥至恒重的基准邻苯二甲酸氢钾约3g,照上法标定。每1ml氢氧化钠滴定液(0.5mol/L)相当于102.1 mg 的邻苯二甲酸氢钾。 氢氧化钠滴定液(0.1mol/L)取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.6g,照
上法标定。每1ml氢氧化钠滴定液(0.1mol/L)相当于20.42 mg 的邻苯二甲酸氢钾。 如需用氢氧化钠滴定液(0.05mol/L、0.02mol/L、或0.01mol/L)时,可取氢氧化钠滴定液(0.1mol/L)加沸过的冷水稀释制成,必要时可用盐酸滴定液(0.05molL、0.02molL或0.01molL)标定浓度。 5 氢氧化钠滴定液(0.1mol/L)的浓度C(mol/L)按下式计算: M C(mol/L)= V 204.2 式中V:滴定所耗氢氧化钠滴定液的体积(ml) M:基准邻苯二甲酸氢钾的称取量(mg); 204.2与每1ml的氢氧化钠滴定液(1mol/L)相当以mg表示的邻苯二甲酸氢钾的质量; 6 注意事项 1固体氢氧化钠应放在表面皿上或小烧杯中称量,不能在称量纸上称量,因为氢氧化钠极易吸潮,因而称量速度尽量快。 2滴定前,应检查橡皮管内和滴定管尖处是否有气泡,如有气泡应排除,否则影响其读数,会给测定带来误差。 3盛放基准物的3个锥形瓶应编号,以免混淆,防止过失误差。 4有效期为3个月,若过有效期则需重新标定。 5用饱和氢氧化钠液制备应新沸冷水制成而且应陈化6小时左右。排除碳酸钠干扰与二氧化碳。 6制备饱和氢氧化钠时应分多次加入氢氧化钠固体,过饱和后应放置三天后取上清液,应一次取出避免倒流而冲浑液体。 7也可用新制热蒸馏水,但制好后应放至室温,尽量避免二氧化碳干扰。 8基准物(基准物质是分析化学中用于直接配制标准溶液或标定滴定分析中操作溶液浓度的物质。)应在乳钵中研细,利于溶解,在终点前基准应全溶解,否则结果有误。 9标定前贮存聚乙烯塑料瓶中,用虹吸法取用,进气管前端用钠石灰和棉花过滤,定期或钠石灰变色后更换,防止二氧化碳影响浓度。 10工作时应佩戴酸碱手套,防护服等。 11室温下密封存放至阴凉处。