
A.钠熔成小球并在液面上游动
B.有气体生成
C.试管底部有银白色物质生成
D.溶液变浑浊
4.相同质量的铝,分别与足量的强酸、强碱反应,产生氢气体积比为 1:1 .
5. 某无色溶液中放入铝片后有氢气放出,则下列离子在该溶液中肯定可以大量共存的是(A )
A.Na +
B.Mg 2+
C.S 2-
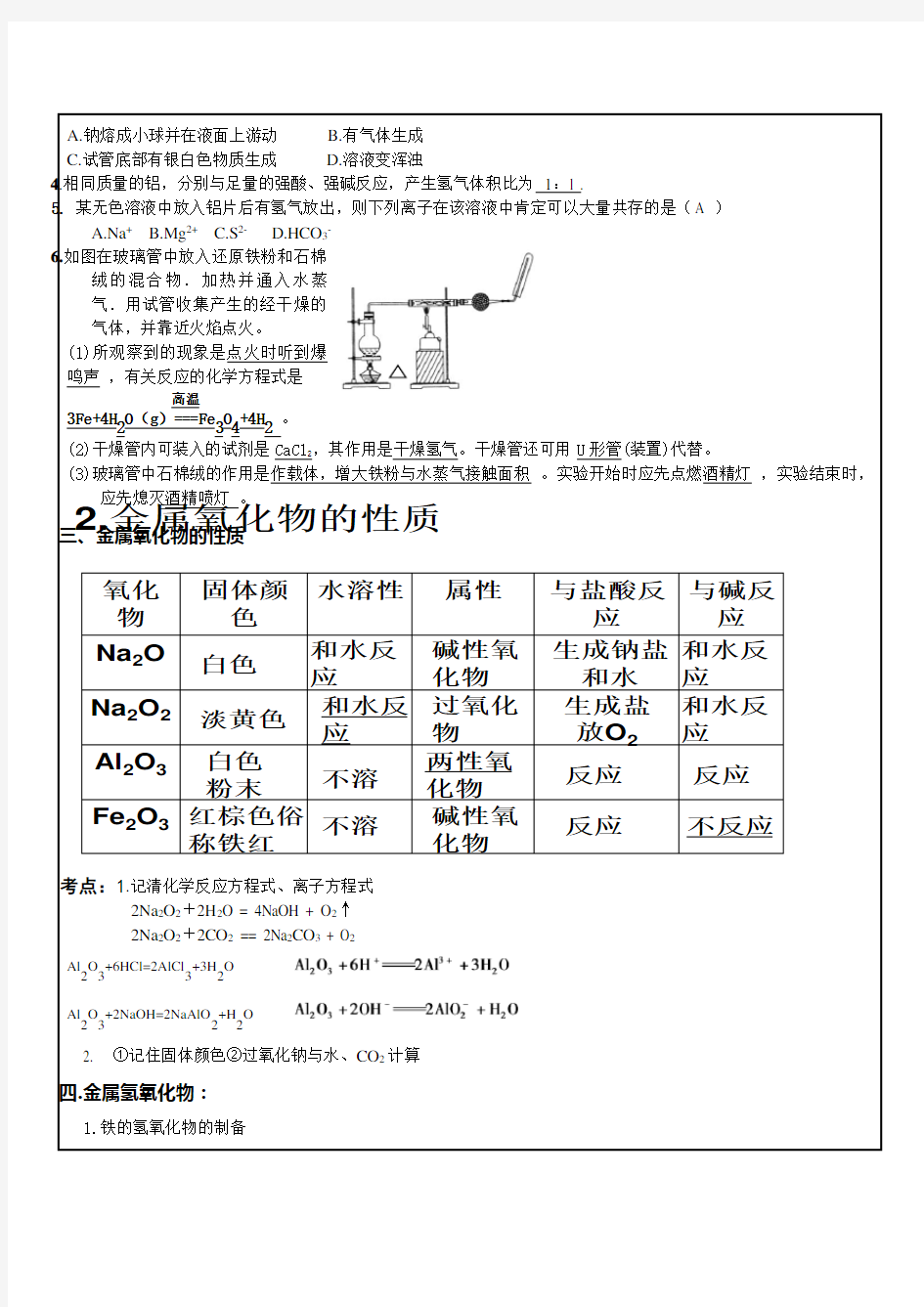
D.HCO 3- 6.如图在玻璃管中放入还原铁粉和石棉
绒的混合物.加热并通入水蒸气.用试管收集产生的经干燥的气体,并靠近火焰点火。
(1)所观察到的现象是点火时听到爆鸣声 ,有关反应的化学方程式是
高温
3Fe+4H 2O (g )===Fe 3O 4+4H 2
。
(2)干燥管内可装入的试剂是CaCl 2,其作用是干燥氢气。干燥管还可用U 形管(装置)代替。
(3)玻璃管中石棉绒的作用是作载体,增大铁粉与水蒸气接触面积 。实验开始时应先点燃酒精灯 ,实验结束时,
应先熄灭酒精喷灯 。
三、金属氧化物的性质
与盐酸反
应
属性Fe 2O 3
Al 2O 3Na 2O 2Na 2O 与碱反应水溶性固体颜色氧化物白色淡黄色
红棕色俗称铁红
和水反应
和水反应
不溶不溶2.金属氧化物的性质
白色
粉末
碱性氧化物碱性氧化物
过氧化物
两性氧化物生成钠盐和水生成盐放O 2反应反应
和水反应
和水反应反应不反应
考点:1.记清化学反应方程式、离子方程式
2Na 2O 2+2H 2O = 4NaOH + O 2↑ 2Na 2O 2+2CO 2 == 2Na 2CO 3 + O 2
Al 2O 3+6HCl=2AlCl 3+3H 2O Al 2O 3+2NaOH=2NaAlO 2+H 2
O 2. ①记住固体颜色②过氧化钠与水、CO 2计算
四.金属氢氧化物:
1.铁的氢氧化物的制备
6.为下面操作,选合适的图像。
7、在一定条件下,将钠与氧气反
应的生成物1.5 9溶于水,所得溶液恰好能被80 ml 。浓度为0.50 mol /L 的HCl 溶液中和,则该生成物的成分是 (C)
A .Na 2O
B .Na 2O 2
C .Na 2O 和Na 2O 2
D .Na 2O 2和NaO 2 五、盐考点:
2、溶解,加入CaCl 2溶液,产生沉淀的是碳酸钠。
Na 2CO 3+ CaCl 2= 2NaCl + CaCO 3
1、加热固体,产生能使石灰水变浑浊的无色气体的是碳酸氢钠。
[怎样鉴别Na 2CO 3和NaHCO 3]
2NaHCO 3 = Na 2CO 3+ H 2O + CO 2
[Na 2CO 3和NaHCO 3相互转化]
Na 2CO 3
NaHCO 3
通入CO 2
加热加入NaOH
2NaHCO 3=Na 2CO 3+H 2O+CO 2NaHCO 3+NaOH=Na 2CO 3+H 2O Na 2CO 3+H 2O+CO 2= 2NaHCO 3
1.下列说法中不正确的是(c )
A.人类历史上使用最早的合金是青铜
B.司母戊鼎是我国目前已发现的最重的青铜器
C.目前世界上使用量最大的合金是铝合金
D.目前世界上用途最广的合金是钢
2.下列有关金属的叙述正确的是(B)
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素在化合物中一定显正价
C.金属元素在不同化合物中的化合价均相同
D.酸根离子中一定不含金属原子
3、下列说法正确的是(B)
A 合金钢不含非金属元素
B合金钢和碳素钢都含碳元素
C碳素钢是由铁和碳元素组成的化合物
D碳素钢是由铁和碳通过化合反应而形成的
解析:合金钢是在碳素钢中加入铬、锰、钨、硅等不同元素而形成的,合金钢中也含有非金属元素;合金是混合物。
4、用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察时看到火焰呈黄色,下列判断正确的是( B )
A.只含Na+
B.一定含Na+,可能含有K+
C.既含有Na+,又含有K+
D.可能含有Na+,可能还含有K+
第四章非金属及其化合物复习
一.硅
1.相关反应
Si
物理性质晶体硅:灰黑色固体、金属光泽熔点高、硬而脆
化学性质与非金属反应Si + O2 △SiO2
与氢氟酸反应Si + 4HF = SiF4↑+ 2H2↑
与强碱溶液反应Si + 2NaOH + H2O = Na2SiO3 + 2H2↑
③漂白原理:Ca(ClO)2 + CO2 + H2O = CaCO3↓+ 2HClO (在溶液中)漂白慢Ca(ClO)2 + 2HCl = CaCl2 + 2HClO 漂白快
④久置失效发生的反应:Ca(ClO)2 + CO2 + H2O = CaCO3+ 2HClO2HClO
光照
或加热
2HCl + O2↑
5.Br2、I2在不同溶剂中的颜色
水苯或汽油四氯化碳
Br2黄~橙橙~橙红橙~橙红
I2深黄~褐淡紫~紫红紫~深紫
6.置换反应Cl2 + 2NaBr = Br2+ 2NaCl Br2 + 2KI = I2 + 2KBr ∴氧化性Cl2 >Br2 >I2
7.I2遇淀粉溶液后,溶液呈蓝色 I- 氧化剂
——————→I2
三.氮
1.氮的氧化物
NO:无色气体、有毒(同CO)、难溶与水2NO + O2 = 2NO2
NO2:红棕色气体、有毒、与水反应3NO2 + 2H2O = 2HNO3 + NO
2.有关NO与O2或NO2与O2混合通入水中,液面上升一定高度时用的方程式
4NO2 + O2 + 2H2O = 4HNO3 4NO+ 3O2 + 2H2O = 4HNO3
3.硝酸
物理性质无色液体、有刺激性气味、能以任意比溶于水
化学性质
酸的通性
强
氧
化
性
与金属氧化物3FeO + 10HNO3 = 3Fe(NO3)3 + NO↑+ 5H2O
与金属
3Cu + 8HNO3(稀) = 3Cu(NO3)2 +2NO↑+ 4H2O
Cu + 4HNO3(浓) = Cu(NO3)2 +2NO2↑+ 2H2O 与非金属 C + 4HNO3(浓) △CO2↑+ 4NO2↑+ 2H2O
不稳定性4HNO3
光照
或加热
4NO2↑+ O2↑+ H2O
4.氨( NH3 )
物理性质无色气体、有刺激性气味、密度小于空气、1:700溶于水
化学性质与H2O NH3 + H2O NH3·H2O NH4++ OH-与酸NH3 + HCl = NH4Cl
氨的
催化氧化
4NH3 + 5O2
催化剂
加热
4NO + 6H2O
实验室制取原理
NH4+ + OH-△NH3↑+ H2O
2NH4Cl +Ca(OH )2△2NH3↑+ CaCl2 + 2H2O
5.实验室制取干燥NH3的方法:
制取原理:2NH4Cl +Ca(OH )2△2NH3↑+ CaCl2 + 2H2O
气体成分:NH3(H2O )
除水用试剂:碱石灰
(不用浓H2SO4 、CaCl2原因是:2NH3 + H2SO4 = (NH4)2SO4 ; CaCl2 + 8NH3 =CaCl2·8NH3 ) 6.受热易分解NH3·H2O △NH3↑+ H2O NH4HCO3 △NH3↑+ CO2↑+ H2O
7.氨水中的微粒
分子:H2O NH3·H2O NH3离子:NH4+H+ OH-
四.硫
1.SO2的性质
最全高中数学 (经典版) 第一章算法初步 1.1.1 算法的概念 1、算法概念:在数学上,现代意义上的“算法”通常是指可以用计算机来解决的某一类问题是程序或步骤,这些程序或步骤必须是明确和有效的,而且能够在有限步之内完成. 2. 算法的特点: (1) 有限性:一个算法的步骤序列是有限的,必须在有限操作之后停止,不能是无限的. (2) 确定性:算法中的每一步应该是确定的并且能有效地执行且得到确定的结果,而不应当是模棱两可.
(3) 顺序性与正确性:算法从初始步骤开始,分为若干明确的步骤,每一个步骤只能有一个确定的后继步骤,前一步是后一步的前提,只有执行完前一步才能进行下一步,并且每一步都准确无误,才能完成问题. (4) 不唯一性:求解某一个问题的解法不一定是唯一的,对于一个问题可以有不同的算法. (5) 普遍性:很多具体的问题,都可以设计合理的算法去解决,如心算、计算器计算都要经过有限、事先设计好的步骤加以解决. 1.1.2 程序框图 1、程序框图基本概念: (一) 程序构图的概念:程序框图又称流程图,是一种用规定的图形、指向线及文字说明来准确、直观地表示算法的图形。 一个程序框图包括以下几部分:表示相应操作的程序框;带箭头的流程线;程序框外必要文 字说明。 学习这部分知识的时候,要掌握各个图形的形状、作用及使用规则,画程序框图的规则如下: 1、使用标准的图形符号。 2、框图一般按从上到下、从左到右的方向画。 3、除判断框外, 大多数流程图符号只有一个进入点和一个退出点。判断框具有超过一个退出点的唯一符号。 4、判断框分两大类,一类判断框“是”与“否”两分支的判断,而且有且仅有两个结果; 另一类是多分支判断,有几种不同的结果。5、在图形符号内描述的语言要非常简练清楚。(三)、算法的三种基本逻辑结构:顺序结构、条件结构、循环结构。 1、顺序结构:顺序结构是最简单的算法结构,语句与语句之间,框与框之间是按从上到下 的顺序进行的,它是由若干个依次执行的处理步骤组成的,它是任何一个算法都离不开的一
高中化学重要知识点详细总结一、俗名 无机部分: 纯碱、苏打、天然碱、口碱:Na2CO3小苏打:NaHCO3大苏打:Na2S2O3石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4·.H2O 莹石:CaF2重晶石:BaSO4(无毒)碳铵:NH4HCO3 石灰石、大理石:CaCO3生石灰:CaO 食盐:NaCl 熟石灰、消石灰:Ca(OH)2芒硝:Na2SO4·7H2O (缓泻剂) 烧碱、火碱、苛性钠:NaOH 绿矾:FaSO4·7H2O 干冰:CO2明矾:KAl (SO4)2·12H2O 漂白粉:Ca (ClO)2、CaCl2(混和物)泻盐:MgSO4·7H2O 胆矾、蓝矾:CuSO4·5H2O 双氧水:H2O2皓矾:ZnSO4·7H2O 硅石、石英:SiO2刚玉:Al2O3 水玻璃、泡花碱、矿物胶:Na2SiO3铁红、铁矿:Fe2O3磁铁矿:Fe3O4黄铁矿、硫铁矿:FeS2铜绿、孔雀石:Cu2 (OH)2CO3菱铁矿:FeCO3赤铜矿:Cu2O 波尔多液:Ca (OH)2和CuSO4石硫合剂:Ca (OH)2和S 玻璃的主要成分:Na2SiO3、CaSiO3、SiO2过磷酸钙(主要成分):Ca (H2PO4)2和CaSO4重过磷酸钙(主要成分):Ca (H2PO4)2天然气、沼气、坑气(主要成分):CH4水煤气:CO和H2硫酸亚铁铵(淡蓝绿色):Fe (NH4)2 (SO4)2溶于水后呈淡绿色 光化学烟雾:NO2在光照下产生的一种有毒气体王水:浓HNO3与浓HCl按体积比1:3混合而成。 铝热剂:Al + Fe2O3或其它氧化物。尿素:CO(NH2) 2 有机部分: 氯仿:CHCl3电石:CaC2电石气:C2H2 (乙炔) TNT:三硝基甲苯酒精、乙醇:C2H5OH 氟氯烃:是良好的制冷剂,有毒,但破坏O3层。醋酸:冰醋酸、食醋CH3COOH 裂解气成分(石油裂化):烯烃、烷烃、炔烃、H2S、CO2、CO等。甘油、丙三醇:C3H8O3 焦炉气成分(煤干馏):H2、CH4、乙烯、CO等。石炭酸:苯酚蚁醛:甲醛HCHO 福尔马林:35%—40%的甲醛水溶液蚁酸:甲酸HCOOH 葡萄糖:C6H12O6果糖:C6H12O6蔗糖:C12H22O11麦芽糖:C12H22O11淀粉:(C6H10O5)n 硬脂酸:C17H35COOH 油酸:C17H33COOH 软脂酸:C15H31COOH 草酸:乙二酸HOOC—COOH 使蓝墨水褪色,强酸性,受热分解成CO2和水,使KMnO4酸性溶液褪色。二、颜色 铁:铁粉是黑色的;一整块的固体铁是银白色的。Fe2+——浅绿色Fe3O4——黑色晶体 Fe(OH)2——白色沉淀Fe3+——黄色Fe (OH)3——红褐色沉淀Fe (SCN)3——血红色溶液FeO——黑色的粉末Fe (NH4)2(SO4)2——淡蓝绿色Fe2O3——红棕色粉末FeS——黑色固体 铜:单质是紫红色Cu2+——蓝色CuO——黑色Cu2O——红色CuSO4(无水)—白色CuSO4·5H2O——蓝色Cu2(OH)2CO3—绿色Cu(OH)2——蓝色[Cu(NH3)4]SO4——深蓝色溶液 BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl 、Mg (OH)2、三溴苯酚均是白色沉淀 Al(OH)3白色絮状沉淀H4SiO4(原硅酸)白色胶状沉淀 Cl2、氯水——黄绿色F2——淡黄绿色气体Br2——深红棕色液体I2——紫黑色固体 HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾 CCl4——无色的液体,密度大于水,与水不互溶KMnO4--——紫色MnO4-——紫色 Na2O2—淡黄色固体Ag3PO4—黄色沉淀S—黄色固体AgBr—浅黄色沉淀 AgI—黄色沉淀O3—淡蓝色气体SO2—无色,有剌激性气味、有毒的气体 SO3—无色固体(沸点44.8 0C)品红溶液——红色氢氟酸:HF——腐蚀玻璃 N2O4、NO——无色气体NO2——红棕色气体NH3——无色、有剌激性气味气体 三、现象: 1、铝片与盐酸反应是放热的,Ba(OH)2与NH4Cl反应是吸热的; 2、Na与H2O(放有酚酞)反应,熔化、浮于水面、转动、有气体放出;(熔、浮、游、嘶、红) 3、焰色反应:Na 黄色、K紫色(透过蓝色的钴玻璃)、Cu 绿色、Ca砖红、Na+(黄色)、K+(紫色)。 4、Cu丝在Cl2中燃烧产生棕色的烟; 5、H2在Cl2中燃烧是苍白色的火焰; 6、Na在Cl2中燃烧产生大量的白烟; 7、P在Cl2中燃烧产生大量的白色烟雾; 8、SO2通入品红溶液先褪色,加热后恢复原色; 9、NH3与HCl相遇产生大量的白烟;10、铝箔在氧气中激烈燃烧产生刺眼的白光; 11、镁条在空气中燃烧产生刺眼白光,在CO2中燃烧
高中历史必修三知识点总结人教版 专题一:中国古代的思想 本单元主题:中国传统文化主流思想的演变(儒家思想的产生和发展历程) 春秋儒家思想的出现战国孟子荀子发展儒家思想秦朝焚书坑儒西汉 “罢黜百家,独尊儒术”,确立儒家思想的统治地位魏晋南北朝儒学危机唐宋 后三教合一宋明理学明清对传统儒学的批判 一、孔子与老子 (一)孔子 1、生平著述:春秋鲁国人,“三家一创”;《诗》《书》《礼》《易》《春秋》和《乐》 2、学说: ①政治学说:A、“仁”(仁者爱人)B、“礼”(“克己复礼”)C、“为政以德” ②哲学观点(天命观,畏天命):“敬鬼神而远之” ③教育思想:“有教无类”“因材施教”“知之为知之,不知为不知”;“温故而知新”;“学而不思则罔,思而不学则殆”;“当仁不让于师” 3、历史地位: ①所倡导的儒家思想被后人发扬光大,成为中国传统文化的主流。 ②在世界文化史上具有重要的影响。 ③后人整理孔子言行为《论语》,尊孔子为圣人,历世景仰。 (二)老子: 1、生平著述:道家学派创始人;《道德经》 2、学说: ①哲学思想: A、“道”是万物的本源,“天法道,道法自然”。 B、辩证法思想:事物是矛盾对立的,并可互相转化; ②政治学说:“无为而治” 3、历史地位: ①是中国哲学史上第一个探讨宇宙本源的哲学家②对中国文化产生了深远的影响。 二、战国时期的百家争鸣 (一)百家争鸣的历史背景: 1、生产力发展和社会大变革是百家争鸣出现的根本原因 2、分裂的政局和社会变革时代,造成思想和言论的空前自由 3、私学兴起,教育相对普及,培养了大批人才 4、动荡的兼并局势,各国君主都想称霸争雄,所以竟相礼贤下士、招揽人才 (二)儒家:孟子和荀子 1、孟子 ①孟子的思想 A仁政学说B性善说C义利观:养浩然之气;先义后利、舍生取义; ②历史地位:A《孟子》成为四书之一B他被称为“亚圣” 2、荀子 ①荀子的思想: A“天行有常”、“制天命而用之”B、性恶论C 政治思想:“以礼为主,礼法并施” ②荀子思想的历史地位 A、被视作儒家异端 B、唯物思想在中国哲学上具有深远影响 (三)墨家
高一化学必修三知识点归纳 【原子结构与性质】 1能级与能层 ⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。 能级交错:由构造原理可知,电子先进入4s轨道,后进入3d轨道,这种现象叫能级交错。说明:构造原理并不是说4s能级比3d能级能量低(实际上4s能级比3d能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。 (2)能量最低原理现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。 (3)泡利(不相容)原理:基态多电子原子中,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli)原理。 (4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund)规则 洪特规则特例:当p、d、f轨道填充的电子数为全空、半充满或全充满时,原子处于较稳定的状态。 4.基态原子核外电子排布的表示方法 (1)电子排布式①用数字在能级符号的右上角表明该能级上排布的电子数,这就是电子排布式,例如K:1s22s22p63s23p64s1。 ②为了避免电子排布式书写过于繁琐,把内层电子达到稀有气体元素原子结构的部分以相应稀有气体的元素符号外加方括号表示,例如K:[Ar]4s1。 ③外围电子排布式(价电子排布式) (2)电子排布图(轨道表示式)是指将过渡元素原子的电子排布式中符合上一周期稀有气体的原子的电子排布式的部分(原子实)或主族元素、0族元素的内层电子排布省略后剩下的式子。每个方框或圆圈代表一个原子轨道,每个箭头代表一个电子。如基态硫原子的轨道表示式为 二.原子结构与元素周期表 1.一个能级组最多所容纳的电子数等于一个周期所包含的元素种类2n2。但一个能级组不一定全部是能量相同的能级,而是能量相近的能级。 2.元素周期表的分区 (1)根据核外电子排布 确定元素在周期表中位置的方法 ?若已知元素序数Z,找出与之相近上一周期的惰性气体的原子序数R,先确定其周期数。再根究Z—R的值,确定元素所在的列,依照周期表的结构数出所在列对应的族序数。 ③若已知元素的外围电子排布,可直接判断该元素在周期表中的位置。如:某元素的外围电子排布为4s24p4,由此可知,该元素位于p区,为第四周期ⅥA族元素。即能层为其周期数,最外层电子数为其族序数,但应注意过渡元素(副族与第Ⅷ族)的能层为其周期数,外围电子数应为其纵列数而不是其族序数(镧系、锕系除外)。 (2)主族元素价电子数=族序数,副族元素IIIB--VIII族价电子数=族序数IB,IIB价电子的最外层数=族序数 (3)各区元素化学性质及原子最外层电子排布特点 S区ns1-2p区ns2np1-6、d区(n-1)d1-9ns1-2、ds区(n-1)d10ns1-2 三.元素周期律
高中生物必修三知识点汇编 第一章 一、细胞的生活的环境: 1、单细胞(如草履虫)直接与外界环境进行物质交换 2、多细胞动物通过内环境作媒介进行物质交换 养料 O2养料 O2 外界环境血浆组织液细胞(内液) 代谢废物、CO2淋巴代谢废物、CO2 内环境 细胞外液又称内环境(是细胞与外界环境进行物质交换的媒介) 其中血细胞的内环境是血浆 淋巴细胞的内环境是淋巴 毛细血管壁的内环境是血浆、组织液 毛细淋巴管的内环境是淋巴、组织液 3、组织液、淋巴的成分与含量与血浆相近,但又不完全相同,最主要的差别在于血浆中含有较多的蛋 白质,而组织液淋巴中蛋白质含量较少。 4、内环境的理化性质:渗透压,酸碱度,温度 ①血浆渗透压大小主要与无机盐、蛋白质含量有关;无机盐中Na+、cl-占优势 细胞外液渗透压约为770kpa 相当于细胞内液渗透压; ②正常人的血浆近中性,PH为7.35-7.45与HCO3-、HPO42-等离子有关; ③人的体温维持在370C 左右(一般不超过10C )。 二、内环境稳态的重要性: 1、稳态是指正常机体通过调节作用,使各个器官系统协调活动,共同维持内环境的相对稳定状态。 内环境成分相对稳定 内环境稳态温度 内环境理化性质的相对稳定酸碱度(PH值) 渗透压 ①稳态的基础是各器官系统协调一致地正常运行 ②调节机制:神经-体液-免疫 ③稳态相关的系统:消化、呼吸、循环、排泄系统(及皮肤) ④维持内环境稳态的调节能力是有限的,若外界环境变化过于剧烈或人体自身调节能力出现障碍时
3、组织液、淋巴的成分与含量与血浆相近,但又不完全相同,最主要的差别在于血浆中含有较多 的蛋白质,而组织液淋巴中蛋白质含量较少。 4、内环境的理化性质:渗透压,酸碱度,温度 ①血浆渗透压大小主要与无机盐、蛋白质含量有关;无机盐中Na+、cl-占优势 细胞外液渗透压约为770kpa 相当于细胞内液渗透压; ②正常人的血浆近中性,PH为7.35-7.45与HCO3-、HPO42-等离子有关; ③人的体温维持在370C 左右(一般不超过10C )。 ④维持内环境稳态的调节能力是有限的,若外界环境变化过于剧烈或人体自身调节能力出现障碍时 内环境稳态会遭到破坏 2、内环境稳态的意义:机体进行正常生命活动的必要条件 第二章 三、神经调节: 1、神经调节的结构基础:神经系统 细胞体 神经系统的结构功能单位:神经元树突 突起神经纤维 神经元在静息时电位表现为外正内负 功能:传递神经冲动 2、神经调节基本方式:反射 反射的结构基础:反射弧
高考化学知识归纳总结(打印版) 第一部分化学基本概念和基本理论 一.物质的组成、性质和分类: (一)掌握基本概念 1.分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒. (2)按组成分子的原子个数可分为: 单原子分子如:He、Ne、Ar、Kr… 双原子分子如:O2、H2、HCl、NO… 多原子分子如:H2O、P4、C6H12O6… 2.原子 原子是化学变化中的最小微粒。确切地说,在化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子构成的。 3.离子 离子是指带电荷的原子或原子团。 (1)离子可分为: 阳离子:Li+、Na+、H+、NH4+… 阴离子:Cl–、O2–、OH–、SO42–… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、Na2SO4… ②电解质溶液中:盐酸、NaOH溶液… ③金属晶体中:钠、铁、钾、铜… 4.元素 元素是具有相同核电荷数(即质子数)的同—类原子的总称。 (1)元素与物质、分子、原子的区别与联系:物质是由元素组成的(宏观看);物质是由分子、原子或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)—同素异形体。 (3)各种元素在地壳中的质量分数各不相同,占前五位的依次是:O、Si、Al、Fe、Ca。 5.同位素 是指同一元素不同核素之间互称同位素,即具有相同质子数,不同中子数的同一类原子互称同位素。如H有三种同位素:11H、21H、31H(氕、氘、氚)。 6.核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素、可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但它们的质子数和电子数相同。核外电子排布相同,因而它们的化学性质几乎是相同的。 7.原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有几下几种类型:根(如SO42-、OHˉ、CH3COOˉ等)、官能团(有机物分子中能反映物质特殊性质的原子团,如—OH、—NO2、—COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。 8.基 化合物中具有特殊性质的一部分原子或原子团,或化合物分子中去掉某些原子或原子团后剩下的原子团。 (1)有机物的官能团是决定物质主要性质的基,如醇的羟基(—OH)和羧酸的羧基(—COOH)。 (2)甲烷(CH4)分子去掉一个氢原子后剩余部分(·CH3)含有未成对的价电子,称甲基或甲基游离基,也包括单原子的游离基(·Cl)。
第一单元中国传统文化主流思想的演变 第1课百家争鸣 课程标准: 知道诸子百家,认识春秋战国时期百家争鸣局面形成的重要意义;了解孔子、孟子和荀子等思想家以及儒家思想的形成。 基础知识: 1、“百家争鸣”出现在的背景:春秋战国时期,中国社会发生重大变 革经济:井田制瓦解。 政治:周王室衰微,诸侯士大夫崛起。(分封制瓦解) 阶级关系:士阶层的活跃。 教育学术:从“学在官府”到“学在民间”,平民百姓也开始接受教育。 2、主要流派: (1) 道家学派:老子和庄子,主张“无为而治”,把世间万物看作 是相对的。 (2)儒家学派:孔子、孟子和荀子。 (3)墨家学派:墨子主张“兼爱”“非攻”“尚贤”“节用” 。 (4)法家学派:韩非子主张以法治国。 3、“百家争鸣”意义 (1)是中国历史上第一次思想解放运动。 (2)是中国学术文化、思想道德发展史上的重要阶段,奠定了中国思想文化发展 的基础。 (3)形成了中国的传统文化体系,也形成了中国思想文化兼容并包和宽容开放的 特点。 4、儒家学派主要主张 孔子孟子荀子 同仁的思想“爱人”仁政仁义、王道民本思想为政以德民贵君轻君舟民水 异人性论性相近性善论性恶论 考点突破: 1、孔子的思想是如何体现人文精神的? 提示:人文精神指的是,以人为中心,肯定人的尊严和价值。 (1)“仁”的思想有利于建立良好的人际关系,为提倡人文精神提供宽松社会环 境。 (2)“有教无类”等教育主张,保证了个性发展,推动了个人素质的提高。 2、孟子提出“民为贵,社稷次之,君为轻” ,我们如何认识这种“民本”思想?提示:从孟子的阶级属性出发来分析。 孟子代表当时的新兴地主阶级,他的主张从根本上讲是为了实现本阶级的利益。 孟子认识到人民的力量的强大,有利于缓和阶级矛盾、促进社会的发展,在某种程度上体现了儒家的民本思想,但不能就说是“民主意识” 。 从根本上讲,孟子是地主阶级思想家,其“民贵”的主张是为了更长久稳固地统 治压迫人民,“君轻”也是为了更有效地保证君主统治剥削人民。 3、你认为诸子百家中,对当时的封建统治者最有用的是哪一派?为什么? 法家。
一、焓变反应热 1.反应热:一定条件下,一定物质的量的反应物之间完全反应所放出或吸收的热量 2.焓变(ΔH)的意义:在恒压条件下进行的化学反应的热效应(1).符号:△H(2).单位:kJ/mol 3.产生原因:化学键断裂——吸热化学键形成——放热 放出热量的化学反应。(放热>吸热) △H 为“-”或△H <0 吸收热量的化学反应。(吸热>放热)△H 为“+”或△H >0 ☆常见的放热反应:①所有的燃烧反应②酸碱中和反应 ③大多数的化合反应④金属与酸的反应 ⑤生石灰和水反应⑥浓硫酸稀释、氢氧化钠固体溶解等☆常见的吸热反应:①晶体Ba(OH)2·8H2O与NH4Cl ②大多数的分解反应 ③以H2、CO、C为还原剂的氧化还原反应④铵盐溶解等 注:①需要加热的反应,不一定是吸热反应;不需要加热的反应,不一定是放热反应 ②通过反应是放热还是吸热,可用来比较反应物和生成物的相对稳定性。 如C(石墨,s) C(金刚石,s)△H3= +1.9kJ/mol,该反应为吸热反应,金刚石的能量高,石墨比金属石稳定。 二、热化学方程式 书写化学方程式注意要点: ①热化学方程式必须标出能量变化。 ②热化学方程式中必须标明反应物和生成物的聚集状态(g,l,s分别表示固态,液态,气态,水溶液中溶质用aq表示) ③热化学反应方程式要指明反应时的温度和压强。 ④热化学方程式中的化学计量数可以是整数,也可以是分数 ⑤各物质系数加倍,△H加倍;反应逆向进行,△H改变符号,数值不变 三、燃烧热 1.概念:25 ℃,101 kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量。燃烧热的单位用kJ/mol表示。 ※注意以下几点: ①研究条件:101 kPa ②反应程度:完全燃烧,产物是稳定的氧化物。 ③燃烧物的物质的量:1 mol ④研究内容:放出的热量。(ΔH<0,单位kJ/mol) 四、中和热 1.概念:在稀溶液中,酸跟碱发生中和反应而生成1mol H2O,这时的反应热叫中和热。 2.强酸与强碱的中和反应其实质是H+和OH-反应,其热化学方程式为: H+(aq) +OH-(aq) =H2O(l) ΔH=-57.3kJ/mol 3.弱酸或弱碱电离要吸收热量,所以它们参加中和反应时的中和热小于57.3kJ/mol。 4.中和热的测定实验
必修三unit1 1.take place / happen / break out 无被动 2.starve to death 饿死 starve to do 渴望 做 .. starve for 渴望 得到 .. 3.in memory of 纪念 4.dress up 穿上盛装,打扮 5.p lay a trick / tricks on play a joke / jokes on 6.a ward sb. sth.=award sth. to sb.授予某 人某物 reward sb. for sth. 因 ... 而报答,奖赏某人 reward sb. with sth. 用 ...报答,酬谢某人 7.look forward to doing *以介词 to 结尾的短语 pay attention to (doing) devote? to (doing) attach? to (doing) attach great importance to... 认为 ...很重要8. without permission. 未经许可 permit doing sth. permit sb.to do sb be permitted to do 9. turn up 出现 ,调高 turn down 拒绝,调低 turn out (to be ) 结果是 turn to sb (for help) 求助 10 keep one ’ s word守信用;履 行诺言 hold one ’ s breath屏息;屏气 11.apologize to sb for sth make an apology to sb for sth 11. set off ( for.. .) = set out ( for...) 动身,出发 12. remind sb. of sth. /sb.使某人想起?remind sb. to do sth. 提醒某人做某事 14.mean to do 打算做 mean doing 意味着 15 be satisfied with 对?感到满意satisfying 令人满意的 16 lead to 导致;通向,通往 17.It is/was obvious that。。。很明显??
一、“百家争鸣”局面出现的原因及评价 1、原因: (1)春秋战国时期,中国社会发生重大变革。社会地位较低的士,受到各诸侯国统治者的重用。他们代表本阶层或政治派别的利益和要求,提出自己的主张。 (2)政治和经济大变动,导致教育和学术领域也发生变化。社会上形成一些以传播文化、发展学术为宗旨的学者和思想流派。这些学者和思想流派,被称为“诸子百家”。 (3)学派之间的互相诘难、批驳,形成了“百家争鸣”的局面;同时,各家彼此吸收、融合,逐步形成了中国的传统文化体系。 新-课-标-第-一-网 2、评价: “百家争鸣”是中国历史上第一次思想解放运动,是中国学术文化、思想道德发展史上的重要阶段,奠定了中国思想文化发展的基础。成为中国传统文化的源头。 二、孔子和早期儒学 1、孔子生平:孔子姓孔名丘字仲尼,春秋晚期鲁国人,是著名的思想家、教育家和政治理论家,儒家学派的创始人,后人尊称“至圣”。 2、早期儒学: (1)孔子创立儒家学派。孔子的思想核心是“仁”。他认为仁就是爱人,人与人之间要互相爱护,融洽相处;要做到待人宽容,“已所不欲,勿施于人”。孔子强调统治者要以德治民,爱惜民力,取信于民,反对苛政和任意刑杀。孔子首创私人讲学,主张“有教无类”,打破了贵族垄断文化教育的局面。 (2)孟子和荀子是儒家学派的两位重要代表人物。孟子发展了孔子“仁”的思想,主张实行“仁政”,进一步提出“民为贵,社稷次之,君为轻”的民本思想。在伦理观上,孟子主张“性本善”。 荀子也主张统治者施政用“仁义”和“王道”,以德服人,并提出“君者舟也,庶人者水也。水则载舟,水则覆舟”的著名论断。 (3)孟子、荀子对儒家思想加以总结和改造,又吸收了一些其他学派的积极合理成分,使儒学体系更加完整,儒家思想更能适应社会的需要。 三、道家和法家 1、道家: (1)老子,道家学派的创始人。老子认为世界万物的本原是“道”。他强调一切要顺应自然,提倡清静无为、知足寡欲。他指出社会动荡的根源,在于人们的行为违背了自然,提出“无为而治”的政治主张。 (2)庄子,继承和发展了老子的学说。 2、法家: 法家学派的集大成者是战国末期的韩非子。主张君主要以法治国,利用权术驾驭大臣,以绝对的权威来震慑臣民,提出了系统的法治理论。法家把君主的权力提高到极点,迎合了建立大一统专制国家的历史发展趋势。 第2课“罢黜百家,独尊儒术" 【基础解读】
高一数学必修三知识点总结 【篇一】高一数学必修三知识点总结 1.一些基本概念: (1)向量:既有大小,又有方向的量. (2)数量:只有大小,没有方向的量. (3)有向线段的三要素:起点、方向、长度. (4)零向量:长度为0的向量. (5)单位向量:长度等于1个单位的向量. (6)平行向量(共线向量):方向相同或相反的非零向量. ※零向量与任一向量平行. (7)相等向量:长度相等且方向相同的向量. 2.向量加法运算: ⑴三角形法则的特点:首尾相连. ⑵平行四边形法则的特点:共起点【篇二】高一数学必修三知识点总结 一、集合有关概念 1、集合的含义:某些指定的对象集在一起就成为一个集合,其中每一个对象叫元素。 2、集合的中元素的三个特性: 1.元素的确定性; 2.元素的互异性; 3.元素的无序性 说明:
(1)对于一个给定的集合,集合中的元素是确定的,任何一个对象或者是或者不是这个给定的集合的元素。 (2)任何一个给定的集合中,任何两个元素都是不同的对象,相同的对象归入一个集合时,仅算一个元素。 (3)集合中的元素是平等的,没有先后顺序,因此判定两个集合是否一样,仅需比较它们的元素是否一样,不需考查排列顺序是否一样。 (4)集合元素的三个特性使集合本身具有了确定性和整体性。 3、集合的表示:{…}如{我校的篮球队员},{太平洋,大西洋,印度洋,北冰洋} 1.用拉丁字母表示集合:A={我校的篮球队员},B={1,2,3,4,5} 2.集合的表示方法:列举法与描述法。 注意啊:常用数集及其记法: 非负整数集(即自然数集)记作:N 正整数集N*或N+整数集Z有理数集Q实数集R 关于“属于”的概念 集合的元素通常用小写的拉丁字母表示,如:a是集合A的元素,就说a属于集合A记作a∈A,相反,a不属于集合A记作a?A 列举法:把集合中的元素一一列举出来,然后用一个大括号括上。 描述法:将集合中的元素的公共属性描述出来,写在大
高二历史必修三知识点总结 第一课“百家争鸣”和儒家思想的形成 “百家争鸣”背景: 1.经济:生产力发展井田制瓦解地主出现封建经济形成初步发展 2.政治:诸侯争霸分封制崩溃 3.阶级:原来社会地位较低的士在社会生活中活跃起来受到各诸侯 国统治者的重用 4.文化:从学在官府到学在民间 影响 1.逐步形成了中国的传统文化体系 2.奠定了中国思想文化发展的基础 3.百家争鸣是中国历史上第一次思想解放运动 人物 孔子(儒家,春秋晚期): 思想核心“仁”政治思想(1)以德治民(2)恢复西周的礼乐制度主张克己复礼(3)主张有教无类教育方法是因材施教(4)人性论性相近习相远 孟子(儒家,战国末):(1)政治思想主张实行仁政(2)民为贵社稷次之君为轻的民本思想(3)伦理观性本善(4)价值观舍生取义 荀子(儒家,战国末):(1)政治思想仁义王道以德服人(2)民本思想君舟民水(3)伦理观性本恶(4)朴素唯物思想制天命以用之老子(道家,春秋晚期)客观唯心体系(1)哲学思想世界万物本原
是道(2)辩证法思想祸福相依(3)政治主张无为而治 庄子(道家,战国末)(1)主观唯心主义哲学思想(2)世间万物相对(3)崇尚自然主张超越功利去追求精神自由社会批判精神 韩非子(法家,战国末)(1)认为历史是发展的统治者应时而变(2)依法治国系统了法制理论,皇帝独尊皇权至上厚今薄古以法治国君主专制中央集权 墨子(墨家,战国初)兼爱,非攻节俭,尚贤 第二课“罢黜百家,独尊儒术” “罢黜百家独尊儒术”背景 (1)边疆危机(2)土地兼并(3)亡国问题(4)黄老学说无为而治已经无法适应新时代要求(5)加强中央集权 汉武帝即位面临的社会问题 匈奴威胁,边患不止,诸侯坐大威胁中央,土地豪强势大,黄老学说无法适应新形势需要 影响 利于社会恢复,利于社会稳定(积极) 致使地方势力膨胀,不利于加强中央集权(消极) “罢黜百家独尊儒术” 内容: 提出春秋大一统和罢黜百家独尊儒术的主张,目的加强中央集权的需要
高中化学必修一知识点总结(人教版) 必修1全册基本内容梳理 第一部分:从实验学化学 一、化学实验安全 1、(1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。 (2)烫伤宜找医生处理。 (3)浓酸撒在实验台上,先用Na2CO3 (或NaHCO3)中和,后用水冲擦干净。浓酸沾在皮肤上,宜先用干抹布拭去,再用水冲净。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。 (4)浓碱撒在实验台上,先用稀醋酸中和,然后用水冲擦干净。浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。 (5)钠、磷等失火宜用沙土扑盖。 (6)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。 二.混合物的分离和提纯 分离和提纯的方法分离的物质应注意的事项应用举例 过滤用于固液混合的分离一贴、二低、三靠如粗盐的提纯 蒸馏提纯或分离沸点不同的液体混合物防止液体暴沸,温度计水银球的位置,如石油的蒸馏中冷凝管中水的流向如石油的蒸馏
萃取利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂用四氯化碳萃取溴水里的溴、碘 分液分离互不相溶的液体打开上端活塞或使活塞上的凹槽与漏斗上的水孔,使漏斗内外空气相通。打开活塞,使下层液体慢慢流出,及时关闭活塞,上层液体由上端倒出如用四氯化碳萃取溴水里的溴、碘后再分液 蒸发和结晶用来分离和提纯几种可溶性固体的混合物加热蒸发皿使溶液蒸发时,要用玻璃棒不断搅动溶液;当蒸发皿中出现较多的固体时,即停止加热分离NaCl和KNO3混合物 三、离子检验 离子所加试剂现象离子方程式 Cl-AgNO3、稀HNO3 产生白色沉淀Cl-+Ag+=AgCl↓ SO42- 稀HCl、BaCl2 白色沉淀SO42-+Ba2+=BaSO4↓ 四.除杂 注意事项:为了使杂质除尽,加入的试剂不能是“适量”,而应是“过量”;但过量的试剂必须在后续操作中便于除去。 五、物质的量的单位――摩尔 1.物质的量(n)是表示含有一定数目粒子的集体的物理量。 2.摩尔(mol): 把含有6.02 ×1023个粒子的任何粒子集体计量为1摩尔。 3.阿伏加德罗常数:把6.02 X1023mol-1叫作阿伏加德罗常数。 4.物质的量=物质所含微粒数目/阿伏加德罗常数n =N/NA
最全高中数学 必修三知识点总结归纳(经典版)
第一章算法初步 1.1.1算法的概念 1、算法概念: 在数学上,现代意义上的“算法”通常是指可以用计算机来解决的某一类问题是程序或步骤,这些程序或步骤必须是明确和有效的,而且能够在有限步之内完成. 2. 算法的特点: (1)有限性:一个算法的步骤序列是有限的,必须在有限操作之后停止,不能是无限的. (2)确定性:算法中的每一步应该是确定的并且能有效地执行且得到确定的结果,而不应当是模棱两可. (3)顺序性与正确性:算法从初始步骤开始,分为若干明确的步骤,每一个步骤只能有一个确定的后继步骤,前一步是后一步的前提,只有执行完前一步才能进行下一步,并且每一步都准确无误,才能完成问题. (4)不唯一性:求解某一个问题的解法不一定是唯一的,对于一个问题可以有不同的算法. (5)普遍性:很多具体的问题,都可以设计合理的算法去解决,如心算、计算器计算都要经过有限、事先设计好的步骤加以解决. 1.1.2程序框图 1、程序框图基本概念: (一)程序构图的概念:程序框图又称流程图,是一种用规定的图形、指向线及文字说明来准确、直观地表示算法的图形。 一个程序框图包括以下几部分:表示相应操作的程序框;带箭头的流程线;程序框外必要文字说明。
(二)构成程序框的图形符号及其作用 学习这部分知识的时候,要掌握各个图形的形状、作用及使用规则,画程序框图的规则如下: 1、使用标准的图形符号。2、框图一般按从上到下、从左到右的方向画。3、除判断框外,大多数流程图符号只有一个进入点和一个退出点。判断框具有超过一个退出点的唯一符号。4、判断框分两大类,一类判断框“是”与“否”两分支的判断,而且有且仅有两个结果;另一类是多分支判断,有几种不同的结果。5、在图形符号内描述的语言要非常简练清楚。 (三)、算法的三种基本逻辑结构:顺序结构、条件结构、循环结构。 1、顺序结构:顺序结构是最简单的算法结构,语句与语句之间,框与框之间是按从上到下的顺序进行的,它是由若干个依次执行的处理步骤组成的,它是任何一个算法都离不开的一种基本算法结构。 顺序结构在程序框图中的体现就是用流程线将程序框自上而 下地连接起来,按顺序执行算法步骤。如在示意图中,A 框和B 框是依次执行的,只有在执行完A 框指定的操作后,才能接着执 行B 框所指定的操作。 2、条件结构: 条件结构是指在算法中通过对条件的判断 根据条件是否成立而选择不同流向的算法结构。
高中化学有机知识点总结 1.需水浴加热的反应有: (1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化( 4 )糖的水解 凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大 落,有利于反应的进行。 2.需用温度计的实验有: (1)、实验室制乙烯 170℃)(2)、蒸馏( 3 )、乙酸乙酯的水解(70-80℃)(4)(制硝基苯(50- 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。3.能与Na反应的有机物有:醇、酚、羧酸等——凡含羟基的化合物。 4.能发生银镜反应的物质有: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。 5.能使高锰酸钾酸性溶液褪色的物质有: (1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物 (2)含有羟基的化合物如醇和酚类物质 (3)含有醛基的化合物 (4)具有还原性的无机物(如SO2 、FeSO4 、KI 、HCl、H2O2、HI 、H2S、H2 SO3 等)不能使酸性高锰酸钾褪色的物质有:烷烃、环烷烃、苯、乙酸等 6.能使溴水褪色的物质有: 含有碳碳双键和碳碳三键的烃和烃的衍生物(加成) 含醛基物质(氧化) 【1】遇溴水褪色苯酚等酚类物质(取代) 碱性物质(如NaOH、Na2 CO3)(氧化还原――歧化反应) 较强的无机还原剂(如SO2、KI 、FeSO4、H2S、H2SO3 等) 【2】只萃取不褪色:液态烷烃、环烷烃、苯、甲苯、二甲苯、乙苯、卤代烃、酯类(有 机溶剂) 7.密度比水大的液体有机物有:溴乙烷、溴苯、硝基苯、四氯化碳等。 8、密度比水小的液体有机物有:烃、大多数酯、一氯烷烃。 9.能发生水解反应的物质有:卤代烃、酯(油脂)、二糖、多糖、蛋白质(肽)、盐。 10.不溶于水的有机物有:烃、卤代烃、酯、淀粉、纤维素。 11.常温下为气体的有机物有: 分子中含有碳原子数小于或等于 4 的烃(新戊烷例外)、一氯甲烷、甲醛。 12.浓硫酸(H2SO4)、加热条件下发生的反应有: 苯及苯的同系物的硝化、磺化、醇的脱水反应、酯化反应、水解反应。 13.能被氧化的物质有: 含有碳碳双键或碳碳叁键的不饱和化合物(KMnO)4、苯的同系物、酚 大多数有机物都可以燃烧,燃烧都是被氧气氧化。 醇(还原)(氧化)醛(氧化)羧酸。 14.显酸性的有机物有:含有酚羟基和羧基的化合物。
历史必修三知识点总结 专题一中国传统文化主流思想的演变 一、春秋战国时期的百家争鸣 1、百家争鸣 (1)争鸣的背景:社会大变革。包括:井田制瓦解,分封制崩溃,战争频繁,私学兴起。 (2 )争论的问题:核心问题是如何治国(德治、仁政啊,法治,无为而治),还有人性问题、 人与人的关系问题、人与自然的关系问题等。 (3)争鸣的影响:是一次思想解放运动,奠定了中国传统思想文化发展的基础。2、孔子、孟子和荀子与儒家思想的形成 (1)孔子的成就思想上:创立儒学,提出“仁”、“礼”和“德治”的主。教育上:创办私学,总结出一些教育教学方法。 典籍上:编订“六经”。 [附]孔子的重要言论己欲立而立人;己欲达而达人;己所不欲,勿施于人。有教无类,因材施教。道之以德,齐之以礼。为政以德,譬如北辰,居其所而众星拱之。 (2)孟子的主:人性善,民贵君轻,仁政。 [附]孟子的重要言论民为贵,社稷次之,君为轻。天时不如地利,地利不如人和。 (3)荀子的主:人性恶,通过学“礼”来改变;可以利用自然规律来造福人类。[附]荀子的重要言论君舟也,民水也,水能载舟,亦能覆舟。天行有常??制天命而用之。 二、汉代儒学成为正统思想 1、董仲舒的主:大一统;罢黜百家,独尊儒术;天人合一,天人感应,君权神授。(另:三纲 五常) 2、汉武帝的措施:罢黜百家,独尊儒术;设立太学,推广儒学。[目的:加强专制集权。影响:加强了专制集权,儒学成为正统思想] 三、宋明理学 1、程朱理学 (1)“二程”(理学的开创者)指程颐、程颢,其主要观点有:天理是万物的本原,伦理道德就是天理,天理的核心是“仁”。
(2)朱熹(理学的集大成者)的主要观点是:理气论;存天理,灭人欲。 2、王阳明(守仁)的心学观点是:理在心中(心即理也,心外无物);致良知(加强道德修养, 克服人欲,恢复人原有的善良本性);知行合一(知和行都产生于心,要用良知来支配自己的行为实践) 四、明清之际的儒学 1、贽“离经叛道”(反正统,异端)观点:反对“圣人”;认为人的物质生活就是天理。 2、明清之际三大思想家指:黄宗羲(著《明夷待访录》)、顾炎武(著《日知录》、《天下郡国 利病书》)、王夫之,三人思想的共同之处有:反对君主专制,提倡工商皆本,主经世致用。顾炎武还有“天下兴亡,匹夫有责”的思想,王夫之在哲学方面成就突出。 [言论:黄—天下为主,君为客;天下之治乱,不在一姓之兴亡,而在万民之忧乐;以“天下之法”取代“一家之法”;公其是非于学校。顾—人君之于天下,不能以独治也??以天下之权,寄天下之人]五、儒学的兴衰历程:见提纲 专题二古代中国的科学技术与文学艺术 一、科技成就 1、四大发明出现及完成:造纸—西汉墓出土了纸,东汉有“蔡侯纸”;指南针—战国名“司南”,宋时用于航海;火药—唐宋时用于军事;印刷—隋唐出现雕版印刷,《金刚经》是世界上迄今所知最早的有确切日期的印刷品,北宋毕升发明活字印刷。 2、四大发明对世界文明的影响:造纸、印刷—文化发展、思想解放(文艺复兴、宗教改革), 火药—资产阶级革命、资产阶级政权,指南针—新船路、世界市场==== 总之,使世界进入资 本主义时代。 二、汉字与书画 1、汉字的起源和演变:甲骨文—小篆—隶书—楷书-行书(看书本识别各种字体),总趋势由繁到简。 2、中国书画 (1 )书法家:东晋王羲之(书圣,《兰亭序》为“天下第一行书”),唐朝欧阳询、颜真卿、柳公权(擅长楷书)等。 (2)中国画的分类:人物画、山水画、花鸟画;元明清时期文人画成就突出。 三、文学成就 (1)诗经:收录了西周到春秋的三百多首诗,分风、雅、颂三部分,是现实主义的源头、儒家经典。 (2)楚辞:屈原是代表人,《离骚》是代表作、浪漫主义源头。(“风”骚“”并称) (3)汉赋:词藻华丽,手法夸,容丰富,反映大一统景象。代表人物有司马相如、衡等。
高中化学必修二知识点总结 第一单元 1——原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。 2——元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外); (2)同一主族的元素的最高正价、负价均相同 (3) 所有单质都显零价 3——单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 4——元素的金属性与非金属性(及其判断) (1)同一周期的元素电子层数相同。因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增; (2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。 判断金属性强弱 金属性(还原性)1,单质从水或酸中置换出氢气越容易越强 2,最高价氧化物的水化物的碱性越强 非金属性(氧化性)1,单质越容易与氢气反应形成气态氢化物 2,氢化物越稳定 3,最高价氧化物的水化物的酸性越强(1—20号,F最强;最体一样)5——单质的氧化性、还原性 一般元素的金属性越强,其单质的还原性越强,其氧化物的阳离子氧化性越弱; 元素的非金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。 推断元素位置的规律 判断元素在周期表中位置应牢记的规律: (1)元素周期数等于核外电子层数; (2)主族元素的序数等于最外层电子数。 阴阳离子的半径大小辨别规律 由于阴离子是电子最外层得到了电子而阳离子是失去了电子 6——周期与主族 周期:短周期(1—3);长周期(4—6,6周期中存在镧系);不完全周期(7)。 主族:ⅠA—ⅦA为主族元素;ⅠB—ⅦB为副族元素(中间包括Ⅷ);0族(即惰性气体) 所以, 总的说来 (1) 阳离子半径<原子半径 (2) 阴离子半径>原子半径 (3) 阴离子半径>阳离子半径 (4 对于具有相同核外电子排布的离子,原子序数越大,其离子半径越小。 以上不适合用于稀有气体! 专题一: 第二单元