
期末冲刺专题复习(二)
非金属元素及其化合物
一.氯及其化合物
1.氯气⑴物理性质: 色、有 气味、 溶于水、密度比空气大的有毒气体。
⑵化学性质 ①与金属反应【能将变价金属(如Fe 、Cu )氧化至最高价】
与Na 反应:方程式: 现象:剧烈燃烧,火焰呈 色,生成 固体 与Fe 反应:方程式: 现象:产生 色烟,产物溶于水呈 色 与Cu 反应:方程式: 现象:产生 色烟,产物溶于水呈 色 ②与非金属的反应
与H 2反应: 现象: 色火焰,瓶口出现 , ③与H 2O 的反应(歧化反应)
④与碱溶液反应(歧化反应) 【氯气尾气吸收,84消毒液制备】;
; 【制取漂白粉】
; ⑷氯气制法
①制备原理: MnO 2 + 4HCl (浓)=====△MnCl 2 + Cl 2↑+ 2H 2O (实验室制备)
②发生装置:固+液气
③除杂:
氯气中HCl : , 氯气中H 2O : ④收集:用 法或 ; 验满: a.观察法(黄绿色);
b.湿淀粉KI 试纸;现象: ⑤尾气处理:
2.氯水的成分及其性质
⑴液氯、新制氯水、久置氯水对比(右上角表格一) ⑵新制氯水各成分的检验 (右上角表格二)
⑴次氯酸(HClO )的性质
①弱酸性:HClO 的酸性小于H 2CO 3: NaClO + H 2O + CO 2===NaHCO 3 + HClO
②不稳定性: ③强氧化性、漂白性:杀菌、消毒 ⑵次氯酸盐
次氯酸盐的稳定性 次氯酸。漂白剂或消毒剂漂白或消毒原理是先生成次氯酸,利用次氯酸强氧化性,杀毒、漂白。
漂白粉漂白原理: 4.卤族元素【氟(F )、氯(Cl )、溴(Br )、碘(I )、】 ⑴卤族单质物理性质
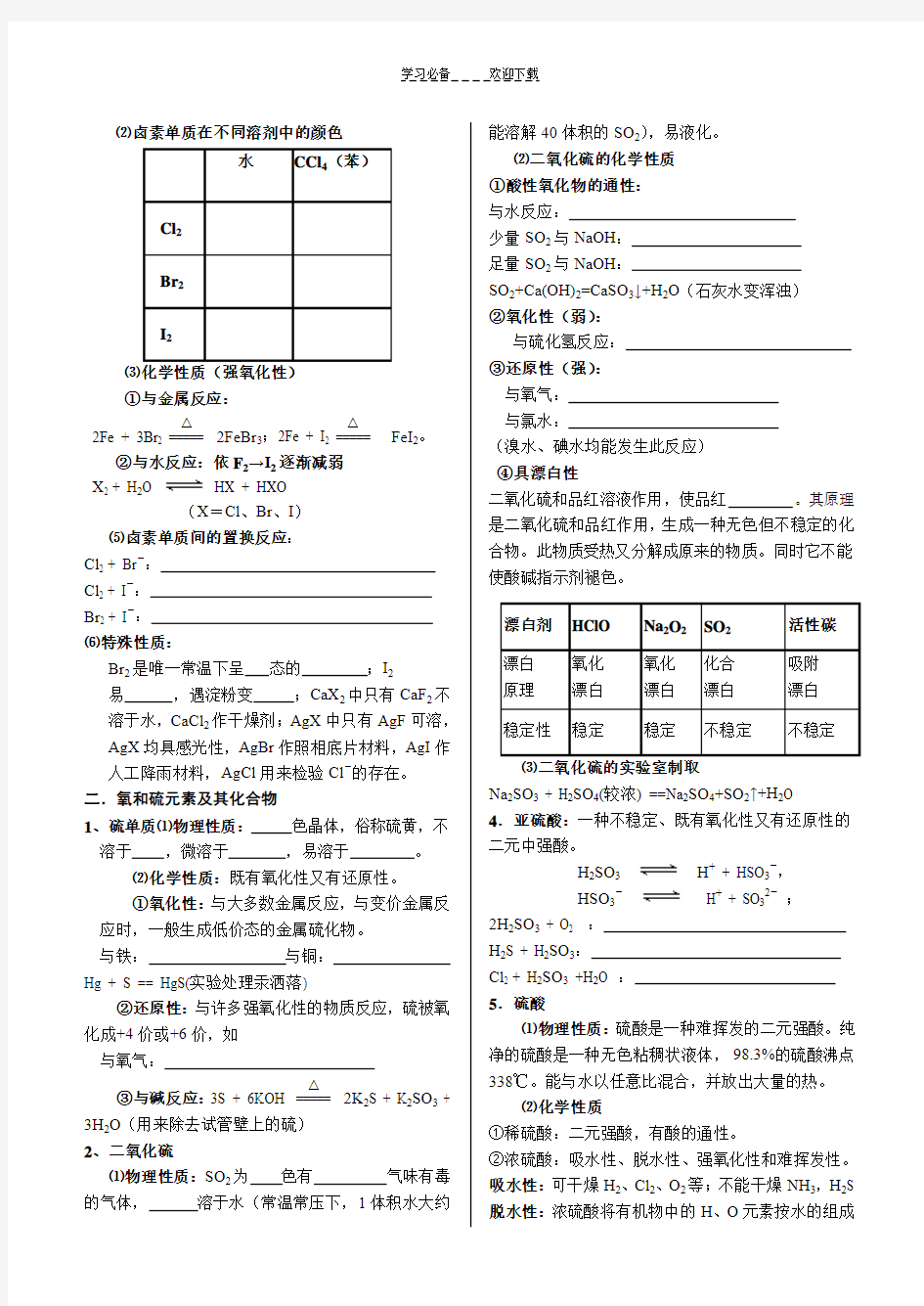
⑵卤素单质在不同溶剂中的颜色
①与金属反应:
2Fe + 3Br 2 =====△ 2FeBr 3;2Fe + I 2 =====△
FeI 2。 ②与水反应:依F 2→I 2逐渐减弱 X 2 + H 2O
HX + HXO (X =Cl 、Br 、I )
⑸卤素单质间的置换反应:
Cl 2 + Br -
: Cl 2 + I -: Br 2 + I -: ⑹特殊性质:
Br 2是唯一常温下呈 态的 ;I 2
易 ,遇淀粉变 ;CaX 2中只有CaF 2不溶于水,CaCl 2作干燥剂;AgX 中只有AgF 可溶,AgX 均具感光性,AgBr 作照相底片材料,AgI 作人工降雨材料,AgCl 用来检验Cl -
的存在。 二.氧和硫元素及其化合物
1、硫单质⑴物理性质: 色晶体,俗称硫黄,不溶于 ,微溶于 ,易溶于 。 ⑵化学性质:既有氧化性又有还原性。 ①氧化性:与大多数金属反应,与变价金属反应时,一般生成低价态的金属硫化物。
与铁: 与铜: Hg + S == HgS(实验处理汞洒落)
②还原性:与许多强氧化性的物质反应,硫被氧化成+4价或+6价,如
与氧气:
③与碱反应:3S + 6KOH =====△
2K 2S + K 2SO 3 + 3H 2O (用来除去试管壁上的硫) 2、二氧化硫
⑴物理性质:SO 2为 色有 气味有毒的气体, 溶于水(常温常压下,1体积水大约
能溶解40体积的SO 2),易液化。 ⑵二氧化硫的化学性质 ①酸性氧化物的通性:
与水反应: 少量SO 2与NaOH : 足量SO 2与NaOH : SO 2+Ca(OH)2=CaSO 3↓+H 2O (石灰水变浑浊) ②氧化性(弱):
与硫化氢反应: ③还原性(强):
与氧气: 与氯水: (溴水、碘水均能发生此反应) ④具漂白性
二氧化硫和品红溶液作用,使品红 。其原理是二氧化硫和品红作用,生成一种无色但不稳定的化合物。此物质受热又分解成原来的物质。同时它不能使酸碱指示剂褪色。
Na 2SO 3 + H 2SO 4(较浓) ==Na 2SO 4+SO 2↑+H 2O 4.亚硫酸:一种不稳定、既有氧化性又有还原性的二元中强酸。
H 2SO 3H + + HSO 3-
,
HSO 3
-
H + + SO 32-
;
2H 2SO 3 + O 2 :
H 2S + H 2SO 3:
Cl 2 + H 2SO 3 +H 2O : 5.硫酸
⑴物理性质:硫酸是一种难挥发的二元强酸。纯净的硫酸是一种无色粘稠状液体, 98.3%的硫酸沸点338℃。能与水以任意比混合,并放出大量的热。 ⑵化学性质
①稀硫酸:二元强酸,有酸的通性。
②浓硫酸:吸水性、脱水性、强氧化性和难挥发性。 吸水性:可干燥H 2、Cl 2、O 2等;不能干燥NH 3,H 2S 脱水性:浓硫酸将有机物中的H 、O 元素按水的组成
比脱去(蔗糖的碳化等)。
强氧化性:使铁、铝钝化。
A.加热时能够氧化大多数金属:
与铜反应:
B.加热时能氧化许多非金属:
与炭反应:
C.能氧化许多的具还原性的化合物:
H2S + H2SO4(浓) == S↓+ SO2↑+ 2H2O
三.氮及其化合物
1.氮气
物理性质:无色无味难溶于水比空气稍轻的气体。化学性质:
①与氢气反应:
②与金属镁反应
③与氧气反应:
2.氮的氧化物
⑴物理性质:
NO:色有毒气体。于水。
NO2:色、刺激性气味气体。
⑵化学性质:
NO不与水反应,易与氧气反应,用排水法收集。
NO2与水反应:
*若NO与O2混合气体溶于水恰好全部生成硝酸:4NO+3O2+2H2O===4HNO3
*若NO2与O2混合气体溶于水恰好全部生成硝酸:4NO2+O2+2H2O===4HNO3
3.氨与铵盐
⑴氨气
①物理性质:无色、刺激性气味气体,易液化(可作制冷剂),溶于水(1:700)。
②化学性质
A.与水反应:
一水合氨很不稳定,受热会分解:
氨水成分:分子:;
阳离子:;
阴离子:;
注意:氨水、酒精的密度随着浓度的增大而减小。B.与酸的反应(检验氨气的一种方法)
(白烟)
C.氨气的催化氧化(工业制硝酸的反应之一)
⑵铵盐:无色晶体,均易溶于水。
①受热易分解(一般非氧化性的铵盐):
NH4Cl =====
△
NH3↑+ HCl↑;
NH4HCO3=====
△
NH3↑+CO2↑ + H2O
氧化性酸的铵盐产物比较复杂。
②与碱反应:(铵盐与碱受热能产生氨气)
⑶氨气的制取
①反应原理:
②装置:固固加热装置(与制氧气类似)。
③收集:法。
④干燥:碱石灰,不能用浓H2SO4、无水CaCl2。
⑤检验:
A.使湿润的色石蕊试纸变。
B.蘸的玻璃棒接近瓶口,产生。
4.硝酸
⑴物理性质:无色、易挥发液体(“发烟”现象);密度大于水,浓度越大,密度越大;极易溶于水。
⑵化学性质
①酸的通性:
②不稳定性:
保存方法:密封、棕色瓶、玻璃塞、阴凉处。
③强氧化性(冷浓硝酸使铁铝钝化)
A.与金属反应(除Au、Pt外):
铜与稀硝酸:
铜与浓硝酸:
注意:浓硝酸氧化性强于稀硝酸强于浓硫酸;一般而言硝酸与不活泼金属反应浓硝酸的还原产物是NO2,稀硝酸的还原产物是NO。
B .与非金属反应
与炭反应:
四.碳、硅及其化合物 1.碳单质
⑴同素异形体: ⑵化学性质:碳在常温下性质比较稳定,很难被氧化,但在点燃或加热的条件下也能跟其它物质发生化学反应。
①还原性:C+CuO=====△
CO↑+Cu ; C+H 2O(g) =====高温
CO+H 2(水煤气)
②可燃性:C+O 2=====点燃CO 2;2C+O 2=====点燃
2CO 2.二氧化碳
⑴物理性质:无色无味,密度比空气大的气体,微溶于水,固体CO 2叫做“ ”。 ⑵化学性质:
①氧化性(与C 、Mg 的反应)
CO 2+C : ; CO 2+2Mg : 。 ②酸性氧化物(与碱及碱性氧化物的反应) CO 2+Ca(OH)2: ; CO 2+CaCO 3+H 2O : ③与盐的反应
Ca(ClO)2+H 2O+CO 2: ; Na 2SiO 3+H 2O+CO 2: ; ⑷制法:
①工业制法:煅烧石灰石: ; ②实验室制法:石灰石和稀盐酸反应原理: ; 装置:“固+液→气”或启普发生器
4.硅⑴物理性质: 色、金属光泽;熔、沸点高,硬度大(结构与金刚石类似),半导体。 ⑵化学性质:
①常温下,可与F 2、HF 、强碱反应: ②加热时可与O 2等物质反应
⑶用途:可以用来制 、硅整流器、太阳能电池(半导体),还可以用来制造变压器铁芯(含硅4%的钢具有良好导磁性),及耐酸设备(含硅15%左右的钢具有良好的耐酸性)等。
⑸硅的制法
提纯:Si + 2Cl 2 =====高温
SiCl 4 ;
SiCl 4 + 2H 2 =====高温
Si + 4HCl↑ 5.二氧化硅(SiO 2)
⑴存在: 晶体硅 无定形硅(非晶硅)
⑵物理性质:硬度 、熔点 , 溶于水。、 ⑶化学性质:
①酸性氧化物的通性:SiO 2是酸性氧化物,是H 2SiO 3的酸酐,但不溶于水:
SiO 2+CaO : SiO 2+2NaOH : (盛强碱液试剂瓶用橡皮塞的原因) ②弱氧化性:SiO 2+2C =====高温
Si+2CO↑
③特性: (雕刻玻璃) ⑷用途:
①SiO 2是制造 的主要原料。 ②石英制作石英玻璃、石英电子表、石英钟等。 ③水晶常用来制造电子工业的重要部件、光学仪器、工艺品等。
④石英砂常用作制玻璃和建筑材料。 6.硅酸盐
(1)常用硅酸盐是Na 2SiO 3,俗称“泡花碱”,易溶于水,其水溶液称为水玻璃,是一种矿物胶,需密封保存,因为: ; (2)硅酸盐改写为氧化物形式(顺序为:较活泼金属氧化物·金属氧化物·二氧化硅·水)
如Al 2(Si 2O 5)(OH)4:Al 2O 3·2SiO 2·2H 2O 7.无机非金属材料 (1)制备玻璃的原料: 原理:
(2)制水泥的原料:
(3)制陶瓷的原料:
非金属元素专题复习 考试说明要求:了解常见非金属元素(H、C、O、N、Si S、Cl)的单质及其化合物性质和用途。 (第一课时) 【引入】一、元素化合物的复习方法 落实存在、性质、制备、用途四要点。 【举例】(1)从位置出发,以Cs为例。位置:第六周期,IA族。→结构特点:最外层只有一个电子,原子半径大。→比Na、K更活泼的金属元素,具强的金属性。→应隔绝空气保存;与水反应剧烈,可能发生爆炸;与氧气迅速反应,主要产物肯定不是Cs2O。 (2)从结构出发:已知某元素原子有六个电子层,最外层2个电子→最外层电子数少,电子层数多,应是活泼金属,金属性大于钙→与水剧烈反应;氢氧化物是可溶性强碱;碳酸盐、硫酸盐均不溶于水。 (3)从性质出发:某单质能从水中置换出O2。→非金属性大于氧,应为最活泼的非金属元素F→在周期表的右上角,第二周期ⅦA族→可与绝大多数金属、非金属甚至某些稀有气体直接反应;化合价只有-1价;几乎无法用氧化剂将F-氧化成F2。 分析: 归纳: 例1 BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称,若知:①在BGO中,锗处于其最高价态。②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中铋具有最外层8个电子稳定结构。③BGO可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物所含氧的总质量相同。请填空: (1)锗和铋的元素符号分别是____、____。(2)BGO晶体的化学式是____。 (3)BGO晶体所含铋氧化物的化学式是____。 分析:Ge:第Ⅳ主族元素,最高正价+4;最高价氧化物GeO2。 Bi:第Ⅴ主族元素,最外层5个电子→满足8电子稳定结构应形成共价键数目:8-5=3→BiCl3→在BGO中铋为+3价→氧化物Bi2O3。 设BGO化学式为mGeO2·nBi2O3 有:2m=3n m∶n=3∶2m=3n=2 →BGO化学式为3GeO2·2Bi2O3(或Bi4(GeO4)3) 答案:略。 归纳思维过程:位置→最外层电子数→成键情况→实际价态→化学式 即:位置→结构→性质 3.以结构为主线,以元素周期律为指导,联系类型、掌握递变。
第十八章非金属元素小结预习提纲 第18章非金属元素小结 第一节非金属单质的结构和性质 要求:1、了解非金属单质中的共价键数为8-N(H2为2-N)。 2、第2周期中的O、N为什么易形成多重键? 3、第3、4周期的S、Se、P、As等则易形成单键? 4、非金属单质按其结构和性质大致可分为哪三类? 5、掌握单质Cl2、S、P、Si和B与NaOH反应的方程式。 一、非金属单质的结构和物理性质 1. 小分子单质(单原子分子和双原子分子) 分子晶体,熔点、沸点都很低。 2. 多原子分子单质(P4、As4、S8 ) 分子晶体,熔沸点稍高于第一类单质。 3. 大分子单质(金刚石、晶态硅和单质硼)包括过渡型晶体,如石墨、黑磷、灰砷.原子晶体,熔沸点极高,难挥发。 二、非金属单质的化学反应 1.活波非金属与金属元素反应 2.非金属元素之间反应 3.大部分非金属单质不与水反应 4.非金属单质一般不与非氧化酸反应,但可与浓硝酸、浓硫酸及王水反应. 5.大部分非金属单质可和碱反应,有时是歧化反应 第二节分子型氢化物 同一周期分子型氢化物从左到右稳定性增强,还原性减弱,水溶液酸性增强 同一族分子型氢化物从上到下稳定性减弱,还原性增强,水溶液酸性增强 分子型氢化物的热稳定性:与组成氢化物的非金属元素的电负性有关, 非金属与氢的电负性相差越大, 所生成的氢化物越稳定。 分子型氢化物的热稳定性, 在同一周期中从左到右依次增加; 在同一族中, 从上到下依次减小。 分子型氢化物的标准生成自由能或标准生成焓越负,氢化物越稳定。 还原性(An-失电子的能力):除HF外,其它分子型氢化物都有还原性,其变化规律与稳定性的增减的规律相反,稳定性大的氢化物,还原性小。 分子型氢化物的还原性,在同一周期中从左到右依次减小;在同一族中,从上到下依次增加。 因为在周期表中,从右向左,自上而下,元素半径增大,电负性减小,失电子的能力依上述方向递增,所以氢化物的还原性也按此方向增强。 水溶液酸碱性和无氧酸的强度:分子型氢化物在水溶液中的酸碱性和该氢化物在水中给出或接受质子能力的相对强弱有关。非金属分子型氢化物大多为酸,少数为碱,而水为两性。 结构:分子型氢化物酸性的强弱决定于与质子直接相连的原子的电子密度的大小,若该原子的电子密度越大,对质子的引力越强,酸性越小,反之酸性越大。 第三节含氧酸 一、最高氧化态氢氧化物的酸碱性 非金属元素氧化物的水合物为含有一个或多个OH基团的氢氧化物。R(OH)n
如何比较元素非金属性的相对强弱? 黄明建 一、原子得电子能力的强弱是元素非金属性强弱的本质反映 原子 ..得电子能力的强弱与元素非金属性的强弱正相关,即: 元素原子得电子的能力越强,元素的非金属性就越强。 而原子得电子能力的强弱是由原子结构决定的。 对于原子核外电子层数相同 ......的元素来说,核电荷数越大,原子半径越小,核对外层电子的吸引力越大,原子得电子的能力就越强,元素的非金属性越强; 对于原子最外层电子数相同 ........(或外围电子层排布相似)的元素来说,核外电子层数越多,原子半径越大,核对外层电子的吸引力越小,原子得电子的能力就越弱,元素的非金属性越弱。 据此,“非金属单质与化合物间的置换反应”就常常成为判断元素非金属性强弱的一个重要依据。 二、以置换反应判断元素非金属性强弱需注意的问题 以置换反应作为判断元素非金属强弱的依据,须有一个大前提——非金属单质 .....在反 .. 应中是作 ...,这样才能保证据此判断的结果不与元素非金属性强弱的本质相悖。....氧化剂 例如,下面几个反应: Cl2 + 2NaBr =2NaCl + Br2………………① Cl2 + H2S =2HCl + S↓………………② Br2 + 2KI =2NaBr + I2………………③ O2 + 2H2S =2H2O + 2S↓………………④ 反应①②均是Cl2作氧化剂,分别从NaBr溶液和氢硫酸中置换出Br2和S,表现出Cl比Br和S原子得电子能力都要强,所以元素的非金属性强弱次序是: Cl>Br Cl>S 反应③是以Br2作氧化剂,从KI溶液中置换出I2;反应④是以O2作氧化剂,从氢硫酸中置换出S;表现出Br比I原子得电子能力强、O比S原子得电子能力强,所以元素的非金属性强弱次序是: Br>I O>S 但是,有些置换反应就不宜用于判断元素非金属性的相对强弱。例如:
第十八章非金属元素小结 18-1 按周期表位置,绘出非金属元素单质的结构图,并分析它们在结构上有哪些特点和变化规律。 解:非金属元素的晶体结构大多数是分子晶体,也有少数原子晶体和过渡型层状晶体。在分子晶体中又可分为两类:一类是以小分子为结构单元,如单原子分子的稀有气体和双原子分子的H2,卤素(X2),O2、N2等;另一类是以多原子分子为结构单元,如S8、Se8、P4等。它们在周期表中的位置如图所示: 从结构图可知:位于非金属—金属交界线附近的元素,其单质的结构比较复杂,其特点是增大配位数,接近金属的结构,如B—C—Si—As—Te,都是以共价键结合成 的无限分子,不论是简单或复杂结构,在单质的结构中非金属元素明显地表 现出它们各自固有的共价特征。 18-2 为什么氟和其它卤素不同,没有多种可变的正氧化态? 解:因为氟原子价层没有空的轨道,基态只有一个未成对电子,只能形成一个共价单键; 再由于氟在所有元素中电负性最大,因此,没有多种可变的正氧化态。
18-3 小结P区元素的原子半径、电离能、电子亲合能和电负性,在按周期表递变规律的同时,还有哪些反常之处?说明其原因。 解:原子半径:r Ga< r Al ,因为Ga是第四周期元素,从Al→Ga,次外层第一次开始出现10个d电子,由于d电子对核电荷屏蔽效应小,导致有效核荷Z*比没有d 电子时要大,对最外层电子引力增大,故Ga的半径反常地比Al的小。 电离能:(1)ⅤA族N、P、As的IE1分别大于ⅥA族同周期O、S、Se的IE1,因为前三者价电子层均为半满。 (2)ⅢA第四周期Ga的IE1略大于第三周期的Al,原因和原子半径反常同理。 电子亲合能:(1)第二周期N、O、F的电子亲合能均分别小于第三周期同族的P、S、 Cl。因为第二周期元素原子半径特别小,电子对间排斥作用大。 (2)同一周期从左到右,稀有气体的电子亲合能最小,因为稀有气体价电 子层全满。 电负性:按阿莱—罗周电负性标度,第四周期的Ga、Ge、As、Se的x AR均分别比第三周期的Al、Si、P、S要大,其原因和第四周期P区元素Z*和r变化的反常同 理。 18-4 概括非金属元素的氢化物有哪些共性? 解:(1)均为共价型,常温下为气体或挥发性液体。 (2)同一族氢化物,其熔、沸点除NH3、H2O、HF由于氢键反常地高以外,其余均从上至下渐增。 (3)除HF外,其他非金属元素氢化物都有还原性,同一族氢化物从上至下还原性渐增,同一周期氢化物从左至右还原性递减。 (4)非金属元素氢化物相对于水而言,大多数是酸,其酸强度同一族从上到下递增; 同一周期从左至右也递增。少数氢化物如NH3 、PH3在H2O中表现碱性,H2O 是两性物,既可是酸也可是碱。CH4不表现酸碱性。 18-5 已知下列数据: △f Gm? (H2S,aq) = -27.9kJ·mol?1 △f Gm? (S2?,aq) = 85.8kJ·mol?1 △f Gm? (H2Se,aq) = 22.2 kJ·mol?1 △f Gm? (Se2?,aq) = 129.3kJ·mol?1 试计算下列反应的△r Gm?和平衡常数K:
专题一常见得非金属元素 考点一碳、硅及其重要化合物 1.理淸知识主线 错误!H」错误!一错误!0—错误! Ch 错误!II」错误!一错误!O?(H2S错误!O3) 2.注意网络构建 3.扫除知识盲点 (1)工业上制备粗硅,就是用过量得C与S i02高温下反应,由于C过量,生成得就是C0而不就是CO?, 该反应必须在隔绝空气得条件下进行. (2 )氢氟酸不能用玻璃容器盛放;NaOH溶液能用玻璃试剂瓶,但不能用玻璃塞。 (3 )酸性氧化物一般能与水反应生成酸,但SiCh不溶于水;酸性氧化物一般不与酸作用,但Si02能与HF 反应. (4)硅酸盐大多难溶于水,常见可溶性硅酸盐就是硅酸钠,其水溶液称为泡花碱或水玻璃,但却就是盐溶液。 (5)H^CCh得酸性大于H2SQ3得,所以有Na2SiO3+C 02(少量)+H/)M=H2SiO3 I +Na?CO3,但高温下NazCCh+SiO]错误!Na2SiO3+CO2t也能发生,原因可以从两方而解释:①硅酸盐比碳酸盐稳左:②从化学平衡角度,由髙沸点难挥发固体Si O2制得低沸点易挥发得CO2。 (6)SiO2不导电,就是制作光导纤维得材料;Si就是半导体,就是制作光电池得材料. (7)水泥、玻璃与陶瓷就是三大传统无机非金属材料;碳化硅、氮化硅等就是新型无机非金属材料. 【题组训练】 题组一重要反应必练 1。按要求书写反应方程式. (1)制水煤气:C+H2O(g)错误ICO + Iho (2)制备粗硅:2C+SiO]错误!2 CO t +Si o (3 ) Mg 在CO?中燃烧:2Mg+C 0 ,错误! 2 MgO+Co (4)“水滴石穿”得反应原理(用离子方程式表示):CaCO3+CO2+112O== C a21 + 211 C ! e (5)“钟乳石”得形成过程(用化学方程式表示):CaC0 3 +CO2+ H2O =C a (HCO3) 2, Ca(HC0处错误! CaCO3 I +CO21 +H2O。 (6)向饱与NazCOs溶液中通入过量CO?得离子方程式:2Na'+C0错CO2+H_>O= 2 NaHC 03I 0 (7)Si与氢氟酸得反应得化学方程式:S i+4HF=SiF4f+2H2t 0 (8 ) Si与N aOII溶液反应得离子方程式:S i 4-2OH + II2O=SiO错误!+2H2 f。 (9)Si02与氢氟酸得反应得化学方程式:SiO2+4HF===SiF4 t +2H2O. (10)S i O2与NaOII溶液反应得离子方程式:S i O2+2OH ==SiO错误! + H20. (11)向Na2SiO3溶液中通入过量CO2得离子方程式:SiO错误!+2CO2+2H> O=H2SiO5 I +2HC0 错误!。 题组二重要实验探究 3.单晶硅就是信息产业中重要得基础材料。通常用碳在髙温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度4 50?500 °C),四氯化硅经提纯后用氢气还原可得高纯硅?以下就是实验室制备四氯化硅得装置示意图。相关信息如下: a.四氯化硅遇水极易水解; b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应得氯化物; Co 请回答下列问题:
第十八章 非金属元素小结之教案 18-1 非金属元素单质的结构和性质 18-1-1 非金属元素单质的结构特点(C 级掌握) 非金属单质分子组成与晶体结构 有人提出8-N 规则,N 代表非金属元素在周期表中的族数,则该元素在单质分子中的共价数等于8-N 。 18-1.1:非金属单质按其结构和性质大致分成哪三类?每一类具有哪些通性?各类并举出至少一例说明。(C 级掌握) 18-1-2 非金属元素单质的性质 18-1.2:试举出六种可与强碱反应的非金属单质,这些反应都是歧化反应吗?(B 级了解) 18-2 分子型氢化物 18-2-1 氢化物的熔沸点(C 级掌握) 同一族中,沸点从上到下递增,但第2周期的NH 3、H 2O 及HF 的沸点异常地高,这是由于分子间存在着氢键,分子的缔合作用特别强的缘故。 18-2.1:简述H 2O,H 2S,H 2Se,H 2Te 熔点和沸点的变化规律并解释原因。(C 级重点掌握) 18-2.2: 为什么H 2O 的沸点比HF 还高?(A 级掌握) 18-2-2 热稳定性 一:变化规律(C 级重点掌握) 同一周期中,从左到右热稳定性逐渐增加:在同一族中,自上而下热稳定性逐渐减小。 二:理论解释(B 级掌握) 1。电负性差值的关系 非金属与氢的电负性相差越远,所生成的氢化物越稳定;反之,不稳定。 2。与△f G θ或△f H θ 的关系 这些氢化物的标准生成自由能△f G θ或标准生成焓△f H θ 越负,氢化物越稳定。 18-2.3:HF,HCl,HBr,HI 热稳定性的变化规律如何?可用哪些热力学函数来进行判断?如何判断?(C 级掌握) 18-2-3 还原性 一:变化规律(C 级重点掌握) 除了HF 以外,其它分子型氢化物都有还原性,且变化规律如下: CH 4 NH 3 H 20 HF SiH 4 PH 3 H 2S HCl GeH 4 AsH 3 H 2Se HBr (SnH 4) SbH 3 H 2Te HI 二:理论解释(B 级掌握)
元素金属性、非金属性强弱的判断依据 元素金属性、非金属性与其对应单质或离子的还原性、氧化性有着密不可分的关系,她们具有统一性,其实质就就是对应原子得失电子的能力,那么,如何判断元素金属性、非金属性强弱呢?这主要应从参加反应的某元素的原子得失电子的难易上进行分析,切忌根据每个原子得失电子数目的多少进行判断。下面就针对元素金属性、非金属性强弱的判断方法做一简要分析与总结。 一、元素金属性强弱判断依据 1、根据常见金属活动性顺序表判断 金属元素的金属性与金属单质的活动性一般就是一致的,即越靠前的金属活动性越强,其金属性越强。 。。。。。。Na Mg Al Zn Fe 。。。。。。 单质活动性增强,元素金属性也增强 需说明的就是这其中也有特殊情况,如Sn与Pb,金属活动性Sn﹥Pb,元素的金属性就是Sn﹤Pb,如碰到这种不常见的元素一定要慎重,我们可采用第二种方法。 2、根据元素周期表与元素周期律判断 同周期元素从左到右金属性逐渐减弱,如第三周期Na ﹥Mg ﹥Al;同主族元素从上到下金属性增强,如1中所述,Sn与Pb同属Ⅳ主族,Sn在Pb的上方,所以金属性Sn﹥Pb。 3、根据物质之间的置换反应判断 通常失电子能力越强,其还原性越强,金属性也越强,对于置换反应,强还原剂与强氧化剂生成弱还原剂与弱氧化剂,因而可由此进行判断。如:Fe + Cu2+ === Fe2+ + Cu 说明铁比铜金属性强。这里需说明的就是Fe对应的为Fe2+,如:Zn + Fe2+ === Zn2+ + Fe 说明金属性Zn﹥Fe,但Cu +2Fe3+ === Cu2+ + 2Fe2+,却不说明金属性Cu﹥Fe,而实为Fe﹥Cu。 4、根据金属单质与水或酸反应的剧烈程度或置换氢气的难易判断 某元素的单质与水或酸反应越容易、越剧烈,其原子失电子能力越强,其金属性就越强。 如Na与冷水剧烈反应,Mg与热水缓慢反应,而Al与沸水也几乎不作用,所以金属性有强到弱为Na ﹥Mg ﹥Al;再如:Na、Fe、Cu分别投入到相同体积相同浓度的盐酸中,钠剧烈反应甚至爆炸,铁反应较快顺利产生氢气,而铜无任何现象,根本就不反应,故金属性强弱:Na ﹥Mg ﹥Al。 5、根据元素最高价氧化物对应水化物的碱性强弱判断 如从NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物可得知金属性:Na ﹥Mg ﹥Al。 6、根据组成原电池时两电极情况判断 通常当两种不同的金属构成原电池的两极时,一般作负极的金属性较强。如Zn与Cu比较时,把Zn与Cu用导线连接后放入稀硫酸中,发现铜片上有气泡,说明锌为负极,故金属性Zn﹥Cu。但也应注意此方法判断中的特殊情况,如铝与铜用导线连接后放入冷浓硝酸中,因铝钝化,铜为负极,但金属性却为Al﹥Cu。 7、根据金属阳离子氧化性强弱判断
第九单元非金属元素 一、非金属通论 1、结构和位置 (1)非金属元素在周期表中的位置 在目前已知的112种元素中,非金属有16种(外加6种稀有气体元素)。除氢外,非金属元素地都位于周期表的右上方。H元素在左上方。F为非金属性最强的元素。 (2)非金属元素的原子结构特征及化合价 ①与同周期的金属原子相比较最外层电子数较多(一般为4~7个,H为1个,He为2个,B为3个),次外层都是饱和结构(2、8、或18电子结构)。 ②与同周期的金属原子相比较,非金属原子核电荷数较大,原子半径较小,化学反应中易得电子,表现氧化性。 ③最高正价等于族序数,对应最低负价等于族序数减8;如S、N、Cl等还呈现变价。 2、非金属单质 (1)几种重要固态非金属单质的结构和物理性质
(2)重要气、液态非金属单质的结构和物理性质 (3)结构与单质的化学性质 3、非金属单质的制备 (1)原理:化合态的非金属有正价态或负价态。 0R R ne n ??→?- ++,0 R R ne n ??→?- -- (2)方法: ① 氧化剂法,如: MnO 2+4HCl (浓)==MnCl 2+Cl 2↑+2H 2O 22 2Br Br Cl ?→?- ,22)(Cl g HCl O ?→ ?(地康法制氯气) ② 还原剂法,如: Si SiO C ?→?2,242H SO H Zn ?→?
③ 热分解法,如: 23 O KClO ??→?加热 ,24 H C CH +??→?高温 ④ 电解法,如: 电解水制H 2、O 2,氯碱工业制Cl 2等。 ⑤ 物理法,如: 工业上分离液态空气得N 2(先)、O 2(后) 4、非金属气态氢化物 (1)分子构型与物理性质 ⅣA ——RH 4 正四面体结构,非极性分子; ⅤA ——RH 3 三角锥形,极性分子; ⅥA ——H 2R 角型(或“V “型)分子,极性分子; ⅦA ——HR 直线型,极性分子。 固态时均为分子晶体,熔沸点较低,常温下H 2O 是液体,其余都是气体。 (2)化学性质 ① 稳定性及水溶液的酸碱性 非金属元素原子跟氢原子通过共价键形成气态氢化物,一般元素的非金属性越强,跟氢化合能力越强,生成的气态氢化物越稳定,因此气态氢化物的稳定性是非金属性强弱的重要标志之一。 ② 还原性 a . 与O 2:NH 3→NO ,H 2S →SO 2(或S ),HCl →Cl 2。 b . 与Cl 2:H 2S →S ,HBr →Br 2,NH 3→N 2 。 c . 与Fe 3+:H 2S →S ,HI →I 2。 d . 与氧化性酸:H 2S+H 2SO 4(浓)→,HBr 、HI 分别与浓硫酸及硝酸反应 e . 与强氧化剂:H 2S 、HCl 等可与酸性KMnO 4作用。
判断元素金属性非金属性强弱的方法 在化学教学活动过程中,常常会遇到判断元素金属性、非金属性强弱的问题。对这个问题把握不好,往往会造成对与之相关联的其他问题的理解和错误处理。本文就中学化学教学中如何判断元素金属性、非金属性强弱的方法做一小结,以期对中学生的化学学习有所帮助。 一、利用元素在周期表中的位置判断 在元素周期表中,同周期元素从左至右,金属性逐渐减弱,非金属性逐渐增强(稀有气体元素除外);同主族元素从上到下,金属性逐渐增强,非金属性逐渐减弱。因此,除稀有气体元素外,金属性最强的元素铯(Cs)位于周期表的左下角,非金属性最强的元素氟(F)位于周期表的右上角。 二、利用单质与水或非氧化性酸反应置换出氢气的难易程度判断元素金属性强弱 元素的单质与水或非氧化性酸反应置换出氢气越容易(反映越剧烈),其金属性越强;反之,金属性越弱,如金属钠(Na)与冷水反应不及钾(K)剧烈,金属钾与冷水反应甚至可听到爆鸣声,所以钠的金属性比钾弱。镁(Mg)与盐酸反映剧烈放出氢气,铝与盐酸缓慢反映放出氢气,所以镁的金属性比铝强。 三、可利用单质与H2反应生成气态氢化物的难易及氢化物的稳定性判断元素非金属性强弱 单质与H2化合生成气态氢化物越容易,生成的气态氢化物越稳定,则元素的非金属性越强。如卤素按氟(F)、氯(Cl)、溴(Br)、碘(I)的顺序,其单质与H2反应越来越难,氢化物(HX)的稳定性也越来越弱,所以卤素的非金属性按氟、氯、溴、碘顺序逐渐减弱。 四、利用最高价氧化物对应水化物的酸(碱)性强弱判断 若元素的最高价氧化物对应的水化物的酸(碱)性越强,则其非金属性(金属性)也越强。如酸性HNO3>H2CO3,则非金属性N>C;碱性NaOH>Mg(OH)2,则金属性Na>Mg。 五、利用单质与盐溶液的置换反应判断 依据盐溶液与金属作用规律,位于金属活动性顺序中前面的金属可以把位于其后面的金属从其盐溶液中置换出来,这样就可利用金属与盐溶液的置换反应来判断两种金属的活动性强弱。如铁(Fe)能从硫酸铜(CuSO4),溶液中置换出Cu,则Fe的金属性比Cu强。非金属间也存在类似的作用规律(常见非金属的活动性顺序F>O>Cl>Br>I>S)。所以可根据Cl2与NaBr溶液间的置换反应,判
龙文教育学科老师个性化教案
2HClO 光照 或加热 2HCl + O2↑ 5.Br2 、I2在不同溶剂中的颜色 水苯或汽油四氯化碳 Br 2黄~橙橙~橙 红 橙~橙 红 I2深黄~褐淡紫~紫 红紫~深紫 6.置换反应 Cl2 + 2NaBr = Br2+ 2NaCl Br2 + 2KI = I2 + 2KBr ∴氧化性 Cl2 >Br2 >I2 7.I2遇淀粉溶液后,溶液呈蓝色 I- 氧化剂——————→ I2 三.氮 1.氮的氧化物 NO:无色气体、有毒(同CO)、难溶与水 NO2:红棕色气体、有毒、与水反应 反应:2NO + O2 = 2NO2 3NO2 + 2H2O = 2HNO3 + NO 2.有关NO与O2或NO2与O2混合通入水中,液面上升一定高度时用的方程式 4NO2 + O2 + 2H2O = 4HNO3 4NO+ 3O2 + 2H2O = 4HNO3 3.硝酸 物理性质无色液体、有刺激性气味、能以任意比溶于水 化学性质 酸的通性 强 氧 化 性 与金属氧化 物 3FeO + 10HNO3 = 3Fe(NO3)3 + NO↑+ 5H2O 与金属 3Cu + 8HNO3(稀) = 3Cu(NO3)2+2NO↑+ 4H2O Cu + 4HNO3(浓) = Cu(NO3)2 +2NO2↑+ 2H2O 与非金属 C + 4HNO3(浓) △ CO2↑+ 4NO2↑+ 2H2O 不稳定性4HNO 3 光照 或加热 4NO2↑+ O2↑+ H2O 4.氨 ( NH3 ) 物理性质无色气体、有刺激性气味、密度小于空气、1:700 溶于水 化学性质 与H2O NH3 + H2O NH3·H2O NH4++ OH-与酸NH3 + HCl = NH4Cl 氨的 催化氧化 4NH3 + 5O2 催化剂 加热 4NO + 6H2O 实验室制取原 理NH4+ + OH-△ NH3↑+ H2O
专题一常见的非金 属元素
仅供学习与交流,如有侵权请联系网站删除 谢谢2 专题一 常见的非金属元素 考点一 碳、硅及其重要化合物 1.理清知识主线 C -4 H 4C 0 ―→C +2O ―→C +4O 2 Si -4H 4Si 0 ―→Si +4O 2(H 2S i +4 O 3) 2.注意网络构建 3.扫除知识盲点 (1)工业上制备粗硅,是用过量的C 和SiO 2高温下反应,由于C 过量,生成的是CO 而不是CO 2,该反应必须在隔绝空气的条件下进行。 (2)氢氟酸不能用玻璃容器盛放;NaOH 溶液能用玻璃试剂瓶,但不能用玻璃塞。 (3)酸性氧化物一般能与水反应生成酸,但SiO 2不溶于水;酸性氧化物一般不与酸作用,但SiO 2能与HF 反应。 (4)硅酸盐大多难溶于水,常见可溶性硅酸盐是硅酸钠,其水溶液称为泡花碱或水玻璃,但却是盐溶液。 (5)H 2CO 3的酸性大于H 2SiO 3的,所以有Na 2SiO 3+CO 2(少量)+H 2O===H 2SiO 3↓+Na 2CO 3,但高温下Na 2CO 3+SiO 2=====高温 Na 2SiO 3+CO 2↑也能发生,原因可以从两方面解释:①硅酸盐比碳酸盐稳定;②从化学平衡角度,由高沸点难挥发固体SiO 2制得低沸点易挥发的CO 2。 (6)SiO 2不导电,是制作光导纤维的材料;Si 是半导体,是制作光电池的材料。 (7)水泥、玻璃与陶瓷是三大传统无机非金属材料;碳化硅、氮化硅等是新型无机非金属材料。 【题组训练】 题组一 重要反应必练 1.按要求书写反应方程式。 (1)制水煤气:C +H 2O(g)=====高温 CO +H 2。 (2)制备粗硅:2C +SiO 2=====高温2CO ↑+Si 。 (3)Mg 在CO 2中燃烧:2Mg +CO 2=====点燃 2MgO +C 。 (4)“水滴石穿”的反应原理(用离子方程式表示):CaCO 3+CO 2+H 2O===Ca 2++2HCO - 3。 (5)“钟乳石”的形成过程(用化学方程式表示):CaCO 3+CO 2+H 2O===Ca(HCO 3)2,Ca(HCO 3)2=====△ CaCO 3↓+CO 2↑+H 2O 。 (6)向饱和Na 2CO 3溶液中通入过量CO 2的离子方程式:2Na ++CO 2- 3+CO 2+H 2O===2NaHCO 3↓。 (7)Si 和氢氟酸的反应的化学方程式:Si +4HF===SiF 4↑+2H 2↑。 (8)Si 和NaOH 溶液反应的离子方程式:Si +2OH -+H 2O===SiO 2- 3+2H 2↑。 (9)SiO 2和氢氟酸的反应的化学方程式:SiO 2+4HF===SiF 4↑+2H 2O 。 (10)SiO 2和NaOH 溶液反应的离子方程式:SiO 2+2OH -===SiO 2- 3+H 2O 。 (11)向Na 2SiO 3溶液中通入过量CO 2的离子方程式:SiO 2-3+2CO 2+2H 2O===H 2SiO 3↓+2HCO - 3。 题组二 重要实验探究 3.单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。相关信息如下: a .四氯化硅遇水极易水解; b .硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
专题4 非金属元素及其化合物 一、考点、热点回顾(易混点) (一).无机非金属材料的主角—硅 1、硅(Si ) 含量:硅在地壳中含量为 (O:48.6,Si26.3,硅土90),居第 位。 (1)工业制硅: ①制取粗硅;SiO 2+2C 高温Si+2CO↑ ②提纯:与Cl 2反应:Si+2Cl 2高温SiCl 4 ③制精硅:与H 2反应:SiCl 4+2H 2高温Si+4HCl (2)与F 2反应:242()Si F SiF g += 与HF 反应:42Si 4HF SiF 2H +=+ 与NaOH 反应:↑+=++232222H SiO Na O H NaOH Si (3)与O 2反应:(研细) 与H2反应:(易自燃) 与FeO 反应: 2、二氧化硅(SiO 2) (1)二氧化硅(可用于制造光导纤维) 物理性质:SiO 2是 溶于水的固体,熔、沸点 ,硬度 。 (2)与HF 反应 ,利用此反应可用HF 的溶液来 刻蚀 玻璃。 与酸性氧化物CaO 反应:3Si CaO CaSiO +===高温 与NaOH 反应方:2232SiO NaOH Na SiO H O +=+ 思考:实验室中盛放NaOH 溶液的试剂瓶用 塞不用 塞,试解释其原因? (3)与C 反应:2SiO C SiC CO +=+ (4)CO 2与SiO 2性质比较 CO 2 SiO 2 状态 无色无味气体 无色晶体 与H 2O 反应 CO 2+H 2O=H 2CO 3 不反应 与碱NaOH 反应 CO 2+2NaOH=Na 2CO 3+H 2O SiO 2+2NaOH=Na 2SiO 3+H 2O 与碱性氧化物CaO 反应 CO 2+CaO=CaCO 3 SiO 2+CaO=CaSiO 3
第十五章非金属元素小结p645 8.试从结构观点分析含氧酸强度和结构之间的关系。用鲍林规则判断下列酸的强弱: N Pka N PKa (1) HClO 0 ~+7 (2)HClO2 1 +2 (3)H3AsO3 0 ~+7 (4)HIO3 2 -3 (5)H3PO3 1 +2 (6)HBrO3 2 -3 (7)HMnO4 3 -8 (8)H2SeO4 2 -3 (9)HNO2 1 +2 (10)H6TeO6 0 +7 9.试说明为什么下列各组酸的强度是: (1)HI>HBr>HCl>HF 从I-到F-,X增强,r减小,电子密度增大,对H+的吸引力增强 (2)HClO4> H2SO4>H3PO4>H4SiO4 从左到右,R n+电荷降低,r增大,R n+对O-H氧原子上电子对的吸引力减弱,O-H键极性减弱,更不易断键电离出H+。 (3)HNO3>HNO2 HNO3中N3+,HNO2中N+,前者电荷更高,r更小,吸引O-H氧原子电子对的能力更强(4)HIO4>H5IO6 HIO4中3个非羟基氧原子,H5IO6中仅一个非羟基氧原子,非羟基氧原子从R n+吸引电子,故其越多。R n+的正电荷越强,越有利于其从O-H氧原子吸引电子对,使O-H极性增强而于发生离解。 (5)H6TeO6>H2SeO4 H2SeO4 Se6+周围2个非羟基氧原子,H6TeO6无非羟基氧原子 11.Na2CO3和CaCO3的标准溶解焓变ΔS Ho分别为-24.69KJ.mol-1和-12.13KJ.mol-1。试参照表15-8,15-9的数据计算两者的标准溶解自由能变化ΔS Go,并用此数据对两者在水中的溶解性作出判断。分析两者水溶性不同的原因。 ?S SoNa2CO3=2?S SoNa+(aq)+ ?S So(CO32-(aq))=2×28.8-116.7=-59.1J.mol-1 ?S SoCaCO3=? S So(Ca2+(aq))+ ?S So(CO32-(aq))=-94.1-116.7=-210.8J.mol-1.K-1 ?GoS(Na2CO3)=-24.69-298×(-59.1)/1000=-7.078KJ ?GoS(CaCO3)=-12.13-298×(-210.8)/1000=50.688KJ Na2CO3(S)==2Na+(aq)+CO32-(aq) ΔS So(Jmol-1K-1) 28.8 -116.7 ΔS SoNa2CO3=ΣΔS So=2×28.8+1×(-116.7)=-59.1J.mol-1.K-1 ΔS GoNa2CO3=ΔS HoNa2CO3-TΔS SoNa2CO3 =-24.69-298×(-59.1)/1000 =-7.078(KJ) Ca2CO3(S)==Ca2+(aq)+CO32-(aq) ΔS So(Jmol-1.K-1) -94.1 -116.7 ΔS SoCaCO3=-94.1-116.7=-210.8J.mol-1.K-1 ΔS GoCaCO3=ΔS HoCaCO3-TΔS SoCaCO3 =-12.13-298×(-210.8)/1000
龙文教育学科老师个性化教案 教师学生姓名上课日期 学科化学年级高三教材版本浙教版 学案主题非金属及其化合物的性质 课时数量 (全程或具体时 间) 第( 7 )课 时 授课时段 教学目标 教学内容 氮硫的性质 个性化学习问 题解决 针对该知识点的应用性比较大设计教学! 教学重 点、难点 该部分知识点的计算类以及实用性很强要好好把握! 教学过程 非金属及其化合物 一.硅 1.相关反应 Si 物理性质 晶体硅:灰黑色固体、金属光泽熔点高、 硬而脆 化学 性质 与非金属反应Si + O 2 △ SiO2 与氢氟酸反应Si + 4HF = SiF4↑+ 2H2↑ 与强碱溶液反 应 Si + 2NaOH + H2O = Na2SiO3 + 2H2↑ 粗硅工业制取SiO2 + 2C 高温 Si + 2CO↑ SiO2 物理性质熔点高、硬度大、纯净的晶体俗称水晶 化 学 性 质 与氢氟酸反应SiO2 + 4HF = SiF4↑+ 2H2O 与强碱溶液反应SiO2 + 2NaOH = Na2SiO3 + H2O 与盐反应 SiO2 + Na2CO3 高温 Na2SiO3 + CO2↑ SiO2 + CaCO3 高温 CaSiO3 + CO2↑ H2SiO3 物理性质白色沉淀 化学 性 质 与强碱溶液反应H2SiO3 + 2NaOH = Na2SiO3 +2H2O 加热H 2SiO3 △ H2O + SiO2 实验室制取原理Na2SiO3 + 2HCl = H2SiO3↓+ 2NaCl 2.三大传统无机非金属材料 水泥玻璃陶瓷原料石灰石黏土纯碱、石灰石、石英(过量)黏土设备水泥回转窑玻璃窑 原理复杂的物理化学变化 SiO2 + Na2CO3 高温 Na2SiO3 + CO2↑ SiO2 + CaCO3 高温 CaSiO3 + CO2↑成分 硅酸二钙2CaO·SiO2硅酸三钙 3CaO·SiO2 Na2SiO3 CaSiO3 SiO2
专题十一 常见非金属元素 [考纲要求] 常见非金属元素(如H 、C 、N 、O 、Si 、S 、Cl 等):(1)了解常见非金属元素单质及其重要化合物的制备方法,掌握其主要性质及其应用;(2)了解常见非金属元素单质及其重要化合物对环境的影响;(3)以上各部分知识的综合应用。 考点一 碳、硅及其重要化合物 硅元素的非金属性不强,但其具有“亲氧”特性,使硅元素在自然界中没有游离态,只有化合态,其主要以二氧化硅和硅酸盐的形式存在。对于碳、硅两元素,复习时应从以下几个方面掌握。 1.树立物质转化思想 (1)理清知识主线 C -4 H 4←―C 0 ―→C +2 O ―→C +4 O 2 Si -4 H 4←―Si 0 ―→ Si +4 O 2(H 2Si +4 O 3) (2)形成网络构建 2.扫除易忘知识盲点 (1)硅元素位于元素周期表中金属与非金属的分界线附近,具有部分金属性,如①晶体硅具有金属光泽和特殊导电性;②单质主要表现出还原性;③单质能和碱溶液反应生成氢气。 (2)工业上制备粗硅,是用过量的C 和SiO 2在高温下反应,由于C 过量,生成的是CO 而不是CO 2,该反应必须在隔绝空气的条件下进行。 (3)氢氟酸不能用玻璃容器盛放;NaOH 溶液能用玻璃试剂瓶,但不能用玻璃
塞。 (4)酸性氧化物一般能与水反应生成酸,但SiO 2不溶于水;酸性氧化物一般不与酸作用,但SiO 2能与HF 反应。 (5)硅酸盐大多难溶于水,常见可溶性硅酸盐是硅酸钠,其水溶液称为泡花碱或水玻璃,但却是盐溶液。硅胶(mSiO 2·nH 2O)是一种很好的无毒干燥剂。 (6)H 2CO 3的酸性大于H 2SiO 3的,所以有Na 2SiO 3+CO 2(少量)+H 2O===H 2SiO 3↓+Na 2CO 3,但高温下Na 2CO 3+SiO 2=====高温Na 2SiO 3+CO 2↑也能发生,原因可从两方面解释:①硅酸盐比碳酸盐稳定;②从化学平衡角度,由高沸点难挥发的固体SiO 2制得低沸点易挥发的CO 2气体。 (7)硅、二氧化硅和硅酸盐的化学性质相对稳定,广泛用于制造各种材料,如硅——半导体材料、太阳能电池帆板等;二氧化硅——光导纤维、其他光学材料、耐高温材料、耐磨材料、饰品等,并用于生产新型陶瓷;硅酸盐——陶瓷、玻璃、水泥等传统无机非金属材料的主要成分,作耐高温材料、防火材料,制造硅胶等。 题组一 重要反应规范书写 1.用方程式回答下列问题。 (1)Mg 在CO 2中燃烧。 2Mg +CO 2=====点燃 2MgO +C 。 (2)“水滴石穿”的反应原理(用离子方程式表示)。 CaCO 3+CO 2+H 2O===Ca 2++2HCO -3。 (3)“钟乳石”的形成过程(用化学方程式表示)。 CaCO 3+CO 2+H 2O===Ca(HCO 3)2, Ca(HCO 3)2=====△ CaCO 3↓+CO 2↑+H 2O 。 (4)向饱和Na 2CO 3溶液中通入过量CO 2的离子方程式。 2Na ++CO 2- 3+CO 2+H 2O===2NaHCO 3↓。 (5)氢氟酸不能用玻璃瓶盛放,其原因是(用化学方程式表示)。 SiO 2+4HF===SiF 4↑+2H 2O 。 (6)盛放NaOH 溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示)。
非金属元素专题复习讲义 专题复习内容 1.元素及其化合物内容学习的方法 2.非金属元素的概述 3.氢气、水的知识小结 重点、难点剖析及典型例析 (一)学习方法指导 1.每族元素抓住代表物.重点讨论该元素的单质、氧化物、氢化物、酸、碱或盐等有关知识. 2.注意该族元素与其代表物在结构、性质上的相似性、递变性和特殊性. 3.研究结构应分三层次考虑. (1)原子结构(价电子数、原子半径、核电荷数等) (2)分子结构(主要指化学键的种类及牢固程度) (3)晶体结构(构成微粒、微粒间的作用力、空间构型等) 4.理清下列关系. 5.元素化合物知识网络化 元素化合物的知识在中学化学教材中占有较重的比例,内容繁多锁碎,要尽可能以最佳的方法或方式来总结成网络图,主线明确、脉络清晰. (二)非金属元素在周期表中的位置及结构特点. (1) 除H外,非金属元素均在“阶梯线”的右上方 (2) 非金属元素(包括稀有元素)均在主族(零族) (3) 最外层电子数一般≥4(H.B除外) (4) 原子半径比同周期金属半径小.(稀有元素除外) (三)非金属元素的性质及递变规律 1.单质: (1)结构:除稀有气体外,非金属原子间以共价键结合.非金属单质的成键有明显的规律性.若它处在第N族,每个原子可提供8-N个价电子去和8-N个同种原子形成8-N个共价单键,可简称8-N规则;(H遵循2-N规则).如ⅦA族单质:x-x;H的共价数为1,H-H,第ⅥA族的S,Se、Te共价单键数为8-6=2,第ⅤA族的P、As共价单键数8-5=3.但第二周期的非金属单质中N2、O2形成多键. 2.熔沸点与聚集态 它们可以分为三类: ①小分子物质.如:H2、O2、N2、Cl2等,通常为气体,固体为分子晶体. ②多原子分子物质.如P4、S8、As等,通常为液态或固态.均为分子晶体,但熔、沸点因范德华力较大而比①高,Br2、I2也属此类,一般易挥发或升华. ③原子晶体类单质,如金刚石、晶体硅和硼等,是非金属单质中高熔点“三角区”,通常为难挥发的固体. 3.导电性
非金属元素及其化合物小结 广东省湛江一中王国安 本章是一个很重要的章节,是中学化学的重点、难点之一,是化学学习中不可缺少的环节。 一、新课标内容 通过实验了解氯、氮、硫、硅等非金属及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响。 二、知识重点与学习难点 (一)物理性质 Cl2、N2是气体,S、Si是固体;Cl2有毒;都难溶于水(Cl2的溶解性稍大一些);Cl2是黄绿色,S是淡黄色,N2是无色。 单纯地记忆这些知识是很枯燥的,如何巧妙而又牢固地掌握这些知识呢?比如将这些知识运用到物质的分离方面、Cl2万一泄漏时如何躲避及中毒时的救护等实用方面,通过理论结合实际,不仅学习具有了趣味性,而且主动地去学习、思考,你的记忆也牢固了,自然做题就更得心应手了。 (二)化学性质 因为是典型的非金属,所以Cl2、S、N2常作氧化剂;Si的性质很稳定,在常温下除与F2、HF 和强碱外不跟其他物质起反应。 (三)单质的性质比较 下边的这些方程式是一些基本的重点,也是难点。 1.Cl2的性质很活泼,发生的反应很多,而N2、Si 则比较稳定,能和它们发生反应的物质很少,即使反应也比较难,所以Cl2是重点,S次之。 2.Cl2的氧化性强,S次之,所以生成的产物的化合价有区别:Cl2与变价金属反应时得相应金
属元素的高价产物,而S 与之反应则得低价产物。 3.NaOH 与S 的反应,体现出与Cl 2 的相似性,反应式为:3S+6NaOH △==2Na 2 S+Na 2SO 3+3H 2O 。 还有一些引申的内容:反应Cl 2 与Ca(OH)2的反应以及漂白粉的成分、氯水的成分及性质,与 HNO 3 的有关反应、卤素的性质、SO 2 的漂白性、NO 2 的吸收等,也都是我们要留意的知识点。 (四)几种化合物的性质比较 (1)浓H 2SO 4、浓HNO 3、稀HNO 3都是强氧化剂,是中学里的重点和难点,有关反应很 多,注意归纳和记忆。其共同点是:能氧化大多数金属和非金属和低价化合物,并生成其高价产物, 而S 或N 元素的化合价则降低,一般降到+4或+2价。 (2)Fe 、Al 在冷的浓HNO 3或浓H 2SO 4中会产生钝化现象,即在金属表面形成一层致密的氧化膜,阻止金属继续与浓酸发生反应。 (3)金属和HNO 3反应生成的不是H 2。 3.NH 3 NH 3的性质:NH 3+HCl=NH 4Cl 。类似的反应很多,要会写,对应的实验现象应注意。 NH 3的制备:2NH 4Cl+Ca(OH)2 △ ====== 2NH 3↑+CaCl 2+2H 2O 。反应物是固体,不能排水收集。