
2019届高三考前选择题冲刺训练——实验专题
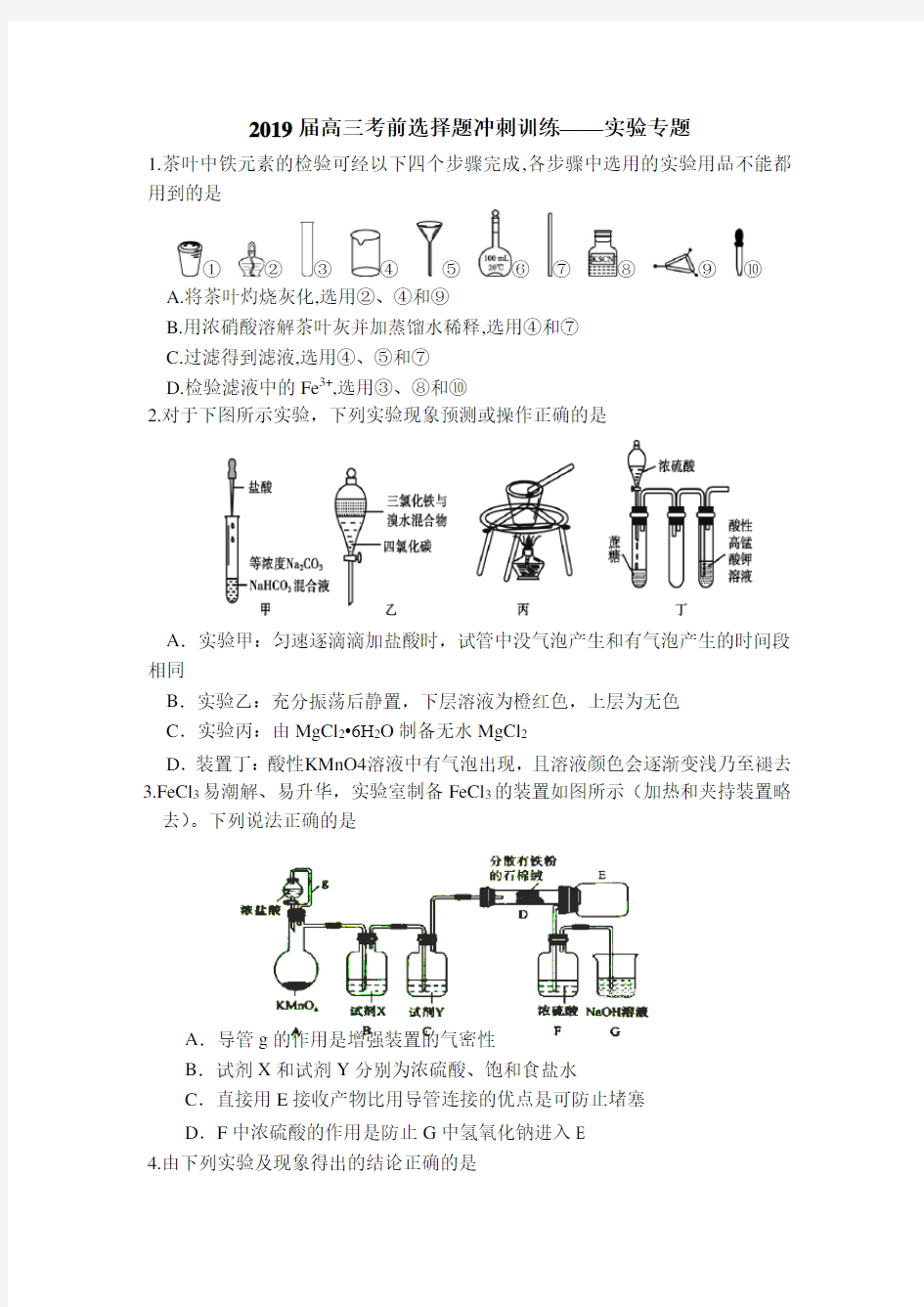
1.茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是
①②③④⑤⑥⑦⑧⑨⑩
A.将茶叶灼烧灰化,选用②、④和⑨
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+,选用③、⑧和⑩
2.对于下图所示实验,下列实验现象预测或操作正确的是
A.实验甲:匀速逐滴滴加盐酸时,试管中没气泡产生和有气泡产生的时间段相同
B.实验乙:充分振荡后静置,下层溶液为橙红色,上层为无色
C.实验丙:由MgCl2?6H2O制备无水MgCl2
D.装置丁:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去3.FeCl3易潮解、易升华,实验室制备FeCl3的装置如图所示(加热和夹持装置略去)。下列说法正确的是
A.导管g的作用是增强装置的气密性
B.试剂X和试剂Y分别为浓硫酸、饱和食盐水
C.直接用E接收产物比用导管连接的优点是可防止堵塞
D.F中浓硫酸的作用是防止G中氢氧化钠进入E
4.由下列实验及现象得出的结论正确的是
实验
现象结论
A SO2 与H2S气体混合产生淡黄色沉淀氧化性: SO2>S
B 向盛有FeSO4溶液的试管中滴入
氯水,然后滴入KSCN溶液滴入KSCN后溶
液变为红色
原FeSO4溶液已被空气中O2氧
化变质
C 试管中盛有Cu(NO3)2溶液,底部
有少量铜,向其中加入稀硫酸
铜粉逐渐溶解铜可与稀硫酸反应
D 向2 支盛有2mL 相同浓度的
NaOH溶液的试管中分别滴入2
滴相同浓度的AlCl3和MgCl2溶
液,振荡并静置前者无沉淀,后
者有白色沉淀
Ksp[Al(OH)3]>Ksp[Mg(OH)2]
5.下列实验方案设计不能达到实验目的的是
选项实验目的实验方案
A 检验FeCl2溶液中的FeCl2是否
被氧化
向该溶液中滴加硫氰化钾溶液
B 证明H2CO3酸性比H2SiO3强Na2CO3和SiO2在高温下熔融反应
C 除去Cu粉中混有的CuO 向混合物中滴加适量稀硫酸
D 证明CH2CHCHO中含有醛基向新制银氨溶液中滴少量丙烯醛并用水浴加热
6.实验室用H2还原SiHCl3(沸点:31.85 ℃)制备纯硅的装置如下图所示(夹持装置和尾气处理装置略去)。下列说法正确的是
A.装置Ⅱ、Ⅲ中依次盛装的是浓硫酸、冰水
B.实验时,应先加热管式炉,再打开盛装稀硫酸的分液漏斗
C.为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液
D.该实验中制备氢气的装置也可用于氧氧化钠稀溶液与氯化铵固体反应制备氨气
答案解析
1.【答案】A
【解析】A.将茶叶灼烧灰化,应在坩埚中加热,用到的仪器有①、②和⑨,必要时还可用到三脚架或铁架台带铁圈,不需要④,故A正确;
B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,应在烧杯中进行,可用玻璃棒搅拌,选用④和⑦,故B错误;
C.过滤时用到④、⑤和⑦,故C错误;
D.检验滤液中的Fe3+,可用胶头滴管取少量滤液于小试管中,用KSCN溶液检验,用到的仪器有试管、胶头滴管和滴瓶等,即③、⑧和⑩,故D错误。
2.【答案】D
【解析】A.同浓度时碳酸钠比碳酸氢钠的碱性强;匀速逐滴滴加盐酸时,盐酸首先与碱性强的碳酸钠反应,产生弱碱性的碳酸氢钠。此时,溶液中没有气泡产生;然后,继续滴加盐酸,盐酸再与弱碱性的碳酸氢钠反应,此阶段有气泡产生,根据题目中量的关系,这两个阶段所消耗的盐酸的量的比应为1:2,则试管中没气泡产生和有气泡产生的时间应为1:2,故A错误;
B.四氯化碳把溴萃取到下层,所以下层会变为橙红色,但三氯化铁溶液仍然在上层,上层应为黄色,故B错误;
C.应在HCl的气流中加热,否则无法制备得到无水MgCl2。故C错误;
D.浓硫酸与蔗糖反应会生成二氧化碳和二氧化硫气体,使溶液中有气泡出现,二氧化硫具有还原性,能与高锰酸钾反应从而使KMnO4溶液颜色逐渐变浅乃至褪去,故D正确。
3 .【答案】C
【解析】A.导管g的作用应该是平衡气压使液体能够顺利滴下,故A错误。
B.试剂X和试剂Y应该分别是饱和食盐水和浓硫酸,否则得不到纯净干燥的氯气,故B错误。
C.用E装置接收产物,空间大能防止堵塞,故C正确。
D.F中浓硫酸的作用应是防止水气进入E装置导致氯化铁水解,故D错误。
4.【答案】A
【解析】 A. SO2与H2S气体反应生成S和水,则产生淡黄色沉淀,可知氧化性: SO2 > S,故A正确;
B.氯水可氧化亚铁离子,由现象不能说明原FeSO4溶液已被空气中O2氧化变质,故B错误;
C. Cu与稀硫酸不反应,酸性条件下Cu、硝酸根离子发生氧化还原反应,则铜粉逐渐溶解,故C错误;
D.NaOH足量,不能比较Ksp,且氢氧化铝可溶于NaOH,结论不合理,故D
错误。
5.【答案】B
【解析】A.亚铁离子被氧化,则混有铁离子,可知向该溶液中滴加硫氰化钾溶液,若溶液变血红色,可检验被氧化,故A正确;
B. Na2CO3和SiO2在高温下反应,不是强酸制取弱酸的反应,则不能比较
H2CO3酸性比H2SiO3强,故B错误;
C. CuO与硫酸反应,而Cu不能,则向混合物中滴加适量稀硫酸可溶除杂,故C正确;
D.碳碳双键与银氨溶液不反应,-CHO 与银氨溶液反应,则向新制银氨溶液中滴少量丙烯醛并用水浴加热可检验-CHO 故D正确。
6.【答案】C
【解析】A.装置Ⅲ需水浴加热,目的是使SiHCl3气化,与氢气反应,故A错误;
B.应先通入氢气,以排出装置内空气,防止在加热时爆炸,故B错误;
C.检验是否含有铁,加入盐酸生成氯化亚铁,加入过氧化氢可生成氯化铁,然后用KSCN检验,故C正确;
D.氨气易溶于水,不能用氢氧化钠稀溶液制备氨气, 故D错误。