
【肺癌篇】精准医疗到底精准了啥?看看在肺癌治疗
中的进展
肺癌是临床精准医疗研究较为成熟的一种疾病,目前已找到一系列相关的疾病
驱动基因,如EGFR、ALK、ROS1等,并开发出了相应的靶向药物,如吉非替
尼、西妥昔单抗等。虽然靶向药物治疗比传统化疗效果更好,但只有携带特定透
分子遗传标记的人群才可从中受益,且在使用过程中容易产生耐药性,这些都
极大影响了靶向药物的临床应用。下文主要探讨精准医疗在肺癌研究中的进
展。
肺癌分子特异性差异显著
测序技术的发展为肿瘤发生机制的探索带来了新的契机,研究发现肺癌患者体
内可以改变正常蛋白表达的基因突变高达150种,比其他的恶性肿瘤高出30-
60倍,这可能是肺癌发生率偏高的原因之一。
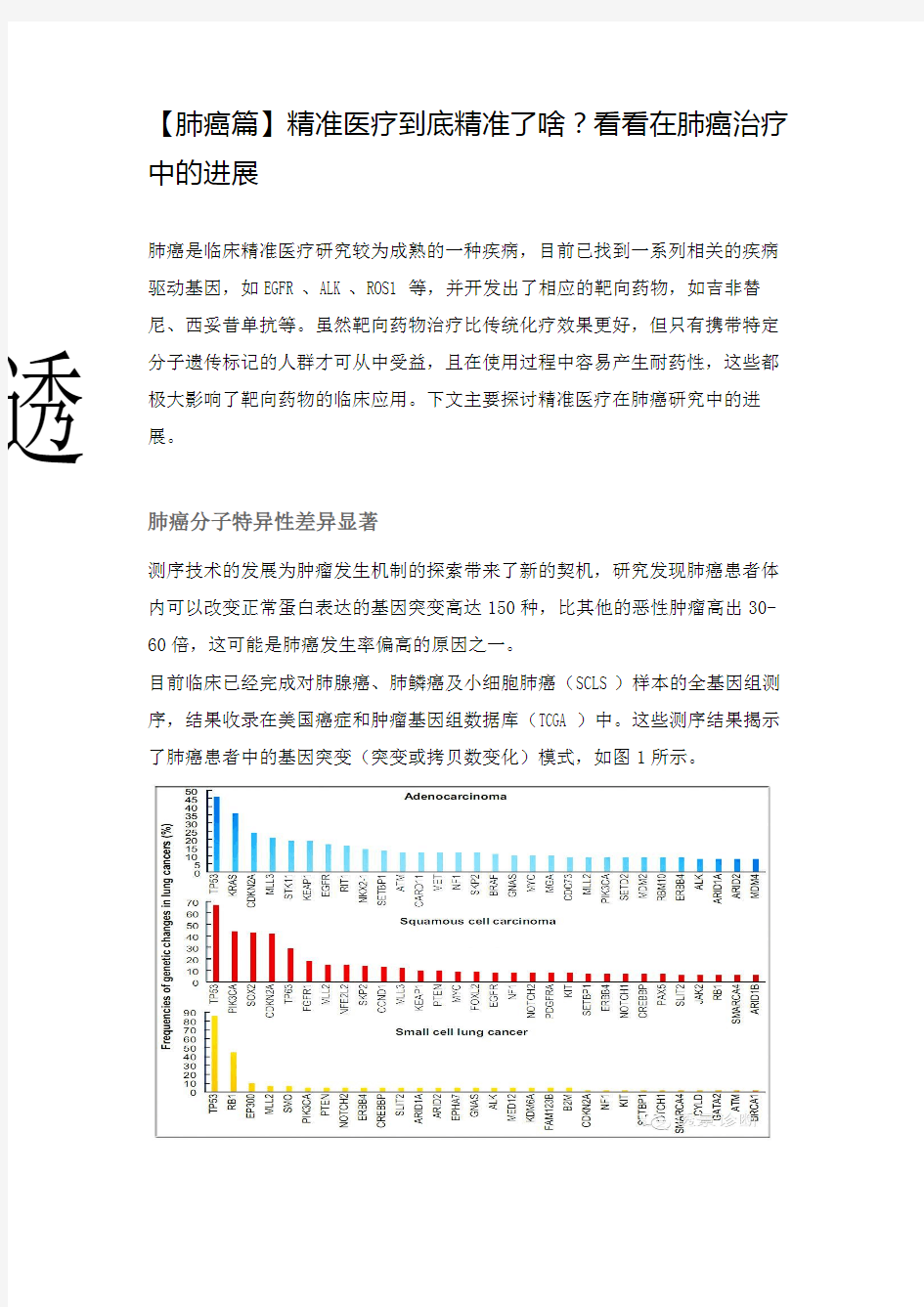
目前临床已经完成对肺腺癌、肺鳞癌及小细胞肺癌(SCLS)样本的全基因组测
序,结果收录在美国癌症和肿瘤基因组数据库(TCGA)中。这些测序结果揭示
了肺癌患者中的基因突变(突变或拷贝数变化)模式,如图1所示。
图1 不同组织类型肺癌基因突变分子模式
测序结果显示无论哪种类型的肺癌患者,TP53都是突变频率最高的基因(肺腺癌中为46%,
小细胞肺癌中为86%),但3种组织类型的基因突变图谱差异显著:肺腺癌中除了TP53以透
外的另4种突变频率最高的基因为KRAS、CDKN2A、MLL3和STK11,鳞癌则为PIK3CA、
SOX2、CDKN2A和TP63,而小细胞肺癌则是RB1、EP300、MLL2和SMO。虽然这些突
变都可能改变关键蛋白的表达水平或蛋白构象,导致正常生理功能发生改变,从而促进癌症
的发生发展(如KARS基因突变后其产物构象发生变化,激活了下游信号通路,诱导癌变发
生),但目前临床开发的靶向药物还非常少,只有有限的几种靶向药物,如靶向EGFR的药
物如吉非替尼、埃罗替尼及阿法替尼及靶向ALK、ROS1和MET的克里唑替尼等。
肺癌治疗之EGFR靶向治疗
表皮生长因子受体(EGFR)是肺癌的主要驱动基因,也是目前临床应用比较成
熟的靶向治疗基因,该突变在3种肺癌中都能检测到,肺腺癌患者中最高,常
见于女性或非吸烟患者。临床采用EGFR抑制剂(吉非替尼和埃罗替尼)治疗肺
癌患者的过程中发现EGFR突变与治疗敏感度有关,后续研究证实EGFR突变可
作为临床评估EGFR靶向药物疗效的指标。
EGFR基因突变的位点及频率多种多样(如图2),研究发现只有携带EGFR特定
突变位点的患者,采用吉非替尼或埃罗替尼进行治疗才能显著延长其无进展生
存期。最常见的突变位点位于开放阅读框的19号外显子和21号外显子的
L858R位点,约占已知肺癌患者EGFR突变的85%。携带这些突变的患者对EGFR
抑制剂治疗非常敏感,可选用吉非替尼、埃罗替尼或阿法替尼(二代EGFR抑制
剂)进行治疗,疗效显著。此外18号外显子的G719和21号外显子的L861Q突
变对EGFR 抑制剂也有一定的敏感性,但20号外显子的插入突变患者(占4-10%)对EGFR 靶向治疗完全无响应,疗效很差,可能是因为这些插入突变并不能提高药物与靶标的亲和力。
图2 肺癌EGFR 突变模式 对于携带特定EGFR 突变的肺癌患者,吉非替尼等靶向药物无疑是他们的福音,遗憾的是治疗过程中患者总是不可避免的获得耐药性(产生耐药的中位时间一般为10-13个月)。耐药性产生的机制有很多:1)EGFR 的20号外显子二次突变T790M ;2)癌基因MET 或HER2扩增;3)KRAS 基因突变;4)酪氨酸受体激酶(AXL )和胞外信号调节激酶(ERK )的活化;5)转录因子NF-κB 或白细胞介素-6受体的活化激活了STAT3通路。其中最常见的是EGFR 的T790M
突变,约一半以上的肺癌患者耐药后都能检测到该突变。
临床为了抵制耐药性的产生,开发了第二代的EGFR 抑制剂阿法替尼,与吉非替尼不同的是阿法替尼属于不可逆抑制剂,可同时抑制EGFR 家族中2种以上的受体。临床验证实验发现该药对T790M 突变患者也有一定疗效。但阿法替尼的副作用更为严重,常伴随腹泻或皮疹等不良反应。另外一种潜在药物为依鲁替尼,是不可逆的BTK 抑制剂,也是FDA 批准作为套细胞淋巴瘤和慢性淋巴细胞白血病治疗药物。最近研究发现该药可诱导EGFR 突变的非小细胞肺癌细胞凋亡,包括携带T790M 突变的细胞,且该药可与其他靶向药物兼容治透
疗,因此对于T790M突变的肺癌患者,依鲁替尼也许能成为良好的辅助药
物,为T790M突变患者带来更好的治疗效果。
肺癌治疗之ALK、ROS1靶向治疗
间变性淋巴激瘤酶(ALK)基因重排是非小细胞肺癌(NSCLC)中另外一种疾病透
驱动因子,其中微管相关类蛋白4(EML4)基因与ALK的融合是最常见的重排
模式,在NSCLC患者中发生率约为4-5%,大部分患者有以下特征:年轻、女
性、无或仅有少量吸烟史。2007年Soda首次证实EML4-ALK是NSCLC的驱动基
因。
图3 ALK融合基因信号通路示意图
ROS1-RET融合基因是新发现的肺腺癌驱动基因,突变频率约为1%。该融合基因是一种独
立的肺腺癌分子亚型,很少与ALK-EML4融合基因同时出现在一个肿瘤患者中,可能因为
ROS1与ALK两者的蛋白序列一致性超过77%。
目前临床针对ALK和ROS1的靶向药物都是克里唑替尼,该药物也是Met基
因的抑制剂。研究发现60%以上ALK-EML4阳性的肺癌患者,采用克里唑替
尼进行治疗时可维持病情稳定,效果好的甚至可诱导肿瘤萎缩。这些阳性患者
的无进展生存期约为8-10个月(中位时间)。而传统的化疗方法的治疗灵敏透
度仅为20%,其无进展生存期也只有2-3个月。
此外,临床研究显示克里唑替尼在ROS1突变阳性的肺癌患者中疗效显著,
ROS1重排阳性的进展期NSCLC患者对克里唑替尼的治疗敏感度为72%,疗
效持续的中位时间为17.6个月,比ALk重排阳性的患者更长(8-10个月)。
NSCLC患者在采用克里唑替尼进行治疗的过程中同样会产生耐药性,这可能是
治疗过程中,肿瘤细胞异常激活了其他可选的旁支信号通路,如KIT扩增或者
EGFR活化等。患者体内可能同时存在多种耐药机制,这也就意味着联合的靶
向治疗可能成为战胜抗药性的重要方法。
基因检测找到受益群体才是靶向治疗的关键
虽然目前已经建立了相应的癌症基因组数据库(TCGA),临床也开发了系列相
关的靶向治疗药物(图4),但大多都是基于西方人群的研究,而基因突变在
不同人种间差异很大:欧美国家肺腺癌患者中EGFR突变率只有10-17%,但在
亚洲地区达到了30%-65%,因此亚洲人群对EGFR靶向治疗敏感度号。相反,
KRAS突变在白种肺腺癌患者中检出率为35%-50%,但在中国患者中低于5%。
图
4 肺癌相关的靶向治疗药物及其相应通路示意图
此外,不同的肺癌患者之间,由于抽烟状态、性别、生存的环境不同,所患疾病的组织类型存在差异,更重要的是他们的突变模式同样差异显著。因此在对肺癌患者进行靶向治疗之前,必须检测患者的基因突变模式,尤其是EGFR 、ALK 、ROS1、KRAS 等可能影响靶向药物疗效的基因突变,从而筛选出有效的受益人群,给与针对性的治疗,并在治疗过程中定期监测患者突变,关注耐药性产生时间,及时发现并调整治疗方案,为肺癌患者带来最大的生存希望。
透
图文为Tellgen原创,欢迎转载,转载请注明出处,谢谢!
参考文献:
透
1、Fang B, Mehran R J, Heymach J V, et al. Predictive biomarkers in precision medicine
and drug development against lung cancer[J]. Chinese journal of cancer, 2015, 34(1): 1-
15.
2、Richer A L, Friel J M, Carson V M, et al. Genomic profiling toward precision medicine
in non-small cell lung cancer: getting beyond eGFR[J]. Pharmacogenomics and
personalized medicine, 2015, 8: 63.
非小细胞肺癌治疗现状及进展 发表时间:2018-05-16T12:08:06.730Z 来源:《医师在线》2018年1月下第2期作者:武明君姚兵通讯作者[导读] 目前非小细胞肺癌的治疗以多学科综合治疗模式为最有效治疗方法。 (青海大学附属医院;青海西宁810000) 摘要:在我国恶性肿瘤发病率中肺癌处于第一位,其中以非小细胞肺癌为主要类型,约占80%以上,非小细胞肺癌的治疗方式越来越多样化,治疗方案从单纯外科治疗发展到以外科为主的多学科综合治疗时代。 关键字:非小细胞肺癌;治疗进展 随着我国经济的快速发展,导致环境污染加重,在我国肺癌的发病率正快速增长, 肺癌已成为我国恶性肿瘤死亡率的首位。其中,非小细胞肺癌(non-small cell lung cancer,NSCLC)是肺癌的主要类型,占80%以上,NSCLC起病隐匿,就医时多数已经处于中晚期,5年生存率低,其中高龄患者占多数,约50%肺癌患者年龄>65 岁[1]。随着诊疗技术的不断发展,非小细胞肺癌的治疗方式越来越多样化,治疗方案从单纯外科治疗发展到以外科为主的多学科综合治疗时代。 1.外科手术治疗 目前非小细胞肺癌的治疗以多学科综合治疗模式为最有效治疗方法,目前外科手术主要有以下几种方式:肺段切除术或楔形切除术、肺叶切除手术、袖式肺叶切除术、全肺切除术、扩大切除术、微创手术治疗。随着术前诊断技术的不断提高,特别是纵膈镜、PET-CT等应用于临床,对于非小细胞肺癌能够进行准确的分期,为临床治疗提供有效的治疗指导。目前对于非小细胞肺癌除Ⅲb、Ⅳ期外,应以外科手术治疗为主,只要患者身体素质良好,基本手术原则均应为解剖性肺叶切除+肺门纵膈淋巴结清扫术,也可在微创技术下行解剖性肺叶切除+淋巴结清扫术,Ⅲa期如肿瘤过大或侵犯周围重要器官可在行新辅助化疗后,根据化疗后复查结果考虑是否行肺癌根治术,Ⅳ期、Ⅲb期及部分Ⅲa不可手术者均应以化疗及放疗为主[2]。 2.常规化疗 非小细胞肺癌起病隐匿,发现时患者多数已处于晚期,很多病人因此错过手术最佳时期,化疗成为晚期肺癌重要治疗方式,其次ⅢA-ⅢB非小细胞肺癌,常因肿瘤体积或位置原因侵犯或包绕邻近组织或器官,导致常规手术很难将其彻底切除,使用化疗可降低TNM分期,提高手术疗效。对于不可手术的Ⅲb期及部分Ⅲa不可手术者,使用化疗可延长患者生存期,ECOG1549研究中对比了紫杉醇+顺铂,吉西他滨+ 顺铂,多西他赛+顺铂,紫杉醇+卡铂四种化疗方案在NSCLC 上的疗效。结果显示从缓解率(15%-21%),中位生存期(7.4-8.2个月)和1年生存率(31% -36%)来看,4组间无显著差异,因此对于晚期NSCLC,其中的任何一个方案均为同样可以接受的治疗选择,自此奠定了第三代化疗药物联合铂类在NSCLC化疗的一线治疗地位[3]。联合化疗与支持治疗相比,使用含铂类药物的联合化疗方案能显著控制肺癌临床进展,延长中位生存期,提高生活质量[4]。但由于联合化疗不良反应较大,恶心呕吐、脱发、免疫力降低等临床表现,对于高龄及有联合化疗禁忌证的患者应使用单药化疗,以减少化疗带来的副反应。另外长期应用铂类药物会产生耐药性,因此用非铂类化疗方案替代铂类,即可提高生存率而不会像铂类化疗影响生活质量的化疗药物,成为临床研究的热点。 3.分子靶向治疗 分子靶向治疗是近十年来NSCLC上取得最重要的突破。不同分子分型的明确以及更精确靶向药物的发展,使对不同驱动基因改变的靶向治疗更加精确和有效。分子靶向治疗是指利用肿瘤细胞与正常细胞之间分子,细胞生物学上的差异,针对细胞受体基因调控分子等信号传导为靶点的治疗具有靶向性的表皮生长因子受体阻断剂已进入临床应用通过促进细胞凋亡抗血管生成抗分化增殖等方面实现抗肿瘤作用分子靶向治疗比传统的化疗具有更高的选择性,不良反应小,是今后肿瘤治疗的趋势[5]。随着越来越多的治疗性分子靶点的发现和明确,通过特定分子分型改变的肿瘤类型可能相比传统的组织学分型更能精确的指导临床,将来基于驱动基因的改变也成为肿瘤的重要特征,基于分子靶向治疗的肿瘤分型将能够更有效的指导临床进行治疗选择。 4.放疗 近年来三维适型放疗及超分割放疗在临床广泛应用,放疗在早期非小细胞肺癌治疗中可以对肿瘤靶区高剂量照射,对局部晚期非小细胞肺癌的同步放疗化疗能明显提高局部控制率及生存率由于肺癌早期诊断相对困难,大部分患者就诊属于中晚期,手术不能根除瘤体较大的肿瘤,某些肿瘤已有远处转移,因此放疗对肺癌有重要价值放疗分为根治性放疗手术与放射综合治疗及腔内放疗,心肺功能不全以及其他不适合手术的患者,给予放疗常有较好的效果能手术切除的Ⅱ-Ⅲa期患者术前化疗可减小瘤体,提高手术切除率,术后化疗可防止肿瘤复发但目前高剂量放疗亦有较多的并发症,故应联合化疗放疗化疗同步进行疗效优于序贯及单一治疗,但因不良反应大,部分患者中断或延长放疗时间,影响了疗效考虑到患者耐受较差,目前国内各医疗机构仍多选用序贯或交替模式多项临床试验证实了放疗影响患者预后,但仍需进行前瞻性的随机对照试验确认[6]。 5.中医治疗 中医药在治疗NSCLC方面积累了较为宝贵的临床应用经验,如康莱特注射液、艾迪注射液等都取得比较好的疗效。肺癌患者术前、术后使用中药治疗,能够通过提高免疫系统功能、降低血液黏度、影响肿瘤细胞周期以及诱导肿瘤细胞凋亡的方式来抑制肺癌细胞生长,防止肺癌发生转移[7]。杨宏刚等[8]对57例NSCLC患者研究表明,采用手术化疗辅助益气扶正中药汤剂,可以减轻化疗不良反应,增强患者免疫功能,提高患者远期生存率。对于晚期肺癌患者,机体发生远处转移,自身免疫力降低,不能耐受手术及放化疗患者使用中医治疗可以改善患者症状提高生活质量延长生存期某些中药甚至可以使肿瘤缩小防止转移中医治疗可进一步提高其他方法的疗效,也可以改善手术及放疗化疗后的免疫功能低下状态非小细胞肺癌发病率高,因此中药与放疗化疗的综合治疗亦可以防止复发转移以及改善预后此外中医治疗肿瘤并发症也具有较好的作用,如对合并胸水肿瘤热咯血等的治疗中医既可作为综合治疗的手段之一,又可作为一种多因素结合基础上的组方治疗,具有多靶点全面兼顾和个体化治疗的优势。 6.免疫治疗 国际上已将免疫治疗同手术放疗化疗并列为四大治疗模式,细胞因子疗法单克隆抗体疗法肿瘤杀伤细胞的继承性免疫疗法及其抗癌多糖基因疗法已逐步发展,随着分子生物技术和免疫学的发展,免疫治疗将日趋成熟与完善,生物免疫治疗主要包括被动免疫治疗、主动免疫治疗和免疫检查点抑制剂这三类[9]。分子生物学指导下的精确治疗是目前肿瘤治疗发展的趋势。无论是传统的化疗,方兴未艾的分子靶向治疗还是新兴的生物免疫治疗,特定的药物基因组学、分子分型的的指导是不可或缺的。
Advances in Clinical Medicine 临床医学进展, 2018, 8(9), 837-843 Published Online November 2018 in Hans. https://www.doczj.com/doc/0614238863.html,/journal/acm https://https://www.doczj.com/doc/0614238863.html,/10.12677/acm.2018.89140 Present Situation and Progress of Lung Cancer Therapy Zhi Yang, Chunlong Lin Department of Respiratory, Yueyang Second People’s Hospital, University of South China, Yueyang Hunan Received: Oct. 20th, 2018; accepted: Nov. 6th, 2018; published: Nov. 13th, 2018 Abstract The lung cancer incidence is increasing year by year, and it is the most common malignant tumor in clinic. Treatment includes surgery, chemotherapy, radiotherapy, molecular targeted therapy, immunotherapy, and so on. Surgery, chemotherapy and radiotherapy are the main treatments for lung cancer. However, only 20% to 30% patients are clinically suitable for surgical treatment. The traditional chemotherapy regiment has limited efficacy. The 5-year survival rate is still less than 15%, and the side effects of radiotherapy are relatively large. At present, the new treatment me-thods, such as molecular targeted therapy, immunotherapy, iodine 125 seed stereotherapy and so on, have enriched the treatment of lung cancer. This article reviews the current treatment status and the latest development trend of lung cancer. Keywords Lung Cancer, Small Cell Lung Cancer, Non-Small Cell Lung Cancer, Treatment 肺癌治疗的现状与进展 杨志,林春龙 南华大学岳阳市二人民医院呼吸内科,湖南岳阳 收稿日期:2018年10月20日;录用日期:2018年11月6日;发布日期:2018年11月13日 摘要 肺癌发病率成逐年递增趋势,是临床最常见的恶性肿瘤,治疗方法包括手术、化疗、放疗、分子靶向治疗、免疫治疗等。手术、化疗、放疗是肺癌主要治疗手段,但是临床适宜手术治疗的病人只有20%~30%,
中国肺癌杂志2014年3月第17卷第3期 Chin J Lung Cancer, March 2014, Vol.17, No.3 ·综述· 非小细胞肺癌免疫治疗进展 何圆 尤长宣 【摘要】 肺癌是全球范围内癌性死亡的首要因素,发病率、死亡率高,预后较差,急需开发一种新的高效低毒疗法。作为术后辅助或是姑息治疗手段,免疫治疗为非小细胞肺癌患者提供了一个新的治疗方向。免疫疗法作用机理各不相同,如免疫检测点受体抑制剂(抗CTLA4抗体、抗PD-1抗体、抗PD-L1抗体)、主动性免疫疫苗(L-BLP25脂质体疫苗、Belagenpumatucel-L 疫苗、MAGE-A3蛋白疫苗)、过继性免疫疫苗(CIK 细胞)等,研究表明免疫治疗非小细胞肺癌肿瘤缓解率较前提高,前景值得期待,II 期/III 期临床试验亦在进一步探索其临床应用价值。本文就当前非小细胞肺癌免疫疗法原理、临床试验、不良反应及待解决问题作一概述。 【关键词】 肺肿瘤;免疫治疗;进展 Advances in Immunotherapies for Non-small Cell Lung Cancer Yuan HE 1 , Changxuan YOU 2 1 Graduate Student of Southern Medical University, Guangzhou 510515, China; 2Department of Oncology, Nanfang Hospital, Southern Medical University, Guangzhou 510515, China Corresponding author: Changxuan YOU, E-mail: ycx6026@https://www.doczj.com/doc/0614238863.html, 【Abstract 】 Globally, Lung cancer is the leading cause of cancer-related death of high morbidity and mortality with poor prognosis, which needs some more effective and less toxic therapies. The immunotherapies offer a novel approach for the treatment of patients with non-small cell lung cancer (NSCLC) in both the adjuvant and palliative disease settings. A number of promising immunotherapies based on different mechanism have now been evaluated showing an increasing response rate. Moreover, further phase II/III clinical trials will be indicated to explore its value. These include checkpoint inhibitors (anti-CT-LA4 antibody, anti-PD-1 antibody, anti-PD-L1 antibody), active vaccination (L-BLP25 liposome vaccine, Belagenpumatucel-L vaccine, MAGE-A3 protein vaccine) and adoptive vaccination (CIK cells). The purpose of this paper will draw a summary on the theory, clinical trials, toxicity and problems to be solved of the immunotherapies in NSCLC. 【Key words 】 Lung neoplasms; Immunotherapies; Progress This study was supported by the grants from National Natural Science Foundation of China (No.81071847), Guangdong Natural Science Foundation (No.S2011010003881), Guangdong Provincial Science and Technology Project (No.2012B031800394), Wu Jieping Medical Foundation Funded Special Clinical Research Projects (No.320.6799.1118)(all to Changxuan YOU). DOI: 10.3779/j.issn.1009-3419.2014.03.17 本研究受国家自然科学基金项目(N o.81071847)、广东省自然科学基金项目(No.S 2011010003881)、广东省科技项目(No.2012B031800394)和吴阶平医学基金会临床科研专项资助项目(No.320.6799.1118)资助 作者单位:510515 广州,南方医科大学2013级研究生(何圆);510515 广州,南方医科大学南方医院肿瘤科(尤长宣)(通讯作者:尤长宣,E-mail: ycx6026@https://www.doczj.com/doc/0614238863.html, ) 肺癌是全球范围内首个癌症相关性死亡因素,非小细胞肺癌(non-small cell lung cancer, NSCLC )约占肺癌总数80%-85%,吸烟、环境污染(厨房油烟、煤炭燃烧、汽车尾气)等构成肺癌发病的主要原因。早期接受治疗NSCLC 患者超过40%会出现肿瘤复发,因此晚期 NSCLC 患者5年生存率不到15%,预后较差[1]。以铂类为基础的标准化疗方案治疗NSCLC ,患者肿瘤缓解率仅为20%-35% ,中位生存期(median overall survival, mOS )为10个月-12个月,分子靶向治疗与化疗方案相比,可延长NSCLC 患者无疾病生存期(progression-free survival, PFS ),但患者mOS 未获益[2]。因此标准治疗或因严重不良反应(恶心、呕吐、骨髓毒性等)或因经济学毒性(分子靶向药物价格较昂贵)已使其处于治疗瓶颈水平,急需开发一种新的NSCLC 疗法。目前免疫治疗NSCLC 在I 期/II 期临床试验中结果良好:肿瘤缓解率提高、毒副作用小、患者易耐受,这将为NSCLC 治疗开发新领域。
肺癌外科治疗现状和进展 首都医科大学肺癌诊疗中心 首都医科大学附属北京朝阳医院胸外科 李辉 一、外科方法在肺癌分期中的现状和地位 肺癌分期治疗目前已成为共识,准确的分期对治疗方案的正确制订十分重要。现行的肺癌分期主要包括临床分期(cTNM,cStage) 、病理分期(p TNM,pStage) 和再治疗分期(rTNM,rStage) ,此外尚有不成熟的分子分期( mTNM,mStage) 。临床分期的准确率有限,与外科病理分期相比仍然存在相当误差。纵隔镜、胸腔镜等外科方法可明显提升肺癌分期的准确率,是目前肺癌最准确的分期方法。 常用的非外科术前分期法包括X线胸片、胸部CT、磁共振显像、单光子发射型计算机断层扫描(SPECT)和正电子发射断层扫描(PET)等,但这些方法各有优缺点,而且敏感性、特异性和准确性均有不足。 外科分期( sTNM) 包括手术前分期(纵隔镜检查术、胸腔镜术等) 和术中分期(术中纵隔淋巴结清扫) 。为了进一步提高分期的准确性,达到病理分期水平,外科分期手段正倍受重视并逐渐推广应用。 纵隔镜检查术是评估肺癌手术前纵隔淋巴结状况最准确的手段,敏感性、特异性高达90 %和100 % ,特别是在N2 、N3 的排除上非常有意义。纵隔镜检查术对提升肺癌术前分期水平有重大意义,某些发达国家已将之作为肺癌治疗前的常规检查和分期金标准。国内该工作虽然起步不晚,但目前的状况依然是认识不足、发展不均、普及不力。纵隔镜检查术相关的并发症如出血、气胸、纵隔炎、喉返神经损伤、颈切口感染的发生率< 3 % ,严重并发症如大血管损伤、食管撕裂、气管撕裂的发生率0. 2 %~0. 5 % ,死亡率几乎为零,属于相当安全、成熟的手术。 胸腔镜对纵隔肿物活检的准确率为91.9 %。对临床N0 和N1患者,胸腔镜的假阴性率高达25 % ,应用意义不大,而对临床N2 患者,胸腔镜的诊断准确率为63% ,胸腔镜的相关并发症发生率为8.57%。另外,胸腔镜必须双腔气管插管及单肺通气,
肺癌射频消融治疗现状与进展 在我国,肺癌占全部恶性肿瘤死亡的22.7%,是恶性肿瘤死亡的首位原因。而该病主要在中老年患者中发病,这些人往往存在合并症,不适合常规开胸手术,于是许多新的治疗方法应运而生,包括微创外科、CT引导下射频消融(radiofrequency ablation,RFA)和立体定向放射治疗等。从目前研究的结果看,肺叶切除仍然是早期肺癌的标准治疗方法。但是对妥协性患者(compromised patients)可以行电视胸腔镜下的局限性切除术(包括肺段切除和楔形切除),而对高风险不能耐受微创手术的患者,RFA和立体定向放射治疗是很好的选择,二者究竟孰优孰劣,还需要进行前瞻性研究。RFA作为一种局部微创治疗手段,已显示出良好的疗效和安全性,日益受到重视。在2009年第45届美国临床肿瘤协会年会,美国临床肿瘤学会(ASCO)及第13届世界肺癌大会(WCLC)上,来自美国、欧洲、日本及中国的肺癌研究者分别报告了RFA治疗不能手术切除的早期肺癌临床疗效,结果令人鼓舞。 一、RFA的原理 RFA是对靶肿瘤施以频率460~500 kHz的射频电流,使肿瘤组织内的极性分子处于一种激励状态,发生高速震荡摩擦产热,局部温度可达60 ℃~120 ℃。肿瘤组织对热的耐受能力较正常组织差,当组织温度高于50 ℃时,即出现凝固性坏死,温度高于60 ℃时,组织细胞内线粒体、溶酶体、蛋白质和DNA出现不可逆的变性,最终凝固和坏死,同时使肿瘤周围的血管组织凝固形成一个反应带,使之不能继续向肿瘤供血,并有利于防止肿瘤转移。另外,射频的热效应可增强机体的免疫力,从而抑制肿瘤生长。 由于肺部正常组织可通过肺部大血管的血液循环和呼气散热,并且起着绝缘的效果,使能量可以充分集中在病变部位,加之肺部肿瘤组织的血流量低,散热困难,热量积聚,温度升高快,成为一个巨大的储热库,因此肺肿瘤非常适合RFA治疗,为心肺功能差,不能耐受手术的早期肺癌患者提供了一种新的治疗方法。 二、RFA治疗肺癌的基础研究 1979年Sugaar等对肺部恶性肿瘤进行RFA治疗,发现加热不仅使肿瘤细胞发生变性坏死,还可使肿瘤的血管通透性增强、血细胞渗出,进一步导致血管壁坏死、管腔闭塞;坏死的肿瘤细胞刺激淋巴细胞聚集,增强机体免疫系统活性,进一步杀伤机体残存瘤细胞。Goldberg 等于1995年和1996年在兔肺上进行了RFA的实验研究,结果发现RFA治疗后发生热凝固性坏死,周围组织逐渐出现炎症反应、水肿、出血;7 d后坏死灶出现纤维组织增生;1个月支气管上皮和肺泡上皮增生,肺泡开始重建;2~3个月增生纤维组织逐渐被吸收,恢复正常组织结构。Miao等对兔的VX2肺癌模型进行RFA治疗,结果显示:3个月后对照组所有动
肺癌的诊断和治疗近况 肺癌是最常见的恶性肿瘤之一,在男性恶性肿瘤中居首位。发病率连续上升,特别在大城市情况更为明显,其病死率在城市人口恶性肿瘤死亡中居首位。但肺癌的诊断和治疗还存在很多问题,十多年前的资料显示,明确肺癌的患者70%~80%为晚期,早期肺癌的诊断率为10%;肺癌总的5年生存率为10%~13%,但T1N0期的5年生存率可高达80%。近年来,肺癌的诊断和治疗取得了不少进展。在美国,据最新的资料显示,肺癌的发病率及死亡率已出现下降的趋势。(一)诊断方面 (1)痰 常规涂片、染色找癌细胞阳性率很低。近年来,为提高其敏感性,对痰细胞学检查引入了分子生物学方法,并使人们重新认识痰细胞学检查在早期诊断的重要作用。 A.痰标本的免疫染色:应用单克隆抗体检测痰标本,可使检测阳性率明显提高,但特异性为70%~88%左右。 B.痰标本中肺癌相关基因的检测:应用PCR的方法对痰中脱落细胞进行肺癌相关基因的检测,可检测出P53突变、K-ras突变 等。从而提供了一种从痰发现肿瘤细胞的方法。 (2)支气管肺泡灌洗液(BALF) 支气管肺泡灌洗液中有肺泡巨噬细胞、淋巴细胞及正常或异常的上皮细胞。利用分子生物学的方法检测BALF中基因的改变,从而更早的发现肺癌。 (3)外周血 外周血中存在多种可溶性的肿瘤特异性标志物,传统的免疫细胞化学方法是用单克隆抗体去检测肿瘤患者外周血中的特异性抗原,特异性较低。目前已经能够用分子生物学的方法来检测外周血中肿瘤细胞的异常DNA,或直接检测外周血中的肿瘤细胞。 A. 癌标志物:迄今尚无任何一种可靠的血清癌标志物用于诊断或普查 肺癌。目前已用于临床测定的如组织多肽抗原(TPA)、癌胚抗原(CEA)、鳞癌抗原(Scc-Ag)、CYFRA21—1等对NSCLC的诊断有一定意义。神经特异性烯醇酶(NSE)、蛙皮素(bombesin)、肌酸磷酸激酶同工酶BB(CPK—BB)、胃
2020CSCO小细胞肺癌和非小细胞肺癌抗血管治疗研 究进展汇总 基于肿瘤形成的“土壤环境”理论,抗血管治疗一直是临床肿瘤治疗的重要药物类型。此次CSCO的抗血管专场,来自全国各地的多位专家,分别就肿瘤抗血管治疗的各个议题进行专题讲解。于此,为读者朋友汇总来自范云教授的《小细胞肺癌的抗血管治疗》和来自褚天晴教授的《非小细胞肺癌抗血管生成药物治疗专家共识》。纵览临床抗血管治疗的研究发展。助力患者朋友学会应用抗血管治疗。 小细胞肺癌的抗血管治疗 小细胞肺癌的靶向治疗上,因为均为失败的研究结果,在这里不为读者赘述。我们详解一下抗血管治疗部分的成绩。 1.贝伐单抗:与化疗联合,可提升PFS,OS无改善,失败为主。 提起抗血管药物,早年主要以贝伐单抗的研究为主,多通过与EP/IP化疗的联合,多药一线或二线治疗广泛期小细胞肺癌患者,结果显示,患者的PFS是有提升的,但是最终的OS分析没有显著统计学差异。因此,目前贝伐单抗在小细胞肺癌的应用没有积极推荐。
2.国产抗血管小分子:安罗替尼/阿帕替尼后线单挑小细胞肺癌获佳绩,跻身治疗框架内! 后续随着国产抗血管小分子药物阿帕替尼/安罗替尼的出现,以及治疗方案的设计,逐渐出现了阳性的研究结果。如安罗替尼≥3线治疗广泛期小细胞肺癌患者,获得了7.3:4.9月的PFS延长,HR=0.53,下降了47%的死亡风险!安罗替尼后线治疗小细胞肺癌的适应症也获得国家NMPA 的批准,激起了国内对于抗血管小分子药物在肺癌应用的全方位拓展。 由范云教授领衔开展的呃一项阿帕替尼3线/4线治疗晚期SCLC的II期研究中,有效率为17.5%,疾病控制率为75%,OS 5.8月。也获得了不错的临床疗效。 3.免疫+抗血管联合二线初尝试创佳绩,获国际认可!
非小细胞肺癌脑转移的治疗 肺癌是发病率及死亡率很高的恶性肿瘤,主要原因为早期诊断难度较大,确诊时多为中晚期并已经发生远处转移,错过了最佳手术时机,而且经治疗后易局部复发。非小细胞肺癌(NSCLC)多发生远处转移,脑为常见部位之一,5%-10%的NSCLC患者可出现脑转移,并且20%的肺癌患者在首次确诊时已出现脑转移。肺癌患者发生脑转移多伴有严重的神经系统功能改变、生存期短、生活质量差、预后不良,中位生存期(MST)为3-12个月。肺癌患者入院后行全面系统的检查既提高脑转移临床检出率,还可以尽早的选择合适的临床治疗方法。目前治疗肺癌脑转移的方法有外科手术、化疗、放疗、靶向及免疫治疗等,本文将一一讲述非肺癌脑转移治疗的新进展。
转移部位: 脑转移分为脑实质转移和脑膜转移。实质转移最常见部位为大脑半球,随后依次为小脑、脑干。脑膜转移少见,预后更差。肺癌脑转移发生率较其他恶性肿瘤高,约20-65%的患者会在病程中出现。SEER数据称,非转移性腺癌、鳞癌、大细胞癌脑转移发生风险分别为11%、6%、12%。小细胞肺癌首诊时发病率即为10%,存活2年以上患者发生率达60-80%。 临床症状: 非小细胞肺癌脑转移患者临床表现主要为头痛、呕吐、视神经乳头水肿三大主征;还可出现复视、黑朦、视力减退、头晕、淡漠、意识障碍、二便失禁、脉搏徐缓、血压增高等。精神症状(性情改变、反应迟钝、痴呆等)常见于额叶转移;癫痫多见于额叶,其次为颞叶、顶叶;感觉障碍多见于顶叶肿瘤;运动障碍表现为肿瘤对侧肢体肌力减弱或完全瘫痪;失语症多见于优势大脑半球语言中枢转移瘤;视野损害多见于枕叶、顶叶、额叶深部;丘脑转移可产生丘脑综合征(对侧感觉缺失和/或刺激症状、对侧不自主运动);小脑半球肿瘤易出现爆破性语言、眼球震颤、患侧肢体协调动作障碍、同侧肌张力减低、腱反射迟钝、易向患侧跌倒;小脑蚓部肿瘤易引发步态不稳、行走困难、站立后向后倾倒;第四脑室可早期出现积水、颅内压增高。脑干转移出现交叉性瘫痪(病灶侧脑神经周围型瘫痪、对侧肢体中枢性瘫痪伴感觉障碍),根据受损脑神经可定位转移瘤位置:第Ⅲ对位于中脑;ⅤⅥⅦⅧ对位于脑桥;ⅨⅩⅪⅫ对位于延髓。
中医治疗肺癌的研究进展 肺癌是我国常见的恶性肿瘤之一,是目前发病率和死亡率两个“第一”的恶性肿瘤,严重威胁着人类的健康和生命。据世界卫生组织(WHO)统计,每年全世界估计有超过120万新肺癌患者,死亡约110万人。近二十年我国的肺癌发病率以每年11%的速度递增,预计到2025年,我国将成为世界第一肺癌大国,每年将有90万人死于肺癌。肺癌生物学特性十分复杂,恶性程度高,由于肺癌早期诊断困难,就诊时70%-80%已属晚期,因此肺癌的预后极差,86%的患者在确诊后5年内死亡。只有15%的患者在确诊时病变局限,其5年生存率可达到50%。目前手术、放疗和化疗仍是治疗肺癌的主要方法。但是放、化疗药物多耐药现象及其严重的毒副作用,也妨碍了肺癌治疗的发展,对晚期肺癌的疗效和生存质量,放化疗的毒性和敏感作用等方面存在不可克服的自身缺陷。因此中医药在综合治疗中起着不可忽视的作用,中医药治疗肿瘤已有数千年的历史,形成了一套独特的理论体系,主张治病求本、整体调理、多方入手及全身治疗。多成分、多靶点、多途径是中医药治疗肿瘤的特点,既注重攻邪消瘤,更重视患者整体状况的改善,治病以人为本,强调“治病留人”,重视患者生存质量的提高,实现“带瘤生存”的状况。多年来的临床实践表明,中西医结合可治疗肺癌术后并发症,减少术后复发和转移,减轻放化疗的不良反应,提高了疗效,延长了生存期,改善了肿瘤患者的生存质量。 1中医对于肺癌的认识 肺癌在传统医学中称谓不一,在中国传统医学中,属“息贲”、“肺痈”、“肺瘘”、“虚损”等范畴,早在距今约3500多年的殷商时期,古人对于肿瘤就有发现,殷墟甲骨文上已经记载有“瘤”的病名,这是现今中医记载肿瘤最早的文献。此后,经过几千年的不断继承和发展,中医对肿瘤的认识日渐完善。祖国中医学的经典著作《内经》、《难经》、《神农本草经》、《伤寒杂病论》以及历代各家学说和临床治疗经验奠定了坚实的理论和临床基础,与近代科学发展成果和中西医学渗透交融,形成了目前中医药抗癌研究的繁荣局面。 1.1中医古籍对肺癌病名的描述 肺癌是发生于支气管上皮、支气管粘液腺、细支气管上皮以及肺泡上皮等肺部的恶性上皮性肿瘤。肺癌为有形之块,中医以“积”、“瘕”名之,相当于中医古籍中“肺积”、“息贲”、“肺痈”、“劳嗽”等疾病的范畴。 《难经·五十六难》说:“肺之积,名曰息贲,在右胁下,覆大如杯,久不已,令人洒淅寒热,喘咳,发肺痈”。宋《寄生方》曰:“息贲之状,在右胁下,覆大如杯,喘息奔溢是为肺积,诊其脉浮而毛,其色白,其病气逆,背痛少气,喜忘目瞑,肤寒,皮中时痛,或如虱啄,或如针刺”。以上所述与肺癌淋巴管转移而引起的腋下及锁骨上淋巴结肿大的体征颇为相似而息贲的症候“令人洒淅寒热,喘咳,发肺痈”与肺癌产生的咳嗽、气急、发热等症相似。这里虽未述及有痰血,但“发肺痈”一句包含了痰血的症状,因此肺之积的息贲,类似现在晚期肺癌的症象。 对于肺癌的发病与预后,《杂病源流犀烛》所提到的“邪积胸中,阻塞气道,气不得通,为痰,……为血,皆邪正相搏,邪气胜,正不得制之,遂结成形而有块”,说明了肺中积块的产生与正虚邪侵,气机不通,痰血搏结有关,对于后世研究肺癌的发病与治疗,具有重要的启迪意义。申斗垣“癌发”指出:“四十岁以上,血亏气衰,厚味过多所生,十全一二”。《外科证治》强调:“诸患易逝,独肺中患毒难觉……,及咳嗽口干咽燥,此皆肺中生毒之证也”。 对于肺癌常见的临床表现咳嗽、咳血胸痛、短气、痰饮也有有关论述《素问·咳论》说:“肺咳之状,咳而喘,吸有音,甚则唾血”。《内经》所载:“咳嗽脱形,脉小数疾,大肉枯稿,……胸中气满,喘息不便”,与肺癌晚期出现恶病质时临床表现相似。《脉要精微论》说:“肺脉搏坚而长,当病唾血”。金元时期李东垣治疗肺积所用的息贲丸,所治之症颇似肺癌症状。《景岳全书》指出:“劳嗽声哑,声不出或喘息气促者,引肺脏败也,必死”,这与晚期肺癌的临床表现相同,并明确指出预后不良。《金匮要略》所论:“饮后水流于胁下,咳唾引痛,谓之悬饮;咳逆倚息,短气不得卧,其形如肿,谓之支饮”,被认为包括了“胸腔积液”,其所谈治则方剂,为后世所推崇。 1.2肺癌的中医病因病机 肺主气,司呼吸,主宣发肃降,主通调水道。《活人机要》云:“状人无积,虚人则有之”。《医宗必读》曰:“积之成也,正气不足,而后邪气踞之”。若正气内虚或者享赋不足,则肺
晚期非小细胞肺癌的维持治疗 晚期非小细胞肺癌(NSCLC)在经过初始治疗病情控制后,为稳定病情在耐药产生前采用具有良好耐受性的化疗药物或靶向药物或中医药维持治疗,这一模式已被大多数患者接受。化疗药物及靶向药物维持治疗尚有较多争议,中医药维持治疗已显示较多优势。 标签:晚期非小细胞肺癌;维持治疗;中医药治疗 肺癌是全球范围内发病率和死亡率最高的恶性肿瘤,在我国无论城市或是乡村,男性或是女性,死亡率最高的恶性肿瘤都是肺癌,80%以上的肺癌是非小细胞肺癌,70%的肺癌患者在诊断时已经为晚期或局部晚期[1]。晚期NSCLC患者往往伴有广泛的脏器转移,对于行为状态评分(PS)为0,1和2的患者,采用含铂双联方案化疗4~6周期,有效率为20%~40%,但大部分患者会在3~4个月病情出现进展,所以近年来随着现代医学对肿瘤治疗的认识和理念的更新,提出了肿瘤维持治疗这一概念。 1晚期NSCLC维持治疗现状 1.1晚期NSCLC的化疗维持治疗目前晚期非小细胞肺癌治疗NCCN指南推荐一线标准化疗方案为含铂双联方案,如吉西他滨+顺铂,紫杉醇+顺铂(卡铂),多西他赛+卡铂,培美曲赛+顺铂,完成4~6周期后,当病情达到完全缓解、部分缓解或稳定,采用其中一种非铂类药物维持治疗,目前常用吉西他滨1000mg/m2第1,8每3w重复,多西他赛35mg/m2,第1,8,15每4w重复,有研究证实此二药在维持化疗中可见患者无疾病进展生存(PFS)延长的生存益处。培美曲赛600mg/m2,第1d,每3d重复,此药已经被美国FDA批准用于用于标准一线治疗后无进展晚期非肺鳞癌患者的维持治疗[2]。此三药静点时间短,不良反应轻,耐受性良好。 1.2晚期NSCLC的靶向维持治疗分子靶向治疗是利用肿瘤细胞与正常细胞之间的分子生物学差异,通过封闭受体,抑制血管生成,阻断信号传导等机制作用于肿瘤细胞特定的靶点,进而抑制肿瘤生长及转移。以表皮生长因子受体(EGFR)为靶点的抗肿瘤靶向药物主要有酪氨酸激酶抑制剂(EGFR-TKI),吉非替尼和厄洛替尼,其对于EGFR突变NSCLC的疗效已被认可,对于EGFR野生型其作用仍有争议。埃可替尼是我国资质研制的EGRF-TKI类药物,二、三线治疗NSCLC有效且安全,对于既往化疗失败的晚期NSCLC具有较优的疗效和安全性。贝伐单抗是针对肿瘤血管内皮生长因子(VEGF)的靶向药物,其在晚期NSCLC的维持治疗中在PFS的延长上也获得了阳性结果[3]。 1.3晚期NSCLC化疗及靶向维持治疗存在的争议虽然晚期NSCLC维持治疗取得了一定的进展,但目前尚无相关的研究提供循证医学证据,维持治疗是在保证较好的生活质量,在可耐受的不良反应范围内进行的治疗,但化疗药物具有毒性积累的副作用,多次维持化疗很可能会造成患者的生活质量下降,免疫功能
小细胞肺癌最前沿治疗综述 一、小细胞肺癌总论 小细胞肺癌(SCLC)约占所有新发病肺癌总数的15%~20%。美国监测、流行病、最终结果(SEER)数据库的流行病学调查显示,在过去的30年中,SCLC的年发病率呈下降趋势。中国SCLC发病率虽然 没有经过系统的调查,但总体上没有明显下降趋势,并存在着治疗不规范、重视程度不够的问题,与非小细胞肺癌(NSCLC)相比基础 和临床研究较少,缺少循证医学证据。 与其他恶性肿瘤相似,SCLC的治疗也秉承分期治疗的原则,手术仅适用于早期患者,能实施手术的患者仅占全部患者的5%。因此,化疗、放疗仍是SCLC治疗的主要策略。近年来胸部放疗使局限期SCLC 患者的3年生存率大约提高了5%,使胸部复发风险降低约25%,而预防性全脑照射(PCI)治疗也进一步改善了SCLC的临床预后。 在20世纪60年代前,SCLC的治疗以手术为主,但远期疗效欠佳。此后两项随机临床试验的结果否定了手术治疗的地位,化放疗成为SCLC的主要治疗手段。近年来,多项研究显示,包括外科治疗的多学科综合治疗可改善患者生存。目前的共识是,对确定为临床I期(TN)的SCLC患者可行外科切除术治疗,但术前需要进行纵膈01-2分期。 目前,前瞻性临床研究的方向主要围绕Ⅱ~Ⅲ期SCLC患者接受手术治疗能否获益,以及新辅助治疗和辅助治疗孰优孰劣等。 胸部放疗既往局限期SCLC单独行化学治疗的胸部复发率高达 1
75%~90%,上世纪90年代的两项荟萃分析结果显示,在化疗中加入胸部放疗能够延长局限期SCLC患者的生存期。目前化疗联合胸部放疗已成为局限期SCLC的标准治疗。 目前认为,联合胸部放疗的化疗方案以依托泊苷联合顺铂(EP)方案最具生存获益优势。2002年有随机Ⅲ期临床试验直接对比了EP与环磷酰胺联合表柔比星、长春新碱(CEV)方案的疗效,入组患者中有214例局限期SCLC患者,结果显示EP方案联合胸部放疗的生存获益优于CEV方案。 随着化疗药物研究的不断深入,伊立替康联合顺铂(IP)方案已被美国国立综合癌症网络(NCCN)采纳为广泛期SCLC的一线方案。对于IP方案是否也能够与放疗联合用于局限期SCLC的治疗,有多项研究初步证实其具有较好的耐受性及疗效。日本西部胸部肿瘤协作组的一项Ⅱ期临床研究显示,EP方案联合同步胸部放疗序贯IP方案巩固化疗是局限期SCLC患者的可选治疗方案,但仍需Ⅲ期研究进一步证实。2010年美国临床肿瘤学会(ASCO)年会的一项回顾性研究显示,IP序贯IP联合放疗治疗局限期SCLC,与EP联合放疗相比有更好的中位生存期(MST)和2年生存率,且毒性可耐受。虽然该研究仅为回顾性研究,病例数较少,尚需头对头前瞻性随机临床试验来验证,但为我们未来的研究方向带来启示。 据统计,广泛期SCLC胸部复发率超过50%。既往单中心临床试验显示,对于化疗后达到胸外病灶完全缓解及胸部病灶至少部分缓解的患
2020NCCN非小细胞肺癌指南要点 2020年6月,美国国家综合癌症网络(NCCN)发布了非小细胞肺癌(NSCLC)指南2020年第6版。那么,新版指南中NSCLC精准治疗的药物选择有哪些?NSCLC治疗的进展情况如何?接下来,让我们盘点部分亮点研究,一探究竟。 以下是NCCN指南《2020.V6版》更新的要点(相较于V5版): 靶向治疗 (一)指南建议检测的靶点1:EGFR、ALK、ROS1、BRAF、NTRK、MET、RET
1、EGFR基因突变: 首选方案:奥希替尼(1类);其他方案:厄洛替尼(1类)或阿法替尼(1类)或吉非替尼(1类)或达克替尼(1类)或厄洛替尼+雷莫芦单抗;一定条件下可用方案:厄洛替尼+贝伐珠单抗(2B类)。 2、ALK基因突变: 首选方案:阿来替尼(1类);其他方案:布加替尼(1类)或色瑞替尼(1类);一定条件下可用方案:克唑替尼(1类)。 3、ROS1基因重排: 首选方案:克唑替尼或恩曲替尼;其他方案:色瑞替尼; 4、BRAF V600E 突变:
首选方案:达拉菲尼+曲美替尼;其他方案:维莫非尼或达拉菲尼;一定条件下可用方案:初始的全身治疗方案。 5、NTRK 基因融合阳性: 首选方案:拉罗替尼或恩曲替尼;一定条件下可用方案:初始的全身治疗方案。 6、MET外显子14跳跃突变: 首选方案:卡马替尼;一定条件下可用方案:克唑替尼或初始的全身治疗方案。 7. RET重排: 首选方案:Selpercatinib;一定条件下可用方案:卡博替尼或凡德他尼(2B类)。 (二)2020年ASCO靶向新进展: 在今年的ASCO会议上,多项EGFR敏感突变相关研究数据公布。其中,III期NEJ02研究旨在评估贝伐珠单抗联合厄洛替尼用于EGFR敏感NSCLC患者的疗效,结果显示2,贝伐珠单抗联合厄洛替尼可明显改善PFS。在真实世界研究中发现3,VEGF抑制剂联合厄洛替尼对比单药厄洛替尼,PFS和DOR明显改善。目前,奥希替尼已获批用于
中国Ⅲ期非小细胞肺癌诊疗专家共识 Ⅲ期NSCLC的分类和定义 III期NSCLC分期复杂,针对不同分期治疗模式不尽相同。共识根据世界肺癌研究会TNM分期第8版将III期NSCLC分为ⅢA、ⅢB 和ⅢC期,根据肿瘤是否具有手术切除的可能性,Ⅲ期NSCLC可分为可切除、不可切除和潜在可切除3类。 ●可手术切除:包括ⅢA N0~1、部分单站纵隔淋巴结转移且淋巴结短径<2cm 的N2和部分T4(相同肺叶内存在卫星结节)N1 ●不可手术切除:包括部分ⅢA、ⅢB 和全部ⅢC期,通常包括单站N2纵隔淋巴结短径≥3cm或多站以及多站淋巴结融合成团(CT上淋巴结短径≥2cm)的N2患者,侵犯食管、心脏、主动脉、肺静脉的T4和全部N3患者 ●潜在可切除:包括部分ⅢA和ⅢB期,包括单站N2纵隔淋巴结短径<3cm 的ⅢA期NSCLC、潜在可切除的肺上沟瘤和潜在可切除的T3或T4中央型肿瘤 多学科治疗(MDT)策略 共识提倡采取积极的综合治疗手段,融入多个学科,提供更多高级别的循证证据。 ●建议开展多学科诊疗模式,进行有针对性的个体化治疗
●患者的治疗策略应由胸外科、肿瘤放疗科、肿瘤内科、呼吸内科、病理科和影像科等多学科医师组成的专家团队讨论决定。 诊断分期与治疗前评估 共识强调了进行临床诊断分期的重要性,明确了检查的手段及最佳时间,并提倡针对患者的个体化进行治疗前评估,从而有利于制定适合患者个体的治疗方案。 ●临床分期应通过影像学检查、气管镜、纵隔镜、经支气管超声引导针吸活检、超声内镜等检查手段进行综合评估(共识度:95%) ●患者在开始治疗前4周内进行诊断分期;在初始诊断分期时,均应接受脑MRI检查,排除颅内转移灶;对于有MRI检查禁忌证或不可用时,推荐使用增强脑CT作为替代方法(共识度:100%) ●推荐在制定治疗方案时,应充分评估患者合并疾病,在得到有效治疗后再进行肺癌治疗;体力评分状态(PS)影响患者预后和治疗方案的选择。(共识度:100%) 治疗方案 根据肿瘤是否可手术切除,共识针对III期NSCLC患者明确了不同情况下的最佳治疗方案,可参考下方IIIA,IIIB和IIIC期NSCLC患者诊疗路径:
2015年非小细胞肺癌小分子靶向药物耐药处理共识 小分子靶向药物是肺癌治疗史上的里程碑事件,但其无可避免的原发性和继发性耐药现象,成为进一步提高靶向药物疗效的瓶颈。2013 年3 月8~9 日,中国抗癌协会肺癌专业委员 会和中国抗癌协会临床肿瘤学专业委员会(Chinese Society of Clinical Oncology,CSCO)联合主办了第十届“中国肺癌高峰共识会”,最终形成了非小细胞肺癌(non-small cell lung cancer,NSCLC)小分子靶向药物耐药处理共识[1]。近两年新的研究不断出现,对这一共识有了新的更新 共识一:EGFR 突变型肺癌,建议检测BIM 治疗前应检测EGFR 突变型肺癌的BIM 以判断是否出现原发性耐药。BIM 是BCL-2 蛋白 家族成员,是活性最强的促凋亡蛋白之一。表皮生长因子受体(epidermal growth factor receptor,EGFR)酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)通过BIM 上调引 起带有EGFR 突变的肺癌细胞的凋亡. 其中编码的BH3(the pro.apoptotic BCL-2 homology domain 3)被称为唯一的促凋亡蛋白。东亚人群中BIM 基因的2 号内含子存在 缺失多态性。导致这一人群表达的是缺乏促凋亡活性的BIM 亚型(BH3 缺失),从而引起对EGFR TKI 的原发耐药或削弱TKI 的临床疗效。上海市肺科医院研究发现,12.8% (45/352)的患者缺乏BIM 的多态性,并且其对EGFR 的ORR 为25%,PFS 4.7m,多 因素分析显示,BIM 多态性的缺失是EGFR 突变者预后差的一个独立预后因子[2]。韩国 的团队也报道原发性耐药患者中有19% 的患者具有BIM 多态性[3]。Wu 等的研究显示, 桩蛋白介导细胞内信号调节激酶ERK 活化,可通过BIM 的69 位丝氨酸和Mcl-1 的163 位苏氨酸磷酸化从而调节蛋白的稳定性,下调BCL-2 的表达和上升Mcl-1,从而克服 EGFR 的耐药性[4]。 共识二:根据分子标志物的个体化管理策略:对EGFR TKI 耐药的突变型肺癌,建议再活 检明确耐药的具体机制 Camidge 将EGFR TKI 耐药分为4 类,包括:①出现耐药突变,如T790M 突变;②旁路 激活,如c-MET 扩增;③表型改变,如腺癌向小细胞肺癌转化,上皮细胞向间叶细胞转化(epithelial to mesenchymal transformation,EMT);④下游信号通路激活,如BIM 的 多态性导致EGFR-TKI 的原发耐药,通过MAPK1 扩增直接激活下游增殖信号通路产生EGFR-TKI 的获得性耐药[5]。 50% 的耐药机制是EGFR20 号外显子第790 位点上的苏氨酸为蛋氨酸所取代(T790M),从而改变了ATP 的亲和性,导致EGFR TKI 不能有效阻断信号通路而产生耐药。也有一