核素裂变样品的分析处理
5.1 核素的初步甄别
对核素的甄别是一个复杂的过程:
(1)先挑选一个测量时间较长的能谱,将γ能谱的每个峰对应的能量记录(除开本底峰);
(2)对照已知核数据(考虑峰值左右一小范围),列出每个峰可能会对应的核素,删除从每个峰对应的核素中一部分分支比较小的(本实验考虑将低于3%的忽略,但实际在本实验中分支比小于10%时,其峰一般不能找到),删除半衰期过大过小的核素(依据冷却时间,测量时间,本实验重点考虑半衰期为50-20000s 的核素);
(3)初步归纳可能的核素,然后对照核素图[19],看核素对应γ衰变的几个较大分支比的峰是否存在,如果存在,则暂认为该核素存在,留待截面值分析后确定。
5.1.1 核素89Rb
表5.1.1 89Rb衰变的主要特征γ射线能量及分支比
核素半衰期(s) 全能峰序号能量(keV) 分支比
89Rb 909 E1657.77 0.108188 E2947.73 0.100011 E31031.92 0.629 E41248.14 0.45917 E52195.92 0.14467 E62570.20 0.10693
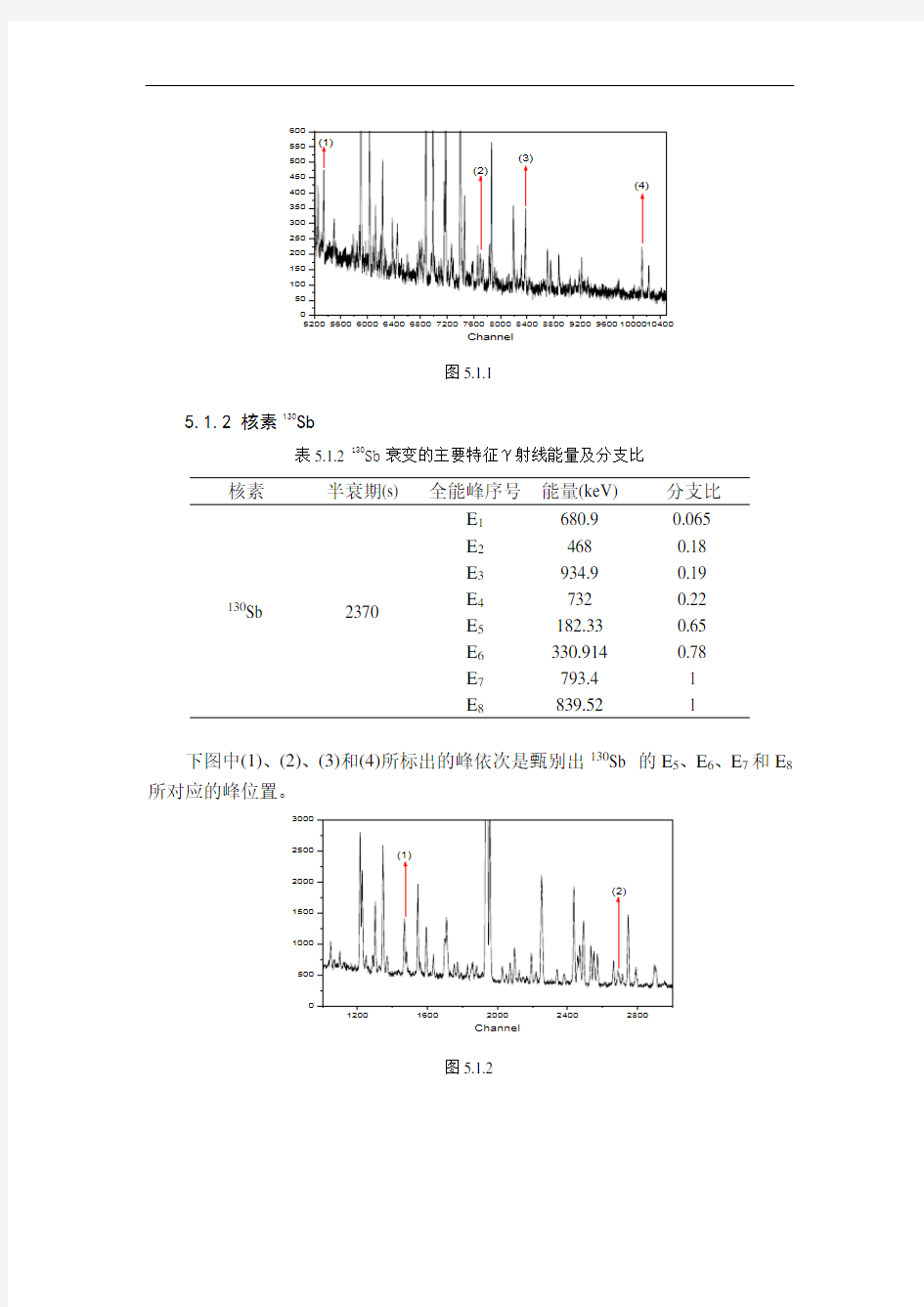
下图中(1)、(2)、(3)和(4)所标出的峰依次是甄别出89Rb 的E1、E2、E3和E4所对应的峰位置。
Channel 图5.1.2
Channel 图5.1.4
Channel
图5.1.5
5.1.5 核素134Te
表5.1.5 134Te衰变的主要特征γ射线能量及分支比核素半衰期(s) 全能峰序号能量(keV) 分支比
134Te 2508 E179.445 0.20945 E2180.891 0.1829 E3201.235 0.0885 E4210.465 0.22715 E5277.951 0.2124 E6435.06 0.1888 E7460.997 0.09735 E8464.64 0.0472 E9565.992 0.18585 E10742.586 0.1534 E11767.2 0.295
Channel
图5.1.7
5.1.6 核素134I
表5.1.6 134I衰变的主要特征γ射线能量及分支比核素半衰期(s) 全能峰序号能量(keV) 分支比
134I 3150 E1405.451 0.073689 E2540.825 0.07656 E3595.362 0.111012 E4621.79 0.106227 E5677.34 0.079431 E6766.68 0.0415338 E7847.025 0.957 E8857.29 0.06699 E9884.09 0.65076 E101072.55 0.149292 E111136.16 0.090915 E121806.84 0.055506
下图中(1)、(2)、(3)和(4)所标出的峰依次是甄别出134
I 的E 4、E 6、E 7和E 10
所对应的峰位置。
C o u n t s
Channel
图5.1.8
5.1.7 核素138Cs
表5.1.7 138
Cs 衰变的主要特征γ射线能量及分支比
核素 半衰期(s)
全能峰序号 能量(keV) 分支比
E 1 408.98 0.0466193
5和E 6Channel
图5.1.9
5.2 样品活化γ能谱分析
中子照射样品发生裂变反应,生成裂变碎片。三个角度,及三种不同能量中子辐照时间较为接近,为6000~7000s左右,冷却时间在4~5min,选取合适的测量时间分析每个角度的测量谱,通过对能谱进行读数,分析,甄别出一些可能的核素。在能谱的甄别工作中,我们对每一特征峰能量处可能的核素按其衰变强度和半衰期进行了筛选,并结合核素的衰变纲图,最终甄别得到了130Sb,138Xe,141Ba,134Te,138Cs,134I,89Rb几个核素的γ特征峰。
活化得到的γ谱图(如4.2中的能谱图可见),谱图并不是很好,本底特别大,尤其是在低能部分,导致核素的一些分支比较小,计数低的全能峰被本底湮没,以致核素的很多峰不能够被发现,使得在进行核素的甄别时,使一些可能存在的核素不能够被确定,因而被舍弃,造成找到裂变碎片减少。还有核素的峰,与其他核素的峰存在重叠,或与本底峰叠加,这种情况使得峰形不规则,不能够准确判断出核素是否存在,只能通过找出该核素的其他峰,来推断出该峰的存在与否,峰的叠加还会使计数的读取上造成很大的困难,计数的不准确使后续的截面分析中出现偏差甚至错误。
本实验得到的能谱相对比于14MeV能区中子轰击238U得到的能谱来说,甄别出的核素基本一致,但对于每个核素在能谱图上发现的全能峰个数较少(被本底湮没),计数也较低,说明相同条件下,232Th被诱发产生裂变的程度低于238U,即相对于每个裂变碎片的截面来说会小一些,在随后的截面值分析中也得到验证。
生物样品分析前处理技术
生物样品的前处理涉及很多方面,但主要应考虑生物样品的种类,被测定药物的性质和测定方法三个方面的问题。1.样品的分离、纯化技术应该依据生物样品的类型。例如,血浆或血清需除蛋白,使药物从蛋白结合物中释出;唾液样品则主要采用离心沉淀除去粘蛋白;尿液样品常采用酸或酶水解使药物从缀合物中释出,当原型药物排泄在尿中时,可简单地用水稀释一定倍数后进行测定。2.根据被测定药物的结构、理化及药理性质、存在形式、浓度范围等,采取相应的前处理方法。例如,药物的酸碱性(pka)、溶解性质涉及到药物的提取手段;是否具有挥发性涉及到能否采用气相色谱法测定;药物的光谱特性及官能团性质涉及到分析仪器的选择、能否制成衍生物及应用特殊检测器的可能性。药物在样品中的浓度相差很大,浓度大的样品,对前处理要求可稍低;浓度越低则样品前处理要求越高。此外,药物在体内常产生许多代谢产物,其中一些代谢物仍具有药理活性,需要与原型药分别测定,因而也要了解药物的药理学性质和药物动力学特性。3.样品于测定前是否需要纯化以及纯化到什么程度均与其后采用的测定方法的不同而不同。即纯化程度与所用测定方法的专属性、分离能力、检测系统对不纯样品污染的耐受程度等密切相关。一般说来,放射免疫测定法由于具有较高的灵敏度和选择性,因此当初步除去主要干扰物质之后即可直接测定微量样品;而对灵敏度和专属性较差的紫外分光光度法,分离要求就要相应高一些;至于常用的高效液相色谱法,为防止蛋白质等杂质沉积在色谱柱上,上柱前需对生物样品进行去蛋白,有时对被测组分进行提取、制备衍生物等前处理。 样品处理步骤与分析方法的选择 (一)去除蛋白质 在测定血样时,首先应去除蛋白质。去除蛋白质可使结合型的药物均出来,以便测定药物的总浓度;去除蛋白质也可预防提取过程中蛋白质发泡,减少乳化的形成,以及可以保护仪器性能(如保护HPLC柱不被沾污),延长使用期限。去除蛋白法有以下几种。 1.加入与水相混溶的有机溶剂加入水溶性的有机溶剂;可使蛋白质的分子内及分子间的氢键发生变化而使蛋白质凝聚,使与蛋白质结合的药物释放出来。常用的水溶性有机溶剂有:乙腈、甲醇、乙醇、丙醇、丙酮、四氢呋喃等。含药物的血浆或血清与水溶性有机溶剂的体积比为1:(1~3)时,就可以将90%以上的蛋白质除去。水溶性有机溶剂的种类不同时,析出的蛋白质形状亦不同;并且所得上清液的pH值也稍有差别,如用乙腈或甲醇时,上清液pH为8.5~9.5,用乙醇或丙酮时,上清液pH为9~10。操作时,将水溶性有机溶剂与血浆或血清按一定比例混合后离心分离,取上清液作为样品。通常分离血浆或血清用的离心机(3000r/min)不能将蛋白质沉淀完全,而采用超速离心机(10000r/min)离心1~2min 便可将析出的蛋白质完全沉淀。离心时应用超速离心机专用的具塞塑料尖底管,可使析出的蛋白质牢固地粘在管底,便于上清液的吸取。 2.加入中性盐加入中性盐,使溶液的离子强度发生变化。中性盐能将与蛋白质水合的水置换出来,从而使蛋白质脱水而沉淀。常用的中性盐有:饱和硫酸铵、硫酸钠、镁盐、磷酸盐及枸橼酸盐等。操作时,如按血清与饱和硫酸铵的比例为1:2,混合,离心(10000r/min)1~2min,即可除去90%以上的蛋白质。所得上清液的pH为7.0~7.7这种利用盐析的方法与有机溶剂提取法并用时,药物的回收率高,因而常常被采用。 3.加入强酸当pH低于蛋白质的等电点时,蛋白质以阳离子形式存在。此时加入强酸,可与蛋白质阳离子形成不溶住盐而沉淀。常用的强酸有:10%三氯醋酸、6%高氯酸、硫酸-钨酸混合液及5%偏磷酸等。含药物血清与强酸的比例为1:0.6混合,离心〈10000r/min)1~2min,就可以除去90%以上的蛋白质。取上清液作为样品。因加入了强酸,上清液呈酸性(pH0~4),在酸性下分解的药物不宜用本法除蛋白。过量的三氯醋酸可经煮沸,分解为氯仿和二氧化碳而被除去;也有用乙醚提取过量三氯醋酸的方法。过量的高氯酸可用碳酸钾、
生物样品前处理 2010-01-08 12:02:45| 分类:生物样品预处理 生物样品的前处理 .生物样品预处理 生物样品的前处理是体内药物分析的一个重要环节,也是整个分离分析过程中最繁琐的一个步骤。与原料药物和制剂相比,生物样品更为复杂:微量药物分布在大量生物介质中,对分析仪器的灵敏度提出了更高的要求;样品中含有大量内源性物质,不仅能与药物及其代谢物结合,而且常干扰测定。因此,生物样品中的药物必须经过分离、纯化与浓集,必要时还需对待测组分进行化学改性处理,从而为最后测定创造良好的条件。传统的样品前处理方法仍为溶剂萃取法,方法耗时、危害人体、污染环境,萃取使用大量溶剂,分析时需浓缩,会导致有效组分的损失。本文仅对近年相关文献报道的几种药物分析过程中生物样品预处理技术及应用进行综述。 超临界流体萃取( supercritical fluid extraction ,SFE) 是环保型分离浓集技术,具有萃取效率和选择性高、省时、萃取溶剂(如便于挥发、提取物较为“干净”、环境污染少、操作条件易于改变等特点,不仅广泛应用于食品、化妆品、环境、医药及一些天然产物的分析,在生物体内药物分析方面也显示出一定的优势[1]。 超临界流体萃取技术的原理是控制超临界流体在高于临界温度和临界压力的条件下,从目标物中萃取成分,当恢复到常压和常温时,溶解
在超临界流体中的成分立即与气态的超临界流体分开。该技术对于挥发性成分、脂溶性成分、小分子萜类及热敏物质等的提取,较传统方法有很多优越性。 常用萃取剂为。由于超临界流体是非极性溶剂,对于低极性和非极性的化合物表现出优异的溶解性能,而对于大多数无机盐、极性较强的物质几乎不溶。通过添加改性剂,如甲醇、乙醇、丙酮、乙酸乙酯和水等,并通过加压改善其溶解性能,使超临界流体萃取技术对生物碱类、黄酮类、皂甙类等的应用也日趋普遍。 针对生物样品中通常含有不同极性组分或含有大量脂溶性成分干 扰的特点,当前研究工作主要集中在如何提高超临界流体的萃取能力及消除脂类干扰两个方面[2]。 固相萃取技术以选择性吸附与选择性洗脱的液相色谱分离原理,对样品进行分离和纯化。 按照所采用固相萃取剂的种类,可将固相萃取法分为3类:正相、反相和离子交换固相萃取。当前固相萃取剂的开发主要侧重于扩大萃取剂的适用范围,将极性、非极性基团,离子交换基团或高分子树脂混合使用的混合型吸附剂,成为目前研究的热点。 根据分析物的极性、溶解度、pKa等理化性质,选取适合的固相萃取柱。对于非离子性物质而言,优先使用极性相似的固相萃取柱,如弱极性或非极性化合物选用、、等非极性柱,极性较强的则使用CN、柱。强离子型分析物则采用离子交换固相萃取。对于某些弱酸或弱碱性化合物,
分析样品前处理技术 课程报告 样品前处理方法:固相萃取(SPE) 班级: 应用化学121班 学号: 201238705131
固相萃取(SPE) 1.基本原理 固相萃取 (Solid Phase Extraction,SPE) 就是利用固体吸附剂将液体样品中的目标化合物吸附,与样品的基体和干扰化合物分离,然后再用洗脱液洗脱或加热解吸附,达到分离和富集目标化合物的目的。 SPE也是一个柱色谱分离过程,分离机理、固定相和溶剂的选择等方面与高效液相色谱(HPLC)有许多相似之处。分离模式有正相(吸附剂极性大于洗脱液极性)、反相(吸附剂极性小于洗脱液极性)等。 1.1.1 正相固定相 正相固相萃取所用的吸附剂都是极性的,用来萃取(保留)极性物质。在正相萃取时目标化合物如何保留在吸附剂上,取决于目标化合物的极性官能团与吸附剂表面的极性官能团之间相互作用,其中包括了氢键、π—π键相互作用、偶极-偶极相互作用和偶极-诱导偶极相互作用以及其他的极性-极性作用。正相固相萃取可以从非极性溶剂样品中吸附极性化合物。 1.1.2 反相固定相 反相固相萃取所用的吸附剂通常是非极性的或极性较弱的,所萃取的目标化合物通常是中等极性到非极性化合物。目标化合物与吸附剂间的作用是疏水性相互作用,主要是非极性-非极性相互作用,是范德华力或色散力。 固相萃取所用的吸附剂也与液相色谱常用的固定相相同,只是在粒度上有所区别。SPE柱的填料粒径(>40μm)要比HPLC填料(3~10μm)大。由于短的柱床和大的粒径,SPE柱效比HPLC色谱柱低得多。因此,用SPE只能分开保留性质有很大差别的化合物。与HPLC的另一个差别是SPE柱是一次性使用。 SPE的操作步骤: 1.2.1 柱预处理 目的之一是除去填料中可能存在的杂质,另一个目的是使填料溶剂化,提高
土壤采样与预处理 一.目的 土壤样品的采集与制备,是土壤分析工作中的一个重要环节,其正确与否,直接影响分析结果的准确性和有无应用价值,必须按科学的方法进行采样和制样。通过实验,初步掌握耕层土壤混合样品的采集和制备方法。 二采样点的确定 三采样布置方法 1.对角线布点法:适用于面积小,地势平坦,污染程度均匀的区域,采样点不少于5个 2.梅花形布点法:适用于面积小,地势平坦,污染程度均匀的区域,采样点5~10个 3.棋盘式:适用于中等面积,地势平坦,污染程度不均匀的区域,采样点10个以上 4.蛇形:适用于大面积,地势不平坦,污染程度不均匀的区域,点数越多越好。 按“随机”“多点”和“多点混合”的原则进行采样 四采样工具 小铁铲(或锄头)、布袋(或塑料袋)、标签、铅笔、钢卷尺、木锤、镊子、土壤筛(18目、60目)、广口瓶、研钵、盛土盘等。 五采样方法 1在确定采样点上,先将2-3mm表土刮去,然后用土钻或小铁铲垂直入土15-20cm左右。每点的取土深度、质量应尽量一致,将采集的各土点样在盛土盘上集中起来,初略选去石砾、虫壳、根系等物质,混合均与,采用四分法,弃去多余的土,直至所需数量未止,一般每个混合土的质量以1kg左右为宜。 由于土壤样品不均匀需多点采样而取土量较大时,应反复以四分法将样品按照测定要求磨细,过一定孔径的筛子,然后混合,平铺成圆形,分成四等分,取相对的两份混合,然后再平分,直到达到自己的要求缩分至所需量。 2装袋与填写标签采好后的土样装入布袋中,立即写标签,一式两份,一份系在布袋外,一份放入布袋内,土样编号、采样地点及经纬度、土壤名称、采样深度、前茬作物及产量、采样日期、采样人等。标签写明同时将此内容登记在专门的记载本上备查。 六、土壤样品的制备 1.土样的风干需要用风干土样,因为风干的土样较易混匀,重复性和准确性都较好。风干的方法为:将采回的土样倒在盘中,趁半干状态把土块压碎,除去植物残根等杂物,铺成薄层并经常翻动,在阴凉处使其慢慢风干。 2.磨碎与过筛风干后的土样,用有机玻璃(或木棒)碾碎后过2mm塑料(尼龙)筛,除去2mm以上的砂砾和植物残体(若砂砾量多时应计算其占土样的百分比)。留下的样品进一步磨细过0.25mm孔径的塑料(尼龙)筛,充分拌匀后装瓶备用。 七注意事项 (1)采样点不能选在天边、路边和刚施过肥的特殊区域。 (2)标签要用铅笔写两个,一个放在袋内,一个贴在袋子上 (3)采样过程中,每处理一份样品后,工具要擦洗干净,严防交叉污染
关于药物分析实验数据处理-----------------------作者:
-----------------------日期:
药物分析实验数据处理 实验数据中各变量的关系可表示为列表式,图示式和函数式。 列表式:将实验数据制成表格。它显示了各变量间的对应关系,反映出变量之间的变化规律。它是标绘曲线的基础。 图示式:将实验数据绘制成曲线。它直观地反映出变量之间的关系。在报告与论文中几乎都能看到,而且为整理成数学模型(方程式)提供了必要的函数形式。 函数式:借助于数学方法将实验数据按一定函数形式整理成方程即数学模型。 熟悉相关和回归的定义,相关系数的定义,直线回归的最小二乘法。 熟悉药品质量标准分析方法验证中各项指标的定义和考察方法。 含量测定方法的评价(效能指标—分析品质因数) :一般常用的分析效能评价指标包括:精密度、准确度、检测限、定量限、选择性、线性与范围、重现性、耐用性等;测定法的效能指标可评价分析测定方法,也可作为建立新的测定方法的实验研究依据。 1.精密度 系指用该法测定同一匀质样品的一组测量值彼此符合的程度。它们越接近就越精密。在药物分析中,常用标准(偏)差(SD或S);相对标准(偏)差(RSD),也称变异系数(CV),表示。 生物样品分析时,常用RSD表示精密度,并可细分为批内(或日内)精密度及批间(或日间)精密度。 批内精密度:是同一次测定的精密度。通常采用高、中、低三种浓度的同一样品各7-10份,每种浓度的样品按所拟定的分析方法操作,一次开机后,一一测定。计算每种浓度样品的SD值及RSD值。批内精密度也可视为日内精密度。所得RSD应争
徐州工程学院 论文报告 题目:样品预处理 学生:骆乃薇 指导教师:刘辉 专业:食品质量与安全 班级:12质量2 目录 1.样品预处理的目的 1 2.样品预处理的原则 1 3.样品预处理的方法 1 3.1有机物破坏法 2 3.2蒸馏法 3 3.3溶剂抽提法 5 3.4色层分离法 7 3.5化学分离法 7 3.6浓缩---------------------------------------------------------------------------9 一目的: 1、测定前排除干扰组分; 2 、对样品进行浓缩。 二原则: ①消除干扰因素; ②完整保留被测组分; ③使被测组分浓缩; 以便获得可靠的分析结果 三方法: 主要有6种。 (一)有机物破坏法 测定食品中无机成分的含量,需要在测定前破坏有机结合体,如蛋白质等。操作方法分为干法和湿法两大类。 1.干法灰化 原理:将样品至于电炉上加热,使其中的有机物脱水、炭化、分解、氧化,在置高温炉中灼烧灰化,直至残灰为白色或灰色为止,所得残渣即为无机成分。
2.湿法消化 原理:样品中加入强氧化剂,并加热消煮,使样品中的有机物质完全分解、氧化,呈气态逸出,待测组分转化为无机物状态存在于消化液中。 常用的强氧化剂有浓硝酸、浓硫酸、高氯酸、高锰酸钾、过氧化氢等。 湿法消化的优缺点 优点:(1)有机物分解速度快,所需时间短。 (2)由于加热温度低,可减少金属挥发逸散的损失。 缺点:(1)产生有害气体。 (2)初期易产生大量泡沫外溢。 (3)试剂用量大,空白值偏高。 3. 紫外光分解法 高压汞灯提供紫外光。85±5 ℃,加双氧水。 4. 微波高压消煮器。 食品样品最多只要10分钟(2.5 MPa); 其它方法: 1. 高压密封消化法——120~150℃,数小 时,要求密封条件高。 2.自动回流消化仪。 (二)蒸馏法 利用液体混合物中各种组分挥发度的不同而将其分离。 常压蒸馏 蒸减压蒸馏 馏水蒸气蒸馏 方 法 1.常压蒸馏 适用对象:常压下受热不分解或沸点不太高的物质。 蒸馏釜:平底、圆底 冷凝管:直管、球型、蛇型 注意:1. 爆沸现象。(沸石、玻璃珠、 毛细管、素瓷片) 2. 温度计插放位置。 3. 磨口装置涂油脂
实验一 土壤样品的采集与处理 土壤样品的采集是土壤分析工作中的一个重要环节,是关系到分析结果和由此得出的结论是否正确的一个先决条件。由于土壤特别是农业土壤的差异很大,采样误差要比分析误差大若干倍,因此必须十分重视采集具有代表性的样品。此外,应根据分析目的和要求采用不同的采样方法和处理方法。 一、土壤样品的采集 (一)采样时间 土壤中有效养分的含量随季节的改变而有很大变化。分析土壤养分供应情况时,一般都在晚秋或早春采样。同一时间内采取的土样,其分析结果才能相互比较。 (二)采样方法 采样方法因分析目的和要求的不同而有所差别: 1.土壤剖面样品 研究土壤基本理化性质,必须按土壤发生层次采样。 2.土壤物理性质样品 如果是进行土壤物理性质测定,须采原状样品。 3.土壤盐分动态样品 研究盐分在剖面中的分布和变动时,不必按发生层次取样,而自地表起每l0cm 或20cm 采集一个样品。 4.耕层土壤混合样品 为了评定土壤耕层肥力或研究植物生长期内土壤耕层中养分供求情况,采用这种方法。 (1)采样要求 在采样时,要求土样有代表性,因此需多点取样,充分混合,布点均匀,混合样品的取样数量应根据试验区的面积以及地力是否均匀而定,通常为5~20个点,采样深度只需耕作层土壤0~20cm ,最多采到犁底层的土壤,对作物根系较深的,可适当增加采样深度。 (2)采样方法 根据地形、样点数量和地力均匀程度布置采样点。面积不大,比较方正,可采用对角线取样法;面积较大,形状方正,肥力不匀的地块可采用棋盘式采样方法(方格取样法);面 积较大,形状长条或复杂,肥力不匀的地块多采用蛇形取样法(折线取样法)见图1所示 图1 采样点分布 采集混合样品时,每一点采取的土样,深度要一致,上下土体要一致;采土时应除去地面落叶杂物。采样深度一般取耕作层土壤20 cm 左右,最多采到犁底层的土壤,对作物根系较深的土壤,可适当增加采样深度。 对角线取样法 棋盘式取样法蛇形取样法法
目录 中文摘要 (2) 英文摘要 (3) 一、土壤污染 (5) (一)土壤污染概述 (5) (二)土壤污染的现状 (5) (三)土壤污染的危害 (5) (四)造成土壤污染的原因 (6) 二、土壤消解 (7) (一)研究进展 (8) (二)消解原理 (8) (三)实验仪器和药品 (10) (四)电热板消解法 (10) (五)全自动消解法 (11) (六)微波消解法 (12) (七)元素测定阶段 (12) 三、综述 (13) 参考文献 (15)
摘要 我国土壤污染的总体形势严峻,部分地区土壤污染严重,由土壤污染引发的农产品质量安全问题和群体性事件逐年增多。工业生产中矿山的开采冶炼、造纸、汽车尾气的排放,以及农业生产活动中含重金属污水灌溉农田、污泥的农业利用、肥料的土壤施用都给环境带来了污染。个别农药在其组成中含有Hg、As、Cu、Zn等金属。磷肥中含较多的重金属,使地球上的许多土壤被重金属污染。重金属元素不仅以单一元素污染土壤,同时多种重金属在土壤中共存时,它们之间还存在协同、拮抗作用,而且随着农药、化肥、污泥的大量施用,进一步加剧了土壤的复合污染。目前我国受Pb、Cu、Cd、As、Cr、Zn等重金对土壤污染和水污染的种类和数量随着工业的发展而越来越多,许多研究表明,重金属Cd2+可使高等植物的叶绿体含量明显降低,Cd2+,Pb2+和Zn2+等重金属离子对高等植物叶绿体的光合电子传递也有抑制作用,严重影响了农作物的生长,而且对土壤微生物活性和酶活性有一定质量影响。土壤重金属污染日益加重,己远远超过土壤的自净能力。因而,防治土壤重金属污染,保护有限的天然土壤资源,己成为突出的全球性问题。由于土壤类型种类的繁多,不同地区土壤差异很大,为了及时了解土壤中重金属的成分及含量,对土壤进行消解是测量土壤内重金属含量的常用方法之一。本文采用电热板消解,全自动消解和微波消解三种方式,分别选用常用的酸体系对三种类型的土壤进行消解,重点对铜(Cu)、锌(Zn)、铅(Pb)、镉(Cd)、铬(Cr)5种重金属元素进行分析。 关键词:土壤污染;土壤污染;土壤消解;电热板消解;全自动消解;微波消解
中药代谢组学研究中生物样品前处理方 法 (作者:_________ 单位:___________ 邮编:___________ ) 作者:邹忠杰,梁生旺,袁经权,龚梦鹃 【摘要】总结中药代谢组学研究中生物样品(尿液、血液)的前处理 方法,主要包括:尿液中加入缓冲液提供相同的pH值和离子强度, 保持代谢物化学位移的恒定。利用有机溶剂沉淀法除去血液中的大分子物质,增加色谱柱的性能和使用寿命。血液和尿液样品在进行GC'MS分析前要进行衍生化处理。同时,对尿液和血液的采集与储存方法进行了总结。 【关键词】中药;代谢组学;样品前处理 Abstract: In order to reduce the chemical shift variati on ,the pH and the con siste ncy of io nic stre ngth were con trolled by add ing buffer to uri ne samples. In an alysis of blood,efficie nt removal of macromolecules such as protei ns by orga nic solve nt precipitatio n before injectio n in to an analytical LC column was important in enhancing the performanee and extending column lifetime. Sample derivatization of blood
sample and urine sample before GC:MSanalysis was needed. And methods of collecti on and storage of urine and blood samples were also reviewed. Key words:traditional Chinese medicine; metabonomics; pretreatme nt 代谢组学(metabonomics)是继基因组学、转录组学和蛋白质组学后新兴的一种组学方法,是系统生物学的重要组成部分。中药“多组分、多靶点、整合调节作用”的特点与代谢组学整体性、系统性、综合性相吻合。因此,以代谢组学为主体的系统生物学研究方法可能是现代科学中可以概括中医药抽象整体观思想的重要途径。王广基等对 代谢组学技术在中医药关键科学问题研究中的应用前景进行了分析[1]。作者综述了代谢组学技术在中药整体疗效、作用机制及安全性等研究中的应用[2]。 代谢组学研究中的分析手段主要包括核磁共振谱(NMR)气相色谱拟质谱(GC以MS和液相色谱拟质谱(LC拟MS)等各种高通量、高分辨、高灵敏度的谱学技术[3]。NMR由于其具有很高的重现性、一次实验中实现对各种化合物的同时测定、信号强度与其摩尔浓度成正比,可以很容易进行定量分析、借助各种2D A N MR技术可以在对复杂样品不进行进一步分离的前提下实现结构鉴定等诸多优点而被广泛应用[4]。高分辨魔角旋转核磁共振技术(high拟resolution magic拟angle拟spinning NMF^pectroscopy)可以使研究者不经过提取等繁琐的步骤直接对完整的组织进行测定[5]。L C):MS特
土壤分析样品的采集和 处理方法 标准化管理部编码-[99968T-6889628-J68568-1689N]
Ⅰ-土壤分析样品的采集和处理方法配方施肥是一种以最少的肥料投入得到农作物最高产量的农业新技术,这一技术的基础是测出土壤中已有的养分含量,然后根据种植作物的品种、目标产量决定该施什么肥、施多少肥。 土壤样品采集是决定分析结果是否准确的重要环节,因此请严格按下列方法采集土样。 对作物根系较浅的种植地只需取耕层20厘米深的土壤,对作物根系较深的种植地如小麦应适当增加深度,果园土壤样品在耕层40厘米深处采集,采样点的多少可根据试验区耕地面积大小和地形而定,地块面积较小的要采5个点以上,地块面积较大的应采20个点以上。取样点的分布最好采用S型采样法或十字交叉法。(见图一) 采来的样品数量太多可用四分法弃去一部分保留1斤土样即可(见图二)。其方法是:把采来的土样倒在干净的木板或塑料布上,用手将土块捏碎,用镊子夹去土样中的作物根系、昆虫、石块等杂物,放于室内阴凉通风处风干,注意不能在阳光下曝晒及火烤,以免发生氧化反应。把风干后的土样用木棍或玻璃瓶碾碎(不可用金属制品),然后用1—2毫米筛子筛一遍。把筛过的土样平铺成四方形,如数量仍然很多,可再用四分法处理,直至所需数量为止,一般用50克土样即可,完成土样处理后,请填写土壤登记表。 注:如一户有几个土样或几户各有一个土样可将土壤登记表分别填好,并在土样包装上做上与登记表同样内容的标记,以免搞错。 避免在粪堆底上和同一垄上以及田边,路边,沟边和特殊地形部位采样。 采样时在确定的采样点上用小土铲向下切取一片片的土样样品,每个样品点采取的土壤厚、薄、深、浅、宽、狭应大体一致,集中起来混合均匀。 有机肥分析样品的采集和处理方法:堆肥、厩肥、沤肥、草塘肥、沼气肥、牲畜粪尿以及人粪尿等都是有机肥,这些肥料大都是很不均匀的,采样时应注意多点取样,一般应在翻堆混匀后,选择10—20个采样点,大块和散碎的肥料比例相近,把采到的若干样品放在一块干净的塑料布上,送入室中风干,摊开晾干,再把样品弄碎、剪细、混匀,再用四分法缩分至500克左右,磨细并全部通过1毫米孔径筛子,装入样品瓶中。 如果有机肥样品中夹有较多石块,应捡出另外称重,并计算其占原有样品的百分数,如需测定有机肥料中的NH4和NO3,则需用新鲜样品,即不经风干立即进行测定。 粪尿和沼气肥是液体和固体混合肥,可先混匀在未分层前取出500毫升左右放入密闭容器中,用玻璃棒将固体充分捣碎,在分析称样前应反复振摇容器充分混匀。 四分法: Ⅱ-土壤养份测试方法
第四节 生物样品分析的前处理技术 一般要在测定之前进行样品的前处理,即进行分离、纯化、浓集,必要时还需对待测组分进行化学衍生化,从而为测定创造良好的条件。 生物样品进行前处理的目的在于: 1.药物进入体内后,经吸收、分布、代谢,然后排出体外。在体液、组织和排泄物中除了游离型(原型)药物之外,还有药物的代谢物、药物与蛋白质形成的结合物、以及药物或其代谢物与内源性物质,如葡萄糖醛酸、硫酸形成的葡萄糖醛酸甙(glucuronides)、硫酸酯(sulphates)缀合物等多种形式存在,需要分离后测定药物及代谢物; 2.生物样品的介质组成比较复杂。如在血清中既含有高分子的蛋白质和低分子的糖、脂肪、尿素等有机化合物,也含有Na +、K+、X-等无机化合物]。其中影响最大的是蛋白质,若用HPLC法测定药物浓度时,蛋白质会沉积在色谱柱上发生堵塞,严重影响分离效果。因此,为了保护仪器,提高测定的灵敏度,必须进行除蛋白等前处理。 一、常用样品的种类、采集和贮藏 生物样品包括各种体液和组织,但实际上最常用的是比较容易得到的血液(血浆、血清、金血)、尿液、唾液。在一些特定的情况下选用乳汁、脊髓液、精液等。 (一)血样 血浆(plasma)和血清(serum)是最常用的生物样品。 血浆中的药物浓度反映了药物在体内(靶器官)的状况,因而血浆浓度可作为作用部位药物浓度的可靠指标。 供测定的血样应能代表整个血药浓度,因而应待药物在血液中分布均匀后取样。 由采集的血液制取血浆或血清。 血浆的制备 将采取的血液置含有抗凝剂(如:肝萦、草酸盐、拘橡酸盐、EDTA、氟化钠等)的试管中,混合后,以2500~3000rpm离心5min使与血细胞分离,分取上清液即为血浆。 血清的制备 将采取的血样在室温下至少放置30min到1h,待凝结出血饼后,用细竹捧或玻璃棒轻轻地剥去血饼,然后以2000~3000rpm离心分离5~10min,分取上清液.即为血清。 血浆比血清分离快,而且制取的量多,其量约为全血的一半。 血浆及血清中的药物浓度测定值通常是相同的。基于上述原因,现在国外多采用“专用血清”来测定药物的浓度。 血样的采血时间间隔应随测定目的的不同而异。 如进行治疗药物浓度监测(therapeutic drug monitoring,TDM)时,则应在血中药物浓度达到稳态后才有意义。但每种药物的半衰期不同,因此达到稳态的时间也不间,取样时间也随之不同。 采取血样后,应及时分离血浆或血清,并最好立即进行分析。如不能立即测定时,应妥善储存。血浆或血清样品不经蒸发、浓缩,必须置硬质玻璃试管中完全密塞后保存。 要注意采血后及时分离出血浆或血清再进行储存。若不预先分离,血凝后冰冻保存,则因冰冻有时引起细胞溶解从而妨碍血浆或血清的分离或因溶血影响药物浓度变化。 (二)唾液 唾液由腮腺、颌下腺、舌下腺和口腔粘膜内许多散在的小腺体分泌液混合组成的,平时所说的唾液就是指此混合液。 唾液的相对密度为1.003~1.008;pH值在6.2~7.6之间变动,分泌量增加时趋向碱性而接近血液的pH值;通常得到的唾液含有粘蛋白,其粘度是水的1.9倍。 唾液的采集应尽可能在剌激少的安静状态下进行。一般在漱口后15min收集。 也可以采用物理的(如嚼石蜡块、橡胶、海绵)或化学的(如酒石酸)等方法剌激,使在短时间内得到大量的唾液。 唾液中含有粘蛋白,唾液的粘度由粘蛋白的含量多少而定。 用唾液作为样品测定药物浓度有几个优点: 1.与采取血样不同,患者自己可以不受时间和地点的限制,很容易地反复采集; 2.采集时无痛苦无危险; 3.有些唾液中药物浓度可以反映血浆中游离型药物浓度 (三)尿液
环境样品前处理技术及其进展一 1.样品前处理在分析化学中的地位 一个完整的样品分析过程,包括从采样开始到写出报告,大致可以分为以下五个步获:(1)样品采集,(2)样品处理,(3)分析测定,(4)数据处理,(5)报告结果.统计结果表明〔幻,上述五个步骤中各步所需的时间相差甚多,各步所需的时间占全部分析时间的百分率为:样品采集6.%,样品处理61.0%,分析测试6.%;数据处理与报告27.0%.其中,样品处理所需的时间最长,约占整个分析时间的三分之二.这是因为在过去几十年中,分析化学的发展集中在研究方法的本身,如何提高灵敏度、选择性、及分析速度;如何应用物理与化学中的理论来发展新颖的分析方法与技术,以满足高新技术对分析化学提出的新目标与高要求;如何采用高新技术的成果改进分析仪器的性能、速度、及自动化的程度,因而忽视了对样品前处理方法与技术的研究,造成目前这种严峻的局面.目前,花在样品前处理上的时间,比样品本身的分析测试所需的时间,几乎多了一个数量级.通常分析一个样品只需几分钟至几十分钟,而分析前的样品处理却要几小时甚至几十小时.因此,样品前处理方法与技术的研究引起了广大分析化学家的关注,各种新技术与新方法的探索与研究已成为当代分析化学的重要课题与发展方向之一,快速、简便、自动化的前处理技术不仅可以省时、省力,而且可以减少由于不同人员的操作及样品多次转移带来的误差,对避免使用大量溶剂及减少对环境的污染也有深远的意义.样品前处理研究的深入开展必将对环境分析化学的发展起到积极的推动作用,达到一个新的高度. 2.样品前处理的目的 从环境中采集的样品,无论是气体、液体或固体,几乎都不能未经处理直接进行分析测定.特别是许多环境样品以多相非均一态的形式存在,如大气中所含的气溶胶与飘尘,废水中含的乳液、固体微粒与悬浮物,土城中还有水份、微生物、砂砾及石块等. 所以,采集的环境样品必须经过处理后才能进行分析测定。 经过前处理的样品,首先可以起到浓缩被测痕量组份的作用,从而提高方法的灵敏度,降低最小检测极限.因为环境样品中有毒有害物质的浓度很低,难以直接测定,经过前处理富集后,就很容易用各种仪器分析测定,从而降低了测定方法的最小检测极限;其次可以消除基体对测定的干扰,提高方法的灵敏度。否则基体产生的讯号可以大到部份或完全掩盖痕量被测物的讯号,不但对选择分析方法最佳操作条件的要求有所提高,而且增加了测定的难度,容易带来较大的测量误差;还有通过衍生化的前处理方法,可以使一些在通常检测器上没有响应或响应值较低的化合物转化为具有很高响应值的化合物,如硝基烃在目前各种检测器上响应值均较低,把它还原为氨基烃再经三氟乙酸衍生处理后,生成带电负性很强的化合物,它们在电子捕获检测器上具有极高的灵敏度.衍生化通常还用于改变被侧物质的性质,提高被测物与基体或其他干扰物质的分离度,从而达到改善方法灵敏度与选择性的目的,此外,样品经前处理后就变得容易保存或运翰。因为环境样品浓度低,
土壤样品采集与处理实验 报告 Prepared on 22 November 2020
实验一土壤样品的采集与处理 土壤样品的采集是土壤分析工作中的一个重要环节,是关系到分析结果和由此得出的结论是否正确的一个先决条件。由于土壤特别是农业土壤的差异很大,采样误差要比分析误差大若干倍,因此必须十分重视采集具有代表性的样品。此外,应根据分析目的和要求采用不同的采样方法和处理方法。 一、土壤样品的采集 (一)采样时间 土壤中有效养分的含量随季节的改变而有很大变化。分析土壤养分供应情况时,一般都在晚秋或早春采样。同一时间内采取的土样,其分析结果才能相互比较。 (二)采样方法 采样方法因分析目的和要求的不同而有所差别: 1.土壤剖面样品研究土壤基本理化性质,必须按土壤发生层次采样。 2.土壤物理性质样品如果是进行土壤物理性质测定,须采原状样品。 3.土壤盐分动态样品研究盐分在剖面中的分布和变动时,不必按发生层次取样,而自地表起每l0cm 或20cm 采集一个样品。 4.耕层土壤混合样品为了评定土壤耕层肥力或研究植物生长期内土壤耕层中养分供求情况,采用这种方法。 (1)采样要求 在采样时,要求土样有代表性,因此需多点取样,充分混合,布点均匀,混合样品的取样数量应根据试验区的面积以及地力是否均匀而定,通常为5~20个点,采样深度只需耕作层土壤0~20cm ,最多采到犁底层的土壤,对作物根系较深的,可适当增加采样深度。 (2)采样方法 根据地形、样点数量和地力均匀程度布置采样点。面积不大,比较方正,可采用对角线取样法;面积较大,形状方正,肥力不匀的地块可采用棋盘式采样方法(方格取样法);面积较大,形状长条或复杂,肥力不匀的地块多采用 土时应除去地面落叶杂物。采样深度一般取耕作层土壤20cm 左右,最多采到犁底层的土壤,对作物根系较深的土壤,可适当增加采样深度。 对角线取样法 棋盘式取样法蛇形取样法法
实验一土壤样品的采集与处理 土壤样品的采集是土壤分析工作中的一个重要环节,是关系到分析结果和由此得出的结论是否正确的一个先决条件。由于土壤特别是农业土壤的差异很大,采样误差要比分析误差大若干倍,因此必须十分重视采集具有代表性的样品。此外,应根据分析目的和要求采用不同的采样方法和处理方法。 一、土壤样品的采集 (一)采样时间 土壤中有效养分的含量随季节的改变而有很大变化。分析土壤养分供应情况时,一般都在晚秋或早春采样。同一时间内采取的土样,其分析结果才能相互比较。 (二)采样方法 采样方法因分析目的和要求的不同而有所差别: 1.土壤剖面样品研究土壤基本理化性质,必须按土壤发生层次采样。 2.土壤物理性质样品如果是进行土壤物理性质测定,须采原状样品。 3.土壤盐分动态样品研究盐分在剖面中的分布和变动时,不必按发生层次取样,而自地表起每l0cm或20cm采集一个样品。 4.耕层土壤混合样品为了评定土壤耕层肥力或研究植物生长期内土壤耕层中养分供求情况,采用这种方法。 (1)采样要求 在采样时,要求土样有代表性,因此需多点取样,充分混合,布点均匀,混合样品的取样数量应根据试验区的面积以及地力是否均匀而定,通常为5~20个点,采样深度只需耕作层土壤0~20cm,最多采到犁底层的土壤,对作物根系较深的,可适当增加采样深度。 (2)采样方法 根据地形、样点数量和地力均匀程度布置采样点。面积不大,比较方正,可采用对角线取样法;面积较大,形状方正,肥力不匀的地块可采用棋盘式采样方法(方格取样法);面积较大,形状长条或复杂,肥力不匀的地块多采用蛇形取 1 对角线取样法棋盘式取样法蛇形取样法法 层的土壤,对作物根系较深的土壤,可适当增加采样深度。
土壤样品采集与处理实 验报告 Document number:WTWYT-WYWY-BTGTT-YTTYU-2018GT
实验一土壤样品的采集与处理 土壤样品的采集是土壤分析工作中的一个重要环节,是关系到分析结果和由此得出的结论是否正确的一个先决条件。由于土壤特别是农业土壤的差异很大,采样误差要比分析误差大若干倍,因此必须十分重视采集具有代表性的样品。此外,应根据分析目的和要求采用不同的采样方法和处理方法。 一、土壤样品的采集 (一)采样时间 土壤中有效养分的含量随季节的改变而有很大变化。分析土壤养分供应情况时,一般都在晚秋或早春采样。同一时间内采取的土样,其分析结果才能相互比较。 (二)采样方法 采样方法因分析目的和要求的不同而有所差别: 1.土壤剖面样品研究土壤基本理化性质,必须按土壤发生层次采样。 2.土壤物理性质样品如果是进行土壤物理性质测定,须采原状样品。 3.土壤盐分动态样品研究盐分在剖面中的分布和变动时,不必按发生层次取样,而自地表起每l0cm 或20cm 采集一个样品。 4.耕层土壤混合样品为了评定土壤耕层肥力或研究植物生长期内土壤耕层中养分供求情况,采用这种方法。 (1)采样要求 在采样时,要求土样有代表性,因此需多点取样,充分混合,布点均匀,混合样品的取样数量应根据试验区的面积以及地力是否均匀而定,通常为5~20个点,采样深度只需耕作层土壤0~20cm ,最多采到犁底层的土壤,对作物根系较深的,可适当增加采样深度。 (2)采样方法 根据地形、样点数量和地力均匀程度布置采样点。面积不大,比较方正,可采用对角线取样法;面积较大,形状方正,肥力不匀的地块可采用棋盘式采样方法(方格取样法);面积较大,形状长条或复杂,肥力不匀的地块多采用 土时应除去地面落叶杂物。采样深度一般取耕作层土壤20cm 左右,最多采到犁底层的土壤,对作物根系较深的土壤,可适当增加采样深度。 对角线取样法 棋盘式取样法蛇形取样法法
土壤样品预处理方法 D.1 全分解方法 D.1.1普通酸分解法 准确称取0.5 g(准确到0.1 mg,以下都与此相同)风干土样于聚四氟乙烯坩埚中,用几滴水润湿后,加入10 mLHCl(ρ1.19g/mL),于电热板上低温加热,蒸发至约剩5 mL时加入15 mLHNO3(ρ1.42g/mL),继续加热蒸至近粘稠状,加入10 ml HF(ρ1.15g/m L)并继续加热,为了达到良好的除硅效果应经常摇动坩埚。最后加入5 ml HClO4(ρ1. 67g/Ml),并加热至白烟冒尽。对于含有机质较多的土样应在加入HClO4之后加盖消解,土壤分解物应呈白色或淡黄色(含铁较高的土壤),倾斜坩埚时呈不流动的粘稠状。用稀酸溶液冲洗内壁及坩埚盖,温热溶解残渣,冷却后,定容至100 mL或50 mL,最终体积依待测成分的含量而定。 D.1.2 高压密闭分解法 称取0.5 g风干土样于内套聚四氟乙烯坩埚中,加入少许水润湿试样,再加入HNO3(ρ1.42g/mL)、HCl04(ρ1.67g/mL)各5 mL,摇匀后将坩埚放入不锈钢套筒中,拧紧。放在180 ℃的烘箱中分解 2 h。取出,冷却至室温后,取出坩埚,用水冲洗坩埚盖的内壁,加入3 mL HF(ρ1.15g/mL),置于电热板上,在100 ℃~120 ℃加热除硅,待坩埚内剩下约2 ~3 mL溶液时,调高温度至150 ℃,蒸至冒浓白烟后再缓缓蒸至近干,按1.1同样操作定容后进行测定。 D.1.3 微波炉加热分解法 微波炉加热分解法是以被分解的土样及酸的混合液作为发热体,从内部进行加热使试样受到分解的方法。目前报导的微波加热分解试样的方法,有常压敞口分解和仅用厚壁聚四氟乙烯容器的密闭式分解法,也有密闭加压分解法。这种方法以聚四氟乙烯密闭容器作内筒,以能透过微波的材料如高强度聚合物树脂或聚丙烯树脂作外筒,在该密封系统内分解试样能达到良好的分解效果。微波加热分解也可分为开放系统和密闭系统两种。开放系统可分解多量试样,且可直接和流动系统相组合实现自动化,但由于要排出酸蒸气,所以分解时
【讨论】生物样本前处理技术 样本前处理技术在分析方法中占有极其重要的地位,很多分析问题都可以通过样本前处理解决,本文将对样本前处理过程中遇到的问题和样本前处理方法进行综述,以期形成一个系统。本文将分为 1.样本分类及采集 2.初步处理 3.游离药物分离 4.萃取技术 5.萃取后过程 五个部分进行分别阐述。 其中有不少为个人观点,希望各位战友能不吝指正(纠正错字,纠正观点,进行讨论都欢迎),希望和园内战友共同学习。 -------------------------------------------------------------------------------- 楼主快点介绍吧。 -------------------------------------------------------------------------------- 1.1 生物样本分类 生物样本多种多样,有血浆、血清、全血、淋巴、唾液、各种组织、毛发、尿液、胆汁、泪液、脊髓液、汗液、乳汁、羊水、粪便以及呼出的气体。(以下文字主要摘自《体内药物分析》姚彤伟编著 2001年)生物样品可大致分为 ①均匀样品:血液、尿液、唾液、胆汁、脑脊液、淋巴液、乳汁和性腺分泌液等体液; ②非均匀样品:心、肝、脾、肺、肾、胃、肠、生殖器官、脑、体脂、胸腺肾上腺和骨骼肌等11种器官、组织。 Ruth Endacott[1]总结了临床样本采集时需要注意的问题以使采样够用和适用。 [1]:Endacott R, Botti M. Clinical research 3: sample selection. Intensive Crit Care Nurs. 2005 Feb;21(1):51-5. 1.2 生物样品采集 1.2.1 血样 组成 血样包括血浆、血清和全血,其中最常用的是血浆。一般认为,药物在体内达到稳定状态时,血浆中药物浓度是与药物在作用点的浓度紧密相关的,即血浆中药物浓度可以反映药物在体内(靶器官)的状况,而且血浆中药物浓度的数据报道较多,可供借鉴。 欲借助血药浓度来了解药物体内的转运规律和用于剂量调整, 应待药物在血液中分布均匀后再取样。直接抽取动脉血或自心脏取血无疑是最理想的方法,因为动脉血中的药物已充分混匀,但此法仅适用于动物实验研究。就采血方式而言,目前使用较多的方法是自静脉采血,并且视采血次数的多少和实验方法需要,一般每次采血1-5ml。做动物实验时,采血量不宜超过动物总血量的十分之一,以免因血流动力学改变而影响研究结果。表1列出常见动物的采血方法。标准的犬类或猫类动物收集血样方法参见Lucas RL 的综述。血样储存及储存条件参见下表2。 血浆及血清 血浆(plasma)的取得是在加肝素、草酸盐、枸橼酸等抗凝剂的全血经离心后分取上层清液,其量约为全血的一半。血清(serum)则是由血液中纤维蛋白原等影响下引起血块凝结而析出,离心后取上层清液而得,血块凝结时,往往易造成药物吸附的损失。通过制备后的血清一般可以得到全血的40%,而血浆会比血清多,大约占全血的50%,个体差异较大。 血清和血浆有以下三点区别:1。血清中没有纤维蛋白原 2。血清中无参与凝血机制的血浆
土壤样本的预处理。 称取1 g磨细土样于150Ⅱll锥形瓶中,加入浓HNO 5 ml、浓HCI 15 ml,摇匀,置于电热板上,以低温加热分解。逐渐提高温度,当瓶中内容物激烈反应过后,取下锥形瓶,稍冷却,加入HC1 5 ml,继续加热分解,直至瓶中内容物呈近似白色浆状物,并冒高氯酸白炯。取下锥形瓶,稍冷却,加入去离子水5 ml冲洗瓶壁,再加热至冒白烟,并持续10 min。取下锥形瓶,冷却至室温后,加入1N HCI溶液l0 ml及去离子水l0 rI1l,在电热板上加热熔解盐类。取下锥形瓶,静置,用中速定量滤纸过滤于50 ml容量瓶中,用l% HNO 反复洗涤锥形瓶及滤纸,洗涤液一并过滤于容量瓶中,冷却,并用l% HNO 稀释至刻度,摇匀待测 样品处理与分析 植物样品用蒸馏水洗净、烘干、粉碎,全部过0.5 mm尼龙筛。采用干灰化法,称取2.0 g植物样品于瓷坩埚中,在电热板上进行碳化,待试样烧至无烟 后移人马弗炉内,逐步升温至525%进行灰化,灰化时间为8 h,若灰分中残存的炭较多,冷却后加入几滴浓硝酸,蒸发至于后,在马弗炉中继续完全灰化。 灰化完全后,在瓷坩埚中加入3 ml浓盐酸溶解灰分,必要时过滤,然后用5%的HNO 将上述滤液定容至100 ml容量瓶。土壤样品经80 c【=烘干后,全部通过百目筛,称取0.5 g过筛后的土样,依次加入6 ml硝酸、3 ml氢氟酸和2 ml高氯酸,在微波消解罐中进行消解,消解条件见表1。 消解完全后,将消解管取出,用水浴法将剩余的酸挥发直至没有刺鼻气味,然后用5%的硝酸将消解管中的残留物洗出、定容至100 ml容量瓶。使用原子吸收分光光度计测量土壤和植物样本中铅、锌、铜含量时,首先用稀释后的铅、锌、铜标准溶液做出标准曲线,然后再分别对土壤和植物样本进行检测。同一样品反复测量次数不少于3次,取平均值。 土壤污染的危害及种类 土壤污染是指具有生理毒性的物质或过量的植物营养元素进入土壤而导致土壤性质恶化和植物生理功能失调的现象。土壤污染可导致土壤组成、结构、功能发生变化,进而影响植物正常生长发育,造成有害物质在植物体内累积,通过食物链危害人畜健康,或经地面径流、土壤凤蚀,使污染物向其他地方转移。土壤有一定的自净能力,但土壤一旦被污染,就很难恢复,特别是重金属污染。 土壤污染大致可分为无机污染物和有机污染物两大类。无机污染物主要包括酸、