精品好文档,推荐学习交流
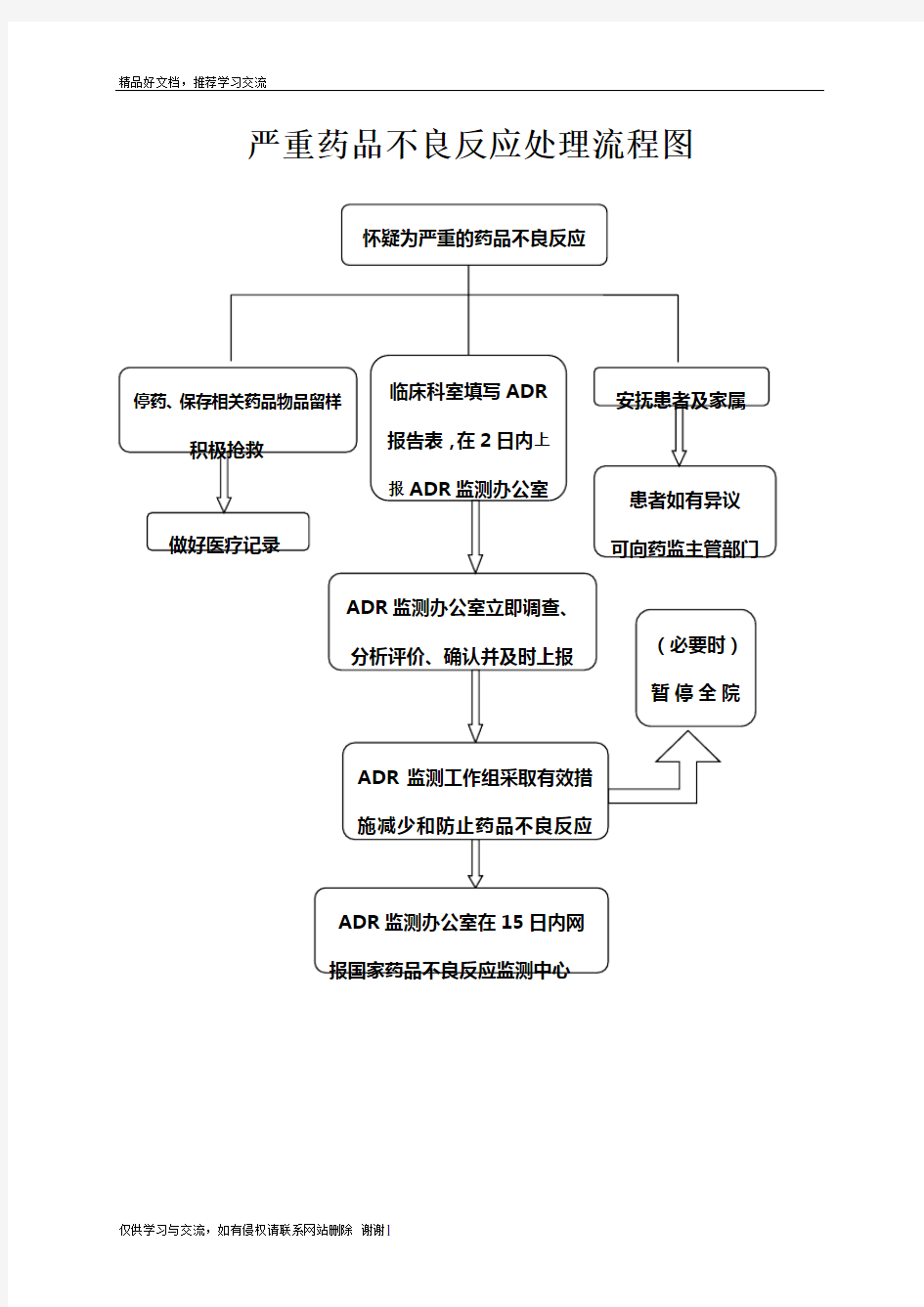
严重药品不良反应处理流程图
仅供学习与交流,如有侵权请联系网站删除谢谢1
永宁县中医医院 药品效期管理制度与流程 为进一步加强药品效期管理,确保药品质量,减少医院损失,使药剂科的药品管理更加规范化,特制定本制度。 责任人:库管、药剂科主任及成员。 内容: 1、药品的有效期是指在规定的储存条件下,能保证其质量的期限药品。有效期是根据药品的稳定性的不同,通过稳定性试验,研究和留样观察合理制定的。 2、药品应标明有效期,未标明有效期或更改有效期的,按劣药处理,验收员应拒绝收货。 3、药品的采购应根据我院临床用药的需要对购进药品的数量进行科学预计,并应遵循勤购勤销的原则,尽量减少药品库存。采购药品时尽量选择距失效期较远的药品(生物制品不少于六个月、其它药品不少于一年)。距失效期不到6个月的药品不得购进,不得签收、入库,对效期不足6个月药品,加强养护管理及陈列检查。 4、按照药品的储存条件,采用避光、干燥、冷藏等措施加以保管。 5、药库保管员要严格填写入库验收记录,必须将药品的供应单位、名称、规格、产地厂家、单价、生产批号、有效期等书写完整。
6、根据一般处理规律,适量制定申领计划,避免药品挤压失效。 7、存放药品时掌握,先进先出,近期先出,旧货未尽,新货不出的原则。 8、各药房从药库领取药品时,应控制品种、数量和有效期,既要保障临床用药的需要,又要防止过期失效。 9、药房对距失效期3个月的常用药品不能领用,必须计算在药品用完有1个月的时间。 10、效期药品管理责任到人,每位药房成员划分药品效期责任区,每月查看,近效期药品登记在效期本上,以便动态监测。 11、及时处理过期失效药品,严格杜绝过期失效药品售出。 12、药库保管员要做好药品动态分析记录,对入库2个月不出库的药品反馈给科主任,在了解医院用药情况或再行决定留存或退货。 效期流程图 药品入库→入库验收→合格药品入库→定期检查 ↓ 6个月近效期药品拒收
1.适用范围 本标准适用于本公司药品不良反应(ADR)监察报告。 2.职责 综合部:负责收集、整理ADR的信息,并进行分析、评估、分类。 负责组织讨论ADR处理方案(措施),以及方案(措施)的制订,提交审批。 负责ADR处理方案(措施)的具体实施、跟踪、监督、检查及所有资料的收集、 整理、建档。并将ADR报告给药品监督管理部门。 质量部:负责组织对B型ADR进行生产过程及质量检验、质量监督管理方面的调查。 3.内容 3.1.定义 3.1.1.药品不良反应(简称ADR) 药品不良反应主要是指合格药品在正常用法用量下出现的与用药目的无关的或意外的有害反应。 药品不良反应包括药品引起的副作用、毒性反应、后遗反应、过敏反应、特异质反应、致畸、致癌、致突变作用以及对生育力的影响等。根据药物不良反应的临床表现与药物药理作用的关系,一般将药品不良反应分为A型和B型。 3.1.2.A型药品不良反应 是指由于药物的药理作用增强所引起的不良反应,其程度轻重与用药剂量有关,一般容易预测,发生率较高而死亡率较低。 3.1.3.B型药品不良反应 是指与药物常规药理作用无关的异常反应,通常难以预测在具体病人身上是否会出现,在药物研究阶段的常规毒理学试验中难以发现,一般与用药剂量无关,发生率较低但死亡率较高。 3.2.范围 3.2.1.所有危及生命、致残直到丧失劳动能力或死亡的不良反应。 3.2.2.新药投产使用发生的各种不良反应。 3.2.3.疑为药品所引致的突变、癌变、畸形。 3.2. 4.各种类型的过敏反应。 3.2.5.非麻醉药品产品的药物依赖性。 3.2.6.疑为药品间相互作用导致的不良反应。 3.2.7.其它一切意外的不良反应。
药品不良反应/ 事件报告表 首次报告□ 跟踪报告□ 编码: 报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□ 不良反应事件名称:不良反应事件发生时间:年月日不良反应/ 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页) 不良反应/ 事件的结果:痊愈□好转□ 未好转□ 不详□ 有后遗症□ 表现: 死亡□ 直接死因:死亡时间:年月日 停药或减量后,反应/ 事件是否消失或减轻?是□ 否□不明□ 未停药或未减量□再次使用可疑药品后是否再次出现同样反应/ 事件?是□ 否□ 不明□ 未再使用□
电子邮箱: 签名:××× 药 品 不 良 反 应 / 事 件 报 告 表示例 不良反应 / 事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页) 一般格式为:患者因×××疾病于×××月×××日(必要时应详细到×××时分)以×××途径给予×××药品,×××剂量,用药×× ×时间出现×××反应(反应描述须明确、具体) ,×××时间后给予是否停药及×××处理(包括以×××途径给予×××药品及×××剂 和其他处理措施) ,处理后×××时间患者转归情况。 对原患疾病的影响: 不明显□ 病程延长□ 病情加重□ 导致后遗症□ 导致死亡□ 报告人评价: 肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:××× 报告单位评价: 肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:××× 报告人信息 患者姓名:××× 性别:男□女□ 出生日期: 年 月 日 或年龄: ×× 民族:×× 体重( kg ):×× 联系方式:×××××× 原患疾病:指患者此次入 诊的主要疾病(如果有多 疾病可以补充在相关重要 是备注里面),不能写字 院或就 种慢性 信息或 母缩写。 医院名称:三亚市中医院 病历号 / 门诊号:××××(务必 填写) 既往药品不良反应 / 事件:有□需提供药品通用名称及具体反应 无□ 不详□ 家族药品不良反应 / 事件:有□需提供药品通用名称及具体反应 无□ 不详□ 报告单位类别:医疗机构□ 其他□ 相关重要信息: 吸烟史□ 饮酒史□ 妊娠期□ 肝病史□ 肾病史□ 过敏史□此处是提供有否食物等过敏史 首次报告□ 跟踪报告□ 报告类型:新的□ 严重□ 一般□ 编码: 经营企业□ 生产企业□ 个人□ 其他□ 药 品 批准文号 商品 名称 通用名称 (含剂型) 生产厂 家 生产批号 用法用量 (次剂量、 途径、 日次数) 用药起止时 间 用药原因 怀 疑 药 品 国药准字 此处填写药品的 通用名 称。注射剂 包含注射液和粉 针剂,请认真选择 正确剂型 本次使用药 物的生产批 号 包括每次用药剂 量、 给药途径、 每日给药 次数, 例如,5mg , 口服, 每日 2 次。 指使用药品 的同 一剂量 的开始时 间 和停止时间 填写使用该药品的原因,应详 细填 写。例如:患者高血压病 史,此次因肺部感染而注射氨 苄青霉素引起不良反应,用药 原因栏应填写肺部 感染 并 用 药 品 同上 量, 不良反应 / 事件的结果:痊愈□ 死亡□ 好转□ 直接死因: 未好转□ 不详□ 有后遗症□ 表现: 死亡时间:× 年 × 月 × 日 停药或减量后,反应 / 事件是否消失或减轻? 再次使用可疑药品后是否再次出现同样反应 / 事件? 是□ 否□ 是□ 否□ 不明□ 不明□ 未停药或未减量□ 未再使用□ 关联性评价 联系电话:务必正确填写 职业:医生□ 药师□ 护士□ 其他□ 不良反应 / 事件名称:应填写不良反应中最主要、最明显的症状。 不良反应 / 事件发生时间:× 年 × 月× 日(应填写发生不良反应 / 事件 的确切时间)
近效期药品管理规定与 流程 内部编号:(YUUT-TBBY-MMUT-URRUY-UOOY-DBUYI-0128)
永宁县中医医院 药品效期管理制度与流程 为进一步加强药品效期管理,确保药品质量,减少医院损失,使药剂科的药品管理更加规范化,特制定本制度。 责任人:库管、药剂科主任及成员。 内容: 1、药品的有效期是指在规定的储存条件下,能保证其质量的期限药品。有效期是根据药品的稳定性的不同,通过稳定性试验,研究和留样观察合理制定的。 2、药品应标明有效期,未标明有效期或更改有效期的,按劣药处理,验收员应拒绝收货。 3、药品的采购应根据我院临床用药的需要对购进药品的数量进行科学预计,并应遵循勤购勤销的原则,尽量减少药品库存。采购药品时尽量选择距失效期较远的药品(生物制品不少于六个月、其它药品不少于一年)。距失效期不到6个月的药品不得购进,不得签收、入库,对效期不足6个月药品,加强养护管理及陈列检查。 4、按照药品的储存条件,采用避光、干燥、冷藏等措施加以保管。 5、药库保管员要严格填写入库验收记录,必须将药品的供应单位、名称、规格、产地厂家、单价、生产批号、有效期等书写完整。 6、根据一般处理规律,适量制定申领计划,避免药品挤压失效。 7、存放药品时掌握,先进先出,近期先出,旧货未尽,新货不出的原则。 8、各药房从药库领取药品时,应控制品种、数量和有效期,既要保障临床用药的需要,又要防止过期失效。
9、药房对距失效期3个月的常用药品不能领用,必须计算在药品用完有1个月的时间。 10、效期药品管理责任到人,每位药房成员划分药品效期责任区,每月查看,近效期药品登记在效期本上,以便动态监测。 11、及时处理过期失效药品,严格杜绝过期失效药品售出。 12、药库保管员要做好药品动态分析记录,对入库2个月不出库的药品反馈给科主任,在了解医院用药情况或再行决定留存或退货。 效期流程图 药品入库→入库验收→合格药品入库→定期检查 ↓ 6个月近效期药品拒收 药品出库→领药人员逐盒检查→ 6个月效期药品→拒收 ↓ 3个月效期药品→登记记录 ↓ 1个月效期药品→下架专人管理 ↓ 近效期不能用的 ↓ 退回库房 永宁县中医医院
抗结核药物常见不良反应及处理方法 目的 早期、正确地处理药品不良反应是保证患者依从性、取得治疗成功的关键。 ●保证用药安全,减少医疗纠纷,杜绝医疗事故。 ● 1.药物不良反应概念 ● 2.超敏反应发生机理 ● 3.毒性反应发生机理 ● 4.不良反应临床表现 ● 5.不良反应的临床处理原则 ●定义 药物不良反应是合格药物在正常用法和用量时由药物引起的有害的和不期望产生的反应。 ●分类 副作用(side effect)、毒性反应、依赖性、特异质反应、过敏反应、致畸、致癌和致突变反应药物不良反应 ●超敏反应: 与剂量及疗程无关,一般发生在用药2周以 ●毒性反应: 与剂量及用药时间和药物的蓄积有关 超敏反应发生机理(1) ●结核药物(半抗原)+蛋白质→全抗原→特应机体→特异性抗体或致敏淋巴细胞 ●当再次接触同种药物即可产生超敏性反应 -Ⅰ型超敏反应(速发型) 临床表现: 过敏性休克、支气管哮喘、血管性水肿、瘙痒、皮疹、恶心、呕吐、腹泻、喷嚏、咳嗽、发热等,可引起这种反应的的药物主要有利福平、链霉素、氟喹诺酮类。 Ⅱ型反应(细胞毒型)(1) 在这一类型反应中IgG、IgM类抗体与靶细胞表面相应抗原结合后,在补体、吞噬细胞和NK细胞参与作用下,引起的以细胞溶解或组织损伤为主的病理性免疫反应。 Ⅱ型反应(细胞毒型)(2) 药物+血细胞膜蛋白(血浆蛋白) ↓ 免疫原性 ↓ 机体 ↓ 特异性抗体 ↓再次与药物接触 ┏━━━━━━━━━━━━━━┓ 抗原抗体复合物RBC,WBC,PLT ↓│ ↓ 溶血性贫血、粒细胞减少症和血小板减少性紫癜
Ⅱ型反应(细胞毒型)(3) 临床表现: 主要表现在血液学方面,出现血小板减少、白细胞减少和溶血性贫血。引起此类反应的药物主要有利福平、PAS。 Ⅲ型反应(免疫复合物型) 临床表现: 血清病样反应,有发热、关节痛、荨麻疹、淋巴结肿大、腹痛、蛋白尿、嗜酸性粒细胞增多等,药物热有人认为也属Ⅲ型过敏反应。一般在用药10天发生,热型为稽留热型或弛型,可同时伴有皮疹。引起此类反应的药物主要有利福平、PAS。 Ⅳ型反应(细胞介导或迟发型) 临床表现: 主要是接触性皮炎,一般发生在与药物接触3-12个月,在两手手臂、眼睑、颈等处,表现为皮肤搔痒、发红丘疹、眼睑水肿、湿疹等,停止接触可逐渐消退。各种抗结核药物均可以发生。 毒性反应发生机制 ●毒性反应是由于药物剂量过大或用药时间过长对机体产生的有害作用。 ●毒性反应可分为急性和慢性。 ●减少剂量和缩短用药时间可以防止毒性反应的发生。 ●毒性反应一般是可逆的。 常用药物的主要不良反应—异烟肼 1)周围神经炎:四肢感觉异常,肌肉痉挛等。 2)中枢症状:欣快感,兴奋,记忆力减退,抑郁,中毒性脑病,癫痫发作等。 3)肝脏损害:转氨酶升高,极少有黄疸出现,发生急性肝坏死或肝萎缩者更为罕见。 4)分泌失调:男性乳房增大,柯兴氏综合症,月经不调,阳萎等。 5)血液系统:贫血,白细胞、血小板减少等。 6)过敏反应:皮疹,药物热。 7)胃肠道反应:恶心,呕吐,腹泻,便秘等。 常用药物的主要不良反应—利福类 1)肝损害:多为一过性转氨酶升高,可出现黄疸,亦可引起急性坏死性肝炎。 2)胃肠道反应:恶心,呕吐,腹痛,腹泻等。 3)过敏反应:用于间歇疗法或治疗间断后再用药时易发生过敏反应。表现为流感样综合征等。 4)血液系统反应:骨髓抑制,白细胞、血小板减少;急性溶血性贫血。 5)神经系统:头晕,头痛,疲倦等。 6)其它副反应:血压升高,心律失常,关节肿胀。 常用药物的主要不良反应—吡嗪酰胺 1)肝损害:PZA的肝毒性与剂量、疗程有关。用量大、疗程长不良反应较多见。表现为肝肿大,压痛,转氨酶升高,偶可因肝坏死而造成死亡。 2)关节痛:PZA的代产物吡嗪酸能抑制肾小管对尿酸的清除作用,使尿酸升高,停药48小时恢复正常。 3)胃肠道反应:食欲不振,恶心,呕吐。 4)过敏反应:偶见发热、皮疹、对光过敏、皮肤暴露部位呈鲜红色。 常用药物的主要不良反应—乙胺丁醇 1)表现为:视力下降,视野缩小,眼球运动疼痛,干燥感,异物感,辨色力减弱等 2)其他神经系统反应::周围神经炎,表现为下肢麻木,异物爬行感,感觉过敏及活动障碍,个别可出现听神经损害,听力障碍,声带麻痺等。 3)过敏反应:皮疹,严重可到剥脱性皮炎,血小板减少性紫癜,支气管痉挛导致呼吸困难、过敏性休克等。
标准操作规程 STANDARD OPERATING PROCEDURE 一、目的:规范境外发生的严重药品不良反应处理操作规程。 二、责任:药物警戒总负责人及ADR专员 三、范围:适用于本公司境外发生的严重药品不良反应处理操作规程的确认。 四、内容: 1、进口药品和国产药品在境外发生的严重药品不良反应(包括自发报告系统收集的、上市后临床研究发现的、文献报道的),药品生产企业应当填写《境外发生的药品不良反应/事件报告表》,自获知之日起30日内报送国家药品不良反应监测中心。国家药品不良反应监测中心要求提供原始报表及相关信息的,药品生产企业应当在5日内提交。 2、进口药品和国产药品在境外因药品不良反应被暂停销售、使用或者撤市的,药品生产企业应当在获知后24小时内书面报国家食品药品监督管理局和国家药品不良反应监测中心。 3、收集或获知境外发生的药品不良反应后,要立即进行核实与调查。 3.1药品不良反应报告的确认 通过各种途径收集的药品不良反应,应进行确认。需要确认的内容主要包括:是否为有效报告、是否在报告范围之内、是否为重复报告等。 3.1.1有效报告 首先应确认是否为有效报告。一份有效的报告应包括以下四个元素(简称四要素):可识别的患者、可识别的报告者、怀疑药品、不良反应。如果四要素不全,视为无效报告,应
补充后再报。 “可识别”是指能够确认患者和报告者存在。当患者的下列一项或几项可获得时,即认为患者可识别:姓名或姓名缩写、性别、年龄(或年龄组,如青少年、成年、老年)、出生日期、患者的其他识别代码。提供病例资料的初始报告人或为获得病例资料而联系的相关人员应当是可识别的。对于来自互联网的病例报告,报告者的可识别性取决于是否能够核实患者和报告者的存在,如提供有效的电子邮箱或者其他联系方式。 3.1.2报告范围 对于来自上市后研究或有组织的数据收集项目中的不良反应,经报告者或持有人判断与药品存在可能的因果关系,应该向监管部门报告。其他来源的不良反应,包括监管部门反馈的报告,无论持有人是否认为存在因果关系,均应向监管部门报告。 文献报告的不良反应,可疑药品如确定为本持有人产品,无论持有人是否认为存在因果关系,均应报告;如果确定非本持有人产品的则无需报告。如果不能确定是否为本持有人产品的,应在定期安全性更新报告中进行讨论,可不作为个例不良反应报告。 如果文献中提到多种药品,则应报告怀疑药品,由怀疑药品的持有人进行报告。怀疑药品由文献作者确定,通常在标题或者结论中作者会提及怀疑药品与不良反应之间的因果关系。如果报告人认为怀疑药品与文献作者确定的怀疑药品不同,可在报告的备注中说明。 4、详细了解境外严重药品不良反应的发生、药品使用、患者诊治以及药品生产、储存、流通、既往类似不良反应等情况。 同时,根据省严重药品不良反应/事件处置管理规定,迅速开展生产自查,分析和控制、处理;调查、分析、处理情况应及时报省食品药品监督管理局,抄送市食品药品监督管理局。必要时应当暂停生产、销售、使用和召回相关药品,并报所在地省级药品监督管理部门。
药品不良反应/ 事件报告表 首次报告□跟踪报告□编码: 报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□
药品不良反应/ 事件报告表示例 首次报告□跟踪报告□编码:
1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。 2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。 3. 新的□严重□一般□ (1)新的药品不良反应:是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。 根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应: 1) 导致死亡; 2)危及生命; 3)致癌、致畸、致出生缺陷; 4)导致显著的或者永久的人体伤残或者器官功能的损伤; 5)导致住院或者住院时间延长; 6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 (3)一般:指新的、严重的药品不良反应以外的所有不良反应。 4. 单位名称:必须填写单位的完整全称,如日照市人民医院。 5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。 6. 电话:填写报告部门(即科室)的电话。 7. 报告日期:指上交不良反应/事件报告的时间。新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。有随访信息的,应当及时报告。 8. 患者姓名:填写患者真实全名。 9. 体重:以千克为单位。如果不知道准确体重,请做一个最佳的估计。 10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。 11. 家族药品不良反应/事件及既往药品不良反应/事件情况:请选择正确选项。如果选择“有”,则在报告的空白处清晰叙述。 12. 不良反应/事件名称:应填写不良反应中最主要、最明显的症状。 13. 不良反应/事件发生时间:应填写发生不良反应/事件的确切时间。 14. 病历(门诊)号:请如实填写,便于查找病例,具体分析不良反应/事件。 15. 不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况: 不良反应过程描述应具体、规范,须体现出“3个时间、3个项目和2个尽可能”。 *3个时间:①不良反应发生的时间;②采取措施干预不良反应的时间;③不良反应终结的
药品不良反应报告流程 一般的ADR/ADE病例报告流程 发现ADR/ADE病例 填写ADR/ADE报告表 于发现之日起10日内向ADR监测组报送报告表 分类整理报告表 ADR/ADE病例分析评价~签署关联性评价意见 将关联性评将ADR/ADE报告按规定时限 价意见反馈表信息输入ADR上报市ADR 报告者监测组报告表数监测中心 (以书面形式) 据库 新的、严重的ADR/ADE病例报告流程 发现新的、严重的ADR/ADE病 例 立即填写ADR/ADE报告表 于发现之日起7日内向ADR监测组报送报告表 分类整理报告表 组织专家分析评价~签署关联性评价意见 将ADR/ADE报告将关联性评于发现之日 表信息输入ADR价意见反馈起15日内上 监测组报告表数报告者报市ADR监据库 (以书面形式) 测中心 死亡的、群体性的ADR/ADE病例报告流程 发现死亡的、群体性的ADR/ADE病例 立即报告ADR监测组、医务处
立即报告市ADR立即组织核查 监测中心和行政主管部门及时填写报告表 及时向ADR监测组报送报告表 及时分类整理报告表 及时填写报告表 及时组织专家分析评价~ 签署关联性评价意见 将ADR/ADE报告将关联性评及时报告市表信息输入ADR价意见反馈ADR监测中 监测组报告表数报告者心 据库 (以书面形式) 下面是诗情画意的句子欣赏,不需要的朋友可以编辑删除!! 谢谢!!!!! 1. 染火枫林,琼壶歌月,长歌倚楼。岁岁年年,花前月下,一尊芳酒。水落红莲,唯闻玉磬,但此情依旧。 2. 玉竹曾记凤凰游,人不见,水空流。 3. 他微笑着,在岁月的流失中毁掉自己。
4. 还能不动声色饮茶,踏碎这一场,盛世烟花。 5. 红尘嚣浮华一世转瞬空。 6. 我不是我你转身一走苏州里的不是我。 7. 几段唏嘘几世悲欢可笑我命由我不由天。 8. 经流年梦回曲水边看烟花绽出月圆。 9. 人生在世,恍若白驹过膝,忽然而已。然,我长活一世,却能记住你说的每一话。 10. 雾散,梦醒,我终于看见真实,那是千帆过尽的沉寂。 11. 纸张有些破旧,有些模糊。可每一笔勾勒,每一抹痕迹,似乎都记载着跨越千年万载的思念。 12. 生生的两端,我们彼此站成了岸。 13. 缘聚缘散缘如水,背负万丈尘寰,只为一句,等待下一次相逢。 14. 握住苍老,禁锢了时空,一下子到了地老天荒 15. 人永远看不破的镜花水月,不过我指间烟云世间千年,如我一瞬。 16. 相逢一醉是前缘,风雨散,飘然何处。 17. 虚幻大千两茫茫,一邂逅,终难忘。相逢主人留一笑,不相识,又何妨。 18. 天下风云出我辈,一入江湖岁月催;皇图霸业谈笑间,不胜人生一场醉。 19. 得即高歌失即休,多愁多恨亦悠悠,今朝有酒今朝醉,明日愁来明日愁。 20. 直道相思了无益,未妨惆怅是清狂。 21. 看那天地日月,恒静无言;青山长河,世代绵延;就像在我心中,你从未离去,也从未改变。 22. 就这样吧,从此山水不相逢。 23. 人天自两空,何相忘,何笑何惊人。
药品不良反应相关应急预案及程序 1 2020年4月19日
药品不良反应/事件应急预案及处理程序 一、发生药品不良反应应急预案及处理程序 (一)应急预案 1、应严格适应症,出现不良反应停药报告医生并遵医嘱处理。 2、若为一般过敏反应,情况好转者可继续观察并做好记录。 3、患者在注射或输液时发生反应,如心悸、胸闷、呼吸困难、寒战、面色苍白、皮疹、发热等,就地抢救,必要时行心肺复苏。 4、出现休克者,行抗休克治疗 5、记录患者生命体征、一般情况和抢救过程。 6、及时报告药剂科、护理部。 7、患者家属有异议时,立即按有关程序对输液器具和药物进行封存。 (二)处理程序 停药→报告医生并遵医嘱处理→就地抢救→观察患者生命体征→记录抢救过程→及时上报→保留药物→送检 临床治疗中一旦发现出现药品不良反应,原则上应立即停药,并立即值班医生,同时报告护士长、科主任,停药期间应观察患者,采取简易的处理方法。根据医嘱进行处理,情况严重者立即抢救。 2 2020年4月19日
如怀疑药品质量问题,应与药剂科联系,由药学人员、医护人员共同进行相关药物的封存工作。如发生输液反应时,应将撤下的输液器形成密闭状态,并用无菌治疗巾包裹,标明时间,冷藏备检。 临床科室发现不良反应,填写《药品不良反应报告》,及时报告给药剂科不良反应监督员,并将未填齐项目填写完整。若不良反应症状仍未愈,药学人员将负责继续检测事件发展,并负责与病人沟通进行情况进展登记。 药品不良反应报告时限不良反应发生后各部门需在一周内上报至药剂科,药剂科不良反应监测员及时到科室调查,并将发生情况按月向区药品监督管理局上报。严重不良反应,科室及时上报给药剂科,药品监测员在一周内在线报告国家药品不良反应监测网。死亡病例最快速度及时上报。 出现严重的药品不良反应,应立即停药,给予积极治疗,尽最大可能降低对患者的不利影响,向科室主任报告详细情况,按规定时限填写《药品不良反应报告表》,并将情况分别报告医务科及药剂科。药剂科组织相关人员进行病历讨论,究其不良反应与可疑药品的相关性,若与药品相关,分析是药品质量、多种药物相互作用,还是由于患者自身等原因造成,整理总结后通报全院。 药学人员有义务对医师及患者进行药品不良反应信息的传达和用药安全知识的宣传。 3 2020年4月19日
淮北百缘近效期药品处理方案 一、门店现状 因门店实际销售状况不佳,部分药品滞销,造成药品效期将至,急需销售或退货,为处理门店近效期药房,特制定本方案予以解决。 有效期2年以上的的商品低于8个月的为近效期品种;有效期2年内的商品低于6个月为近效期 二、解决途径 1、进货计划 门店进货计划由班长安排营业员制定,遵循提前备货原则,避免断货现象。营业员须在每个星期一和星期四之前上交计划表(附表1)给班长,由班长核对点菜(因人员有限,暂时由店长报人力资源部,由电脑员代为点菜)。原则:门店单个药品的库存数量不要超过此种药品3个月的销售总量 2、门店点菜 按批号点菜。报计划时按系统供应链中所显示药品所能提供的最好效期进行点菜,如出现效期都不理想的情况,则点少量药品以保证药品不缺货即可,并在计划本上标记。电脑员需在计划本里注明详细情况,如库存为零、效期不好等。如同一药品连续三次点菜库存为零,则反馈至店长处理。 3、药品拒收(涉及成本) 4、工作分工责任化 药品的效期管理责任到人(参照卫生责任区划分:附表1),不定期检查柜台内药品情况,对于有效期2年以上,距离失效期10个月;有效期2年内,距离失效期8个月的药品及时填写在近效期药品一览表(附表2)中,并填报催销表(附表3),及时将信息反馈给店长。店长上报经理办公室,五天内制定相应促销计划,由经理报总公司批准执行。 经理办公室组织每月检查两次(搭配卫生检查——附表4:卫生责任区划分),并进行不定期抽查。如在检查中发现未按上述规定执行的,前两次对责任区员工口头警告,第三次以后,每次按药品零售价的20%的罚款; 若出现药品已经过期还没有申报的情况,经理办公室负全责。 5、近效期产品的促销计划针对不同品种的近效期药品,由经理办公室制定详细的促销计划,由总经理报公司总部审批执行。减少近效期药品的滞销和退货。 6、退货销售、促销均无进展,达到公司总部规定的近效期退货时限药品,店长在每月的1-5号做好退货近效期品种的统计与收集,并报到人力资源部。电脑员在5-10号内上报退货计划给总部业务部审批。待总部审批后由物流托运回总部。 7、报损:回总部沟通篇二:医药公司近效期药品管理规定 医药公司近效期药品管理规定 1.目的:为加强近效期药品管理,保证在合格品库区内没有超过有效期的药品,计算机系统中的药品有效期信息与库内药品有效期信息一致,防止过期失效品销售出库,特制定本管理规定。 2.范围:适用于本公司购进、存储、销售的药品有效期的监控管理。 3.定义: 3.1药品有效期:本规定所称的药品有效期是指在规定的储存条件下,能保证其质量的期限: 3.2近效期药品:本规定所称的近效期是指: (1)药品有效期大于两年(含两年),其距离有效期限只有一年的药品; (2)药品有效期在一年半或一年之内(含一年),且距离有效期限只有三个月的药品。 4.内容: 4.1 购进药品有效期期限的要求 4.1.1采购部门在购进药品时应向供应商明确本公司对购进药品有效期期限的要求。 4.1.2购进药品的有效期期限一般不得低于一年(含一年)。
新的、严重的药品不良反应报告 登记与处理程序 (试行) 1.目的:明确药品不良反应病例报告登记要求,分类办法,登记范围,规范报告登记与处理过程,确保新的、严重药品不良反应报告工作的顺利进行,制订本程序。 2.责任者:药品不良反应监测岗位的工作人员。 3.依据:《药品不良反应报告和监测管理办法》、《河南省药品不良反应报告和监测管理办法实施细则》。 4.登记制度: 各市级中心监测机构要建立药品不良反应报告登记制度,收到报告后进行登记。 适用范围:本文件适用于药品不良反应分析评价过程中所有的新的和严重的病例报告。 药品不良反应报告登记内容应包括:报告编码、药品通用名称、患者姓名、报告单位、报告时间、收到时间、上报时间、生产企业、药品批号、不良反应名称、报告类别。新的一般和新的严重需要注明新的不良反应名称。严重的需要注明转归情况。 药品不良反应报告实行分类登记制,按“新的一般”、“严重的”和“新的严重”进行登记。 5.处理程序 每天要按时登陆全国药品不良反应监测网络,查看是否有上报的新的
或严重的不良反应报告。 依据《药品不良反应报告和监测管理办法》、《河南省药品不良反应报告和监测管理办法实施细则》中规定的报告时限,确认不良反应报告的上报时限是否符合规定的时限要求。不符合规定的转入退回程序。 根据该怀疑药品说明书,分析不良反应报告是否属于新的或严重的不良反应,如属一般的不良反应报告则修改完善,按照一般报告的上报程序进行上报。 对于新的或严重的不良反应报告,应认真核对报告的真实、完整、准确性及填写内容,缺少项目,内容填写不祥,或填写不正确的,必须及时与报告单位或报告人联系,复核报告内容,补充资料。 如在规定时间内未收到补充资料,应敦促报告单位及时上报补充资料。无法补充资料的,予以退回并登记。 对报告进行关联性评价。 新的或严重的不良反应应于15日内报告,市级中心于接到报告之日起3日内审核、评价上报省级中心,省级中心于3日内审核上报国家中心。死亡病例及时上报,同时抄报河南省食品药品监督管理局和河南省卫生厅。 对项报告时限超期的不良反应病例报告,应予以退回,并进行退回登记(登记表见药品不良反应病例报告退回制度-附件)。 对项不符合要求的报告,应及时退回便于报告单位补充资料,并进行退回登记,同时与报告人或市级中心评价人员联系进行说明。 所有合格的新的和严重的病例报告在上报之前要进行登记(登记表见新的、严重药品不良反应报告登记与处理程序-附件)。 6.附件:新的、严重的药品不良反应病例报告登记表(电子表)
药品及医疗器械不良反应监测报告制度和流程 加强药品和医疗器械的安全监管,严格药品和医疗器械不良反应监测工作的管理,确保人体用药安全有效,依据《中华人民共和国药品管理法》及《药品不良反应监测与报告管理办法》,结合本院实际,特制定本制度。 一、各临床科室主任为药品和医疗器械不良反应监测工作的管理人员,负责本科室使用的药品和医疗器械的不良反应情况监测、收集、报告和管理工作。医务科、药房负责全院药品不良反应的监测、收集、报告管理工作。 二、报告范围:药品和医疗器械不良反应报告的范围为药品和医疗器械引起的所有可疑不良反应。 三、报告及处理程序 ○1本院对所使用的药品和医疗器械的不良反应情况进行监测,各岗位(医生、护士、药师)要积极配合做好药品和医疗器械不良反应监测工作,一经发现可疑药品不良反应,应当立即向科主任汇报,填写《药品不良反应/事件报告表》(见附表),并报告至医院药品和医疗器械不良反应监测员(医务科、药房),然后逐级上报。此外,对于新的、严重的不良反应应积极救治患者,做好医疗记录,保存好相关药品、物品的留样,分析查找问题,将损害降至最低。 ○2本院发现可疑药品和医疗器械不良反应群体病例,应当积极救治患者,迅速开展临床调查,分析事件发生的原因,必要时可采取暂停药品的使用等紧急措施,立即向当地药品监督管理
部门报告,同时填写《药品群体不良事件基本信息表》(见附表3)。 ○3发现药品和医疗器械说明书中未载明的可疑严重不良反应病例应当在15日内报告,其中死亡病例须立即报告。其他药品不良反应应当在30日内报告。有随访信息的,应当及时报告。 ○4发现非本院所使用的药品引起的可疑药品不良反应,发现者可直接向当地药品监督管理部门报告。 ○5经核实确认某批号药品发现不良反应或药品监督管理部门已确认有药品不良反应的药品,单位药品质量负责人应立即通知仓库管理员,停止该批号药品发出,就地封存,并及时追回已发出的药品等紧急控制措施。 四、未经当地药品监督管理部门允许的药品不良反应监测资料,任何单位和个人不得向国内外机构、组织、学术团体或个人提供。 五、对新发现的、严重的药品和医疗器械不良反应应进行重点监测,进一步了解药品的临床使用和不良反应发生情况,研究不良反应的发生特征、严重程度、发生率等,开展的药品安全性监测活动。 六、医院鼓励各科室积极及时上报药品不良反应,其上报情况纳入科室评先评优的指标之一。 七、定义: ○1药品和医疗器械不良反应,是指合格药品和医疗器械在正常用法用量下出现的与用药目的无关的有害反应。
附表1 药品不良反应 / 事件报告表 首次报告:√跟踪报告 □ 编码: 报告类型:新的□ 严重□一般√报告单位类别:医疗机构√ 经营企业□生产企业□ 个人□其他□ 患者姓名:王彦性别: 男女√ 出生日期: 1943 年2 月12日 或年龄: 民族:汉 体重 (kg): 56 联系方式: 137******** 原患疾病:胆囊结石慢性胆囊炎医院名称:大安 市第四医院 病历号/门诊 号:20162069 既往药品不良反应/事件:有□ 无 □ 不详√ 家族药品不良反 应/事件:有□ 无□ 不详√ 相关重要信息:吸烟史□ 饮酒史□ 妊娠期□ 肝病史□ 肾病史□ 过敏史√ 其他□ 药品批准文号 商品名 称 通用名 称 (含剂 型) 生产厂家生产批号 用法用量 (次剂 量、途 径、日次 数) 用药起 止时间 用药 原因 怀H20080329 加罗宁注射用扬子江药16030241 5毫克,2016辅助
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡; 2)危及生命; 3)致癌、致畸、致出生缺陷; 4)导致显著的或者永久的人体伤残或者器官功能的损伤; 5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 新的药品不良反应:是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。 报告时限 新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应 30日内报告。有随访信息的,应当及时报告。 其他说明 怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。 并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。 用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。 报告的处理 所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
药品不良反应监测报告制度和流程 加强药品的安全监管,严格药品不良反应监测工作的管理,确保人体用药安全有效,依据《中华人民共和国药品管理法》及《药品不良反应监测与报告管理办法》,结合本院实际,特制定本制度。 一、各临床科室主任为药品不良反应监测工作的管理人员,负责本科室使用的药品的不良反应情况监测、收集、报告和管理工作。医务科、药房负责全院药品不良反应的监测、收集、报告管理工作。 二、报告范围:药品不良反应报告的范围为药品引起的所有可疑不良反应。 三、报告及处理程序 ○1本院对所使用的药品的不良反应情况进行监测,各岗位(医生、护士、药师)要积极配合做好药品不良反应监测工作,一经发现可疑药品不良反应,应当立即向科主任汇报,填写《药品不良反应/事件报告表》(见附表),并报告至医院药品不良反应监测员(医务科、药房),然后逐级上报。此外,对于新的、严重的不良反应应积极救治患者,做好医疗记录,保存好相关药品、物品的留样,分析查找问题,将损害降至最低。 ○2本院发现可疑药品不良反应群体病例,应当积极救治患者,迅速开展临床调查,分析事件发生的原因,必要时可采取暂停药品的使用等紧急措施,立即向当地药品监督管理部门报告,同时填写《药品群体不良事件基本信息表》(见附表3)。 ○3发现药品说明书中未载明的可疑严重不良反应病例应
当在15日内报告,其中死亡病例须立即报告。其他药品不良反应应当在30日内报告。有随访信息的,应当及时报告。 ○4发现非本院所使用的药品引起的可疑药品不良反应,发现者可直接向当地药品监督管理部门报告。 ○5经核实确认某批号药品发现不良反应或药品监督管理部门已确认有药品不良反应的药品,单位药品质量负责人应立即通知仓库管理员,停止该批号药品发出,就地封存,并及时追回已发出的药品等紧急控制措施。 四、未经当地药品监督管理部门允许的药品不良反应监测资料,任何单位和个人不得向国内外机构、组织、学术团体或个人提供。 五、对新发现的、严重的药品不良反应应进行重点监测,进一步了解药品的临床使用和不良反应发生情况,研究不良反应的发生特征、严重程度、发生率等,开展的药品安全性监测活动。 六、医院鼓励各科室积极及时上报药品不良反应,其上报情况纳入科室评先评优的指标之一。 七、定义: ○1药品不良反应,是指合格药品在正常用法用量下出现的与用药目的无关的有害反应。 ○2药品不良反应报告和监测,是指药品不良反应的发现、报告、评价和控制的过程。 ○3严重药品不良反应,是指因使用药品引起以下损害情形之一的反应: 1.导致死亡;
药品效期管理制度 1、效期药品是根据有关规定,表明有效期限的药品。 2、加强效期药品的管理师保证药品使用安全的重要措施之一,个部门要安排专业的人员负责效期药品的管理,防止药品过期失效而造成损失。 3、对于效期药品,库房根据需要有计划的采购,药房也应该根据临床使用情况适量领用,即防止缺货,又防止积压。 4、采购和领用药品要查验效期,凡有效期在六个月内的药品,不得验收入库,特殊情况须经科主任批准。 5、药品上架陈列、堆垛码放要按照效期远近存放,并根据药品性质和贮藏要求分类储存,科学养护。药品出库和调剂要遵循“先进先出”、“近期先出”和“按批号发放”的原则。 6、库房、药房在每个季度末进行盘点时要检查药品的效期,建立效期药品登记簿,而且易于辨识。对于效期药品实施动态监控。凡有效期在六个月内的药品纳入监控范围,悬挂状态标示,每月清点乙烯,三个月之内的纳入重点监控范围。 7、临近效期药品处理流程: ①库房存有接近三个月的药品可退库,或更换新批号,或与临床科室联系。,采取措施,近期药品在规定期限内使用完。在效期药品登记簿中登记处置结果。 ②病区临近效期又暂不用的药品,直接到药房调换远期批号或退回病房,由处置记录。 ③临近效期的库房药品和药房退回的近效期的药品,由药库负责处置。 ④药库对于有效期六个月内的药品及时与销售公司取得联系,适时调换;对于市场经常脱销的药品,要保留合理库存,以免造成浪费。 8、药品在有效期限内发生变色、变质或其它质量异常情况的,不得调剂使用。药品一旦超过有效期限,应立即停止使用并封存,按规定作报废处理。 9、因工作失职,至药品过期失效造成损失的,视情节轻重给予责任部门或者责任人经济处罚。
1.目的:加强本院药品的安全使用和监管,确保病人安全。 2.范围:全院医疗工作人员。 3.定义: 3.1药品不良反应:指合格药品在正常用法用量下出现的与用药目的无关的或意外的有害反应。包 括:副作用、毒性反应、后遗作用、过敏反应、特异质反应、致畸、致癌、致突变反应等。 3.2严重的药品不良反应:指因使用药品引起以下损害情形之一的反应: ①导致死亡; ②危及生命; ③致癌、致畸、致出生缺陷; ④导致显著的或者永久的人体伤残或者器官功能的损伤; ⑤导致住院或者住院时间延长; ⑥导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。 3.3可疑不良反应:指怀疑而未确定的不良反应。 3.4新的药品不良反应:指药品说明书中未载明的不良反应。 4.相关文件 无 5.内容: 5.1药品不良反应上报流程图 5.2根据政策和法规,医院须成立药品不良反应监测小组。
5.2.1药品不良反应小组职责 ①结合本单位实际情况制定相应的药品不良反应报告、处理和监测的工作制度及考核制度。 ②负责组织本单位药品不良反应的教育和培训。 ③组织本单位不良反应监测的学术活动和相关科研过程。 ④配合各级药监局对本单位新的、严重、突发、群发、影响较大并造成严重后果的药品不良 反应的调查,并执行处理决定。 ⑤负责配合政府有关部门对相关不良反应/事件临床资料的调查。 ⑥负责对药品不良反应报告处理制度的监督实施,同时向有关部门汇报。 5.3药品不良反应的报告 5.3.1药品不良反应监测是药品不良反应的检出、处理、评价、上报和预防。各科药品不良反应监测人员负责本科室药品不良反应的监测和上报,不良反应监测小组根据上报数据制定预防措施。 5.3.2药品不良反应实行逐级、定期报告。发现可疑的严重药品不良反应必须及时报告,必要时可以越级报告。 5.3.3报告范围包括药品使用所引起的所有可疑不良反应。 5.3.4全院工作人员,在临床工作中一旦发现药品引起的可疑不良反应,有义务报告药品不良反应兼职人员,由兼职人员通过本院不良反应上报系统及时上报。 5.3.5发现药品说明书中未载明的可疑严重不良反应病例,必须由发现人以及时有效方式报告药品不良反应监测小组,由监测小组成员报告给国家不良反应监测中心,最迟不得超过72小时。 5.3.6发现药品说明书中未载明的其他可疑药品不良反应和已载明的所有药品不良反应病例,由发现人员从医院“病人安全通报系统”中的“不良反应上报系统”进行报告,不良反应监测小组成员分析后通过网络上报国家药品不良反应监测系统。 5.3.7新药监测期内的药品应报告该药品发生的所有不良反应;新药监测期已满的药品,报告该药品引起的新的和严重的不良反应。 5.3.8药品不良反应上报系统的填报应真实、完整、准确。 5.3.9监测小组每月汇总、整理不良反应报告情况,报药剂科主任。每年汇总一次,写出书面报告,上报区药品不良反应监测中心。 5.3.10医院药事管理委员会指定药品不良反应监测小组负责组织医院医疗、药学专家研究药品不良反应预防工作、药品不良反应的教育和培训工作等。
新的严重药品不良反应 报告登记与处理程序 Document number【SA80SAB-SAA9SYT-SAATC-SA6UT-SA18】
新的、严重的药品不良反应报告 登记与处理程序 (试行) 1.目的:明确药品不良反应病例报告登记要求,分类办法,登记范围,规范报告登记与处理过程,确保新的、严重药品不良反应报告工作的顺利进行,制订本程序。 2.责任者:药品不良反应监测岗位的工作人员。 3.依据:《药品不良反应报告和监测管理办法》、《河南省药品不良反应报告和监测管理办法实施细则》。 4.登记制度: 各市级中心监测机构要建立药品不良反应报告登记制度,收到报告后进行登记。 适用范围:本文件适用于药品不良反应分析评价过程中所有的新的和严重的病例报告。 药品不良反应报告登记内容应包括:报告编码、药品通用名称、患者姓名、报告单位、报告时间、收到时间、上报时间、生产企业、药品批号、不良反应名称、报告类别。新的一般和新的严重需要注明新的不良反应名称。严重的需要注明转归情况。 药品不良反应报告实行分类登记制,按“新的一般”、“严重的”和“新的严重”进行登记。 5.处理程序
每天要按时登陆全国药品不良反应监测网络,查看是否有上报的新的或严重的不良反应报告。 依据《药品不良反应报告和监测管理办法》、《河南省药品不良反应报告和监测管理办法实施细则》中规定的报告时限,确认不良反应报告的上报时限是否符合规定的时限要求。不符合规定的转入退回程序。 根据该怀疑药品说明书,分析不良反应报告是否属于新的或严重的不良反应,如属一般的不良反应报告则修改完善,按照一般报告的上报程序进行上报。 对于新的或严重的不良反应报告,应认真核对报告的真实、完整、准确性及填写内容,缺少项目,内容填写不祥,或填写不正确的,必须及时与报告单位或报告人联系,复核报告内容,补充资料。 如在规定时间内未收到补充资料,应敦促报告单位及时上报补充资料。无法补充资料的,予以退回并登记。 对报告进行关联性评价。 新的或严重的不良反应应于15日内报告,市级中心于接到报告之日起3日内审核、评价上报省级中心,省级中心于3日内审核上报国家中心。死亡病例及时上报,同时抄报河南省食品药品监督管理局和河南省卫生厅。 对项报告时限超期的不良反应病例报告,应予以退回,并进行退回登记(登记表见药品不良反应病例报告退回制度-附件)。 对项不符合要求的报告,应及时退回便于报告单位补充资料,并进行退回登记,同时与报告人或市级中心评价人员联系进行说明。