
第十一章 含氮化合物
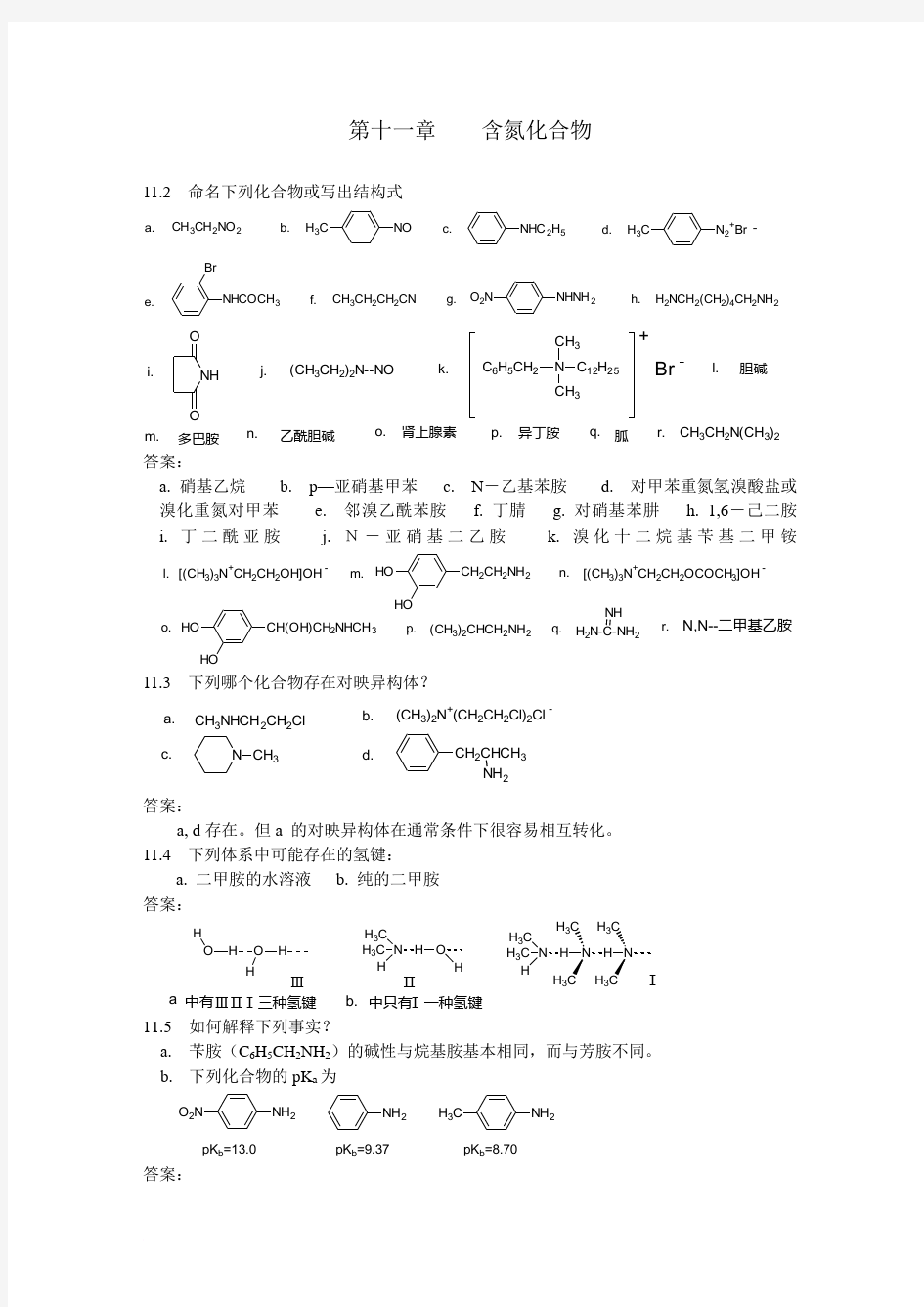
11.2 命名下列化合物或写出结构式
a.
CH 3CH 2NO 2
b.
NO H 3C
c.
NHC 2H 5 d.
H 3C
N 2+Br -
e.
Br
NHCOCH 3
f.
CH 3CH 2CH 2CN
g.
NHNH 2
O 2N
h.
H 2NCH 2(CH 2)4CH 2NH 2
i.
NH O
O
j.
(CH 3CH 2)2N--NO
k.
C 6H 5CH 2
N CH 3CH 3
C 12H 25+
Br -
l.胆碱
m.
多巴胺
n.
乙酰胆碱
o.
肾上腺素
p.
异丁胺
q.胍
r.
CH 3CH 2N(CH 3)2
答案:
a. 硝基乙烷
b. p —亚硝基甲苯
c. N -乙基苯胺
d. 对甲苯重氮氢溴酸盐或溴化重氮对甲苯
e. 邻溴乙酰苯胺
f. 丁腈
g. 对硝基苯肼
h. 1,6-己二胺
i. 丁二酰亚胺
j. N-亚硝基二乙胺
k. 溴化十二烷基苄基二甲铵
[(CH 3)3N +CH 2CH 2OH]OH -
m.HO
CH 2CH 2NH 2
n.
l.[(CH 3)3N +
CH 2CH 2OCOCH 3]OH -
o.HO
HO
CH(OH)CH 2NHCH 3
p.
(CH 3)2CHCH 2NH 2
r.
N,N--二甲基乙胺
q.
H 22
NH
11.3 下列哪个化合物存在对映异构体?
a.CH 3NHCH 2CH 2Cl
b.(CH 3)2N +(CH 2CH 2Cl)2Cl -
c.
N CH 3
d.
CH 2CHCH 3
2
答案:
a, d 存在。但a 的对映异构体在通常条件下很容易相互转化。 11.4 下列体系中可能存在的氢键:
a. 二甲胺的水溶液
b. 纯的二甲胺 答案:
H
H O H
H
N H 3C
H 3C H N H 3C
H 3C H N H H 3H 3H 3H 3 Ⅰ
Ⅱ
Ⅲ
a 中有
Ⅲ Ⅱ Ⅰ Ⅰ 三种氢键 b. 中只有一种氢键
H H
11.5 如何解释下列事实?
a. 苄胺(C 6H 5CH 2NH 2)的碱性与烷基胺基本相同,而与芳胺不同。
b. 下列化合物的pK a 为
O 2N
NH 2
NH 2
H 3C
NH 2
pK b =13.0
pK b =9.37
pK b =8.70
答案:
a. 因为在苄胺中,N未与苯环直接相连,其孤对电子不能与苯环共轭,所以碱性与烷基
胺基本相似。
O 2N
NH 2
--NH 2H 3C
NH 2--NH 2中,硝基具有强的吸电子效应。中N 上孤对电子更多地偏向苯环,
所以与苯胺相比,其碱性更弱。
b.中,甲基具有一定的给电子效应,中N 上而所以与苯胺相比,其碱性略强.使电子云密度增加,
11.6 以反应式表示如何用(+)-酒石酸拆分仲丁胺? 答案:
+_
CH 3CH(NH 2)CH 2CH 3
酒石酸
(+)胺(+)酸盐胺(+)
酸盐
(-)
拆分,而后再分别加 NaOH 析出胺.
物理性质不同可
11.8 下列化合物中,哪个可以作为亲核试剂?
a. H 2NNH 2
b. (C 2H 5)3N
c. (CH 3)2NH
d.
N
e.
N CH 3
f.
NHCH 3
g. (CH 3)4N
+
h.
N CH 3+
答案:
a, b, c, d, e, f 11.9 完成下列转化:
a.NH 2
b.
NH 2
NH 2
O 2N
c.C H 3C O O H
C H 3C O N H 2
d.
CH 3CH 2OH
CH 3CHCH 2CH 3NH 2
NH 2NHCOCH 3
e.
NO 2
N Br
NH 2
N
f.
CH 3
g.
N -H 3C HO
N
答案:
a.HNO 3H 2SO 4
NO 2
Fe HCl
NH 2
b.
NH 2
(CH 3CO)2O
NHCOCH 3
HNO 3NHCOCH O 2
N
H
+
NH 2
O 2N
c.
CH 3COOH (CH 3CO)2O NH 3CH 3CONH 2CH 3COOH 2CH 3COCl
NH 3
CH 3CONH 2
CH 3COOH
3
CH 3COO -
NH 4
CH 3CONH 2
d.
CH 3CH 2OH
CrO 3(Py)2
CH 3CHO
32+
CH 3CH(OH)CH 2CH 3
SOCl 2
CH 3CHCH 2CH 3
CH 3CHCH 2CH 3
NH 2
HCl CH 32Cl
Et 2O
CH 3CH 2MgCl
1)
NH O O
KOH
NK O
O
NCH
O
O CH 3CHCH 2CH 3
CH 3CH +CH 3CHCH 2CH 3
Cl
2NH 2
(CH 3CO)2O NHCOCH 3
NO 2
Fe HCl
NH 2
2
Fe HCl NH 2
Br
NaNO 2HCl
N 2+N
Br
NH 2
N
e.f.
++0
弱CH 3
g.
3
CH 3
O 2N Fe HCl
+CH 3
H 2N NaNO 2HCl
N 2+
Cl
-
H 3C
OH
N
-H 3C
HO
N
11.10
写出
N H
(四氢吡咯)及N CH 3
(N -甲基四氢吡咯)分别与下列试剂反应的主要产
物(如果能发生反应的话)。
a. 苯甲酰氯
b. 乙酸酐
c. 过量碘甲烷
d. 邻苯二甲酸酐
e. 苯磺酰氯
f. 丙酰氯
g. 亚硝酸
h. 稀盐酸 答案:
N H
N
N CH 3
a.C
O b.N
C
O H 3C
c.N
H 3CH 3+ d.
N
C
O COOH
N H 3CH 3
+e.CH 3CH 2
N
C O
×
×
×
×
×
N H
N CH 3
f.N S
O O
g.
N N H 3H
+h.N H 3C
+N H 2
+
Cl -H
Cl -Ⅰ_Ⅰ_NO 2_
11.11 用化学方法鉴别下列各组化合物:
a. 邻甲苯胺 N -甲基苯胺 苯甲酸和邻羟基苯甲酸
b. 三甲胺盐酸盐 溴化四乙基铵 答案:
a.
CH 3
NH 2
NHCH 3
COOH
COOH OH
(B)
(C)
(D)
B
D
A
B
D
C
b.
(CH 3)3N .HCl
(A)
(CH 3CH 2)4N +
Br -(B)
AgNO 3
A
或者用NaOH
A
分层
B均相
由于三甲胺b. p. 3℃,可能逸出,也可能部分溶于NaOH,所以用AgNO 3 作鉴别较好. 11.12 写出下列反应的主要产物:
a.(C 2H 5)3N
+CH 3CHCH 3
Br
b.
[(CH 3)3N +
CH 2CH 2CH 2CH 3]Cl -
+NaOH
c.CH3CH2COCl+NHCH3
H3C
d.
N(C2H5)2
+HNO2
答案:
a.(C2H5)3N+CH3CHCH3
Br (C2H5)3N+CH
CH3
CH3
Br-
b.[(CH3)3N+CH2CH2CH2CH3]Cl-+NaOH[(CH
3
)3N+CH2CH2CH2CH3]+Cl-+Na++OH-
c.CH3CH2COCl+CH3
NHCH3
H3C CH3CH2CON
CH3 d.
N(C2H5)2
+HNO2
N(C2H5)2
NO
11.13N-甲基苯胺中混有少量苯胺和N,N-二甲苯胺,怎样将N-甲基胺提纯?
答案:使用Hinsberg反应.(注意分离提纯和鉴别程序的不同
)
A
NHCH3
B
NH2
C
N
H3C CH
2
CH3
2
CH3
3
(D)
(E)
E 有机相N
CH
SO2CH3
(D)
+
CH3
。
3
纯A
11.14 将下列化合物按碱性增强的顺序排列:
a. CH3CONH2
b. CH3CH2NH2
c. H2NCONH2
d. (CH3CH2)2NH
e. (CH3CH2)4N+OH-
答案:
碱性 e > d > b > c > a
11.15 将苄胺、苄醇及对甲苯酚的混合物分离为三种纯的组分。
CH 2NH 2
(A)
CH 2OH
CH 3
HO
A B
的钠盐
的盐酸盐B
A
HCl
C
11.16 分子式为C 6H 15N 的A ,能溶于稀盐酸。A 与亚硝酸在室温下作用放出氮气,并得到几种有机物,其中一种B 能进行碘仿反应。B 和浓硫酸共热得到C (C 6H 12),C 能使高锰酸钾退色,且反应后的产物是乙酸和2-甲基丙酸。推测A 的结构式,并写出推断过程。 答案:
Ω=
6 2+2+1-152
=0
饱和胺
B 具有CH 3CH
C 4H 9
OH
(可进行碘仿反应)
C
(C 6H 12)
KMnO 4
CH 3COOH +CH 3CHCOOH
3
所以C 为CH 3CH=CHCH
CH 3
CH 3
倒推回去
B CH 3CHCH 2CH
CH 3CH 3A
CH 3CHCH 2CH
NH 23CH 3
╳
第十二章 含硫和含磷有机化合物
12.2 将下列化合物按酸性增强的顺序排列:
SO 3H
SH
SH
OH
a.
b.
c.
d.
答案:
酸性
SO 3H
>
SH
>
SH
>
OH
12.3 写出下列反应的主要产物:
a.
SCH 2CHCOOH
NH 2SCH 2CHCOOH
2
[H]
b.SH +KOH
c.
CH 2SH CHSH CH 2OH
+HgO
d.CH 3CH 2CH 2CH 2SH
HNO 3
e.S S
HNO 3
f.SH
O 2g.SO 3H
H 3C
PCl 3
h.
CH 3(CH 2)4CH 2SH
NaOH
答案:
a.
SCH 2CHCOOH
NH 2SCH 2CHCOOH
2
[H]
HSCH 2CHCOOH
NH 2
b.SH +KOH
SK c.
CH 2SH CHSH CH 2OH
+HgO
CH 2S CHS CH 2OH
Hg
d.CH 3CH 2CH 2CH 2SH
HNO 3
CH 3CH 2CH 2CH 2SO 3H
e.S S
HNO 3
SO 3H
f.SH
O 2S
S g.SO 3H
H 3C
PCl 3SO 2Cl
H 3C
h.
CH 3(CH 2)4CH 2SH
NaOH
CH 3(CH 2)4CH 2SNa
12.6 由指定原料及其它无机试剂写出下列合成路线。
a. 由CH 3CH 2CH 2CH 2OH 合成CH 3CH 2CH 2CH 2SO 2CH 2CH 2CH 2CH 3
b.
由合成CH 3H 3C
SO 2NH CH 3
答案:
a.
CH 3CH 2CH 2CH 2OH
HCl
CH 3CH 2CH 2CH 2Cl
Na 2S
CH 3CH 2CH 2CH 2SCH 2CH 2CH 2CH 3
3CH 2CH 2CH 2SO 2CH 2CH 2CH 2CH 3
b.
CH 3浓24SO 3H NO 2
CH 3
HNO 324H 3C H 3C
Fe +NH 2
3
C
SO 2NH
H 3C
CH 3
KMnO 4
33PCl 3
SO 2Cl 3C
含硫和含磷有机化合物第十五章 写出下列化合物的结构式:.1 (2 (1)硫酸二乙酯)甲磺酰氯)磷酸三苯酯)对硝基苯磺酸甲酯(4(3 -二氯代乙硫醚2 (6),2')对氨基苯磺酰胺(5 (7)二苯砜)环丁砜(8 9()苯基亚膦酸乙酯)苯基亚膦酰氯(10 答案: OO(1)(2)S ClCH S CHCHCHOOCH33322OOO(4)(3)OOPOCHSNO 323O(6)(5)O ClSCHCHCHClCH NHSNH222222OO(7)(8)SSOOO(10)(9)OOH PCl CHOCHP32H : .命名下列化物 2. 答案: )对甲苯环)对羧基苯磺酸(4)巯基乙醇(2)巯基乙酸(3 (1)氯化)碘化环已基二甲基锍(7已基二甲基锍(5)乙硫革甲醇(6)甲)苯基膦酸二乙酯(10N-甲基对甲苯磺酰胺(9四羟甲基磷(8)基乙基氯膦
:.用化学方法区别下列化合物3 答案:不发),HSH(乙硫醇(1)可以用氨水处理,能产生沉淀的为 C-AgNO523). 二甲硫醚SCH(生反应的是CH33为的泡产生气处用NaHCO水溶液理,能可(2)以CO23(甲基磺酸甲CHCHSOH(CHCHSO乙基硫醇),不产生气泡的为323333酯)。(甲CHSCHHSCH氨水处理,3 ()可以用能产生沉淀的为-AgNO3223 SCHCHHOCH硫基乙硫醇),不产生气泡的为(甲基硫基乙醇)。322. )可以用水处理,在室温下发生剧烈反应,产生热效应的为4(COClCH3(对甲苯甲酰氯),而几乎不发生明显反应,出ClSOHC32. 现水与油分层现象的为(对甲苯磺酰氯)4. 试写出下列反应的主要 产物: 答案:(1)+3HCl3+POCl CHOHCHOOP 3333O(2) r H n-CBP n-C-CO)HPHO)(n(+n-CH9423949494(3)CHS2HClCHC+HCHOHCSHHS(CH)CH 6565322SCN2(4)1:1SH+OHCHHSCH222O(5)Li n-CH(1)94CH)S(CH+LiBr
Compounds containing sulfur and phosphorus
含硫和含磷有机化合物的类型和命名; 含硫有机化合物的制法和性质; 有机硫试剂在合成上的应用; 膦、季钅 粦盐的制法和性质; 硫、磷叶立德在有机合成中的应用。 有机硫试剂在合成上的应用; Wittig试剂在合成上的应用。
§15-1 电子结构和成键特征
1 硫、磷的电子构型 O:1s22s22p4 N:1s22s22p3 相似:
ROH SH RSH
S:1s22s22p63s23p43d0 P:1s22s22p63s23p33d0
价电子层的结构相似,可形成结构相似的化合物
OH R O R' R R O C S C H(R') H(R') O R C OH S R C OH
R S R'
醇
酚
醚
醛酮
酸
RNH2
伯胺
R2NH
仲胺
R3N
叔胺
R4NX
季铵盐
RPH2
伯膦
R2PH
仲膦
R3P
叔膦
R4PX
季鏻盐
差异: P比N 、S比O ① 多一层电子,原子半径大 电负性较小 核对外层电子束缚力小 极化变形性(亲核性)大 2P 3P 轨道大小不匹配,侧面交叠小。
C C S P
不稳定 不存在
聚合
C S
S C
C S
② 除3s,3p轨道上的价电子可参与成键外, 能量相近的3d空轨道也可参与成键 P : sp3d杂化-5个单键(PCl5) S: sp3d2杂化-6个单键(SF6)
O R S R' R O S O R' R O S OH R O S O O (O H ) 2 (R O ) 3 P = O R P (O R ') 2 OH
→ 高氧化态化合物
O R P
. 第一章《认识有机化合物》 第一节有机化合物基础第1课时有机化合物的分类 【学习目标】掌握有机化合物分类的一般方法 【学习重点】有机物的常见类别 【学习难点】官能团分类法 【基础扫描】全员参与巩固基础 一、有机化合物的基本特征 1、有机物的定义:组成中含有元素的化合物统称有机物 【注意】⑴有机化合物的组成中必须含有碳元素,但是组成中含有碳元素的化合物,却不一定都是有机物。例如:、、、、 这几类物质组成中都含有碳元素,但是都不是有机化合物 ⑵有机化合物通常又被简称为有机物,它们均为化合物,即有机物中不存在单质 2、有机物的组称元素:有机物的组成元素,除外,通常还含有 等非金属元素 3、有机物的结构特点 ⑴有机物分子中碳原子间均以结合形成或,这是有机物结构的基础 ⑵有机物分子之间均通过结合形成 4、有机物的数量特点 有机物种类繁多,达上千万种。其原因是: ⑴碳原子有个价电子,能与其它原子形成个 ⑵有机物分子中碳原子之间能以、、 三种不同的方式形成共价键,且碳原子之间又能以或的方式结合,形成有机物的基本骨架结构 ⑶有机物中普遍存在现象 5、有机物的性质特点 ⑴溶解性:大多数有机物难溶于,易溶于(如、、等) ⑵可燃性:绝大多数有机物 ⑶耐热性:多数有机物较低,受热易 ⑷导电性:绝大多数有机物为,不能,不易 ⑸化学反应:有机化学反应都比较,一般反应速率,多数需要使用,并常伴有发生【练习1】下列叙述正确的是() A、有机物一定来自有机体内 B、有机物与无机物可以相互转化 C、CO属于有机物 D、AB + CD ==AC +BD 一定属于复分解反应【练习2】下列物质中不属于有机物的是() A、NaCN B、CH3COOH C、甲烷 D、SiC 【练习3】决定有机物种类繁多的原因,不正确的是() A、碳原子间可以有多种排列方式 B、碳原子有4个价电子,可与其他原子形成4个共价键 C、碳原子之间的成键方式较多 D、有机物分子中,碳原子间只能排列成链状 【练习4】人类已知的化合物种类最多的是() A、第I A族元素的化合物 B、第III A族元素的化合物 C、第IV A族元素的化合物 D、第VII A族元素的化合物 【练习5】有机化学主要研究有机化合物所发生的反应,下列化合物中不是有机物的是() A、CO2 B、C2H6 C、HCHO D、CH3OH 【练习6】自然界中化合物的种类最多的是() A、无机化合物 B、有机化合物 C、铁的化合物 D、碳水化合物【练习7】下列物质属于有机物的是() A、Na2CO3 B、CaC2 C、CO(NH2)2 D、CO 【练习8】目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确的是() A、碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键 B、碳原子性质活泼,可以跟多数元素原子形成共价键 C、碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键 D、多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合 【练习9】下列物质属于有机物的是() A、氰化钾(KCN) B、氰酸铵(NH4CNO) C、尿素(NH2CONH2) D、碳化硅(SiC) 【练习10】第一位人工合成有机物的化学家是() A、门捷列夫 B、维勒 C、拉瓦锡 D、牛顿 【练习11】有机化学的研究领域是() ①有机物的组成②有机物的结构、性质③有机合成④有机物应用
第十五章 含硫、含磷有机化合物 教学目的: 了解一些常见的含磷有机化合物,熟悉硫醇、硫酚、硫醚,膦酸和膦酸酯类,磷酸酯和硫代磷酸酯类命名规则,掌握硫醇、硫酚、硫醚的物理和化学性质。 教学重点: 含硫和含磷有机化合物主要作为有机合成试剂使用。 教学难点: 如何理解含硫、含磷有机化合物的特性问题。 第一节含硫有机化合物 一、结构类型与命名 S 原子可形成与氧相似的低价含硫化合物。如:R-SH 硫醇 R-S-R 硫醚C 6H 5-SH 硫酚 —SH 官能团,叫做硫氢基或巯(音求)基。硫醇、硫酚、硫醚等含硫化合物的命名较简单,可在相应的含氧衍生物类名前加上“硫”字即可。例如: 甲硫醇 CH 3SH 2-丙硫醇 (CH 3)2CHSH 二甲硫醚 CH 3SCH 3 2,2‘-二氯二乙硫醚 ClCH 2CH 2SCH 2CH 2Cl 苯甲硫醚 C 6H 5SCH 3 如果-SH 作为取代基命名时,则与其他官能团的命名原则相同。例如: 巯基乙酸 HS-CH 2-COOH 2-氨基-3-巯基丙酸 HS-CH 2-CH(NH 2)-COOH 亚砜、砜、磺酸及其衍生物的命名,也只需在类名前加上相应的烃基名称就可以。例如: CH 3-S-CH 3O S O O S O O OH CH 3 S O O Cl CH 3 S O O H 2N NH 2二甲亚砜 二苯砜 甲磺酸 对甲苯磺酸 对甲苯磺酰氯 对氨基苯磺酰胺 S O O CH 3OH
二、硫醇、硫酚 1. 物理性质和制法 沸点低于相应的含氧化合物,因其极性:S 第一章认识有机化合物 【高考新动向】 【考纲全景透析】 一、有机化合物的分类 1.按碳的骨架分类 链状化合物:如CH3CH2CH2CH3、CH3CH=CH2、HC≡CH等(1)有机化合物脂环化合物:如?, 环状化合物芳香化合物:如 2.按官能团分类 (1)官能团:决定化合物特殊性质的原子或原子团 又:链状烃和脂环烃统称为脂肪烃。 二、有机化合物的结构特点 1.有机化合物中碳原子的成键特点 (1)碳原子的结构特点 碳原子最外层有4个电子,能与其他原子形成4个共价键. (2)碳原子间的结合方式 碳原子不仅可以与氢原子形成共价键,而且碳原子之间也能形成单键、双键或三键.多个碳原子可以形成 长短不一的碳链和碳环,碳链和碳环也可以相互结合,所以有机物种类纷繁,数量庞大.2.有机化合物的同分异构现象 (1)概念 化合物具有相同的分子式,但具有不同结构的现象叫同分异构现象.具有同分异构现象的化合物互为同分异构体. (2)同分异构体的类别 ①碳链异构:由于分子中烷基所取代的位置不同产生的同分异构现象,如正丁烷和异丁烷; ②位置异构:由于官能团在碳链上所处的位置不同产生的同分异构现象,如1丁烯和 2丁烯; ③官能团异构:有机物分子式相同,但官能团不同产生的异构现象,如乙酸和甲酸甲酯; ④给信息的其他同分异构体:顺反异构,对映异构. 3.同分异构体的书写方法 (1)同分异构体的书写规律 ①烷烃 烷烃只存在碳链异构,书写时应注意要全面而不重复,具体规则如下:成直链,一条线;摘一碳,挂中间,往边移,不到端;摘二碳,成乙基;二甲基,同、邻、间. ②具有官能团的有机物 一般书写的顺序:碳链异构→位置异构→官能团异构. ③芳香族化合物 取代基在苯环上的相对位置具有邻、间、对3种. ⑵常见的几种烃基的异构体数目 (1)—C3H7:2种,结构简式分别为: CH3CH2CH2—、 (2)—C4H9:4种,结构简式分别为: ⑶同分异构体数目的判断方法 ①基元法 如丁基有四种,则丁醇、戊醛、戊酸等都有四种同分异构体. ②替代法 如二氯苯(C6H4Cl2)有三种同分异构体,四氯苯也有三种同分异构体(将H替代Cl);又如CH4的一氯代物只有一种,新戊烷[C(CH3)4]的一氯代物也只有一种. ③等效氢法 等效氢法是判断同分异构体数目的重要方法,其规律有: a.同一碳原子上的氢等效; b.同一碳原子上的甲基氢原子等效; 第十五章含硫含磷有机化合物 [目的要求]: 1.掌握硫、磷原子的成键特征,了解含硫、含磷有机化合物的类型和命名。 2.掌握硫醇、硫酚、硫醚、亚砜和砜的制法、性质及有机硫试剂在有机合成上的应用。 3.掌握磺酸制法和性质,了解其衍生物的制法和性质。 4.掌握膦、季鏻盐的制法和魏悌希反应。 5.了解一些有机磷农药。 [教学内容]: 第一节硫、磷原子的成键特征 第二节含硫有机化合物 第三节有机硫试剂在有机合成上的应用 第四节磺酸及其衍生物 第五节含磷有机化合物 §15-1 S、P原子的成键特征 一、电子构型 1.核外电子排布 N 22S21S2 2S22 3P3; O:1S22S2 2P4;S:1S2 2S2 2P63S2 3P4; N7P15O8S16 2.比较 它们能形成相似的共价化合物: R —OH 醇, R 3N 胺; R —SH 硫醇, R 3P 膦 二、P - P π键 1.P -2P π键 (C=O ; C=C ; C=N ) 2.2P -3P π(C=S ) 三、3d 轨道参与成键 1.S 电子跃迁到3d 轨道上,形成由S 、P 、d 轨道组合成的杂化轨道,参与成键。 2.用它的空3d 轨道,接受外界提供的未成键电子对(P 电子对)填充其空轨道,而形成一类新的π键,它是由d 轨道和P 轨道相互重叠而形成的,所以叫做d - P π。(图15-1) 原子体积 电负性 受核的束缚力 和C 成键 O 、N 较小 较大 较大 2P —2P π S 、P 较大 较小 较小 2P —3P π + ++--+ - 四、与胺类似的含S 、P 有机物 §15-2 含硫有机物 一、低价含硫化合物——硫醇、硫酚和硫醚 1.结构和命名 S 原子可形成与氧相似的低价含化合物。—SH 官能团,叫做硫氢基或巯(音求)基。 2.制备 ⑴ 硫醇 硫脲 异硫脲盐 R-S H SH R-S -R 硫醚 硫酚 硫醇 +RX NaSH NaX 乙醇△ +RX S C NH 2 NH 2+△乙醇S C NH 2 R H 2O OH - H 2S RCH 2CH 2SH +RCH=CH 2ThO 2 R-OH +H 2S R-S H +H 2O 400 ℃ 1 23 叔胺 1 23 R 4季铵盐氧化叔胺 1 2 R 3 1 23叔膦 1 23 R 4 季鏻盐 氧化叔膦 1 2 R 3 1 2硫醚 1 23铳盐 亚砜 1 2 第一节有机化合物的分类 [核心素养发展目标] 1.宏观辨识与微观探析:通过认识官能团的结构,微观分析有机物的类别,体会与宏观分类的差异,多角度认识有机物。2.证据推理与模型认知:了解碳原子之间的连接方式,能根据碳原子的骨架对有机物进行分类。 一、按碳的骨架分类 1.按碳的骨架分类 2.相关概念辨析 (1)不含苯环的碳环化合物,都是脂环化合物。 (2)含一个或多个苯环的化合物,都是芳香化合物。 (3)环状化合物还包括杂环化合物,即构成环的原子除碳原子外,还有其他原子,如氧原子(如 呋喃)、氮原子、硫原子等。 (4)链状烃通常又称脂肪烃。 例 1有下列7种有机物,请根据元素组成和碳的骨架对下列有机物进行分类: ⑥ (1)属于链状化合物的是________(填序号,下同)。 (2)属于环状化合物的是________。 (3)属于脂环化合物的是________。 (4)属于芳香化合物的是________。 答案(1)④⑤(2)①②③⑥⑦(3)①③⑥(4)②⑦ 【考点】按碳的骨架分类 【题点】环状化合物 二、按官能团分类 1.烃的衍生物及官能团的概念 (1)烃的衍生物:从结构上看,烃分子中的氢原子被其他原子或原子团所取代而衍生出一系列新的化合物。 (2)官能团:决定化合物特殊性质的原子或原子团。 2.有机物的主要类别、官能团和典型代表物 (1)烃类物质 有机物官能团结构官能团名称有机物类别 CH4烷烃 CH2===CH2碳碳双键烯烃 CH≡CH—C≡C—碳碳三键炔烃 芳香烃 (2)烃的衍生物 有机物官能团结构官能团名称有机物类别 CH3CH2Br —Br 溴原子卤代烃 CH3CH2OH —OH 羟基醇 —OH 羟基酚 CH3—O—CH3醚键醚CH3CHO —CHO 醛基醛 羰基酮 CH3COOH —COOH 羧基羧酸 酯基酯 —NH2氨基 氨基酸 —COOH 羧基 酰胺基酰胺 例 【复习内容】 1、有机化合物的分类 2、官能团 3、有机化合物碳原子的成键特点 4、有机物的同分异构现象 5、有机物同分异构体的书写 6、有机物的命名 7、有机物分离提纯的方法 8、元素分析与相对分子质量的测定 9、分子结构的鉴定 ☆知识点1 有机化合物的分类 组成元素:除含碳元素外,通常还含有 、 、 、硫、磷、卤素等元素。 1、烃按碳架形状分类 、按官能团分类 【对点训练1】 下列物质中不属于有机物的是 ( ) A. 四氯化碳 B. 醋酸 C. 乙炔 D. 足球烯(C 60) 【对点训练2】写出下列官能团或有机基团的名称或符号 —OH________ —CHO________ —COOH_______ 醚键____ 酯基______ 羰基________ 氨基_________ 碳碳双键_______ 碳碳三键________________- 苯基_______ 乙基_______亚甲基_______ (提示:苯基和烃基不属于官能团...........) 【对点训练3】有机物的分类 现有以下几种有机物,请根据按官能团的不同对其进行分类。 (13) (14 (15)CH 3CH 2-O-CH 2CH 3 链烃(脂肪烃) 环烃 烃 如: 如: 通式: 如: 通式: 如: 通式: 如: 饱和链烃: CH 2 —CH 3 ①属于脂肪烃 ; ②属于芳香化合物 ③属于芳香烃 ;④属于卤代烃 ⑤属于醇 ; ⑥属于羧酸 ⑦属于酯______________________;⑧属于醚 ⑨属于酚 ; ⑩属于醛 ☆知识点2 有机化合物的结构特点 1、碳原子最外层有4个电子,可以形成 键、 键、 键。 2、碳原子之间可以连成 状, 状;链和环上都可以带支链、也可以不带支链。 3、许多有机物还存在同分异构现象和同分异构体。(掌握同分异构体概念) 【对点训练4】键线式可以简明扼要的表示碳氢化合物, 这种键线式表示的物质是 A .丁烯 B .丙烷 C .丁烷 D .丙烯 ☆知识点3 烃的命名 1、习惯命名法 碳原子数≤10,依次用甲、乙、丙、丁、 、 、 、 、壬、癸表示。如辛烷。 2、系统命名法 ①选主链,定“某烷”: 分子里最长的碳链。----------------最长 ②定起点,标编号: 主链中离支链较近的一端 ----------最近,最多,最小。 ③把支链作为取代基,写名称 -------- 取代基写在前。相同基,合并算;不同基,简到繁。 例: 3、烯烃、炔烃的命名规则 与烷烃比较:①选择有 的最长链为主链; ②用编号指出 的位置。 ③官能团的编号 (大于、小于)侧链取代基的编号。 【对点训练5】右图有机物的正确命名为 ( ) A .2-乙基-3,3-二甲基戊烷 B .3,3-二甲基-4-乙基戊烷 C .3,3,4-三甲基己烷 D .2,3,3-三甲基已烷 【对点训练6】 下列命名中正确的是 ( ) A .3—甲基丁烷 B .2,2,4,4—四甲基庚烷 C .1,1,3—三甲基戊烷 D .3 - 甲基 - 3—丁烯 ☆知识点4 同系物,同分异构体 1、同系物: 相似,分子组成上相差若干个 原子团的有机物属于同系物。 提示:①结构相似; ②官能团种类和个数相等;③相差若干个CH 2;④属于同类物质,通式相同。 2、同分异构现象 相同, 不同的现象。 烷烃的碳链异构:CH 3 CH 2CH 2CH 3 和CH 3CH (CH 3)CH 3 第一节硫磷原子的成键特征 价电子层构型 O 2S22p4 S 3S23P43d0 N 2S22P3 p 3S23P33d0 1. 由于价电子层构型类似,所以硫、磷原子可以形成与氧、氢相类似的共价键化合物。 醇胺硫醇膦 2. 由于3P轨道比2P轨道比较扩散,它与碳原子的2P轨道的相互重叠不如2P 轨道之间那样有效,以硫、磷原子难以和碳原子形成稳定的P—Pπ键。 如硫醛和硫酮,除了少数芳香硫酮(二苯硫酮)之外,一般不稳定,易于二聚,三聚或多聚成为只含σ键的化合物 3. 硫,磷除了利用3S,3P电子成键外,还可以利用能量上相接近的空3d轨道参 与成键。 3d轨道参与成键有两种方式,一种是s电子跃迁到3d轨道上,形成由s. p. d电子组合而成的杂化轨道 磷原子 sp3d杂化形成五个共价单键 PCl 5 硫原子 sp3d2杂化形成六个共价单键 SF 6 另一种方式是利用它的空3d轨道,接受外界提供的未成键电子对形成 d—Pπ键,如:亚砜,砜,磷酸酯都是含有这种d-Pπ键。 4 硫,磷原子常取sp3杂化态,与胺类似具有四方体构型 叔胺叔膦硫醚 季铵盐季膦盐锍盐 氧化叔胺氧化叔膦亚砜 第二节含硫有机化合物的主要类型和命名 一结构类型 硫原子可以形成与氧相似的低价含硫化合物 硫醇硫酚硫醚 二硫化物亚砜砜 次磺酸亚磺酸磺酸[][] 硫醛硫酮硫代羧酸 硫脲异硫氰酸酯黄原酸酯 二命名 含硫化合物的命名,只需在相应的含氧衍生物类名前加上“硫”字即可。 如: 异丙硫醇 2.2-二氯二乙硫醚 -SH作取代基命名时,与其他官能团的命名原则相同。 巯基乙酸 亚砜、砜、磺酸及其衍生物的命名,也只需在类名前加上相应的烃基就可以了。 二甲亚砜对甲苯磺酸环丁砜 对甲苯磺酰氯对氨基苯磺酰胺 第三节有机硫化合物的性质及在有机合成上的应用 1 硫醇和硫酚 ① 制备 硫脲法 第48讲 认识有机化合物 1.根据分子中碳骨架的形状分类 2.按官能团分类 (1)烃的衍生物:烃分子里的__氢原子__被其他__原子或原子团__取代后的产物。 (2)官能团:决定有机化合物特殊性质的__原子或原子团__。 (3)有机物的主要类别、官能团和典型代表物 __( —C≡C— 溴乙烷C2H __( __ (羰基) __( ____( 1.判断正误,正确的划“√”,错误的划“×”。 (1)CH3CH2CH3既属于链状烃又属于脂肪烃。( √) (2)含有羟基的物质只有醇或酚。( ×) (3)含有醛基的有机物一定属于醛类。( ×) (4)都属于酚类。( ×) (5)含有苯环的有机物属于芳香烃。( ×) 2.按官能团的不同,可以对有机物进行分类,请指出下列有机物的类别,填在横线上。 (1)CH3CH2CH2OH__醇__。(2)__酚__。 (3)__芳香烃__。(4)__酯__。 (5)CCl4__卤代烃__。(6)CH2===CH—CH===CH2__烯烃__。 (7)__羧酸__。(8)CH3CHO__醛__。 有机物的分类与常见官能团的识别 与官能团有关的易错点 (1)醇和酚的结构差别就是羟基是否直接连在苯环上,如属于醇类,则属于酚类。 (2)官能团的书写必须注意规范性,例如碳碳双键为“”,而不能写成“C===C”,碳碳三键为“—C≡C—”,而不能写成“C≡C”,醛基应为“—CHO”,而不能写成“—COH”。 (3)含有醛基的有机物不一定属于醛类,如甲酸甲酯等。 [例1]东晋葛洪《肘后备急方》一书中有“青蒿一握,以水二升渍,绞取汁,尽服之,治疟疾”,《本草纲目》亦有“青蒿治疟疾寒热”之说。医学研究表明其药理作用是青蒿中的青蒿素,青蒿素、双氢青蒿素的结构简式如图,下列有关说法不正确的是( B) A.青蒿素中含有酯基和醚键 B.青蒿素的化学式为C15H21O5 C.青蒿素的某些同分异构体既属于酯又属于多元酚 D.青蒿素在一定条件下可以转化为双氢青蒿素,该过程发生了还原反应 认识有机化合物 一、有机化合物的分类 1.按碳的骨架分类 2.按官能团分类 (1)官能团:决定化合物特殊性质的原子或原子团。 (2)有机物的主要类别、官能团和典型代表物 类别官能团代表物名称、结构简式 烷烃甲烷CH4 烯烃(碳碳双键) 乙烯H2C CH2 炔烃—C≡C—(碳碳三键) 乙炔HC≡CH 芳香烃苯 卤代烃—X(卤素原子) 溴乙烷C2H5Br 醇—OH(羟基) 乙醇C2H5OH 酚苯酚C6H5OH 醚(醚键) 乙醚 CH3CH2OCH2CH3 醛 (醛基) 乙醛CH3CHO 酮(羰基) 丙酮CH3COCH3 羧酸 (羧基) 乙酸CH3COOH 酯 (酯基) 乙酸乙酯 CH3COOCH2CH3 氨基酸 —NH2(氨基) —COOH(羧基) α-氨基乙酸 H2N—CH2—COOH 硝基 化合物 —NO2(硝基) 硝基苯 (1)芳香化合物与脂环化合物的主要区别:是否含有苯环等芳香环。 (2)醇和酚的官能团均为羟基(—OH),区别:羟基是否与苯环直接相连。 (3)含醛基的物质不一定为醛类,如HCOOH、HCOOCH3、葡萄糖等。 (4)苯环不是官能团,但是含有苯环的化合物具有特殊的性质。 二、有机化合物的结构特点 1.有机化合物中碳原子的成键特点 2.有机物结构的表示方法 名称结构式结构简式键线式 丙烯CH3CH CH2 乙醇CH3CH2OH 乙酸CH3COOH 3.同分异构现象和同分异构体 同分异构现象化合物具有相同的分子式,但结构不同,因而产生性质上的差异的现象 同分异构体具有同分异构现象的化合物互为同分异构体 类型碳链异构 碳链骨架不同 如CH3—CH2—CH2—CH3和位置异构官能团位置不同 第一节 认识有机化合物 考纲定位 1.能根据有机化合物的元素含量、相对分子质量确定有机化合物的分子式。2.了解常见有机化合物的结构。了解有机物分子中的官能团,能正确地表示它们的结构。3.了解确定有机化合物结构的化学方法和物理方法(如质谱、红外光谱、核磁共振氢谱等)。4.能正确书写有机化合物的同分异构体(不包括手性异构体)。5.能正确命名简单的有机化合物。6.了解有机分子中官能团之间的相互影响。 考点1| 有机物的分类与结构 (对应学生用书第206页) [考纲知识整合] 1.有机物的分类 (1)根据元素组成分类 有机化合物? ?? ?? 烃:烷烃、烯烃、炔烃、苯及其同系物等 烃的衍生物:卤代烃、醇、酚、醛、羧酸、酯等 (2)根据碳骨架分类 (3)按官能团分类 ①烃的衍生物:烃分子里的氢原子被其他原子或原子团所代替,衍生出一系列新的有机化合物。 ②官能团:决定化合物特殊性质的原子或原子团。 ③有机物的主要类别、官能团 有机物类别官能团名称官能团结构 典型代表物 (结构简式) 烯烃碳碳双键CH2===CH2 炔烃碳碳三键CH≡CH 卤代烃卤素原子—X CH3CH2Cl 醇醇羟基—OH CH3CH2OH 酚酚羟基—OH 醚醚键CH3CH2OCH2CH3醛醛基CH3CHO、HCHO 酮羰基 羧酸羧基 酯酯基CH3COOCH2CH3 氨基酸氨基、羧基—NH2、—COOH (1)有机化合物中碳原子的成键特点 (2)有机物的同分异构现象 a.同分异构现象:化合物具有相同的分子式,但结构不同,因而产生了性质上的差异的现象。 b.同分异构体:具有同分异构现象的化合物互为同分异构体。 (3)同系物 [高考命题点突破] 命题点1 有机物的分类 1.下列物质的类别与所含官能团都正确的是( ) B[A项,羟基连在苯环上的有机物才称为酚,该有机物属于醇类,错误;B项,该物质 第1节认识有机化合物石油和煤重要的烃 1.了解有机化合物中碳的成键特征。 2.了解甲烷、乙烯、苯等有机化合物的主要性质及应用。 3.了解氯乙烯、苯的衍生物等在化工生产中的重要作用。 4.掌握常见有机反应类型。 5.了解有机化合物的同分异构现象,能正确书写简单有机化合物的同分异构体。 甲烷、乙烯、苯的结构和性质 [知识梳理] 1.有机化合物 (1)有机化合物:是指含碳元素的化合物,但含碳化合物CO、CO2、碳酸及碳酸盐属于无机物。 (2)烃:仅含有碳、氢两种元素的有机物。 (3)烷烃:碳原子与碳原子之间以单键构成链状,碳的其余价键全部被氢原子饱和,这种烃称为饱和链烃,也称为烷烃。 2.甲烷、乙烯、苯的比较 烃甲烷乙烯苯 结构式 (或结构 简式) 结构特点碳原子间以单键结合 成链状,剩余的价键 被氢原子“饱和” 分子结构中含有碳碳双键 苯环含有介于碳碳单键 和碳碳双键之间的独特 的键 空间 构型 正四面体形平面形平面正六边形 物理性质无色气体,难溶于水 无色具有特殊气味的透 明液体,密度比水小, 难溶于水 化学性质①稳定性:与强酸、 强碱和强氧化剂等一 般不发生化学反应。 ②燃烧反应的化学方 程式:CH4+ 2O2――→ 点燃 CO2+ 2H2O。 ③取代反应:在光照 条件下与Cl2反应生 成一氯甲烷的化学方 程式:CH4+Cl2――→ 光照 CH3Cl+HCl,同时还 发生取代反应生成二 氯甲烷、三氯甲烷和 四氯化碳 ①燃烧反应的化学方程式: C2H4+3O2――→ 点燃 2CO2+2H2O; 现象:火焰明亮且伴有黑烟。 ②氧化反应:通入酸性KMnO4 溶液中,现象为溶液紫红色退 去。 ③加成反应:通入溴的四氯化 碳溶液中,反应的化学方程式: CH2==CH2+ Br2――→CH2BrCH2Br; 现象:溶液颜色退去。 与H2反应的化学方程式: CH2==CH2+H2――→ 催化剂 △ CH3CH3。 与HCl反应的化学方程式: CH2==CH2+HCl―→CH3CH2OH。 与H2O反应的化学方程式: CH2==CH2+H2O――→ 一定条件 CH3CH2Cl ④加聚反应的化学方程式: n CH2==CH2――→ 引发剂 ①稳定性:不能与酸性 KMnO4溶液反应,也不 与溴水(或溴的四氯化 碳溶液)反应。 ②取代反应 a.卤代反应 苯与液溴发生溴代反应 的化学方程式为 。 b.硝化反应 化学方程式为 。 ③加成反应 苯和H2发生加成反应的 化学方程式为 。 ④燃烧反应 化学方程式:2C6H6+ 15O2――→ 点燃 12CO2+ 6H2O; 现象:火焰明亮,带浓 烟 用途作燃料,制有机溶剂瓜果催熟剂,重要的化工原料重要的有机化工原料,作有机溶剂 (1)烷烃的结构与性质 通式C n H2n+2(n≥1) 结构链状(可带支链)分子中碳原子呈锯齿状排列;碳原子间以单键相连,其余价键均被氢原子饱和 特点一个碳原子与相邻四个原子构成四面体结构;1 mol C n H2n+2含共价键的数目是(3n+1)N A 课题:第一章认识有机化合物专题复习(第1课时) 备课组长: 学习目标: 1、了解有机物的两种分类方法,掌握常见官能团的结构和名称。 2、掌握同分异构体的含义,会判断同分异构体,能正确写出有机物的同分异构体。 3、掌握烃基的概念及烃基的书写,掌握烷烃、烯烃、炔烃及苯的同系物的命名规则,并会判断正确与否。 4、了解研究有机物的一般步骤和方法,掌握蒸馏、重结晶、萃取等分离、提纯有机物的原理和操作步骤。了解质谱、红外光谱、核磁共振氢谱的作用。 学习重点、难点:有机物的命名及同分异构体的书写方法。 【知识链接】整体建构知识网络 饱和链烃:如:烷烃(通式:)代表物 链烃 不饱和链烃C=C脂肪烃烃,官能团 脂环烃:如 环烃 芳香烃:如 分类卤代烃:代表物,官能团 醇:代表物,官能团 酚:代表物,官能团 醚:代表物,官能团 有烃的衍生物 机醛:代表物,官能团 物 酮:代表物,官能团 羧酸:代表物,官能团 酯:代表物,官能团 有机物中碳原子的成键特点: 结构特点定义: 同分异构现象异构,如 分类异构,如 异构,如 习惯命名法 有命名烷烃命名步骤: 机系统命名法烯烃、炔烃命名步骤: 物苯的同系物命名步骤: 基本步骤:分离、提纯→确定→确定→确定 蒸馏 分离、提纯重结晶 研究有机萃取 物的步骤定义: 和方法确定方法:分子中各元素原子的个数比 实验式各元素的质量分数之比 = 方法各原子的相对原子质量之比 实验式 分子式确定 相对分子质量——质谱法 红外光谱 分子结构鉴定 核磁共振谱 【学习过程】 一、烃基和官能团 烃基和官能团不但是有机化学中的重要概念,而且是有机物分类的依据和决定该化合物化学特性的关键结构部分。 *应掌握的烃基除甲基、乙基外,还应知道: 第三章重要的有机化合物 第一节认识有机化合物(第一课时)教案 莒县实验高中姜丹莹 一、学情分析本章教材作为高中有机化学的第一章,起着连接初中有机化学和高中有机化学的“纽带”作用。对于学生而言,一切都是新的,兴趣是最好的老师。学习有机化学时,学生没有任何框架,因此我们可以在开始时不断提高学生的学习兴趣,而不要一味追求难度。 二、教学设想有机化合物在自然界中广泛存在,与人类的生活、生产紧密关联。有机化合物的种类繁多、性质各异,本节以甲烷的性质为核心,让学生通过最简单的有机化合物——甲烷的性质来初步认识有机化合物的性质。因此,本节的教学设计,要在学生初中已有知识和原子结构、化学键知识的基础上,先使学生有甲烷分子中的氢原子能被其他原子逐一取代的印象,又用球棍模型形象地说明了取代反应的本质,帮助他们建立取代反应这一重要的核心概念。本节课采用信息加工模式,充分体现化学和生活的紧密联系。通过讲解甲烷的存在、结构、性质,让学生以甲烷作载体去体会有机化学学习的内容和特点。 三、教学目标 1. 知识与技能 (1)常识性介绍有机化合物的概念及性质上的一些共同特点。 (2)了解甲烷在自然界中的存在。 (3)初步认识甲烷分子的空间结构。 (4)掌握甲烷的重要化学性质,并理解取代反应的含义。 2. 过程与方法 (1)使学生从身边接触的种类不同的有机化合物出发进行联想质疑,初步认识有机化合物种类繁多的原因。 (2)通过对甲烷燃烧、甲烷与氯气光照下反应等实验的观察、思考、分析、推论,引导学生掌握甲烷的化学性质,了解取代反应的概念。 3. 情感态度与价值观 (1)通过“联想?质疑”、“观察?思考”、“迁移?应用”等栏目的活动,激发学生探索未知知识的兴趣,让他们享受到探究未知世界的乐趣。 (2)通过沼气、天然气在日常生活中利用情况的了解,让学生感受到化学科学对生产和社会发展的贡献。 (3)通过瓦斯爆炸的介绍,学生利用已学知识趋利避害,让学生体会了解科学知识的重要性。 (4)利用甲烷性质的学习,提高学生学习有机化学的兴趣。 四、教学重点和难点 甲烷的性质和取代反应 五、教学准备 教学媒体、课件 六、教学方法 问题推进法、探究归纳法、对比总结法 《7.1 认识有机化合物》教案 第一课时有机化合物中碳原子的成键特点 【教学目标】 知识与技能: 1.了解有机化合物常见的分类方法 2.了解有机物的主要类别及官能团 过程与方法:根据生活中常见的分类方法,认识有机化合物分类的必要性。利用投影、动画、多媒体等教学手段,演示有机化合物的结构简式和分子模型,掌握有机化合物结构的相似性。 情感态度与价值观:体会物质之间的普遍联系与特殊性,体会分类思想在科学研究中的重要意义 【教学重难点】 重点:了解有机物常见的分类方法。 难点:了解有机物的主要类别及官能团。 【教学过程】 [引入]通过高一的学习,我们知道有机物就是有机化合物的简称,最 初有机物是指有生机的物质,如油脂、糖类和蛋白质等,它们是从动、植物 体中得到的,直到1828年,德国科学家维勒偶然发现由典型的无机化合物 氰酸铵通过加热可以直接转变为动植物排泄物——尿素的实验事实,从而使 有机物的概念受到了冲击,引出了现代有机物的概念——世界上绝大多数含 碳的化合物。有机物自身有着特定的化学组成和结构,导致了其在物理性质 和化学性质上的特殊性。研究有机物的组成、结构、性质、制备方法与应用 的科学叫有机化学。我们先来了解有机物的分类。 [讲]高一时我们学习过两种基本的分类方法—交叉分类法和树状分类 法,那么今天我们利用树状分类法对有机物进行分类。那么大家先回忆,我 们在必修2接触有机物时利用有机物所含元素种类不同对有机物进行了怎 样的分类? 烃和烃的衍生物,其中烃是只含有碳和氢的化合物。 [讲]今天我们利用有机物结构上的差异做分类标准对有机物进行分类,从结构上有两种分类方法:一是按照构成有机物分子的碳的骨架来分类;二是按反映有机物特性的特定原子团来分类。 [板书]一、按碳的骨架分类 链状化合物:(如32223CH CH CH CH CH ----)(碳原子相互连接成链) 环状化合物: 脂环化合物(如)不含苯环 芳香化合物(如)含苯环 [讲]在这里我们需要注意的是,链状化合物和脂环化合物统称为脂肪族化合物。而芳香族化合物是指包含苯环的化合物,其又可根据所含元素种类分为芳香烃和芳香烃的衍生物。而芳香烃指的是含有苯环的烃,其中的一个特例是苯及苯的同系物,苯的同系物是指有一个苯环,环上侧链全为烷烃基的芳香烃。除此之外,我们常见的芳香烃还有一类是通过两个或多个苯环的合并而形成的芳香烃叫做稠环芳香烃。 [过]烃分子里的氢原子可以被其他原子或原子团所取代生成新的化合物,这种决定化合物特殊性质的原子或原子团叫官能团,下面让我们先来认识一下主要的官能团。 [板书]二、按官能团分类 [投影]表1-1 有机物的主要类别、官能团和典型代表物 双键 苯 第一章有机化合物的结构和性质烃 第一节认识有机化学 【课时目标】 (1)知道有机化学的发展,了解有机化学的研究领域。 (2)掌握有机物的三种分类方法,建立烃和烃的衍生物的分类框架。 (3 )理解同系物和官能团的概念。 第一课时有机化学和官能团、同系物概念 【课前预习】 1 .有机化学就是以有机物为研究对象的学科,它的研究范围包括有机物的_______________________________________ - ______________________ 。有机化学萌发于 _______________ ,创立并成熟于_____________ ,进入是有机化学发展和走向辉煌的时期,21世纪,有机化学进入崭新的发展阶段。 2 .有机化合物的分类通常有三种方法,根据组成元素的种类可分为___________________________________________ 和 ____________ ;根据分子中碳架不同可分为________________________ 和___ 两类;根据所含官能团的不同,烃的衍生物可分为 ____ 等。 3 ?官能团即__________________________________ 。写出下列官能团的结构简式: 双键 ___________________ 叁键 __________________ 苯环______________ 羟基____________________ 醛基 ___________________ 羧基 ___________________ 酯基_________________ 。 4 ?同系物即__________________________________ 。写出下列烃的结构特点及通式: 烷烃 ___________________________________________ 烯烃____________________________________________ 炔烃 ___________________________________________ 苯的同系物______________________________________ 。 【交流?研讨】p6 【归纳小结】1、按元素组成分类 第十一章 含氮化合物 11.2 命名下列化合物或写出结构式 a. CH 3CH 2NO 2 b. NO H 3C c. NHC 2H 5 d. H 3C N 2+Br - e. Br NHCOCH 3 f. CH 3CH 2CH 2CN g. NHNH 2 O 2N h. H 2NCH 2(CH 2)4CH 2NH 2 i. NH O O j. (CH 3CH 2)2N--NO k. C 6H 5CH 2 N CH 3CH 3 C 12H 25+ Br - l.胆碱 m. 多巴胺 n. 乙酰胆碱 o. 肾上腺素 p. 异丁胺 q.胍 r. CH 3CH 2N(CH 3)2 答案: a. 硝基乙烷 b. p —亚硝基甲苯 c. N -乙基苯胺 d. 对甲苯重氮氢溴酸盐或溴化重氮对甲苯 e. 邻溴乙酰苯胺 f. 丁腈 g. 对硝基苯肼 h. 1,6-己二胺 i. 丁二酰亚胺 j. N-亚硝基二乙胺 k. 溴化十二烷基苄基二甲铵 [(CH 3)3N +CH 2CH 2OH]OH - m.HO CH 2CH 2NH 2 n. l.[(CH 3)3N + CH 2CH 2OCOCH 3]OH - o.HO HO CH(OH)CH 2NHCH 3 p. (CH 3)2CHCH 2NH 2 r. N,N--二甲基乙胺 q. H 22 NH 11.3 下列哪个化合物存在对映异构体? a.CH 3NHCH 2CH 2Cl b.(CH 3)2N +(CH 2CH 2Cl)2Cl - c. N CH 3 d. CH 2CHCH 3 2 答案: a, d 存在。但a 的对映异构体在通常条件下很容易相互转化。 11.4 下列体系中可能存在的氢键: a. 二甲胺的水溶液 b. 纯的二甲胺 答案: H H O H H N H 3C H 3C H N H 3C H 3C H N H H 3H 3H 3H 3 Ⅰ Ⅱ Ⅲ a 中有 Ⅲ Ⅱ Ⅰ Ⅰ 三种氢键 b. 中只有一种氢键 H H 11.5 如何解释下列事实? a. 苄胺(C 6H 5CH 2NH 2)的碱性与烷基胺基本相同,而与芳胺不同。 b. 下列化合物的pK a 为 O 2N NH 2 NH 2 H 3C NH 2 pK b =13.0 pK b =9.37 pK b =8.70 答案:化学一轮精品复习学案:第一章 认识有机化合物(选修5)
第十五章 含硫含磷有机化合物
有机化合物的分类学-人教版高中化学选修5学案设计
认识有机化合物 复习 学案(精华版)
含硫和含磷有机化合物
全国通用版2019版高考化学大一轮复习第48讲认识有机化合物优选学案
人教版选修5第1章认识有机化合物学案
高考化学一轮复习有机化学基础第1节认识有机化合物学案选修5
认识有机化合物教案
第一章认识有机化合物专题复习
完整版认识有机化合物第一课时教案
《7.1 认识有机化合物》教案、导学案
(完整版)第一节认识有机化学学案
第十二章 含硫和含磷有机化合物课后习题答案