
_
_
_
_
_
_
_
_
_
_
_
_
_
_
号
场
试
_
_
_
_
_
_
_
_
_
_
_
_
_
_
_
_
_
名题
姓答卷
要试
不学
内化
线试
订考
装拟
模
招
中
年号
2考
2
-
9
1
2
级
班
校
学
金堡中学 2006 年中招模拟考试化学试卷
题序一二三四五总分
得分
说明:全卷满分100 分,考试时间:80 分钟
可能用到的相对原子质量:H:1 O:16 S:32 K:39 Na:23 Al:27
A.大量饮用该物质对人体有益
6. 下列实验操作叙述正确的是()
A. 把块状固体投入直立的试管中
B. 给试管加热时,试管口不要对着人
C. 未用完的药品放回原试剂瓶中
D.实验产生的废液直接倒入下水道
7.牙膏里添加的单氟磷酸钠( Na2POF3)可有效防止龋齿。关于单氟磷酸钠的说法正确的是(
A.它是由钠、磷、氧、氟四个原子组成的
B.它是由钠、磷、氧、氟四种元素组成的
C.单氟磷酸钠中钠、磷、氧、氟元素的质量比为2: 1: 3:1
D.它是由 2 个钠元素、 1 个磷元素、 3 个氧元素、 1 个氟元素组成的
8. 下列操作或现象与分子对应的特性不一致的选项是()
选项操作或现象分子的特性
A 给篮球充气分子间有间隔
B 在花园中可闻到花的香味分子是运动的
C 100mL 酒精和 100mL水混合在一起,体积小于200mL 分子是有质量的
D 加热氧化汞可得到金属汞和氧气分子是可以再分的
9.打雷放电时,空气中极少量氧气会转化成臭氧(3O2= 2O3),下列有关说法中正确的是(
A. 该变化是物理变化
B.O2与 O3都是单质
C.O2与 O3是不同的物质
D.O2与 O3的性质完全相同
10.某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛。在氢氧化镁与胃酸作用的
过程中,胃液 PH变化的情况是()
PH PH PH PH
7777
11. 盐是人体正常生理活动必不可少的物质。这里的盐是指(
时间 /t
)
0 时间 /t
A
时间 /t 0
B
时间 /t 0
D
C
A. NaHCO
B. NaCl
C. CuSO
D. CaCO
3 4 3
12.硅酸盐矿泉具有软化血管的作用,对心脏病、高血压等疾病患者有良好的医疗保健作用。硅酸
钠的化学式为Na2SiO3, 其中硅元素的化合价为()
A. +1
B. +2
C. +3
D. +4
13. 右图装置里所发生的化学反应,其反应类型属于()
A. 化合反应
B. 分解反应
C. 置换反应
D.分解反应
14.甲醛(化学式为: CH2O)是一种无色、有刺激性气味的气体,易溶于水,有毒。为使服装达到防
皱、改善手感等效果,在加工中需添加甲醛。但衣物中残留的甲醛超标会损害人体健康。以下说法
或做法错误的是()
A.甲醛属于有机物
B.甲醛属于氧化物
C.买回服装后先用水洗,有利于除去残留的甲醛
D.新买的服装若有刺激性气味,有可能是甲醛会超标
二、填空(本题有 6 小题共 20 分)
15. ( 4 分)常用的石蕊试液呈色色,遇稀盐酸变色,遇氢氧化钾溶液变
而它可用于检验溶液的性。
16.(4 分)用符号表示下列含义或写出符号的含义:
)① 2 个氢原子② 2个氯分子③氢硫酸
④ Fe3+。
17.( 2 分)著名的发明家诺贝尔经过长期的研究与试验,终于发明了安全炸药—三硝酸甘油酯,
三硝酸甘油酯的化学式为 C3H5N3O9,这种炸药发生爆炸的反应方程式为:
4C3H5N3O9引爆剂12CO↑+10H2O↑+6X↑+O2↑
① X 的化学式是:。②推断X的化学式的依据是。
18.(4 分)汽油是石油炼制产品之一,是汽车的主要燃料。请回答:
①汽油充分燃烧的产物是二氧化碳和水,由此可推断汽油的组成元素一定含有元素。②以汽油为燃料
车尾气中含有一氧化碳、氮的氧化物等大气污染物。目前,减少汽车尾气污染
的措施之一,是在汽油中加入适量的乙醇。乙醇完全燃烧的化学方程
为:。( 2 分)
)
(填编号)
③下列能替代汽油的燃料中,燃烧产物最清洁的是
A. 天然气
B. 乙醇
C. 氢气
19.(3 分)甲和乙两种物质溶解度曲线如图所示:
① 200C 时,甲的溶解度比乙的溶解度
(填“大”或“小” )溶甲
② 400C 时,在 100g 水中加入 80g 甲固解60
体,充分搅拌所得溶液的质量度
是g;/g 40 乙
③
50 C 时,某溶液所溶解的甲和乙物质
都已饱和。把该溶液冷却到室温,有晶
20
体析出,经验发现析出的晶体主要是甲,其原因是(填编号)
0 0
A.50 C 时,甲的溶解度更大
B.50 C 时,乙的溶解度更大
C. 甲的溶解度受温度变化的影响比乙大0 20 40 60 0
C
20.(5 分)今年 5 月,云南省某地一个内装白磷的储罐因泄漏而迅速自发引起大火,
温度(
现场白烟
消防人马上采用冷却罐体,再用沙土围堰填埋的方式灭火,火势很快得到控制。已知白磷和红磷都
是磷元素组成的单质,它们化学性质相似。请回答:
①白磷与红磷比较,在空气中更容易着火燃烧的是;
②白磷燃烧的化学方程式为:;
③消防人员采用的灭火方法原理是:。
·
· · · ·
· 三、(本题有 2 小题,共 18 分)
·
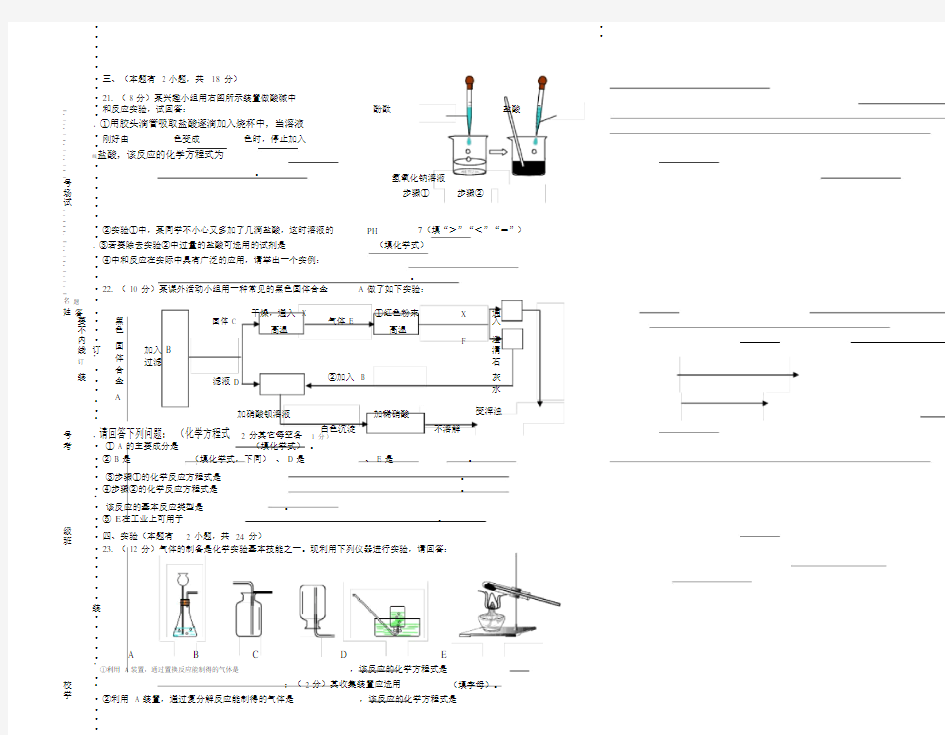
21. ( 8 分)某兴趣小组用右图所示装置做酸碱中 _
·
· 和反应实验,试回答:
酚酞
盐酸
_
·
_
_
·
①用胶头滴管吸取盐酸逐滴加入烧杯中,当溶液
_
_
·
_
刚好由 色变成
色时,停止加入
_
·
_
_
线
盐酸,该反应的化学方程式为
_
_
·
_ 。
_ · 氢氧化钠溶液
号
·
场 步骤① 步骤②
·
试
·
_
_ ·
_
_ ·
_ ②实验①中,某同学不小心又多加了几滴盐酸,这时溶液的 PH 7(填“>”“<”“=”) _
·
_
_
· ③若要除去实验②中过量的盐酸可选用的试剂是
(填化学式)
_
_ ·
_ ④中和反应在实际中具有广泛的应用,请举出一个实例:
_
·
_
_
· 。 _
_
· 22. ( 10 分)某课外活动小组用一种常见的黑色固体合金 A 做了如下实验:
_
名 题 · X 姓 答 · 黑
干燥,通入 X 气体 E ①红色粉末 通 要 · 固体 C 入
不 · 色 高温
高温 F 澄 内 · 固 加入 B
线 订
清 体
订 ·
过滤 石 合
装 · ②加入 B
灰 · 金 滤液 D
水 ·
· A
·
加硝酸钡溶液
加稀硝酸
变浑浊
·
2 分其它每空各 白色沉淀
不溶解
号 ·
请回答下列问题: (化学方程式
1 分)
考
· ① A 的主要成分是 (填化学式) 。
· ② B 是 (填化学式,下同) 、 D 是 、 E 是
。
·
· ③步骤①的化学反应方程式是 。
· ④步骤②的化学反应方程式是
。
·
· 该反应的基本反应类型是 。
· ⑤ E 在工业上可用于 。 级 · 四、实验(本题有 2 小题,共 24 分) ·
班
· 23. ( 12 分)气体的制备是化学实验基本技能之一。现利用下列仪器进行实验,请回答:
· · · · · 装 · · ·
·
A B C D E
·
·
①利用 A 装置,通过置换反应能制得的气体是 ,该反应的化学方程式是 校 ·
;( 2 分)其收集装置应选用 (填字母)。 ·
学
·
②利用 A 装置,通过复分解反应能制得的气体是 ,该反应的化学方程式是
·
· ·
· ·
。( 2 分)
③ A 装置在加药品前,必须进行气密性的检查,其操作是
。( 2 分)
④将制得的氢气通入装有氧化铜粉末的 E 装置,加热,黑色粉末变红,说明氢气具有性。
⑤由于氢气,可用作节日庆典气球的填充气。但由于氢气易燃易爆,所以在有氢气球
的地方,最好放警示牌,请你写上一条警示语:。
24. ( 12 分)某课外活动小组通过Intnet网上资料得知:废弃的定影液中含有一定量的AgNO3。他们从摄影店收集到一些废弃的定影液,准备将其中的银以单质的形式全部回收。于是,他们进行了以下的实
验活动:
( 1)【设计方案】①加入比银活泼的金属单质②除去金属混合物中的杂质
( 2)【小组讨论】
①选择加入的金属(化学方程式 2 分,下同)
甲同学认为:向定影液中加入过量的铜粉,则得到的金属混合物含有银和铜;
乙同学认为:向定影液中加入过量的铁粉,则得到的金属混合物含有银和铁。
你认为同学的方案更合理,其原因是,该方案的化学方
程式为:。②除去银粉中混有的金属
向金属混合物中加入的试剂是,化学方程式为。
( 3)【进行实验】过程如下:
①废弃定影液加较活泼金属(过量)金属混合物 +溶液 A
操作 a
②金属混合物加试剂(适量)Ag+溶液 B
请回答:操作 a 是操作b,需用到的玻璃仪器有:烧杯、玻璃棒和;溶液B中溶质的化学式为。
( 4)【产品验证】请你设计一种简单方法验证得到的银中是否还含有铁粉,方法是:
。( 2 分)
五、计算( 10 分)
25. ( 5 分) 1989 年世界卫生组组织把铝列为食品污染源之一,每人每日的摄入量控制在0.004g 以下。
若在 1kg 米南食品中加入明矾2g【明矾的化学式为:KAl(SO 4) 2· 12H2O】请回答下列问题:
①人从食物中摄入的铝指的是(填字母)。
A. 铝元素
B. 铝单质
C.铝合金
D. 只有明矾
( 2)明矾中各元素的质量比K:Al:S:O:H=;铝元素的质量分数为(计算结果
精确到 0.1%)。
(3)如果某人一天吃了 100g 上述米面食品,通过计算说明其摄入的铝的量是否超过安全摄入量。
(2 分)
26.( 5 分) 25.( 8 分)普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械
零件。现有一块 50.00g 黄铜样品,某同学利用一种未知浓度的稀盐酸来测定样品中Cu 的质量分数。
有关数据如下图。问:
固体质量 /g 反应后溶液质量 /g
图1 图2
50.00 198.25
46.75 158.60
43.50 118.95
40.25 79.30
37.00 39.65
33.75
m1m2盐酸质量/g m1m2盐酸质量/g
(1)黄铜中 Cu 的质量分数。
(2)样品完全反应产生的 H2的质量。
(3)稀盐酸的溶质质量分数。
参考答案
一、选择BBBCB BBCCB BDAB
二、填空
15. 紫红蓝酸碱
16.① 2H ② 2Cl 2 ③ H2S ④带 3 个单位下电荷的铁离子
17.① N2 ②质量守恒定律点燃
18.① C 和 H 2 5 2 点燃2 点燃点燃
② CH OH+3O 2CO+3H O ③ C
19.①小② 160 ③ C
20.①白磷② 4P+5O2 2P2O5点燃③将温度降至白磷的着火点以下,隔绝白磷与空气接触
三、
21.①红色无色NaOH+HCl=NaCl+HO ②<③ NaOH(或 Na CO、NaHCO)
2 2
3 3
④用熟石灰改良酸性土壤(或用氢氧化铝治疗胃酸过多等,合理答案给分)
22. ① C 和 Fe ② H2SO4 FeSO4 CO ③3CO+Fe2O3 高温
3CO2+2Fe
④ Fe+ H SO= FeSO+ H ↑置换反应⑤冶炼金属(或燃料)
2 4 4 2
四、
23. ①氢气Zn+H2SO4= ZnSO4+ H2↑②二氧化碳CaCO2+2HCl=CaCl2+H2O+CO2↑
③在导管处套上带止水夹的橡皮管,然后在长劲漏斗中加入一定量的水至沐过漏斗下端,静置。若
液面静止不动,则装置不漏气;反之,装置漏气。
④还原
24. ( 2)①( 3)过滤⑤气度比空气小严禁烟火
乙铁粉比铜粉更易被除去(或更易得到、更经济)
漏斗FeCl 2(或 FeSO4)④用磁铁接触,看银粉是否被磁铁吸引(或取少量
滴入稀盐酸或稀硫酸,看是不有气泡放出)
五、计算
25. (1) A ( 2) 39: 27: 64: 320:24 5.7%
(3)
2g
× 100g=0.2g 0.2 × 5.7%=.00114g>0.004g超过了安全摄入量1000g
26. (1) 67.5 % (2) 0.5 g (3) 10 %