
第二节镁、铝及其化合物
一、选择题(每小题4分,共48分)
1.(2011·海口调研)下列有关金属铝及其化合物的叙述正确的是() A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.铝既能溶于酸,又能溶于强碱
D.氧化铝只能与酸反应,不能与碱反应
解析:铝在常温下可与O2反应,A错;铝能与氯气反应,B错;氧化铝是两性氧化物,既能与酸反应又能与碱反应,D错。
答案:C
2.(2011·扬州模拟)若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是() A.NH+4NO-3CO2-3Na+
B.Na+Ba2+Mg2+HCO-3
C.NO-3Ca2+K+Cl-
D.NO-3K+AlO-2H+
解析:A项,在酸性条件下因有NO-3,不能生成H2,在碱性条件下,OH-与NH+4不共
存,故A项不符合;B项,HCO-3与H+或OH-均不能大量共存;C项,在碱性条件下符
合题意;D项表示的为酸性条件,含有HNO3,不可能与Al反应放出氢气,且AlO-2和H+不能大量共存。
答案:C
ks5u
3.(2011·潍坊模拟)下列各反应的离子方程式中,错误的是() A.硫酸铝溶液中加入过量的氨水:
Al3++3NH3·H2O===Al(OH)3↓+3NH+4
B.铁片放入过量的稀硝酸中:
3Fe+8H++2NO-3===3Fe2++2NO+4H2O
C.将铝片放入过量NaOH溶液中:
2Al+2OH-+2H2O===2AlO-2+3H2↑
D.偏铝酸钠与过量盐酸反应:
AlO-2+4H+===Al3++2H2O
解析:B项正确离子方程式为:Fe+4H++NO-3===Fe3++NO↑+2H2O。
答案:B
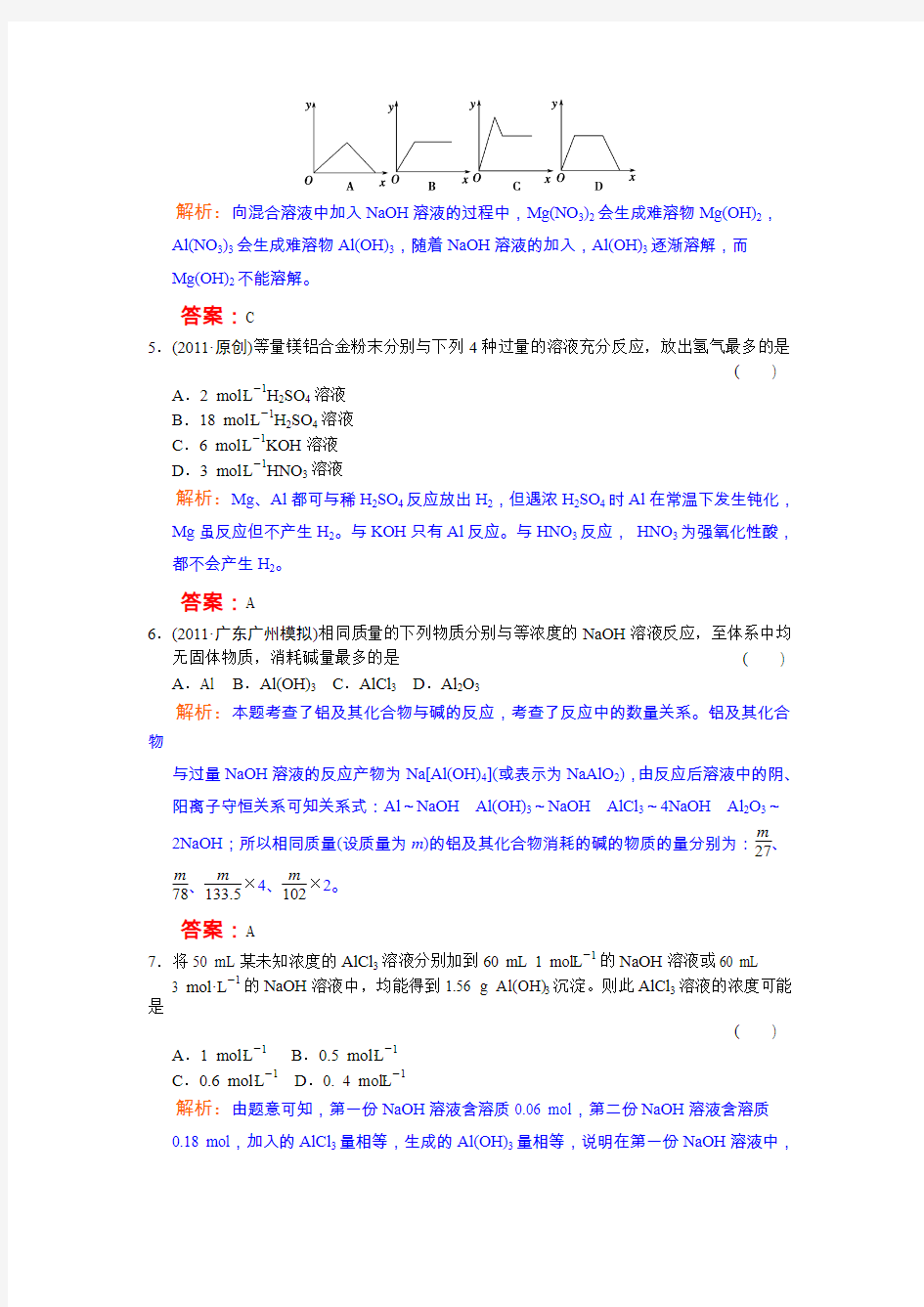
4.(2011·烟台模拟)在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(x)与溶液中沉淀的量(y)的关系示意图中正确的是()
解析:向混合溶液中加入NaOH溶液的过程中,Mg(NO3)2会生成难溶物Mg(OH)2,Al(NO3)3会生成难溶物Al(OH)3,随着NaOH溶液的加入,Al(OH)3逐渐溶解,而
Mg(OH)2不能溶解。
答案:C
5.(2011·原创)等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
() A.2 mol·L-1H2SO4溶液
B.18 mol·L-1H2SO4溶液
C.6 mol·L-1KOH溶液
D.3 mol·L-1HNO3溶液
解析:Mg、Al都可与稀H2SO4反应放出H2,但遇浓H2SO4时Al在常温下发生钝化,Mg虽反应但不产生H2。与KOH只有Al反应。与HNO3反应,HNO3为强氧化性酸,都不会产生H2。
答案:A
6.(2011·广东广州模拟)相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是() A.Al B.Al(OH)3C.AlCl3D.Al2O3
解析:本题考查了铝及其化合物与碱的反应,考查了反应中的数量关系。铝及其化合物
与过量NaOH溶液的反应产物为Na[Al(OH)4](或表示为NaAlO2),由反应后溶液中的阴、阳离子守恒关系可知关系式:Al~NaOH Al(OH)3~NaOH AlCl3~4NaOH Al2O3~
2NaOH;所以相同质量(设质量为m)的铝及其化合物消耗的碱的物质的量分别为:m
27、
m 78、
m
133.5×4、
m
102×2。
答案:A
7.将50 mL某未知浓度的AlCl3溶液分别加到60 mL 1 mol·L-1的NaOH溶液或60 mL
3 mol·L-1的NaOH溶液中,均能得到1.56 g Al(OH)3沉淀。则此AlCl3溶液的浓度可能是
() A.1 mol·L-1B.0.5 mol·L-1
C.0.6 mol·L-1D.0. 4 mol·L-1
解析:由题意可知,第一份NaOH溶液含溶质0.06 mol,第二份NaOH溶液含溶质
0.18 mol,加入的AlCl3量相等,生成的Al(OH)3量相等,说明在第一份NaOH溶液中,
NaOH 不足,Al 3+过量,在第二份NaOH 溶液中NaOH 过量,反应后的Al 元素以Al(OH)3
和AlO -2
的形式存在。 故由反应① Al 3++3OH -===Al(OH)3↓
1 3 1
0.02 mol 0.06 mol 1.56 g 78 g/mol
=0.02 mol ② Al 3++4OH -===AlO -2+2H 2O
1 4
0.03 mol 0.18-0.06 mol
所以c (AlCl 3)=0.02 mol +0.03 mol 0.05 L
=1 mol/L 。 答案:A
8.将5.4 g Al 投入到200.0 mL 2.0 mol/L 的某溶液中有氢气产生,充分反应后有金属剩余。 该溶液可能为 ( )
A .HNO 3溶液
B .Ba(OH)2溶液
C .H 2SO 4溶液
D .HCl 溶液
解析:因HNO 3具有强氧化性,与Al 反应不产生H 2,故A 项首先排除。Al 与碱反应的
关系为Al ~ OH -,Al 与酸反应的关系为Al ~3H +,溶解0.2 mol 的Al 需OH -、H +的物
质的量分别为0.2 mol 、0.6 mol ,Ba (OH)2提供0.8 mol OH -,H 2SO 4提供0.8 mol H +而
HCl 只提供0.4 mol H +,故“剩余金属的情况”只能为D 项。
答案:D
9.(2011·北京门头沟模拟)将15.6 g Na 2O 2和5.4 g Al 同时放入一定量的水中,充分反应后得 到200 mL 溶液,再向该溶液中缓慢通入标准状况下的HCl 气体6.72 L ,若反应过程中 溶液的体积保持不变,则 ( )
A .反应过程中得到6.72 L 的气体(标况)
B .最终得到的溶液中c (Na +)=c (Cl -)+c (OH -
)
C .最终得到7.8 g 的沉淀
D .最终得到的溶液中c (NaCl)=0.15 mol/L 解析:由题n (Na 2O 2)=0.2 mol ,n (Al)=0.2 mol ,发生反应:2Na 2O 2+2H 2O===4NaOH +
O 2↑,2Al +2NaOH +2H 2O===2NaAlO 2+3H 2↑,可知生成气体0.4 mol ,标况下体积为
8.96 L ;加入盐酸先和过量的NaOH 反应,剩余0.1 mol 和NaAlO 2反应生成0.1 mol Al(OH)3:NaAlO 2+HCl +H 2O===NaCl +Al(OH)3↓,最终溶液为0.3 mol NaCl 、0.1 mol NaAlO 2。
答案:C ks5u
10.(2011·安徽联考)硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当SO 2-
4的浓度为 0.20 mol/L 时,加入等体积的0.20 mol/L 的KOH 溶液(混合溶液体积变化忽略不计),使 生成的白色沉淀恰好溶解,那么反应后溶液中K +
的浓度为 ( )
A .0.20 mol/L
B .0.25 mol/L
C .0.225 mol/L
D .0.45 mol/L
解析:Al 3+ + 4OH -===AlO -2+2H 2O 1 4
0.05 mol/L 0.20 mol/L
根据溶液中的电荷守恒3c (Al 3+)+c (K +)=2c (SO 2-4)
c (K +)=2×0.20 mol/L -3×0.05 mol/L =0.25 mol/L 。
答案:B
11.(2009·四川理综,11)向m g 镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标 准状况下的气体b L 。向反应后的溶液中加入c mol/L 氢氧化钾溶液V mL ,使金属离子 刚好沉淀完全,得到的沉淀质量为n g 。再将得到的沉淀灼烧至质量不再改变为止,得 到固体p g 。则下列关系不正确的是 ( )
A .c =1 000b 11.2V
B .p =m +Vc 125
C .n =m +17Vc D.53m
m 解析:向m g Mg 、Al 的混合物中加入适量的稀H 2SO 4,恰好完全反应,溶液中只有 MgSO 4、Al 2(SO 4)3两种物质,且Mg 2+与Al 3+的质量和为m g ;向反应后的溶液中加入 c mol/L KOH 溶液V mL ,使金属离子恰好完全沉淀,发生的反应是:Mg 2++2OH - ===Mg(OH)2↓,Al 3++3OH -===Al(OH)3↓,则得到沉淀的质量是Mg 2+、Al 3+的质量与 NaOH 溶液中OH -质量的质量和,所以n =m +V ×10-3×c ×17=m +1.7×10-2Vc ,C 项
错误。
答案:C
12.(2011·试题调研,江西联考)现有Al 、Cl 2、Al 2O 3、HCl(aq)、
Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,
图中每条线两端的物质之间都可以发生反应,下列推断不合理
的是 ( )
A .N 一定是HCl(aq)
B .X 可能为Al 或Cl 2
C .Y 一定为NaOH(aq)
D .Q 、Z 中的一种必定为Al 2O 3
解析:在Al 、Cl 2、Al 2O 3、HCl(aq)、Al(OH)3、NaOH(aq)中,只有NaOH(aq)能与Al 、 Cl 2、Al 2O 3、HCl(aq)、Al(OH)3五种物质反应,对照转化关系,可知Y 为NaOH(aq)。只 有HCl(aq)能与Al 、Al 2O 3、Al(OH)3、NaOH(aq)四种物质反应,对照图示转化关系可知 N 为HCl(aq),故选项A 、C 正确。选项B ,若X 为Al ,Al 能与Cl 2、HCl(aq)、NaOH(aq)
三种物质反应,而图示给出的是与两种物质反应,所以X 不可能是Al ,但可能是Cl 2。 选项D ,Al 2O 3既能与HCl(aq)反应,也能与NaOH(aq)反应,故Q 、Z 中的一种必定为 Al 2O 3。
答案:B
二、非选择题(本题包括4个大题,共52分)
13.(13分)(2010·浙江金华模拟)A 、B 、C 、D 、E 五种化合物均含有某种短周期常见元素, 它们的转化关系如图所示,其中A 为澄清溶液,C 为难溶的白色固体,E 则易溶于水, 若取A 溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
(1)写出化学式:
A :________、
B :________、
C :________、
D :________、E________。
(2)写出下列反应的离子方程式:
A ―→
B : _____________________________________________________________; A ―→D :______________________________________________________________。 解析:本题的突破口应在B 、
C 两物质上,只要推断出B 、C ,其他物质的推断就很容易
了。在短周期元素的化合物中,既能与盐酸反应,又能与NaOH 溶液反应的,必为两性 物质,又因为B ――→△
C ,故可知C 为Al 2O 3,B 为Al(OH)3,依次推出
D 是AlCl 3,A 与 过量CO 2反应生成Al(OH)3,且A 溶液的焰色反应为浅紫色,则A 为KAlO 2,
E 为 NaAlO 2。相应的化学反应方程式也不难写出。 答案:(1)KAlO 2
Al(OH)3 Al 2O 3 AlCl 3 NaAlO 2 (2)AlO -
2+CO 2+2H 2O===Al(OH)3↓+HCO -3 AlO -2+4H +===Al 3++2H 2O
14.(13分)(2011·滨州质检)实验室可用铝屑、氨水、氢氧化钠溶液、稀硫酸等来制备氢氧化 铝,某同学设计了三种实验方案, }Al 刘Al 3+刘AlO -
2→Al(OH)3 (1)用方案①制备Al(OH)3时使用的药品最好是铝屑、稀硫酸和氨水,不用氢氧化钠代替 氨水的原因是_______________________________________________________________ ________________________________________________________________________;
写出该方案中有关的离子方程式______________________________________________。
(2)用方案②来制备Al(OH)3时,必须注意________的用量,以防止生成的Al(OH)3溶
解。(3)三种方案中,你认为最好的是________(填序号),原因是________________。
解析:分析本题应从Al(OH)3的两性着手,过量的强酸、强碱均能降低Al(OH)3的产率,而Al3+与AlO-2反应制取氢氧化铝,则不存在该问题,故③方案最好。
答案:(1)若用NaOH溶液沉淀Al3+,终点不易控制,因为
Al(OH)3会溶于过量的NaOH溶液,从而影响Al(OH)3的生成量2Al+6H+===2Al3++3H2↑,ks5u
Al3++3NH3·H2O===Al(OH)3↓+3NH+4
(2)稀硫酸(3)③药品用量最少,操作最为简单
15.(13分)(2011·湖南模拟)根据右图所示装置,请回答:
(1)在A中加试剂后,立即打开止水夹C,B中的现象是____,离子方程式是
______________________________________________________
___________。
(2)一段时间后,关闭止水夹C,B中的现象是______________________________,
离子方程式是___________________________________________________________。
解析:装置A为简易启普发生器,可通过止水夹C的控制,装置A中反应产生气体CO2
进入B中或气体将液体压入试管B中,使H+与开始生成的Al(OH)3相遇发生反应。
答案:(1)导管口有气泡冒出,有白色沉淀生成
AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3或2AlO-2+CO2+3H2O=2Al(OH)3↓+CO2-3
(2)A中液体进入B中,液面上升,白色沉淀逐渐溶解
Al(OH)3+3H+===Al3++3H2O
16.(13分)(2011·模拟精选,山东沂水一模)聚合氯化铝晶体的化学式为[Al2(OH)n Cl6-n·x H2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:
(1)搅拌加热操作过程中发生反应的离子方程式:______________________________、
____________________________________________。
(2)生产过程中操作B和D的名称均为________(B和D为简单操作)。
(3)反应中副产品a是________(用化学式表示)。
(4)生产过程中可循环使用的物质是________(用化学式表示)。
(5)调节pH至4.0~4.5的目的是________________________________________。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯
净。生产过程中C物质可选用()
A.NaOH B.Al C.氨水D.Al2O3E.NaAlO2
解析:由于铝灰中含Al2O3、Al,还有SiO2等杂质,加入盐酸搅拌使Al元素进入溶液,发生反应Al2O3+6H+===2Al3++3H2O,2Al+6H+===2Al3++3H2↑,和SiO2等杂质分离,采取过滤的方法得到AlCl3溶液。溶液降温熟化调节pH至4.0~4.5,增大AlCl3溶液
的pH,通过促进其水解而结晶析出。AlCl3水解生成的HCl易挥发,挥发出的HCl经水喷
淋吸收又生成盐酸,这个过程中可以循环利用盐酸。(6)为了不引进新的杂质,可以选择B和D。
答案:(1)Al
O3+6H+===2Al3++3H2O2Al+6H+===2Al3++3H2↑
2
(2)过滤(3)H2(4)HCl
(5)促进AlCl3水解,使晶体析出(6)BD
铁铜钠镁铝及其重要化合物的相互转化关系铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑ 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑ 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑ 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑MgCO3+2HCl=MgCl2+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO +COΔ Cu + CO2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO高温2Fe+3CO2 冶炼金属原理Fe3O4+4CO高温3Fe+4CO2 冶炼金属原理WO3+3CO高温W+3CO2 冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O 2CH3OH+3O2点燃2CO2+4H2O C2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4= Fe+ MgSO4 溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+ Cu (NO3)2 Cu+2AgNO3=2Ag+ Cu(NO3)2 红色金属表面覆盖一层银白色物质镀银Zn+CuSO4= Cu+ZnSO4 青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解Na2O+2HCl=2NaCl+H2O 白色固体溶解CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+ H2O 白色固体溶解
镁、铝及其化合物知识点整理 一.Mg、Al的化学性质 1.与非金属反应 (1)与O2反应:常温下与空气中的O2反应生成一层的氧化物薄膜,所以镁、铝都有抗的性能。镁能在空气中燃烧:,铝在纯氧中燃烧: (2)与卤素单质、硫等反应: [特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。 镁在空气中燃烧时有三个反应发生:, , ②燃烧时都放出大量的热,发出耀眼的白光。利用镁的这种性质来制造照明弹。 ③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。 2.与H2O反应 Mg、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气。 3.与酸反应置换出H2 Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓H2SO4,冷浓硝酸中发生现象。所以可用铝制容器贮存冷的或。 4.与某些氧化物反应 (1)镁与二氧化碳反应:2Mg+CO22MgO+C [特别提醒]:“CO2不能助燃”的说法是不全面的,CO2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。 (2)铝热反应(与Fe2O3反应): 铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。 [特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe2O3、FeO、Fe3O4、Cr2O3、V2O5、MnO2等。 ②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。 ③KClO3作为引燃剂,也可以用Na2O2代替。 5.与碱反应 镁不与碱反应,铝与碱液反应:2Al+2NaOH+6H2O2NaAlO2+4H2O+3H2↑ 简写:
铝及其化合物的化学方程式和离子方程式 一、铝 1、铝在氧气中燃烧: 2、铝在氯气中燃烧: 3、铝和硫共热: 4、铝与稀硫酸反应: 5、铝和氢氧化钠溶液反应: 6、铝和浓硫酸共热: 7、铝和浓硝酸共热: 8、铝和稀硝酸反应: 8、铝和硝酸银溶液反应: 9、铝与硫酸铜溶液反应: 10、铝和氧化铁高温下反应: 11、铝和四氧化三铁高温共热: 12、铝和氧化铜高温共热: 13、铝和二氧化锰高温共热: 二、氧化铝 1、氧化铝与稀硫酸反应: 2、氧化铝与氢氧化钠溶液反应: 3、电解氧化铝的熔融液: 三、氢氧化铝 1、氢氧化铝与稀硫酸反应: 2、氢氧化铝与氢氧化钠溶液反应: 3、加热氢氧化铝: 四、硫酸铝 1、硫酸铝溶液与氯化钡溶液混合: 2、硫酸铝的水溶液呈酸性: 3、硫酸铝溶液中加入少量的氢氧化钠溶液: 4、向硫酸铝溶液中加足量的氢氧化钠溶液: 5、向硫酸铝溶液中加入少量的氢氧化钡溶液:
6、向硫酸铝溶液中加入足量的氢氧化钡溶液: 7、向明矾溶液中加入少量的氢氧化钡溶液: 8、向明矾溶液中加入足量的氢氧化钡溶液: 9、向硫酸铝溶液中加入氨水: 10、向硫酸铝溶液中加入碳酸钠溶液: 11、向硫酸铝溶液中加入碳酸氢钠溶液: 12、向硫酸铝溶液中加入硫化钠溶液: 13、向硫酸铝溶液中加入硫氢化钠溶液: 14、向硫酸铝溶液中加入硅酸钠溶液: 15、向硫酸铝溶液中加入偏铝酸钠溶液: 五、偏铝酸钠 1、偏铝酸钠溶液呈碱性: 2、偏铝酸钠溶液滴入少量盐酸: 3、向偏铝酸钠溶液加入足量盐酸: 4、向偏铝酸钠溶液通入少量二氧化碳气体: 5、向偏铝酸钠溶液通入足量二氧化碳气体: 6、向偏铝酸钠溶液中加入硫酸铝溶液: 7、向偏铝酸钠溶液中加入氯化铵溶液: 8、向偏铝酸钠溶液中加入氯化铁溶液:
镁铝的重要化合物(二) 一.选择题(共30小题) 1.(2012?西安一模)将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g.另取等质量的合金溶于过量稀硝酸中,生成了6.72L NO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则最终所得沉淀的质量为() A.22.1g B.27.2g C.30g D.19.4g 2.(2012?连云港三模)铝是一种很重要的金属,可以发生一系列反应制备物质,如图所 示. 下列说法错误的是() A.反应①又称铝热反应,可用于野外焊接铁轨 B.反应②、③都有氮气生成,产生等量的氢气时转移的电子数相等 C.常用反应⑥制备Al(OH)3,方法是向Al2(S04)3溶液中滴加足里的NaOH溶液 D.工业上用反应⑦制备铝时,常加人冰晶石以降低氧化铝的熔融温度 3.(2012?徐汇区二模)用下列各组试剂分离FeCl3和AlCl3两种物质的混合物,其中可以达到目的是()A.氨水和盐酸B.氢氧化钠和二氧化碳 C.氢氧化钠和盐酸D.氨水和二氧化碳 4.(2012?邯郸二模)某澄清透明溶液中只可能含有①Al3+,②Mg2+,③Fe3+,④Fe2+,⑤H+,⑥CO32﹣,⑦NO3﹣中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是() A.②⑤⑥⑦B.②③⑤⑦C.①②③⑥⑦D.①②③④⑤⑦ 5.(2012?永州模拟)下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是:①向饱和碳酸钠溶液中通入过量的CO2;②向NaAlO2胶体中逐滴加入过量的稀盐酸;③向AgNO3溶液中逐滴加入过量氨水;④向硅酸钠溶液中逐滴加入过量的盐酸() A.①②B.①③C.①④D.②③ 6.(2012?南昌二模)某溶液中可能含有K+,NH4,Al3+,SO42﹣,向该溶液中滴加Ba(OH)2溶液,溶液中生成的沉淀与加入Ba(OH)2物质的量关系如图所示.下列推断结论一定芷确的是()
专题+镁铝及其重要化合物(教学案) 【考试说明】 1.掌握铝及其重要化合物的主要性质及其应用。 2.掌握镁及其重要化合物的主要性质及其应用。 3.了解铝、镁及其重要化合物的制备方法。【命题规律】 有关Al及其化合物知识在高考中出现频率较高,“铝三角”是命题的出发点。高考中常以选择题型结合离子方程式的书写正误判断、离子共存问题考查Al及其化合物的转化;以化工流程图中铝土矿的开发为载体以填空题型考查镁、铝及其化合物的性质、制备等。 一、铝、镁的性质及应用 1.铝的结构和存在 铝位于元素周期表第三周期ⅢA族,原子结构示意图为然界中的铝全部以化合态的形式存在。 2.金属铝的物理性质 。铝是地壳中含量最多的金属元素。自 银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。 3.金属铝的化学性质写出图中有关反应的化学方程式或离子方程式: O2 ①Al 点燃点燃――→4Al+3O2=====2Al2O3 常温――→形成致密的氧化膜
点燃 ②2Al+3Cl2=====2AlCl3 酸③Al 氧化性酸―――→遇冷的浓硫酸或浓硝酸钝化 非氧化性酸―――→2Al+6HCl===2AlCl3+3H2↑ ④2Al+2NaOH+2H2O===2NaAlO2+3H2↑高温 ⑤2Al+Fe2O3=====Al2O3+2Fe(铝热反应) 4.对比记忆镁的化学性质 铝镁点燃2Mg+O2=====2MgO 与非金属反应能被Cl2、O2氧化点燃3Mg+N2=====Mg3N2 能与沸水反应Mg+与水反应反应很困难△2H2O=====Mg(OH)2+H2↑不反应能在CO2中燃烧:2Mg+点燃CO2=====2MgO+C 与碱反应能溶于强碱溶液能与Fe2O3、M nO2、Cr2O3等与某些氧化物反应金属氧化物发生铝热反应 5.铝的用途 纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。二、铝的重要化合物 1.氧化铝 (1)物理性质:白色固体,难溶于水,有很高的熔点。 (2)化学性质 两性氧化物— 与HCl反应――――→Al2O3+6HCl===2AlCl3+3H2O 与NaOH反应――――→Al2O3+2NaOH===2NaAlO2+H2O 2.氢氧化铝 (1)物理性质
高中化学学习材料 (精心收集**整理制作) 宜阳县实验中学 2011年高考一轮镁铝及其化合物 1.把Ba(OH)2溶液滴入明矾溶液中,使SO42ˉ全部转化成BaSO4沉淀,此时铝元素的主要存在形式是 A、Al3+ B、Al(OH)3 C、AlO2ˉ D、Al3+和Al(OH)3 2.若1.8g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氢气,则该金属是A.Al B.Mg C.Fe D.Zn 3.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应: Tl3++ 2Ag ==Tl+ + 2Ag+。下列推断正确的是 A.Tl+ 的最外层有1个电子 B.Tl3+ 的氧化性比Al3+弱 C.Tl能形成+3价和+1的化合物D.Tl+ 的还原性比Ag强 4.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3 C 高温 2 AlN + 3 CO 下列叙述正确的是 A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 B.上述反应中每生成2 mol AlN,N2得到3 mol电子 C.氮化铝中氮元素的化合价为—3 D.氮化铝晶体属于分子晶体 5.向一定量的下列物质的溶液中逐滴加入氢氧化钠溶液,先生成白色沉淀,后沉淀逐渐溶解.这种物质是 A.MgS04 B.NaAl02 C.A1C13D.FeCl3 6.相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是 A.Al B.Al(OH)3 C.Al Cl3 D.Al2O3 7.将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 8.甲、乙两烧杯中分别装有相同体积、相同pH的氨水和NaOH溶液,各加入10mL 0.1 mol·L-1 AlCl3溶液,两烧杯中都有沉淀生成。下列判断正确的是
镁、铝及其化合物知识点整理 Ⅰ.课标要求 1.通过海水制镁的事例了解镁及化合物的性质. 2.通过合金材料了解铝及化合物的性质. 3.能列举合金材料的重要应用. Ⅱ.考纲要求 1.掌握镁铝及化合物的性质. 2.了解镁铝及化合物在生活.生活中的应用. Ⅲ.教材精讲 一.Mg、Al的化学性质 1.与非金属反应 (1)与O2反应:常温下与空气中的O2反应生成一层致密的氧化物薄膜,所以镁、 铝都有抗腐蚀的性能。镁能在空气中燃烧:2Mg+O 22MgO ,铝在纯氧中燃烧:4Al+ 3O 22Al2O3 (2)与卤素单质、硫等反应:Mg+ Cl 2MgCl2 2Al+ 3Cl 22AlCl3 2Al+ 3S Al2S3 (用于工业制备)Mg+ S MgS [特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。镁在空气中燃烧时有三个反应发生:2Mg+O 22MgO 3Mg+N 2Mg3N22Mg+CO 22MgO+C ②燃烧时都放出大量的热,发出耀眼的白光。利用镁的这种性质来制造照明弹。 ③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。 2.与H2O反应
Mg、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气 Mg+2H 2O(沸水)Mg(OH)2+H2↑2A1+6H2O2A1(OH)3+3H2↑ 3.与酸反应置换出H2 Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓H2SO4,冷浓硝酸中发生钝化现象。所以可用铝制容器贮存冷的浓硫酸或浓硝酸。 4.与某些氧化物反应 (1)镁与二氧化碳反应:2Mg+CO 22MgO+C [特别提醒]:“CO2不能助燃”的说法是不全面的,CO2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。 (2)铝热反应:2Al+ Fe2O32Fe+ Al2O3 铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。 [特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe2O3、FeO、Fe3O4、Cr2O3、V2O5、MnO2等。 ②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。 ③要使用没有氧化的铝粉,氧化铁粉末要烘干。 ④KClO3作为引燃剂,也可以用Na2O2代替。实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。 5.与碱反应 镁不与碱反应,铝与碱液反应:2Al+2NaOH+6H 2O2NaAlO2+4H2O+3H2↑ 简写:2Al+2NaOH+2H 2O2NaAlO2+3H2↑ 二.氢氧化铝 1.物理性质:A l(O H)3是几乎不溶于水的白色胶状固体,具有吸附性。 2.化学性质
镁铝的重要化合物(三) 一.填空题(共15小题) 1.(2014?浙江模拟)某物质M是一种镁基储氢材料.现取84g M在高温条件下加热分解,得到0.5mol固态化合物A(只含有二种短周期元素)和44.8L气体B(气体体积为标准状况下),该气体能使湿润的红色石蕊试纸变蓝.固态化合物A极易与水反应,又有气体B产生. 物质B有如下转化关系:B C D E,E是一种强酸.请回答下列问题: (1)物质A的化学式为_________,属于_________晶体(填“分子”、“离子”、“原子”等). (2)写出M高温分解的化学方程式. (3)将C和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.弱酸F比醋酸酸性稍强,很不稳定,通常在室温下易分解.要制得F溶液,可以往冷冻的其钠盐浓溶液中加入或通入某种物质,下列物质不适合使用的是_________(填序号). a.盐酸b.二氧化碳c.稀硫酸d.二氧化硫 (4)现发现一种活性很强的离子化合物G,其组成为NH5,电子式为_________,NH5与水反应能否产生H2 _________(填“能”与“否”),理由是. (5)现有9.6g镁与极稀的E溶液充分反应无气体产生,加入足量的NaOH溶液并微热,生成B气体(标准状况下)_________L. 2.(2012?江苏)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛. (1)真空碳热还原﹣氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下: Al2O3(s)+AlC13(g)+3C(s)=3AlCl(g)+3CO(g)△H=a kJ?mol﹣1 3AlCl(g)=2Al(l)+AlC13(g)△H=b kJ?mol﹣1 ①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=_________kJ?mol﹣1(用含a、b 的代数式表示). ②Al4C3是反应过程中的中间产物.Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式 为. (2)镁铝合金(Mg17Al12)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得.该合金在一定条件下完全吸氢的反应方程式为Mg17Al122+17H2=17MgH2+12Al.得到的混合物Y (17MgH2+12Al)在一定条件下可释放出氢气. ①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是_________. ②在6.0mol?L﹣1HCl 溶液中,混合物Y 能完全释放出H2.1mol Mg17 Al12完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为_________. ③在0.5mol?L﹣1NaOH 和1.0mol?L﹣1 MgCl2溶液中,混合物Y 均只能部分放出氢气,反应后残留固体物质的X﹣射线衍射谱图如图1所示(X﹣射线衍射可用于判断某晶态物 质是否存在,不同晶态物质出现衍射峰的衍射角不同).在上述NaOH 溶液中,混合物Y 中产生氢气的主要物质是_________
一、知识梳理 (一)钠 1.物理性质 银白色金属,质软,密度比水小钠的密度大于煤油小于水熔点低、具有良好的导电性和导热性。 2.化学性质 (1)与非金属单质的反应 ①Na与O2在点燃的条件下发生反应的化学方程式为:2Na+O2点燃Na2O2。 ②Na在常温下露置于空气中的化学方程式为:4Na+O2===2Na2O ③Na与S的反应为:2Na+S===Na2S (2)与水的反应 ①化学方程式为:2Na+2H2O===2NaOH+H2↑ ②实验现象 a.“浮”:将钠投入水中,钠浮在水面上。说明钠的密度比水小。 b.“熔”:钠熔化成小球。说明钠的熔点低,且该反应是放热反应。 c.“游”:小球在水面上四处游动。说明有气体生成。 d.“响”:有嘶嘶的响声。说明有气体产生且剧烈。 e.“红”:反应后的溶液能使酚酞变红。说明反应生成了碱。 (3)钠用于钛、锆、铌、钽等金属氯化物中置换出金属单质 例如:TiCl4+4Na 700~800℃Ti+4NaCl 3.钠的制取 电解熔融氯化钠 4.钠的保存 实验室中通常把少量钠保存在煤油中,目的是防止Na与空气中的O2和水蒸气发生反应。 (二)钠的几种重要化合物 1.氧化钠和过氧化钠 氧化钠(Na2O) 过氧化钠(Na2O2) 颜色状态白色固体淡黄色固体 电子式 氧化物类型碱性氧化物过氧化物
氧元素化合价-2 -1 阴阳离子数之比1∶2 1∶2 生成条件常温下加热或点燃金属钠 稳定性不稳定,可继续氧化稳定 跟水反应Na2O+H2O===2NaOH 2Na2O2+H2O===4NaOH+O2↑ 跟CO2反应Na2O+CO2===Na2CO32Na2O2+2CO2=== 2Na2CO3+O2 跟酸反应Na2O+2HCl===2NaCl+ H2O 2Na2O2+4HCl=== 4NaCl+2H2O+O2↑用途制NaOH,用途较少作供氧剂、氧化剂、漂白剂等 2.氢氧化钠 俗称:烧碱、火碱、苛性钠。 (1)主要物理性质:白色固体,易吸收空气中的水蒸气而潮解,易溶解于水,并且放出大量的热量,有强腐蚀性。 (2)主要化学性质:为一元强碱,具有碱的通性。 3.碳酸钠和碳酸氢钠 名称及化学式碳酸钠(Na2CO3) 碳酸氢钠(NaHCO3 俗名纯碱、苏打小苏打 颜色、状态白色粉末白色细小晶体 水溶性易溶于水可溶于水 与盐酸反应Na2CO3+2HCl === 2NaCl+H2O+CO2↑ NaHCO3+HCl ===NaCl+H2O+CO2↑ 热稳定性受热难分解 2NaHCO3Na2CO3+H2O+CO2↑ 与NaOH 不反应NaHCO3+NaOH===Na2CO3+H2O 与Ca(OH)2Na2CO3+Ca(OH)2=== CaCO3↓+ 2NaOH NaHCO3+Ca(OH)2===CaCO3↓+NaOH+H2O 或2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O 相互转变(三)镁 1.镁的提取 海水Mg(OH)2MgCl2·6H2O Mg Cl2 MgCl2 加盐酸 浓缩结晶石灰乳脱水电解 贝壳CaO 煅烧水
镁铝的重要化合物(一) 一.选择题(共30小题) 1.下列化学变化中,需加入氧化剂才能实现的是() A.C→CO2B.M nO4﹣→Mn2+C.C uO→Cu D.H2→H2O 2.(2014?淄博二模)下列反应所得溶液中只含一种溶质的是() A.AlCl3溶液中滴入过量NaOH溶液B.Fe2(SO4)3溶液中加入过量铁粉 C.稀HNO3中加入少量铜片D.Ca(ClO)2溶液中通入过量CO2 3.(2014?广东模拟)欲将溶液中的Al3+沉淀完全,最合适的试剂是() A.N aOH溶液B.氨水C.N a2SO4溶液D.N aCl溶液 4.(2014?河南一模)下列有关物质性质的应用不正确的是() A.氯化铝是一种电解质,可用于电解法制铝 B.二氧化硅虽然不与强酸反应,但不能用玻璃器皿盛放氢氟酸 C.生石灰能与水反应,可用来干燥氨气 D.液氨汽化时要吸收大量的热,可用作制冷剂 5.(2014?德州二模)下列有关叙述不正确的是() A.M gO、Al2O3熔点高,可用于制作耐火材料 B.用浓氢氧化钠溶液可除去乙酸乙酯中混有的乙酸、乙醇杂质 C.除去NaCl溶液中的Na2CO3,应选择试剂为盐酸,而不是硝酸 D.油脂在碱性条件下易发生水解,可用于制作肥皂 6.(2014?河北模拟)向溶液X中持续通入过量气体Y,会产生“先浑浊,后澄清”现象的是()A.X:氯化钙溶液Y:二氧化碳B.X:硝酸钡溶液Y:二氧化硫 C.X:氯化铝溶液Y:氨气D.X:偏铝酸钠溶液Y:二氧化氮 7.(2014?莆田模拟)甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是() A.若甲是AlCl3溶液,则丁可能是NaOH溶液 B.若甲是Fe,则丁可能是Cl2 C.若丁是CO2,则甲可能为Mg D.若丁是O2,则乙、丙的相对分子质量可能相差16 8.(2014?江苏模拟)铝是一种很重要的金属,可以发生一系列反应制备物质,如图所示. 下列说法错误的是()
高中化学学习材料 宜阳县实验中学 2011年高考一轮镁铝及其化合物 1.把Ba(OH)2溶液滴入明矾溶液中,使SO42ˉ全部转化成BaSO4沉淀,此时铝元素的主要存在形式是 A、Al3+ B、Al(OH)3 C、AlO2ˉ D、Al3+和Al(OH)3 2.若1.8g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氢气,则该金属是A.Al B.Mg C.Fe D.Zn 3.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应: Tl3++ 2Ag ==Tl+ + 2Ag+。下列推断正确的是 A.Tl+ 的最外层有1个电子 B.Tl3+ 的氧化性比Al3+弱 C.Tl能形成+3价和+1的化合物D.Tl+ 的还原性比Ag强 4.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3 C 高温 2 AlN + 3 CO 下列叙述正确的是 A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 B.上述反应中每生成2 mol AlN,N2得到3 mol电子 C.氮化铝中氮元素的化合价为—3 D.氮化铝晶体属于分子晶体 5.向一定量的下列物质的溶液中逐滴加入氢氧化钠溶液,先生成白色沉淀,后沉淀逐渐溶解.这种物质是 A.MgS04 B.NaAl02 C.A1C13D.FeCl3 6.相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是 A.Al B.Al(OH)3 C.Al Cl3 D.Al2O3 7.将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
第2讲镁、铝及其重要化合物 一、Mg、Al的性质 1.铝的原子结构与物理性质 2.铝的化学性质(写出化学方程式)
3.铝的制备及用途 对比记忆铝、镁的化学性质
3Mg +N 2=====点燃 Mg 3N 2 与CO 2反应 2Mg +CO 2=====点燃 2MgO +C 与水反应 反应很困难 能与沸水反应Mg +2H 2O=====△ Mg(OH)2+H 2↑ 与碱反应 能溶于 强碱溶液 不反应 [(1)铝在空气中耐腐蚀,所以铝是不活泼金属( ) (2)铝箔插入稀硝酸中无现象,说明铝箔表面被HNO 3氧化,形成致密的氧化膜 ( ) (3)1 mol Al 与足量的硫酸或足量的氢氧化钠溶液反应转移电子数相同( ) (4)铝与盐酸反应时,盐酸作氧化剂,铝与氢氧化钠溶液反应时,氢氧化钠作氧化剂( ) (5)铝与少量NaOH 溶液反应得到铝盐,与足量NaOH 溶液反应生成偏铝酸盐( ) (6)工业上电解熔融状态的Al 2O 3制备Al( ) (7)冶炼铝时常用焦炭作还原剂( ) (8)MgO 与Al 粉的混合物也可称为铝热剂( ) 提示:(1)× (2)× (3)√ (4)× (5)× (6)√ (7)× (8)× 二、铝的重要化合物 1.氧化铝 (1)物理性质:白色固体,难溶于水,有很高的熔点。 (2)化学性质: 写出图中有关反应的离子方程式: ①Al 2O 3+6H + ===2Al 3+ +3H 2O ; ②Al 2O 3+2OH - ===2AlO - 2+H 2O 。 2.氢氧化铝 (1)物理性质。 白色胶状不溶于水的固体,有较强的吸附性。 (2)化学性质(用化学方程式表示)。 Al(OH)3的电离方程式为 H + +AlO - 2+H 2O] Al(OH)3Al 3++3OH - ] 酸式电离________________________碱式电离__。 写出图中有关反应的化学方程式或离子方程式:
镁、铝及其化合物知识点整理Ⅰ.课标要求 1.通过海水制镁的事例了解镁及化合物的性质. 2.通过合金材料了解铝及化合物的性质. 3.能列举合金材料的重要应用. Ⅱ.考纲要求 1.掌握镁铝及化合物的性质. 2.了解镁铝及化合物在生活.生活中的应用.Ⅲ.教材精讲 一. Mg、Al的化学性质 1.与非金属反应 (1)与O 2反应:常温下与空气中的O 2 反应生成一层致密的氧化物 薄膜,所以镁、铝都有抗腐蚀的性能。镁能在空气中燃烧: 2Mg+O 22MgO ,铝在纯氧中燃烧:4Al+ 3O 2 2Al 2 O 3
(2)与卤素单质、硫等反应:Mg+ Cl 2 MgCl 2 2Al+ 3Cl 2 2AlCl 3 2Al+ 3S Al 2S 3 (用于工业制备) Mg+ S MgS ③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。 2.与H 2O 反应 Mg 、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气 Mg+2H 2O (沸水) Mg(OH)2+H 2↑ 2A1+6H 2O 2A1(OH)3+3H 2↑ 3.与酸反应置换出H 2 [特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。镁在空气中燃烧时有三个反应发生: 2Mg+O 2 2MgO 3Mg+N 2 Mg 3N 2 2Mg+CO 2 2MgO+C ②燃烧时都放出大量的热,发出耀眼的白光。利用镁的这种性质来制造照明弹。
Mg 、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H 2,其中铝在冷浓 H 2SO 4,冷浓硝酸中发生钝化现象。所以可用铝制容器贮存冷的浓硫酸或浓硝酸。 4.与某些氧化物反应 (1)镁与二氧化碳反应:2Mg+CO 2 2MgO+C [特别提醒]:“CO 2不能助燃”的说法是不全面的,CO 2对绝大多数可燃物是良好的灭火剂,而对K 、Ca 、Na 、Mg 等可燃物却是助燃剂。 (2)铝热反应:2Al+ Fe 2O 3 2Fe+ Al 2O 3 铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V 、Cr 、等。 [特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe 2O 3 、FeO 、Fe 3O 4、Cr 2O 3、V 2O 5、MnO 2等。 ②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。 ③要使用没有氧化的铝粉,氧化铁粉末要烘干。 ④KClO 3作为引燃剂,也可以用Na 2O 2代替。实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。
镁和铝的重要化合物(3节时) 目的要求】: 1. 认识镁和铝的几种重要化合物的性质和主要用途; 2. 认识氧化铝和氢氧化铝的两性和主要用途; 3. 了解复盐和明矾的净水作用。 : 氢氧化铝的两性 : 自学阅读,思考总结,启发引导。 : 第一课时完成镁的重要化合物及氧化铝的物理性质和用途 第二课时完成铝的重要化合物的性质和用途 第三课时简单介绍明矾及知识归纳和拓展,评讲练习 : (第一节时) 〖引言〗:直接引入
〖自学阅读〗:学生阅读课本26-27页 〖投影〗:[思考讨论]: 1. 课本介绍了MgO和MgCl2的哪些知识? 2. MgO有何突出的物理特性?因而有何应用? 3. 自然界无MgO矿石,怎样得到它?有哪些制取途径,哪些途径合理? 4. MgCl2主要用于做什么?如何得到它,什么方法更有实际意义? 5. 从海水中提取MgCl2,最后冶炼Mg,运用了MgCl2什么化学性质? 〖演示实验〗:1.展示MgO和MgCl2的.样品,有学生观察总结物理性质。 2. MgO溶于水,滴加酚酞 〖师生活动〗:教师引导,学生回答、讨论思考题,得出结论。
〖补充讲解〗:海水的综合利用 1. 海水咸、苦的原因;量多:淡水占99%,咸水占1% 2. 海水含盐量高,若全部提取出来,地壳陆地可上升160米 3. 海水淡化问题及将来解决办法的设想 : 一、镁的重要化合物 MgO MgCl2 物理性质熔点很高吸水性,易潮解 1.性质: 酸 HCl 化学性质 MgO + H2O = Mg(OH)2 MgCl2(盐) + 碱 Mg(OH)2
(极少) 盐…… 高温3.制法: MgCO3 === MgO + CO2↑ 海水苦卤 Mg(OH)2 MgCl2 (第二节时) 〖引入〗:直接引入 〖演示实验〗:展示Al2O3和Al(OH)3样品 〖投影〗:[思考讨论]: 1. 有何突出的化学性质? 2. 有化学方程式和离子方程式表示Al2O3和Al(OH)3分别与H2SO4和NaOH的反应。(会考必考) 3. 自然界有Al2O3,却没有Al(OH)3,如何制取Al(OH)3?能否用Al2O3和水反应?为什么? 4. 实验室用铝盐制取Al(OH)3,加NaOH和NH3 H2O哪种好?为什么?
镁铝及其化合物学生教案
镁铝及其化合物 一、物理性质 银白色固体、镁的硬度、熔点均低于铝。 二、原子结构 三、化学性质 1.与非金属反应 2Mg +O 2 =(点燃)2MgO 4Al +3O 2=(△)2 Al 2 O 3 Mg+Cl 2 = (点燃)MgCl 2 4Al+3Cl 2=(△)2AlCl 3 Mg + S= (△)MgS 2Al + 3S=(△)Al 2S 3 3Mg+ N 2=(△)Mg 3 N 2 不 反应 ●镁与铝在常温下均可生成致密的氧化膜,保护金属。 2.与酸反应 Mg + 2H+ = Mg2+ + H 2 ↑(与硝酸反应复杂,浓度不同,还原产物不同) 2Al + 6H+ = 2Al3+ + 3H 2 ↑(常温下遇浓硝酸、冷的浓硫酸钝化) 3.与沸水反应
Mg +H 2O=(△)Mg(OH) 2 +H 2 ↑ Al不 反应,铁与沸水也可反应。 4.与氧化物反应 2Mg + CO 2 =(点燃)2MgO + C 2Al+Fe 3O 4 =(高温)2Fe+ Al 2 O 3 5.与碱反应 镁不反应 2Al + 2H 2O +2NaOH =2NaAlO 2 + 3H 2 ↑ 四、氧化镁与氧化铝(两性氧化物) 1.物理性质 白色固体、密度小、熔点高,用于生产耐火、耐高温材料。 2.化学性质 ●与水反应: MgO+H 2O=Mg(OH) 2 很慢 不反应 ●与酸反应:MgO+2H+=Mg2++H2O Al 2O 3 + 6H+=2Al3++3H 2 O ●与碱反应:不反应 Al 2O 3 + 2OH+=2AlO 2 -+H 2 O 五、氢氧化铝与氢氧化镁 1.物理性质 氢氧化镁是难溶的中强碱,能使酚酞变红。
高中化学学习材料 镁、铝及其重要化合物 一、选择题(包括8小题。1~6只有一个选项符合题意,7~8有两个选项符合题意。) 1.常温下,把钠、镁和铝各一小块分别投入到1mol/L NaOH溶液中,化学反应速率(v)由快到慢的顺序是() A.v钠>v镁>v铝 B.v铝>v钠>v镁 C.v钠>v铝>v镁 D.v铝>v镁>v钠 2.只用胶头滴管和试管,不用其他试剂就可以区别的溶液(浓度均为0.1 mol·-1L)是() ①CaCl2和Na2CO3②Ba(OH)2和NaHCO3 ③稀H2SO4和Na2CO3 ④NaAlO2和盐酸⑤AlCl3和NaOH A.①②③ B.③④⑤ C.①② D.全部 3.若1.8 g某金属跟足量盐酸充分反应,放出2.24 L(标准状况)氢气,则该金属是() A.Al B.Mg C.Fe D.Zn 4.用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如右图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断, 下列说法错误的是() A.实验中发生的反应都是氧化还原反应 B.铝是一种较活泼的金属 C.铝与氧气反应放出大量的热量 D.铝片上生成的白毛是氧化铝和氧化汞的混合物 5.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2yCO3,关于该物 质的说法正确的是() A.该物质属于两性氢氧化物 B.该物质是Al(OH)3和Na2CO3的混合物 C.1 mol NaAl(OH)2yCO3最多可消耗3 mol H+ D.该药剂不适合于胃溃疡患者服用 6.由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如下图转化关系(部 分生成物和反应条件略去)。下列推断不正确的是() A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应 B.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E一定能还原Fe2O3
镁铝及其化合物知识点 SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-
镁、铝及其化合物知识点整理 Ⅰ.课标要求 1.通过海水制镁的事例了解镁及化合物的性质. 2.通过合金材料了解铝及化合物的性质. 3.能列举合金材料的重要应用. Ⅱ.考纲要求 1.掌握镁铝及化合物的性质. 2.了解镁铝及化合物在生活.生活中的应用.Ⅲ.教材精讲 一. Mg、Al的化学性质 1.与非金属反应 (1)与O 2反应:常温下与空气中的O 2 反应生成一层致密的氧化物 薄膜,所以镁、铝都有抗腐蚀的性能。镁能在空气中燃烧: 2Mg+O 22MgO ,铝在纯氧中燃烧:4Al+ 3O 2 2Al 2 O 3
(2)与卤素单质、硫等反应:Mg+ Cl 2 MgCl 2 2Al+ 3Cl 2 2AlCl 3 2Al+ 3S Al 2S 3 (用于工业制 备) Mg+ S MgS ③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。 2.与H 2O 反应 Mg 、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气 Mg+2H 2O (沸水) Mg(OH)2+H 2↑ 2A1+6H 2O 2A1(OH)3+3H 2 ↑ [特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。镁在空气中燃烧时有三个反应发生: 2Mg+O 2 2MgO 3Mg+N 2 Mg 3N 2 2Mg+CO 2 2MgO+C ②燃烧时都放出大量的热,发出耀眼的白光。利用镁的这种性质来制造照明弹。
3.与酸反应置换出H 2 Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H 2 ,其中铝 在冷浓 H 2SO 4 ,冷浓硝酸中发生钝化现象。所以可用铝制容器贮存冷 的浓硫酸或浓硝酸。 4.与某些氧化物反应 (1)镁与二氧化碳反应:2Mg+CO 2 2MgO+C [特别提醒]:“CO 2不能助燃”的说法是不全面的,CO 2 对绝大多 数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。 (2)铝热反应:2Al+ Fe 2O 3 2Fe+ Al 2 O 3 铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。[特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金 属氧化物可以是:Fe 2O 3 、FeO、Fe 3 O 4 、Cr 2 O 3 、V 2 O 5 、MnO 2 等。 ②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。 ③要使用没有氧化的铝粉,氧化铁粉末要烘干。
镁铝及其化合物 一、物理性质 银白色固体、镁的硬度、熔点均低于铝,是由于二者的金属键强度不同造成的。 二、原子结构 镁的第一电离能高于铝,由原子结构决定的。 三、化学性质 1.与非金属反应 2Mg +O2=(点燃)2MgO 4Al +3O2=(△)2 Al2O3 Mg+Cl2= (点燃)MgCl2 4Al+3Cl2=(△)2AlCl3 Mg + S= (△)MgS 2Al + 3S=(△)Al2S3 3Mg+ N2=(△)Mg3N2 不反应 ●镁与铝在常温下均可生成致密的氧化膜,保护金属。 ●镁在空气中点燃,可与N2、O2、CO2反应。 2.与酸反应 Mg + 2H+ = Mg2+ + H2↑(与硝酸反应复杂,浓度不同,还原产物不同)2Al + 6H+ === 2Al3+ + 3H2↑(常温下遇浓硝酸、冷的浓硫酸钝化) 3.与沸水反应 Mg +H2O=(△)Mg(OH)2+H2↑ Al不反应,铁与沸水也可反应。 4.与氧化物反应 2Mg + CO2=(点燃)2MgO + C 2Al+Fe3O4=(高温)2Fe+ Al2O3 5.与碱反应 镁不反应 2Al + 2H2O +2NaOH =2NaAlO2 + 3H2↑ 四、氧化镁与氧化铝(两性氧化物) 1.物理性质 白色固体、密度小、熔点高,用于生产耐火、耐高温材料。 2.化学性质 ●与水反应: MgO+H2O=Mg(OH)2 很慢不反应 ●与酸反应: MgO+2H+=Mg2++H2O Al2O3+ 6H+=2Al3++3H2O ●与碱反应:不反应 Al2O3+ 2OH+=2AlO2-+H2O 五、氢氧化铝与氢氧化镁 1
第二节镁、铝及其化合物 一、选择题(每小题4分,共48分) 1.(2011·海口调研)下列有关金属铝及其化合物的叙述正确的是() A.铝在常温下不能与氧气反应 B.铝不能与氯气反应 C.铝既能溶于酸,又能溶于强碱 D.氧化铝只能与酸反应,不能与碱反应 解析:铝在常温下可与O2反应,A错;铝能与氯气反应,B错;氧化铝是两性氧化物,既能与酸反应又能与碱反应,D错。 答案:C 2.(2011·扬州模拟)若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是() A.NH+4NO-3CO2-3Na+ B.Na+Ba2+Mg2+HCO-3 C.NO-3Ca2+K+Cl- D.NO-3K+AlO-2H+ 解析:A项,在酸性条件下因有NO-3,不能生成H2,在碱性条件下,OH-与NH+4不共 存,故A项不符合;B项,HCO-3与H+或OH-均不能大量共存;C项,在碱性条件下符 合题意;D项表示的为酸性条件,含有HNO3,不可能与Al反应放出氢气,且AlO-2和H+不能大量共存。 答案:C ks5u 3.(2011·潍坊模拟)下列各反应的离子方程式中,错误的是() A.硫酸铝溶液中加入过量的氨水: Al3++3NH3·H2O===Al(OH)3↓+3NH+4 B.铁片放入过量的稀硝酸中: 3Fe+8H++2NO-3===3Fe2++2NO+4H2O C.将铝片放入过量NaOH溶液中: 2Al+2OH-+2H2O===2AlO-2+3H2↑ D.偏铝酸钠与过量盐酸反应: AlO-2+4H+===Al3++2H2O 解析:B项正确离子方程式为:Fe+4H++NO-3===Fe3++NO↑+2H2O。 答案:B 4.(2011·烟台模拟)在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(x)与溶液中沉淀的量(y)的关系示意图中正确的是()
§2-3 镁和铝的重要化合物(二) 教学内容:高二化学(必修)第二章第三节 ?认知目标:了解镁铝化合物的性质、用途。 情感目标:掊养热爱科学的情感,激发科学知识运用于生产,生活实际的愿望。 技能目标:培养观察能力,学习实验操作技能。 ?教学重点:镁铝化合物的化学性质。 ?教学难点:镁铝化合物的用途。 ?教学方法:接受式策略,以实验为基础的启发式。 ? ?教学过程: 二.铝的重要化合物: (一)氧化铝: (二)氢氧化铝Al(OH)3 : (1)氢氧化铝的制取: 由于氧化铝不能溶于水,因而不能用氧化铝与水反应来制取,而只能用可溶性盐与碱反应来制取。 [演示]:氢氧化铝的制取 现象:往可溶性铝盐中加入氨水,出现了大量白色沉淀。 Al2(SO4)3 + 6NH3H2O == 2 Al(OH)3↓ + 3(NH4)2SO4 由学生书写离子方程式。 [思考] 在此实验中,为何用弱碱氨水而不用强碱如氢氧化钠(此问题由学生自己思考,介绍完氢氧化铝的化性后再由学生回答) [结论]:氢氧化铝是一种难溶性的白色胶絮状的氢氧化物。 (2)氢氧化铝的两性: [演示] 氢氧化铝与强酸和强碱的反应: 现象:氢氧化铝既能溶于强酸,又能溶于强碱,是一种典型的两性氢氧化物。
Al(OH)3 + 3H+ == Al3+ + 3H2O Al(OH)3 + OH- == AlO2- + 2H2O [思考]: 往氯化铝的溶液中逐滴加入氢氧化钠溶液会出现什么现象?为什么?提示:会出现先有沉淀,然后沉淀又会消失,其离子方程式如下: Al3+ + 3OH- == Al(OH) 3 ↓ Al(OH) 3 + 3H+ == Al3+ + 3H 2 O 现在可以由学生自己回答刚才提出的问题:为什么制氢氧化铝只能用弱碱而不能用强碱?因为过量的强碱可以使制得的氢氧化铝消失。 [思考] 向1mol/L的氯化铝溶液中逐滴加入1mol/L的氢氧化钠溶液,试描绘出生成沉淀的物质的量与加入的氢氧化钠的体积之间的关系(纵坐标表示生成沉淀的物质的量,横坐标表示加入的氢氧化钠的体积) [提示] 注意沉淀的物质的量的变化与所加入的溶液体积之间的关系(生成最大量与使沉淀完全消失消耗的溶液体积之比为3:1) 0 1 2 3 4 V NaOH(ml) [例题]:向1mol/L和AlCl3溶液10ml中加入1mol/L的NaOH溶液得到 沉淀0.26克,所加NaOH溶液的体积可能为 A.40ml B.72ml C.80ml D.128ml