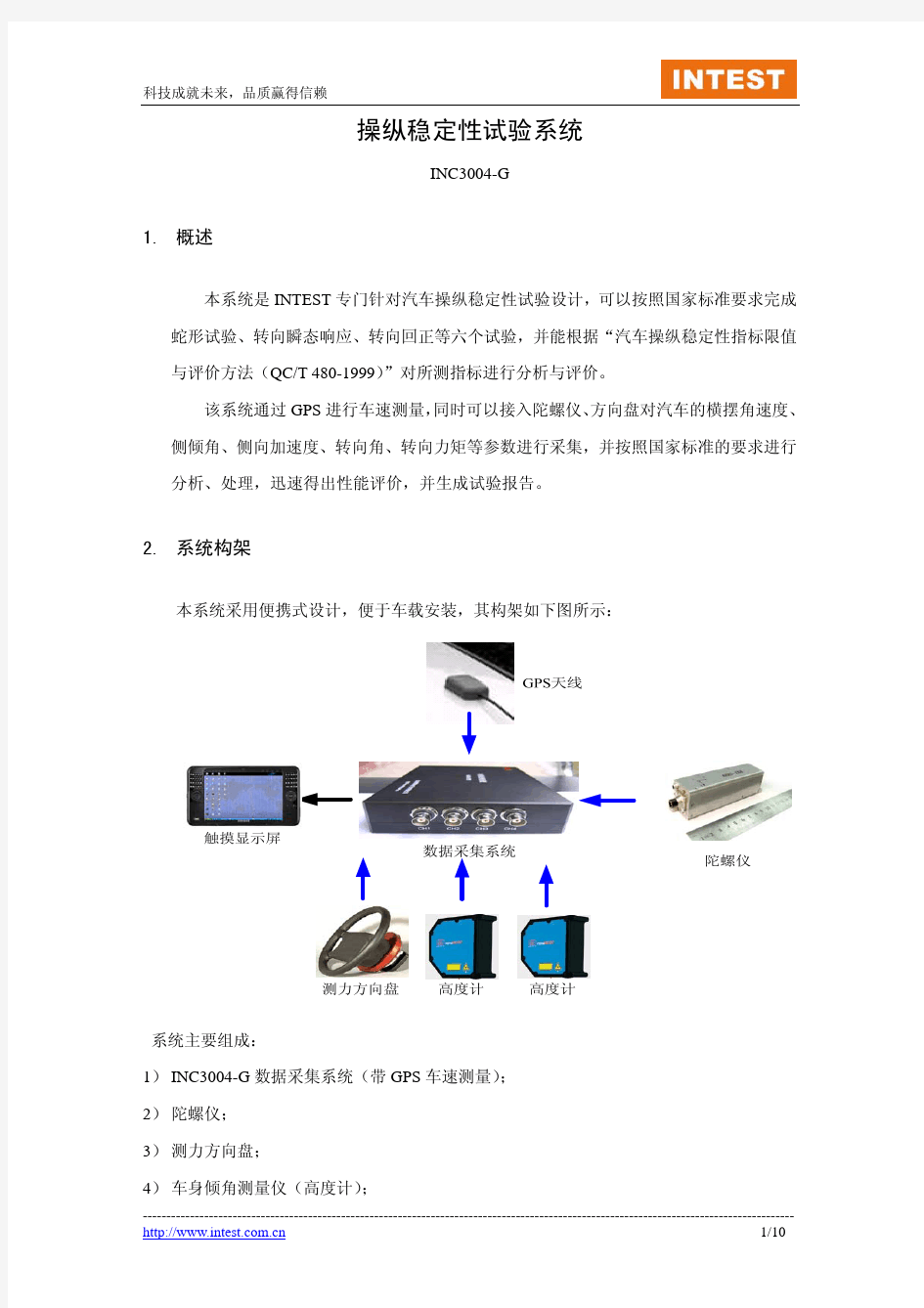

稳定性实验方案(参考) 诊断原料稳定性考核主要包括热稳定性、真实稳定性、运输稳定性及冻融稳定性四部分,工作流程如下图所示,具体方案见下文。 根据抗原和抗体进行分类,此外结合产品的用途,综合考虑上述实验内容的安排和设计,以便满足市场客户需求,合理调配公司资源。现给出各类型开展稳定性评价分具体实验方案。 1 1.1 此外为间2-8℃ 1.2 工作条件下的稳定性考核主要涉及校准品、质控品等的稳定性问题,是基于客户使用的立场开展的用途评价及相关研究。工作重点主要是稳定性基质的筛选和评价、稳定性的持续监测等。 根据项目检测特点,采用不同的稀释液制备客户检测的工作浓度样品,一般主要为低值和高值两个测值样本,通过评价-20℃、2-8℃以及37℃存放一定时间(根据各项目确定)的测值相对偏倚来考核其分析内稳定性结果。分析间稳定性考核主要涉及低值和高值样本的制备过程,要求将当时制备的高浓度蛋白分装冻存于-80℃条件下,需要开展组间分析时,采用重现性实验过程,执行过程的重复制备。分析间评价主要用于考核-20℃条件下存放不稳定的蛋白样品。 持续检测的实验主要目的是站在客户的立场,在较长时间内监测工作浓度蛋白真实稳定性而开展的评价内容。
主要采用相对稳定的检测方法,对热稳定性合格条件下,开展蛋白的使用效果监测,通过重现性实验对比分析实现。例如:采用经过热稳定性评价合格的抗体制备的检测系统,该检测系统批间差异在理想范围内,采用该系统对考核蛋白进行持续检测,持续检测的结果在一定范围内(可以参考绘制质控图,如L-J质控图),判定为稳定性是否合格。该过程不涉及制备环节,是真实地反应蛋白使用时的稳定性,输出内容为校准品或质控品解决方案。 注:用于检测抗体的蛋白,即用于捕获或标记的蛋白,只评价1.1,不涉及1.2。 2 抗体的稳定性实验方案 2.1 发货抗体的稳定性实验 37℃条件存放于 (可以 2.2 工作条件下的稳定性考核主要涉及检测系统的稳定性问题,是基于客户使用的立场开展的用途评价及相关研究。工作重点主要是采用抗体制备的诊断试剂本身的稳定性评价、稳定性的持续监测等。 根据项目检测特点以及检测系统平台方法学而异,采用不同的制备方案建立检测系统,对该检测系统开展的稳定性实验,包括热稳定性和真实的稳定性监测两块。最终输出结果为检测系统的稳定性结论,客户根据该结果可以作为建立检测系统的参照。 将检测系统相关的试剂,分别放于2-8℃以及37℃存放一定时间(根据各项目确定),通过功能性实验来评价检测系统的稳定性,一般以2-8℃和37℃之间的相对偏倚来标识,此外检测系统本身的功能性能也至关重要(如灵敏度、精密度等)。上述指标的检测结果以报告的形式给出,最终达到我们对产品后续性能的足够了解,以便
L- 腈化物稳定性试验报告 一、概述 L-腈化物是L- 肉碱生产过程中的第一步中间体(第二步中间体: L-肉碱粗品;第三步中间体:L-肉碱潮品),由于L- 肉碱生产工艺为 间歇操作,即每生产一步中间体,生产完毕并出具合格检测报告后,存 入中间体仓库,以备下一步生产投料所需。根据本公司L- 肉碱产品的 整个生产周期,L- 腈化物入库后可能存放的最长时间为4 周(约28 天)。以此周期为时间依据制定了L- 腈化物稳定性试验方案,用于验 证L-腈化物在再试验期限内的各项质量指标数据的稳定性,并且能否符 合L- 腈化物的质量标准,此次稳定性试验的整个周期为28 天,具体 的稳定性试验方案以ICH 药物稳定性指导原则为基础制定,以确保L- 腈化化物稳定性试验的可操作性。 二、验证日期 2010 年1 月13 日- 2010 年2 月10 日 三、验证方案 1)样品储存和包装: 考虑到L- 腈化物今后的贮藏、使用过程,本次用于稳定性试验的样品 批次与最终规模生产所用的L- 腈化物的包装和放置条件相同。 2)样品批次选择:此次稳定性试验共抽取三批样品,且抽取样品的批次与 最终规模生产时的合成路线和生产工艺相同
3)抽样频率和日期:从2010.1.13 起,每隔7 天取样一次,共取五次,具体日期为:2010.1.13 、2010.1.20 、2010.1.27 、 2010.2.3 、2010.2.10 ,以确保试验次数足以满足L- 腈化物的稳 定性试验的需要。。 4)检测项目:根据L- 腈化物的质量标准的规定,此次稳定性试验的检测项目共五项,分别为外观、氯含量、熔点、比旋度、干燥失重。这 些指标在L- 腈化物的储存过程中可能会发生变化,且有可能影响 其质量和有效性。 5)试样来源和抽样:L- 腈化物由公司102 车间生产,经检测合格后储存于中间体仓库,本次稳定性试验的L- 腈化物均取自于该中间体仓 库,其抽样方法和抽样量均按照L- 腈化物抽样方案进行抽样。抽 样完毕后直接进行检测分析,并对检测结果进行登记,保存,作为稳 定性数据评估的依据。 四、稳定性试验数据变化趋势分析及评估 通过对三批L- 腈化物的稳定性试验,对其物理、化学方面稳定性资料进行评价,旨在建立未来相似情况下,大规模生产出的L- 腈化物是否适用 现有的再试验期(28天)。批号间的变化程度是否会影响未来生产的
《结构的强度和稳定性试验》活动方案 重庆巴南中学蒲东 一、方案名称:《结构的强度和稳定性试验》 二、方案目标: 技术试验是解决技术问题的重要方法。技术试验有多种作用,如对不同材料进行强度试验,目的在于选择符合设计要求的材料;如对结构进行加载模拟试验,目的在于检测或改进结构的强度。技术试验有多种方式,如撞击试验、承载试验和模拟试验等。 做以下技术试验的目的是使同学们加深对结构的理解,并通过技术试验测试了解影响结构强度和稳定性的多种因素。 三、活动对象:高二年级学生 四、活动时间:2013年3月至5月 五、方案主体: (一)按要求进行试验 1.将3条长30cm,横截面10mm×10mm的木棍销接在一个圆盘上,组成一个三脚架。将三脚架放在光滑的台面上,在三脚架上加载重物,观察三脚架的几何形状发生了什么变化,并记录如下。
2.在三脚架的3条腿处拴上橡皮筋,重复试验1的加载过程,观察橡皮筋的变化,并记录橡皮筋的长度。 思考:橡皮筋发生变化说明了什么。 3.用弹簧测力计替代橡皮筋,重复试验2的加载过程,记录弹簧测力计的读数。 思考:在三脚架结构承载时,若要保持其几何形状基本不变,你有哪些方法。请同学们对三脚架结构进行改进,使其在承载质量不超过5kg时,能保持其几何形状基本不变,在这里我们推荐在三脚架各边增设横档的方法进行改进。 讨论选择横档材料应考虑哪些因素,横档怎样与三脚架连接。 (二)同学们自行设计技术试验方案: 对改进后的三脚下架结构进行承载试验,并写出技术试验报告。 试验目的 1.检验横档材料的选择是否满足设计的要求。 2.检测改进后的三脚下架结构是否能承载5kg的重物。 3.检测三脚架结构中各构件的连接是否牢固。 技术试验过程:
药物稳定性试验指导原则 附录ⅪⅩC药物稳定性试验指导原则 稳定性试验得目得就是考察原料药或药物制剂在温度、湿度、光线得影响下随时间变化得规律,为药品得生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品得有效期、 稳定性试验得基本要求有以下几个方面。(1)稳定性试验包括影响因素试验、加速试验与长期试验。影响因素试验适用于原料药得考察,用1批原料药进行。加速试验与长期试验适用于原料药与药物制剂,要求用3批供试品进行、(2)原料药供试品应就是一定规模生产得,供试品量相当于制剂稳定性实验所要求得批量,原 料药合成工艺路线、方法、步骤应与大生产一致。药物制剂得供试品应就是放大试验得产品(如片剂或胶囊剂在10000片左右或10000粒左右,特殊剂型、特殊品种所需数量、根据具体情况灵活掌握)、其处方与生产工艺应与大生产一致、(3)供试品得质量标准应与各项基础研究及临床验证所使用得供试品质量标准一致、 (4)加速试验与长期试验所用供试品得容器与包装材料及包装方式应与上市产品一致。(5)研究药物稳定性, 要采用专属性强、准确、精密、灵敏得药物分析方法与有关物质(含降解产物及其她变化所生成得产物)得检查方法,并对方法进行验证,以保证药物稳定性结果得可靠性。在稳定性试验中,应重视有关
物质得检查、本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。 一、原料药 原料药要进行以下试验。 (一)影响因素试验 此项试验就是在比加速试验更激烈得条件下进行。其目得就是探讨药物得固有稳定性、了解影响其稳定性得因素及可能得降解途径与降解产物,为制剂生产工艺、包装、贮存条件与建立降解产物得分析方法提供科学依据、供试品可以用一批原料药进行,将供试品置适宜得容器中(如称量瓶或培养皿),摊成≤5mm厚得薄层,疏松原料药摊成≤10mm厚薄层,进行以下实验、 1.高温试验 供试品开口置适宜得密封洁净容器中,60℃温度下放置10天,于第5天与第10天取样,按稳定性重点考察项目进行检测、若供试品有明显变化(如含量下降5%),则在40℃条件下同法进行试验。若60℃无明显变化,不再进行40℃试验。 2。高湿度试验 供试品开口置恒湿密闭容器中,在25℃分别于相对湿度90%±5%条件下放置10天,于第5天与第10天取样,按稳定性重点考察项目要求检测,同时准确称量试验前后供试品得重量,以考察供试品得吸湿潮解性能。若吸湿增重5%以上,则在相对湿度75%±5%条件下,同法进行试验;若吸湿增重5%以下,且其她考察项目符合要求,则不再进行
5.确认内容 6.再确认要求 7.确认结果汇总 8.结果评价 1.目的 明确稳定性试验箱的校验项目、校验条件、校验方法、接受标准、校验周期等,便于检验人员按规程进行稳定性试验箱的校验操作。保证实验室使用的称量点称量的准确性。 2.确认人员及职责
QC分析人员:负责起草确认方案和报告、组织协调开展确认; QC主管:审核确认报告和报告; 质量部长:批准确认报告和报告。 3. 确认前确认 复核人:日期:年月日4. 确认依据及判断标准 4.1确认依据 4.1.1《ZSW系列稳定性试验箱安装使用说明》 4.1.2《环境试验设备温度、湿度校准规范》JJF1101-2003 4.1.3《稳定性试验箱的校验操作规程》(QC-4011) 4.2评判标准 4.2.1性能确认(PQ)
4.2.2 时间 确认 温度 分别 值有℃和 的差值时 发出 5. 5.1 于 按以上要求布放温湿度记录仪探头,将实验设备的温湿度设定到规定的温度,等待温湿度稳定。温湿度稳定后开始读数,每2分钟记录所有测试点的温度一次,在60分钟内共测试30次。 5.2超限度报警时间确认 确认打开箱门至温度和相对湿度分别显示与设定值有2℃和5%RH的差值时报警器均应发出报警声,并记录这个时间;关上箱门记录温湿度恢复至设定值所用的时间。 5.3短信报警功能确认 确认当温湿度超限度时,短信报警功能是否正常运行。
6.再确认要求 6.1再确认周期 6.1.1设备大修后需再校验。 6.1.2由于检修、调整、迁移或其它原因,可能对设备的安装情况、主要技术参数和功能有影响时,应进行再确认。 6.1.3稳定性试验箱每年校验1次,更换部件或对仪器性能有怀疑时,应随时确认。 6.2再确认内容 进行设备的再校验,可针对设备性能中部分必须的项目进行再确认,而不一定要进行全面的确认。 8. 结果评价 起草人/日期: QC审核人/日期:
附件3 特殊医学用途配方食品稳定性研究要求(试行) 一、基本原则 特殊医学用途配方食品稳定性研究是质量控制研究的重要组成部分,其目的是通过设计试验获得产品质量特性在各种环境因素影响下随时间 稳定性研究用样品应在满足《特殊医学用途配方食品良好生产规范》要求及商业化生产条件下生产,产品配方、生产工艺、质量要求应与注册申请材料一致,包装材料和产品包装规格应与拟上市产品一致。 影响因素试验、开启后使用的稳定性试验等采用一批样品进行;加速试验和长期试验分别采用三批样品进行。 (二)考察时间点和考察时间
稳定性研究目的是考察产品质量在确定的温度、湿度等条件下随时间变化的规律,因此研究中一般需要设置多个时间点考察产品的质量变化。考察时间点应基于对产品性质的认识、稳定性趋势评价的要求而设置。加速试验考察时间为产品保质期的四分之一,且不得少于3个月。长期试验总体考察时间应涵盖所预期的保质期,中间取样点的设置应当考虑产品的稳定性特点和产品形态特点。对某些环境因素敏感的产品,应适当增加考 3.检验方法:稳定性试验考察项目原则上应当采用《食品安全国家标准特殊医学用途配方食品通则》(GB 29922)、《食品安全国家标准特殊医学用途婴儿配方食品通则》(GB 25596)规定的检验方法。国家标准中规定了检验方法而未采用的,或者国家标准中未规定检验方法而由申请人自行提供检验方法的,应当提供检验方法来源和(或)方法学验证资料。检验方法应当具有专属性并符合准确度和精密度等相关要求。
四、试验方法 (一)加速试验 加速试验是在高于长期贮存温度和湿度条件下,考察产品的稳定性,为配方和工艺设计、偏离实际贮存条件产品是否依旧能保持质量稳定提供依据,并初步预测产品在规定的贮存条件下的长期稳定性。加速试验条件由申请人根据产品特性、包装材料等因素确定。 %。如在6 温度 %, 25℃±2℃ 长期试验是在拟定贮存条件下考察产品在运输、保存、使用过程中的稳定性,为确认贮存条件及保质期等提供依据。长期试验条件由申请人根据产品特性、包装材料等因素确定。 长期试验考察时间应与产品保质期一致,取样时间点为第一年每3个月末一次,第二年每6个月末一次,第3年每年一次。 如保质期为24个月的产品,则应对0、3、6、9、12、18、24月样品进行
附录ⅩⅠⅩ C原料药与药物制剂稳定性试验指导原则 稳定性试验的目的是考察原料药或药物制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。 稳定性试验的基本要求是:(1)稳定性试验包括影响因素试验、加速试验与长期试验。影响因素试验用一批原料药或一批制剂进行。加速试验与长期试验要求用三批供试品进行。(2)原料药供试品应是一定规模生产的,供试品量相当于制剂稳定性试验所要求的批量,原料合成工艺路线、方法、步骤应与大生产一致。药物制剂供试品应是放大试验的产品,其处方与工艺应与大生产一致。药物制剂如片剂、胶囊剂,每批放大试验的规模,片剂至少应为10 000片,胶囊剂至少应为10 000粒。大体积包装的制剂如静脉输液等,每批放大规模的数量至少应为各项试验所需总量的10倍。特殊品种、特殊剂型所需数量,根据情况另定。(3)供试品的质量标准应与临床前研究及临床试验和规模生产所使用的供试品质量标准一致。(4)加速试验与长期试验所用供试品的包装应与上市产品一致。(5)研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质(含降解产物及其他变化所生成的产物)的检查方法,并对方法进行验证,以保证药物稳定性试验结果的可靠性。在稳定性试验中,应重视降解产物的检查。(6)由于放大试验比规模生产的数量要小,故申报者应承诺在获得批准后,从放大试验转入规模生产时,对最初通过生产验证的三批规模生产的产品仍需进行加速试验与长期稳定性试验。 本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。 一、原料药 原料药要进行以下试验。 (一)影响因素试验 此项试验是在比加速试验更激烈的条件下进行。其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件和建立降解产物分析方法提供科学依据。供试品可以用一批原料药进行,将供试品置适宜的开口容器中(如称量瓶或培养皿),摊成≤5mm厚的薄层,疏松原料药摊成≤10mm厚薄层,进行以下试验。当试验结果发现降解产物有明显的变
持续稳定性考察方案 1.对各品种生产的前三批进行稳定性考察每批拟计划一定量进行 考察其余批次只做一般留样考察留样量为三次复检的全项检验量 2.考察项目:依据《中国药典》 XX版二部中《原料药与药物制剂稳定性试验指导原则》进行确定 3.考察方法: 3.1加速试验: 3.1.1按市售包装在温度40℃± 2℃、相对湿度 75%±5%的条件下放置六个月在试验期间第 1 个月、 2 个月、 3 个月、 6 个月末分别取样一次按稳定性考察要点项目进行检验 3.1.2 在上述条件下如 6 个月内供试品经检测不符合制定的质量标准则应在如下条件温度 30℃± 2℃、相对湿度 65%±5%情况下进行加速试验时间仍为六个月 3.2长期试验: 按市售包装在温度 18~26℃、相对湿度 60%±15%的条件下放置12 个月. 每 3 个月取样一次分别于 0 个月 3 个月 6 个月 9 个月 12个 月末取样按各剂型品种具体的稳定性考察要点项目进行检验12 个月后仍继续考察分别于18 个月 24 个月 36 个月(以此类推)末取样检测将结果与 0 月比较以确定药品有效期 3.3高温试验:
供试品置密封洁净容器中在60℃条件下放置 10 天于第 5 天和第10 天取样检测有关指标如供试品发生显著变化则在40℃下同法进行试验如 60℃无显著变化则不必进行40℃试验 3.4高湿试验: 试品置恒温密闭容器中于25℃相对湿度为 90%±5%条件下放置 10天在第 5 天和第 10 天取样检测检测项目应包括吸湿增重项若吸湿增 重 5%以上则应在 25℃RH75%±5%下同法进行试验;若吸湿增重 5%以 下且其他考察项目符合要求则不再进行此项试验液体可不进行高湿 试验 3.5光照试验:供试品置光照箱或其它适宜的光照容器内于照度 不< 5000Lx 的条件下放置 10 天在第 5 天和第 10 天取样检测 3.6以上为影响因素稳定性研究的一般要求根据药品的性质必要 时可以设计其他试验如酸、碱及氧化降解等 3.7检测时间的规定: 3.7.1取出时间:1个月加速绝不允许提前和推迟;两个月允许±1 天;三个月允许± 1 周;六个月允许± 2 周;一年后允许±四周 3.7.2样品取出先放在常温下一般要求一周内完成检测;温湿度 敏感的产品要及时检测 3.8恒湿条件的获得方式 恒湿条件可以通过在密闭容器如干燥器下部放置饱和盐溶液而获 得根据不同湿度要求可以选择NaCl 饱和溶液 [ 相对湿度为( 75±1)%15.5℃~60℃] 、KNO3饱和溶液 [ 相对湿度为 92.5%25℃] 、NaNO3
药物稳定性试验统计分析方法 在确定有效期的统计分析过程中,一般选择可以定量的指标进行处理,通常根据药物含 量变化计算,按照长期试验测定数值,以标示量%对时间进行直线回归,获得回归方程,求 出各时间点标示量的计算值(y'),然后计算标示量(y')95%单侧可信限的置信区间为y'±z,其中: zt N 2 1(X X) S 2() 2 NXiX (12-21) 式中,t N-2—概率0.05,自由度N-2的t单侧分布值(见表12-4),N为数组;X0—给定自变量;X—自变量X的平均值; Q S(12-22) N2 式中, 22 Q;L yy—y的离差平方和,LyyN L yy bLyy()/ xy ;L xy—xy的离差乘 积之和L xy xy(x)(y)/N;b—直线斜率。 将有关点连接可得出分布于回归线两侧的曲线。取质量标准中规定的含量低限(根据各品种实际规定限度确定)与置信区间下界线相交点对应的时间,即为药物的有效期。根据情况也可拟合为二次或三次方程或对数函数方程。 此种方式确定的药物有效期,在药物标签及说明书中均指明什么温度下保存,不得使用“室温”之类的名词。 例:某药物在温度25±2℃,相对温度60±10%的条件下进行长期实验,得各时间的标示量如表12-4。 表12-4供试品各时间的标示量 时间/月03691218 标示量/%99.397.697.398.496.094.0 以时间为自变量(x),标示量%(y)为因变量进行回归,得回归方程y=99.18-0.26x,r=0.8970,查T单侧分布表,当自由度为4,P=0.05得 tN-2=2.132 S Q N2 3.444 4 0.9279
稳定性试验方案 1 2020年4月19日
Stability Study Protocol for Exhibit Batch of Chloroquine Phosphate Tablets USP, 250mg 规格为250 mg的USP磷酸氯喹片长期、中期及加速稳定性研究方案 Prepared By: Date: 起草者:日期:Reviewed By QA: Date: 审核者:日期: Approved By: Date: 批准者:日期: Starting Date: Completed Date:
文档仅供参考,不当之处,请联系改正。 开始日期:结束日期: 3 2020年4月19日
Contents 目录 1. Purpose目的…………………………………………………………………………………………错误!未定义书签。 2. Scope范围…………………………………………………………………………………………..错误!未定义书签。 3. R e f e r e n c e s参考资料…………………………………………………………………………………..错误!未定义书签。 4. G e n e r a l I n f o r m a t i o n基本信息………………………………………………………………………..错误!未定义书签。 4.1 S t a b i l i t y S a m p l e s稳定性研究样品…………………………………………………………错误!未定义书签。 4.2 P r o d u c t O u t l i n e样品概述………………………………………………………………..……错误!未定义书签。 4.3 F o r m u l a t i o n处方………………………………………………………………………………错误!未定义书签。 4.4 C o n t a i n e r-C l o s u r e S y s t e m s包装……………………………………………………………错误!未定义书签。 4.5 Labeling标签…………………………………………………………………………………..错误!未定义书签。 4.6 S a m p l e s a n d P a c k a g e样品与包装………………………………………………………….错误!未定义书签。
范围:药物制剂。 责任:检验员、QA监控员、化验室主任、质保科科长、质量部负责人。 内容: 稳定性试验的目的是考察原料药或药物制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。 稳定性试验的基本要求是:(1)稳定性试验包括影响因素试验、加速试验与长期试验。影响因素试验用1批原料药进行。加速试验与长期试验要求用3批供试品进行。(2)原料药供试品应是一定规模生产的。供试品量相当于制剂稳定性实验所要求的批量,原料药物合成工艺路线、方法、步骤应与大生产一致。药物制剂的供试品应是放大试验的产品其处方与生产工艺应与大生产一致。药物制剂如片剂、胶囊剂,每批放大试验的规模,片剂至少应为10 000片,胶囊剂至少应为10 000粒。大体积包装的制剂如静脉输液等,每批放大规模的数量至少应为各项试验所需总量的10倍。特殊剂型、特殊品种所需数量,根据具体情况另定。(3)供试品的质量标准应与临床前研究及临床试验和规模生产所使用的供试品质量标准一致。(4)加速试验与长期试验所用供试品的包装应与上市产品一致。(5)研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质(含降解产物及其他变化所生成的产物)的检查方法,并对方法进行验证,以保证药物稳定性试验结果的可靠性。在稳定性试验中,应重视降解产物的检查。(6)由于放大试验比规模生产的数量要小,故申报者应承诺在获得批准后,从放大试验转入规模生产时,对最初通过生产验证的3批规模生产的产品仍需进行加速试验与长期稳定性试验。 本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。 1.原料药 原料药要进行以下试验。 1.1影响因素试验 此项试验是在比加速试验更激烈的条件下进行。其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件与建立降解产物的分析方法提供科学依据。供试品可以用一批原料药进行,将供试品置适宜的开口容器中(如称量瓶或培养皿),摊成≤5mm厚的薄层,疏松原料药摊成≤10mm厚薄层,进行以下
附录ⅩⅠⅩC 原料药与药物制剂稳定性试验指导原则 稳定性试验的目的是考察原料药或药物制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。 稳定性试验的基本要求是:(1)稳定性试验包括影响因素试验、加速试验与长期试验。影响因素试验用一批原料药或一批制剂进行。加速试验与长期试验要求用三批供试品进行。(2)原料药供试品应是一定规模生产的,供试品量相当于制剂稳定性试验所要求的批量,原料合成工艺路线、方法、步骤应与大生产一致。药物制剂供试品应是放大试验的产品,其处方与工艺应与大生产一致。药物制剂如片剂、胶囊剂,每批放大试验的规模,片剂至少应为10 000 片,胶囊剂至少应为10 000 粒。大体积包装的制剂如静脉输液等,每批放大规模的数量至少应为各项试验所需总量的10倍。特殊品种、特殊剂型所需数量,根据情况另定。(3)供试品的质量标准应与临床前研究及临床试验和规模生产所使用的供试品质量标准一致。(4)加速试验与长期试验所用供试品的包装应与上市产品一致。(5)研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质(含降解产物及其他变化所生成的产物)的检查方法,并对方法进行验证,以保证药物稳定性试验结果的可靠性。在稳定性试验中,应重视降解产物的检查。(6)由于放大试验比规模生产的数量要小,故申报者应承诺在获得批准后,从放大试验转入规模生产时,对最初通过生产验证的三批规模生产的产品仍需进行加速试验与长期稳定性试验。 本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。 一、原料药 原料药要进行以下试验。 (一)影响因素试验 此项试验是在比加速试验更激烈的条件下进行。其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件和建立降解产物分析方法提供科学依据。供试品可以用一批原料药进行,将供试品置适宜的开口容器中(如称量瓶或培养皿),摊成≤5mm厚的薄层,疏松原料药摊成≤10mm厚薄层,进行以下试验。当试验结果发现降解产物有明显的变化,应考虑其潜在的危害性,必要时应对降解产物进行定性或定量分析。 (1)高温试验供试品开口置适宜的洁净容器中,60℃温度下放置10 天,于第5 天和第10天取样,按稳定性重点考察项目进行检测。若供试品含量低于规定限度则在40℃条件下同法进行试验。若60℃无明显变化,不再进行40℃试验。 (2)高湿度试验供试品开口置恒湿密闭容器中,在25℃分别于相对湿度90%±5% 条件下放置10天,于第5天和第10天取样,按稳定性重点考察项目要求检测,同时准确称量试验前后供试品的重量,以考察供试品的吸湿潮解性能。若吸湿增重5% 以上,则在相对湿度75%±5%条件下,同法进行试验;若吸湿增重5%以下,其他考察项目符合要求,则不再进行此项试验。恒湿条件可在密闭容器如干燥器下部放置饱和盐溶液,根据不同相对湿度的要求,可以选择NaCl饱和溶液(相对湿度75%±1%,15.5~60℃),KNO3饱和溶液(相对湿度92.5%,25℃)。 (3)强光照射试验供试品开口放在装有日光灯的光照箱或其他适宜的光照装置内,于照度为4500 lx±500 lx的条件下放置10天,于第5天和第10天取样,按稳定性重点考察项目进行检测,特别要注意供试品的外观变化。 关于光照装置,建议采用定型设备“可调光照箱”,也可用光橱,在箱中安装日光灯数支使达到规定照度。箱中供试品台高度可以调节,箱上方安装抽风机以排除可能产生的热量,箱上配有照度计,可随时监测箱内照度,光照箱应不受自然光的干扰,并保持照度恒定,同
Stability Study Protocol for Exhibit Batch of Chloroquine Phosphate Tablets USP, 250mg 规格为250 mg的USP磷酸氯喹片 长期、中期及加速稳定性研究方案 Prepared By: Date: 起草者:日期: Reviewed By QA: Date: 审核者:日期: Approved By: Date: 批准者:日期: Starting Date: Completed Date: 开始日期:结束日期:
Contents 目录 1. Purpose目的 (1) 2. Scope范围 (1) 3. References参考资料 (1) 4. General Information基本信息 (1) 4.1 Stability Samples稳定性研究样品 (1) 4.2 Product Outline样品概述 (2) 4.3 Formulation处方 (2) 4.4 Container-Closure Systems包装 (3) 4.5 Labeling标签 (3) 4.6 Samples and Package样品与包装 (4) 5. Stability Testing稳定性测试 (4) 5.1 Sample Receipt and Storage样品接收与储存 (4) 5.2 Storage Conditions and Testing Time Points储存条件与检测时间点 (4) 5.3 Sampling取样 (5) 5.4 Testing Matrix稳定性测试项目表 (6) 5.5 Parameters and Acceptance Criteria检测项目及质量标准 (6) 5.6 Degradation products降解产物 (7) 6. Data Presentation数据汇总 (7) 7. Reporting报告 (7) 7.1 Intermediate Reports中期报告 (7) 7.2 Summary Report总结报告 (7) 7.3 Stability Documents稳定性文件夹 (7) 8. Appendix附件 (8)
About Author: dr . daniel liu ha been working both in academia insti-tutes and pharmaceutical companies including Novartis, Pfizer , Sanofi-synthelabo, schering-Plough and Johnson&Johnson in the field of clinical studies. dr . liu has extensive experi-ences in the designing, management and execution of global clinical trials, pharmacovigillance and assistant as-sembly of regulatory files for the FDA nda/Ind submissions. on the other hand, he is a member of standing committee of the “chinese association of clinical research” and an editorial Board member of “chinese Journal of new drugs”. dr . liu received his B.sc. in pharmacy and m. sc in pharmaceu-tical chemistry from china Pharmaceu-tical university, nanjing, P .r.china. he then received his Phd in pharmacology from university of Illinois in 99 . 稳定性实验方案设计研究的国际化规范 daniel liu Abstract: This paper reviews international trends in the stability testing of phar-maceutical products, with emphasis on stability during pharmaceutical product development. In particular, it considers the progress toward globalization and harmonization and indicates stability problems, which probably will be the focus of attention for pharmaceutical scientists, pharmaceutical companies and regulators, who are interested in register-ing their products for the global markets in the near future. Attention is specifically directed to monitoring stability in the pharmaceutical product development. 在过去的30年间,药物产品的稳定性实验已从只是检测药物产品中有害物质的变异发展到运用全面的科学原理对药物产品进行综合质控的操作,如今世界各地不同程度地都已开始制定药物产品的稳定性规范。药物产品的稳定性涉及到许多可能导致药物成分降解的因素。药物原料药以及后来制剂中的任何变化都会对药物产品的质量造成影响,并可能导致病人对药物的副作用增加。药物产品有效期的建立就是为了监控药物成分降解对药物效价的影响,它通常是通过一系列正式的涉及到化学,物理学和生物学的稳定性实验而建立的。这些实验过程包括设定实验方案,测试三批以上的样品,在模拟气候条件下和一定时间间隔段观察和对药物原料和制剂样品稳定性进行追踪分析等。由此可见,与药物安全性和有效性质控有关总置信度一样,药物制剂和原料药的稳定性就是建立在这一系列从药物化合物的早期发掘,到最后产品从市场上淘汰的所有阶段的基础上。所以药物稳定性数据通过不断积累,评价和审核而获得的。在任何阶段所需数据量依药物最后的制剂的种类,性质和用途的不同而变化,最终的目的就是建立适当的药物有效期以使药物对病人的安全有效性能得到最大的保证。由于完成稳定性研究要花费的时间较长,所以从开始建立稳定性研究方案时就不仅对产品作尽可能的详尽分析,而且还应考虑ICH指南,欧洲药物审评机构要求和美国FDA稳定性实验要求等。按照这些指南或要求所获得的稳定性数据将有利于药品的全球化注册,并且所制定的药物制剂或原料药有效期和稳定性的公信力也较强。本文将探讨药物工业各研究阶段所进行的稳定性研究方案。与稳定性研究方案有关的ICH指南1,欧洲药物评审机构和FDA对稳定性研究试验设计的要求也将被进行讨论。 1.稳定性研究阶段 药物产品的稳定性可定义为一种药品在特定的容器或密闭系统中可保持药物原有的物理、化学、微生物、治疗、毒理及其相关特质的能力。虽然也有例外,但大多数药物标签上效价的90%一般被公认为可接受的最低效价水平2。药物产品从最初的合成到之后的产品储存的研发过程通常可分为五个阶段。在每个阶段都应监察和记录药物的纯度,杂质含量,以及降解产物的情况。最理想的情况是药物原料的纯度/杂质含量在各个安全性实验,临床 试验评估,制剂研究和稳定性实验中都保持恒定。基本上所有过
Contents 目录Stability Lab
Stability Lab Page 1/ 9
1.Purpose 目的 The purpose of stability testing is to provide evidence of how the Quality, Strength, Degradation Products and Purity of the Chloroquine Phosphate Tablets USP, 250mg will change with time under the influence of environmental room temperature and relative humidity conditions. Data collected from the stability study will enable recommended storage conditions and provide justification for establishing and submitting the data to regulatory authorities for approving the shelf life for marketing purposes. In addition, 3 months of the stability data will be submitted to US FDA as required for submission purposes of the ANDA application. 此稳定性研究的目的是为了考察磷酸氯喹片在环境因素的影响下(例如:温度和湿度)其性质、规格、降解产物和含量等随时间而变化的规律, 依据稳定性研究的数据确定该产品的储藏条件和有效期。 2.Scope 范围 Stability Lab Page 2/ 9
编码: 士的宁对照品变更生产厂家 验证方案 方案起草:_________________日期:年月日方案审核:__________________日期:年月日方案批准:__________________日期:年月日 陕西香菊药业集团有限公司
1.目的:确定上海诗丹德生物技术有限公司生产的士的宁对照品是否可以用于替代中检院生产士的宁对照品,用于我公司郁金银屑片以及马钱子药材、马钱子粉含量测定使用。 2.背景:由于中检院生产的士的宁对照品于2015年下半年开始断货,至今不能采购到中检院生产对照品士的宁,而我公司用于郁金银屑片、马钱子药材、马钱子粉含量测定按照《中国药典》2015年版一部必须使用到士的宁标准品,因此通过本次验证来确定上海诗丹德生物技术有限公司所生产的标准品是否可以替代中检院生产的士的宁标准品,用于我公司郁金银屑片、马钱子粉、马钱子药材的含量测定。 3. 稳定性研究: 3.1.标签:用于对照品溶液变更厂家研究的的溶液瓶上需注明“用于对照品厂家变更验证,且必须注明生产厂家、对照品批号、称量重量、配置人、配置日期等相关信息”。 3.2.对照品溶液配制:根据《中国药典》2015年版一部郁金银屑片、马钱子粉、马钱子药材的含量测定项下对照品溶液制备方法:取士的宁对照品适量,精密称量,加三氯甲烷制成每1ml含士的宁0.3mg的溶液,再精密吸取2ml,置10ml 量瓶中,加甲醇稀释至刻度,摇匀,即得(每1ml中含士的宁0.06mg)。 3.3.分析方法和接受标准: 3.3.1分析方法:色谱条件与系统适应性试验色谱条件与系统适应性以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.01mol/L庚烷磺酸钠与0.02mol/L磷酸二氢钾等量混合溶液(用10%磷酸调节pH值至2.8)(21:79)为流动相;检测波长254nm。理论塔板数按士的宁峰计算应不低于5000。 对照品溶液的制备取士的宁对照品适量,精密称量,加三氯甲烷制成每1ml 含士的宁0.3mg的溶液,再精密吸取2ml,置10ml量瓶中,加甲醇稀释至刻度,摇匀,即得。(每1ml中含士的宁0.06mg) 分别制备两份士的宁对照品溶液(贴上“对照品配置标签”),混匀,定容后对两份对照品溶液分析三次,三次检测峰面积数的RSD值不得过1.5%,以中检院的士的宁对照品为对照测定上海诗丹德对照品的有效含量。通过测定含量与标示含量的差值分析是否可以替换中检院士的宁标准品。
药物稳定性试验指导原则 附录幻X C 药物稳定性试验指导原则 稳定性试验的目的是考察原料药或药物制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输条件提供科学依据,同时通过试验建立药品的有效期。 稳定性试验的基本要求有以下几个方面。 (1)稳定性试验包括影响因素试验、加速试验与长期试验。影响因素试验适用于原料药的考察,用 1 批原料药进行。加速试验与长期试验适用于原料药与药物制剂,要求用 3 批供试品进行。 (2)原料药供试品应是一定规模生产的,供试品量相当于制剂稳定性实验所要求的批量,原料药合成工艺路线、方法、步骤应与大生产一致。药物制剂的供试品应是放大试验的产品 (如片剂或胶囊剂在 10000 片左右或 10000粒左右,特殊剂型、特殊品种所需数量、根据具体情况灵活掌握 )、其处方与生产工艺应与大生产一致。 (3)供试品的质量标准应与各项基础研究及临床验证所使用的供试品质量标准一致。 (4)加速试验与长期试验所用供试品的容器和包装材料及包装方式应与上市产品一致。 (5)研究药物稳定性,要采用专属性强、准确、精密、灵敏的药物分析方法与有关物质 (含降解产物及其他变化所生成的产物 )的检查方法,并对方法进行验证,以保证药物稳定性结果的 可靠性。在稳定性试验中,应重视 有关物质的检查。本指导原则分两部分,第一部分为原料药,第二部分为药物制剂。 一、原料药
原料药要进行以下试验。 (一)影响因素试验此项试验是在比加速试验更激烈的条件下进行。其目的是探讨药物的固有稳定性、了解影响其稳定性的因素及可能的降解途径与降解产物,为制剂生产工艺、包装、贮存条件与建立降解产物的分析方法提供科学依据。供试品可以用一批原料药进行,将供试品置适宜的容器中(如称量瓶或培养皿),摊成≤5mm厚的薄层,疏松原料药摊成≤10mm 厚薄层,进行以下实验。 1.高温试验 供试品开口置适宜的密封洁净容器中,60C温度下放置10天,于第5天和第10天取样,按稳定性重点考察项目进行检测。若供试品有明显变化(如含量下降5%),则在40C条件下同法进行试验。若60C无明显变化,不再进行40C试验。 2.高湿度试验 供试品开口置恒湿密闭容器中,在25C分别于相对湿度90%± 5% 条件下放置10天,于第5天和第10天取样,按稳定性重点考察项目要求检测,同时准确称量试验前后供试品的重量,以考察供试品的吸湿潮解性能。若吸湿增重5%以上,则在相对湿度75%± 5%条件下,同法进行试 验;若吸湿增重5%以下,且其他考察项目符合要求,则不再 进行此项试验。恒湿条件可通过在密闭容器如干燥器下部放置饱和盐溶液实现,根据不同相对湿度的要求,选择NaCl饱和溶液(15.L60C, 相对湿度75%± 1%)或KN03饱和溶液(25C, 相对湿度92.5%)。 3.强光照射试验 供试品开口放在装有日光灯的光照箱或其他适宜的光照装置内,于