
综合研究性实验四:
谷丙转氨酶活性的鉴定及活力单位的测定
一.实验目的
1.用纸层折法观察肝脏丙转氨酶ALT的转氨作用;
2.用分光光度法测定血清丙转氨酶的活力;
3.学习治疗检测SGPT的方法及原理;
4.了解检测肝损伤模型的制备及SGPT在科研中的应用。
二.实验材料与试剂
[一]实验材料
动物肝脏
[二]实验试剂
1.9%NaCl溶液
2.海砂
3.1%谷氨酸溶液(1%KOH溶液中和)
4.%丙酮酸钠溶液(用1%KOH溶液中和)
5.0.1%KHCO3溶液
6.0.025%一溴乙酸溶液(用1%KOH中和)
7.2%乙酸溶液
8.酚的饱和水溶液
将2份酚和2份水(按重量计算)混合后,放入分液漏斗中,振荡。静止24h以后分层,将下部酚层放入瓶中备用。新配制的酚展层剂可以反复使用1周。
9.0.1%水合茚三酮的正丁醇溶液
10.0.1%标准谷氨酸溶液
11.0.1%标准丙氨酸溶液
12.1%KOH溶液
二.谷丙转氨酶活性的鉴定(纸层析法)
[一]实验原理
观察肌肉糜中谷丙转氨酶所催化的氨基移换反应。通过纸层析法检查底物谷氨酸的减少和产物丙氨酸的生成。为防止丙酮酸被肌肉糜中的其它酶所氧化或还原,在反应系统中加入了抑制剂溴乙酸。
[二]实验操作
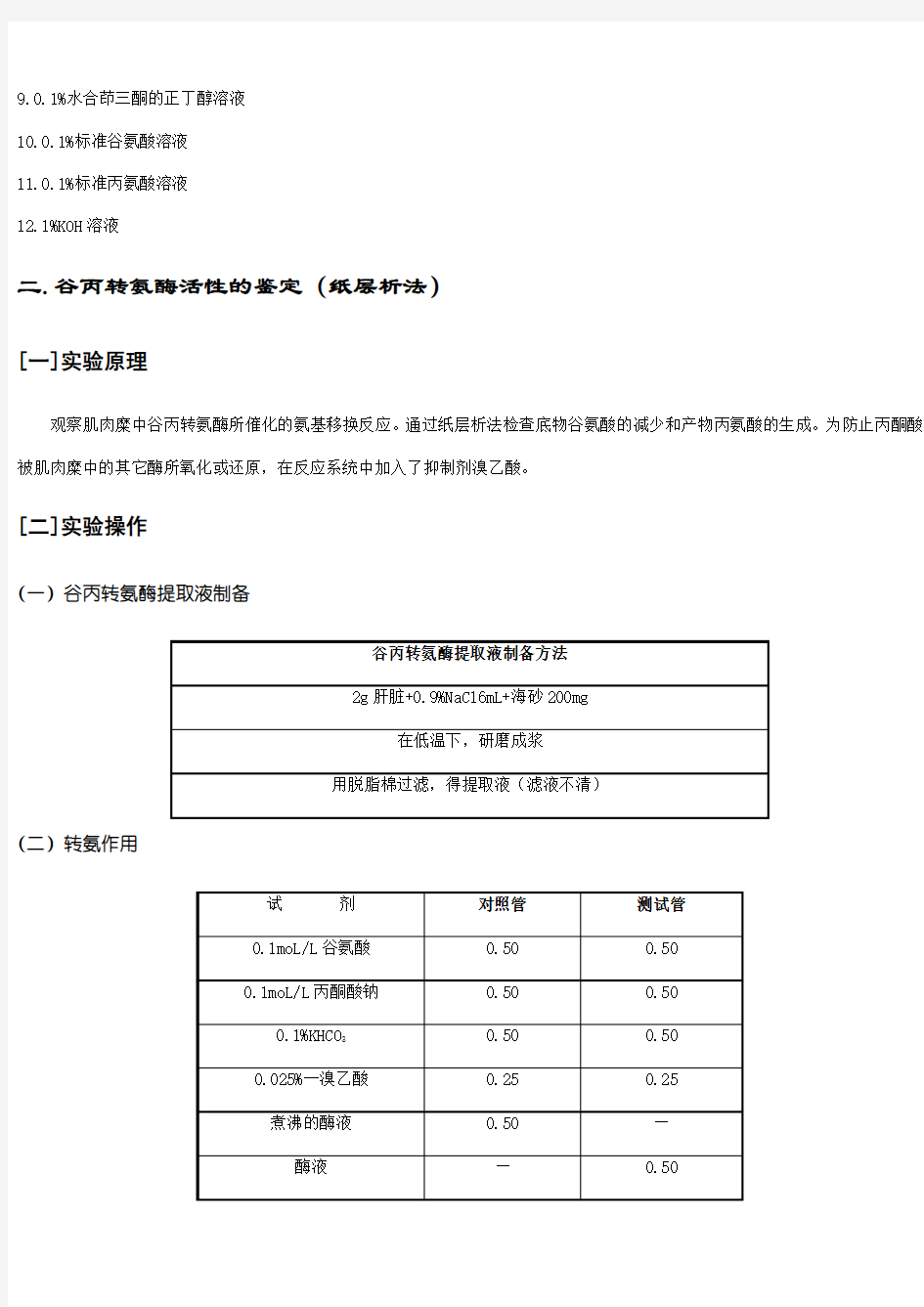
(一)谷丙转氨酶提取液制备
谷丙转氨酶提取液制备方法
2g肝脏+0.9%NaCl6mL+海砂200mg
在低温下,研磨成浆
用脱脂棉过滤,得提取液(滤液不清)
(二)转氨作用
试剂对照管测试管
0.1moL/L谷氨酸0.500.50
0.1moL/L丙酮酸钠0.500.50
0.1%KHCO30.500.50
0.025%一溴乙酸0.250.25
煮沸的酶液0.50—
酶液—0.50
加脱脂棉塞,45℃水浴,1.5h,时时振荡内容物
2%乙酸6滴6滴
沸水浴2min,使蛋白质完全沉下,过滤,作层析
(三)纸层析
1.方法
纸层析方法
取圆形层析滤纸1张,在圆心处用圆规绘出直径为3cm的同心圆
通过中心将滤纸绘成四等分扇形,用毛细管点样2-4次(直径不超过2mm)
在滤纸的圆心上剪一小孔,直径约1-2mm
取一小滤纸条,将下端剪成刷状,在卷成灯芯插入圆形小孔,不能使灯芯突出纸面
将圆形滤纸平放在盛有层析液(水饱和酚)培养皿上,使灯芯向下与溶剂接触
用大小相同的培养皿盖在滤纸上
溶剂通过灯芯上升到滤纸上向四周展层,直到溶剂前沿移至距滤纸边缘约1cm处时停止(展层时间为1h)
80-100℃烘箱干燥,喷洒水合茚三酮的正丁醇溶液,80-100℃显色
2.实验结果
三.血清谷丙转氨酶活力单位测定
[一]实验原理
本实验用丙氨酸和α-酮戊二酸为底物,经转氨作用生成谷氨酸和丙酮酸。丙酮酸与2,4-二硝基苯肼作用生成2,4-二硝基
苯腙,此物质碱性条件下呈棕红色,其颜色的深浅与丙酮酸的含量成正比,可用比色法进行定量测定。通过与标准溶液的比较,即可计算出酶的活力单位数。
[二]实验操作
(一)标准曲线的绘制
1.试剂
(1)1/15 mol/LpH=7.4的磷酸缓冲液
取1/15 mol/L磷酸氢二钠(称取Na2HPO4 9.47g或Na2HPO4·12H2O23.87g,溶于蒸馏水中定容至1000mL)825mL;1/15 mol/L 磷酸二氢钾(称取KH2PO4 9.078g溶于蒸馏水中定容1000mL)175mL混合。
(2)GPT基质液
称α-酮戊二酸,29.2mg(2 mmol/L)及α-L-丙氨酸1.78g(200mmol/L)溶于50mL,pH=7.4的磷酸缓冲液中,加0.1mol/L NaOH 溶液0.5mL,调pH为7.4,然后加磷酸缓冲液定溶至100mL,加少许氯仿防腐,置冰箱中可保存一周。
(3)1mmol/L2,4-二硝基苯肼
称取2,4-二硝基苯肼20mg,溶解于10mL浓盐酸中,以蒸馏水定容至100mL。
(4)2μmol/mL丙酮酸钠标准液
精确称取丙酮酸钠22mg,加磷酸缓冲液溶解后,定容至100mL。临用前配制。
(5)0.4mol/LNaOH溶液
2.方法
对照管测定管
试剂
012345
丙酮酸钠标准液(mL)—0.050.100.150.200.25
GPT基质液(mL)0.500.450.400.350.300.25
pH7.4磷酸缓冲液(mL)0.100.100.100.100.100.10
充分摇匀后,置于37℃水浴,保温10min
2,4-二硝基苯肼(mL)0.500.500.500.500.500.50
充分摇匀后,置于37℃水浴,保温20min
0.4mol/LNaOH(mL) 5.00 5.00 5.00 5.00 5.00 5.00
充分摇匀后,室温静置30min后,520nm波长下比色
A520nm值
相当丙酮酸含量(mol)—0.100.200.300.400.50
相当GPT单位(100mL)—100200300400500
以酶的活力单位数为横坐标,以光吸收值为纵坐标,绘制A520nm与对应的酶活力单位数的标准曲线。
(1)丙酮酸钠标准液mL数×摩尔浓度(2μmol/mL);
(2)GPT活力单位为:每mL血清在37℃与pH=7.4的基质液作用60min,生成1
μmol丙酮酸为一个单位(U)。本实验(临床检验)取血清量为0.1mL,报告数
据以100mL血清计算,因此将实际测得结果×1000即可。
(二)酶活力的测定
对照管测定管
试剂
01
GPT基质液(mL)0.500.50
37℃水浴,预温10min
血清(mL)—0.10
PH=7.4磷酸缓冲液(mL)0.100.00
充分摇匀后,置于37℃水浴,保温60min
2,4-二硝基苯肼(mL)0.500.50
充分摇匀后,置于37℃水浴,保温20min
0.4mol/LNaOH(mL) 5.00 5.00
摇匀后,静置30分钟,520nm波长下比色
A520nm值
查标准曲线的对应值,可得100mL血清中谷丙转氨酶的活力单位数
(三)实验结果
试管比色杯吸光值吸光值纯吸光值
对照管
测定管
查标准曲线得GTP单位
参考数值GTP单位
(四)注意事项
1.所需试剂如基质液、丙酮酸标准液、2,4-二硝基苯肼等均需冷藏;
2.为防止溶血及其他因素对酶活性影响,实验所用器皿应干净、干燥方可使用;
3.丙酮酸钠极易变质,配试剂时应选择外观洁白干燥者,否则应进行重结晶;
4.转氨酶只能用于α-L-Ala,对D-Ala无催化作用。实验室多用α-L-Ala,是因为便宜,如果采用α-L-Aa,则用量需减半;
5.如活性高于500U/100mL,应将血清稀释一定倍数重新测定,结果应×稀释倍数;
6.为保证操作结果可靠,测定酶活性时应恒定pH、保温时间;
7.选用固定分光光度计及比色杯减少误差。
四.GPT/ALT在临床诊断意义及检测方法原理
[一]GPT/ALT在临床诊断中的意义
转氨酶广泛存在于机体的各个组织中,在肝组织中谷丙转氨酶活性较高,在心脏中谷草转氨酶活性较高。在正常新陈代谢中,血清内维持一定水平的转氨酶活性(即正常值)。当组织发生病变时,由于组织细胞肿胀、坏死(或细胞膜破裂),使细胞膜通
透性增高,而导致大量的酶释放至血液中,从而引起血清中相应的谷丙转氨酶和谷草转氨酶活性显著增高。因此测定其活性,对肝、心脏的某些疾病的临床诊断具有重要的参考价值。
[二]丙氨酸氨基转移酶试剂盒使用说明
(一)用途
本试剂用以测定人血清中丙氨酸氨基转移酶活力。
(二)基本原理
底物L-丙氨酸与α-酮戊二酸在ALT作用下生成丙酮酸,生成的丙酮酸在乳酸脱氢酶作用下转化成L-乳酸,同时伴随着NADH 氧化,引起在波长340nm处吸光度下降,下降速率与血清ALT活力成正比。
L-丙氨酸+α-酮戊二酸→丙酮酸+L-谷氨酸
丙氨酸+NADH+H+→L-乳酸+NAD+ +H2O
(三)试剂盒组成
试剂成分含量
溶液A Tris缓冲液(pH=8.5)0.1mol
NADH0.30mmol
LDH≥5.0KU/L
溶液B Tris缓冲液(pH=7.0)0.1mol L-丙氨酸1020mmol
α-酮戊二酸36mmol
(四)仪器
1.具有能在波长340nm处测定生化分析仪
2.30℃、37℃水浴箱
3.定时器
4.准确的加样器
(五)方法
1.二步法
试管样本管空白管
样本0.3mL—
蒸馏水—0.3mL
溶液A 2.0mL 2.0mL
混匀、放设定温度5min
溶液B 1.0mL 1.0mL
混匀,准确记录时间,放设定温度1min后,在波长340nm处,以蒸馏水
校零,连续监测1-2min,计算ΔA/min。
2.一步法
试管样本管空白管
样本0.3mL—
蒸馏水—0.3mL
工作液 3.0mL 3.0mL
混匀,准确记录时间,放设定温度1min后,在波长340nm处,以蒸馏水
校零,连续监测1-2min,计算ΔA/min。
工作液制备:溶液A与溶液B以2:1混合,组成测定工作液。工作液在2-8℃
避光保存,可稳定3周。
(六)实验结果
序号1234
吸光值
ΔA/min
计算公式
计算结果
参考数值
(七)注意事项
1.本液体试剂按IFCC推荐法为基础设计,采用二步法,可防止胆红素的干扰;
2.试剂与样本量可按生化分析仪要求衡比例改变;
3.本试剂线性可达到600 U/L(30℃),或1000 U/L(37℃),当样本中ALT活力超过600 U/L(30℃)或1000 U/L(37℃)时,可用生理盐水稀释,即0.1mL血清加0.2mL生理盐水,测定,结果×3;
4.如试剂变混,或以蒸馏水为空白,工作液在340nm处吸光度<1.0,请勿使用;
5.贮存条件与有效期(试剂在2-8℃,避光保存,有效期为1年;如用一步法,工作液在2-8℃避光保存,可稳定3周)。
五.检测SGPT活性在科学研究中的应用
[一]基本原理
测定SGPT活性可反映出肝细胞的坏死程度,因此是检测肝功能损坏的灵敏指标之一。很多有毒物质易引起肝损伤,造成肝实质细胞的变性及坏死,例如,四氯化碳(CCl4)等化学药物可以诱发动物发生急性中毒性肝炎和肝坏死。因此建立由CCl4诱发病变的动物模型,然后检测SGPT活性,常被用于滋肝补肾中草药物的筛选研究。
[二]应用实例
红缘层孔菌多糖对CCl4中毒小鼠转氨酶(SGPT)活性的影响。
将体重20-22g小白鼠随机分为三组,每组10只。第1组为正常对照,第2组为四氯化碳中毒对照组,第3组为给药组。
给药组以150mg/kg体重的剂量,给小鼠灌胃红缘层孔菌多糖液,每日一次,连续给药7天,其余两组灌胃同体积生理盐水。于末次给药后24h,给药组、四氯化碳中毒对照组均按10mL/kg体重剂量腹腔注射0.1%CCl4豆油溶液,正常对照组注射同体积豆油,16h后,对三组小白鼠摘眼球取血制血清,按King氏法测定谷丙转氨酶活性(100mL血清与与基质液在37℃条件下作用60min,每生成1μmol丙酮酸为1个活性单位)。结果见下表:
红缘层孔多菌多糖对CCl4中毒小鼠SGPT活性的影响
组别SGPT(u%)M±SD P值
正常对照组205±17
CCl4中毒组336±34
P≥0.05
给药组217±13
由表中数据可见,红缘层孔多菌多糖可抑制由四氯化碳损伤肝细胞引起的小鼠血清谷丙转氨酶活性的升高。
肝脏谷丙转氨酶活力测定 进入实验室要注意的问题 安全第一,在实验室中使用挥发性试剂时应在通风橱中进行,以免发生中毒事件;不得在实验室中随意使用明火,因为实验室中有许多易燃易爆药品,使用明火可能引起火灾或引发爆炸事件;不得在实验室吃东西,实验结束后也应将手洗净再吃东西。在实验室中不得嬉戏打闹,更不得用实验药品互相开玩笑。实验中使用药品应尽量节约,不得浪费药品,未使用完的药品因倒人废液缸或指定的容器中,切不可倒入原试剂瓶以免污染试剂。实验完成之前不能离开实验室,如有特殊原因要离开需经实验室负责人批准才能离开。每个实验台内的各种仪器的摆放顺序要牢记,离开实验室前要将仪器按顺序摆放好。养成一个好的习惯。 一.实验目的 了解转氨酶的性质及临床意义,并掌握谷丙转氨酶活力的测定方法 二.实验原理 在氨基酸的分解代谢过程中,联合脱氨基为大多数氨基酸的主要代谢方式,通过转氨基作用与氧化脱氨基的作用偶联而完成。本实验以丙氨酸和 ā-酮戊二酸作为谷丙转氨酶的作用的底物,利用内源性磷酸吡哆醛作为辅酶,在一定条件及时间作用后来测定所生成的丙酮酸的含量来确定其酶的活力。丙酮酸能与2,4二硝基苯肼结合,生成丙酮酸-2,4二硝基苯腙,后者在碱性条件溶液中呈棕色,基吸收光谱的峰为439-530nm,可用于测定丙酮酸的含量。 ā--酮戊二酸与能与2,4二硝基苯肼结合,生成相应的苯腙,但后者在碱性溶液中的吸收光谱与丙酮酸二硝基苯肼稍有差别,在520nm波长处 ā--酮戊二酸二硝基苯腙的吸光度远比丙酮酸2,4二硝基苯腙为低,因此在520nm处吸光度增加的程度与反应体系中的丙酮酸和 ā--酮戊二酸的摩尔比基本上呈线性关系。故可籍此可测定谷丙转氨酶的活力。 三、实验器材 容量瓶100ml 4个500ml 2个;电子天平;玻璃棒;研钵;试管5支;试管架;移液管0.5ml 2支;1ml 2支;5ml 1支;滴管1支;分光光度计,比色皿4个; 四.实验试剂 1标准丙酮酸溶液:准确称取纯化的丙酮酸钠62.5mg,溶于100ml 0.05mol/L H2SO4中,现用现配。 2、谷丙转氨酶底物:称取0.90g L-丙氨酸,29.2mg α-酮戊二酸,先溶于pH7.4 0.1mol/L 的磷酸缓冲液中。然后用1 mol/L NaOH 调节pH到7.4,再用pH7.4 0.1mol/L的磷酸缓冲液定容到100ml,贮存于冰箱中,可使用1周。 3、0.1mol/L pH7.4磷酸缓冲液:称取13.97g K2HPO4和2.69g KH2PO4溶于蒸馏水中,定容到1000ml。 4、0.02% 2,4-二硝基苯肼溶液:称取20mg 2,4-二硝基苯肼溶于少量的1mol/L HCl中。加热溶解,用1mol/L HCl定容到100ml。(后经试验发现取20mg 2,4 - 二硝基苯肼,溶于7ml11.6mol/L的浓盐酸,再定容至100ml效果更好) 5、0.4mol/L NaOH :称取16g NaOH定容到1000ml。 6、0.9%生理盐水:称取0.9gNaCl,定容到100ml。
谷丙转氨酶高的原因有哪些 对于很多身体不适的患者,因为谷丙转氨霉高,造成身体的不适以后,那么很多的患者,为了能尽快让自己了解原因,就想全面了解一下谷丙转氨酶高的原因有哪些?为了你能全面的了解,就来一同看看下面详细的介绍,希望你能尽快康复。 谷丙转氨酶升高的原因,有许多因素,如:急性肝炎、服用药物(尤其是对肝脏有损害的药物)、长期饮酒或一次饮用较大剂量时,以及某些胆道疾病、心脏病时的心力衰竭,发热等等病症,均可引起谷丙转氨酶升高。 单纯转氨酶偏高(肝功能异常)还不能确定是肝炎,确定患上肝炎必须同时具备以下三点才成立。即有肝炎的症状、体征(如 低烧、厌油、恶心、呕吐、乏力、食欲差、肝脏肿痛等)和临床 诊断(如急性黄疸型、慢性迁延型等);血清转氨酶增高;病原学诊断(有抗甲肝抗体是甲型,乙肝病毒表面抗原、e抗原和核心抗 体阳性是乙型)。有些人单纯转氨酶偏高,不排除在检测前因饮
酒过量、剧烈运动、上夜班、感冒或口服某些药物等因素干扰。 谷丙转氨酶主要存在于肝脏、心脏和骨骼肌中。肝细胞或某些组织损伤或坏死,都会使血液中的谷丙转氨酶升高,临床上有很多疾病可引起转氨酶异常,必须加以鉴别—— 心肌炎1、病毒性肝炎这是引起谷丙转氨酶ALT升高最常见的疾病,各类急、慢性病毒性肝炎均可导致谷丙转氨酶ALT偏高。 2、中毒性肝炎多种药物和化学制剂都能引起谷丙转氨酶ALT 升高,但停药后,谷丙转氨酶ALT升高可恢复正常。 3、大量或长期饮酒者谷丙转氨酶ALT升高。 4、肝硬化与肝癌肝硬化活动时,一般都会出现谷丙转氨酶ALT升高,应该积极治疗。 5、胆道疾病胆囊炎、胆石症急性发作时,常有发热、腹痛、恶心、呕吐、黄疸、血胆红素及谷丙转氨酶ALT升高。 6、心脏疾病急性心肌梗塞、心肌炎、心力衰竭时,可使谷丙转氨酶和谷草转氨酶升高,患者常有胸痛、心悸、气短、浮肿。
授课对象:06级检验1-5班 课时:2学时 血清丙氨酸氨基转移酶(ALT)测定(赖氏法) 目标:1.掌握赖氏法测血清ALT的原理及注意事项 2.掌握试剂的配制熟练地制作标准曲线 3.规范地进行ALT测定 4.了解血清ALT测定的临床意义 实验用品:配制试剂用的各种器皿(烧杯、容量瓶、电炉、分析天平等)、37℃水浴箱、721型风光光度计、坐标纸等 原理: 丙氨酸和α-酮戊二酸在血ALT的作用下生成丙酮酸及谷氨酸,在酶反应达到规定时间时,加入2.4-二硝基苯肼-盐酸溶液以终止反应。生成的丙酮酸与入2.4-二硝基苯肼作用,生成丙酮酸入2.4二硝基苯腙,苯腙在碱性条件下显红棕色。根据显色之深浅,求得血清中丙氨酸氨基转移酶活力。 试剂: 1. 0.1molPH7.4磷酸盐缓冲液称取磷酸氢二钠(Na2HPO4AR)11.928g,磷酸二氢钾(KH2PO4AR) 2.176g,加少量蒸馏水溶解并稀释至1000mL。 2. ALP基质液称取DL丙氨酸[CHCH(NH)COOH]1.79g,α-酮戊二酸[COOH (COCOOH)29.2mg于烧杯中,加入0.1mol/L PH7.4磷酸盐缓冲液80mL,煮沸溶解后待冷,用摩尔NaOH溶液调节PH至7.4(约加入0.5ml),再用0.1mol/LPH7.4磷酸盐缓冲液稀释至100mL,混匀,加氯仿数滴,置冰箱保存数周。 3.1mmol/L2.4-二硝基苯肼溶液称取 2.4-二硝基苯肼[(NO)CHNHNH AR]19.8mg,用10mol/L HC110mL溶解,然后加蒸馏水至100mL,置棕色瓶内,冰箱保存。 4.0.4mol/L NaOH溶液。 5.2mmol/L丙酮酸标准液精确称取丙酮酸钠[CHCOCOONa AR]22.0mg于
谷丙转氨酶高的原因 谷丙转氨酶是转氨酶的一种,是肝功能检查时的一项重要指标。谷丙转氨酶在人体处在健康状态时,水平总是维持在40单位以下。但是当某些情况出现时,谷丙转氨酶的水平会超出这个健康线几倍甚至几十倍。 为什么谷丙转氨酶会升高呢? 事实上,谷丙转氨酶高的原因有很多,谷丙转氨酶高在临床上也是相当常见的。 谷丙转氨酶高最常见的原因是各种类型的肝部炎症。肝炎可以使肝细胞损伤或直接坏死,使主要存在于肝细胞中的谷丙转氨酶被大量释放到血液中,导致血液中的谷丙转氨酶水平升高。其中,病毒性肝炎是引起谷丙转氨酶增高的最常见的肝部疾病;此外,乙肝、丙肝、肝硬化、肝结核、肝癌等也都是会引起转氨酶升高的肝部病症。 谷丙转氨酶高的原因还可能是胆道疾病。比如胆囊炎、胆石症、胆结石等,也会有转氨酶升高的表现。 谷丙转氨酶高的原因之三——心脏疾病。比如心肌梗塞、心肌炎、心力衰竭等,也都是引起谷丙转氨酶升高的原因。 谷丙转氨酶高的原因之四:不合理的饮食和长期酗酒。不合理的饮食会造成脂肪在肝脏部位堆积,引发脂肪肝,同时转氨酶升高;而长期酗酒的话,酒精严重伤肝,会导致酒精肝的形成,同时转氨酶升
高。 谷丙转氨酶升高,还有可能是流感、肺结核、伤寒、肺炎等疾病引起的。 谷丙转氨酶高的患者,需要在饮食和药物上多加注意。 先说饮食方面。谷丙转氨酶高的患者一日三餐的饮食应合理搭配,每日要摄取足量的维生素和蛋白质,且荤素相间,并尽量避免辛辣刺激食物入口;饮食要定时定量,尤其要控制晚餐摄入量,进食量要与体力活动相平衡。 再说药物方面。谷丙转氨酶高的 患者除了在饮食方面要做到养肝护 肝,在治疗时还要注意药物的选择, 最好选择那些具有针对性的治疗药 物。如解肝抑酶方等。 还有一个认识误区要向患者解释清楚:已知病毒性肝炎会引起谷丙转氨酶高,而病毒性肝炎又极具传染性;那么是不是转氨酶越高,传染性就越强呢? 实际上,真正具有传染性的时期是病毒性肝炎早期,而此时期谷丙转氨酶的水平还在正常范围之内;等到谷丙转氨酶升高时,病毒的传染性已经明显减弱了。所以,认为谷丙转氨酶越高即表示患者传染性强的,完全是一种误解。
实验五血液中谷丙转氨酶活力的测定 【目的和要求】 了解转氨酶在代谢过程中的重要作用及其在临床诊断中的意义,学习转氨酶活力测定的原理和方法。 【原理】 生物体内广泛存在的氨基移换酶也称转氨酶,能催化α-氨基酸的α-氨基与α-酮基酸的α-酮基互换,在氨基酸的合成和分解、尿素和嘌呤的合成等中间代谢过程中有重要作用。转氨酶的最适pH接近7.4,它的种类甚多,其中以谷氨酸-草酰乙酸转氨酶(简称谷草转氨酶)和谷氨酸-丙酮酸转氨酶(简称谷丙转氨酶)的活力最强。它们催化的反应如下。 正常人血清中只含有少量转氨酶。当发生肝炎,心肌梗死等病患时,血清中转氨酶活力常显著增加,所以在临床诊断上转氨酶活力的测定有重要意义。 测定转氨酶活力的方法很多,本实验采用分光光度法。谷丙转氨酶作用于丙氨酸α-酮戊二酸后,生成的丙酮酸与2,4-二硝基苯肼作用生成丙酮酸2,4-二硝基苯腙。 丙酮酸2,4-二硝基苯腙加碱处理后呈棕色,可用分光光度法测定。从丙酮酸2,4-二硝基苯腙的生成量,可计算酶的活力。 【操作方法】
2,4-硝基苯肼可与有酮基的化合物作用形成苯腙。底物中的α-酮戊二酸与2,4-二硝基苯肼反应,生成α-酮戊二酸苯腙。因此,在制作标准曲线时,须加入一定量的底物,(内含α-酮戊二酸)以抵消由α-酮戊二酸产生的消光影响。 先将试管置于37℃恒温水浴中保温10min以平衡内外温度。向各管内加入0.5ml2,4-二硝基苯肼溶液后再保温20min,最后,分别向各管内加入0.4mol/L氢氧化钠溶液5ml。在室温下静置30min,以0号管作空白,测定520nm的光吸收值。用丙酮酸的微摩尔数为横坐标,光吸收值为纵坐标,画出标准曲线。 2.酶活力的测定:取2支试管并标号,用第1号试管做为未知管,第2号试管做为空白对照管。各加入谷丙转氨酶底物0.5ml,置于37℃水浴内10min,使管内外温度平衡。取血清0.1ml加到第1号试管内,继续保温60min。到60min时,向两支试管内各加入2,4-二硝基苯肼试剂0.5ml,于37℃保温20min,然后再向2支管中加入0.4mol/L氢氧化钠溶液5ml。在室温下静置30min后,测定未知管的520nm波长光吸收值(显色后30min 至2小时内其色度稳定)。在标准曲线上查出丙酮酸的微摩尔数。(用1μmol丙酮酸代表1.0单位酶活力)。计算每100ml血清中转氨酶的活力单位数。 【试剂和器材】 一`试剂 1.试管及试管架 2.吸管 3.恒温水浴 4.分光光度计 二`器材 1.0.1mol/L磷酸缓冲液(pH7.4) 2.2.0μmol/ml丙酮酸钠标准溶液。 取分析纯丙酮酸钠11mg溶解于50ml磷酸缓冲液内[当日配制]。 3.谷丙转氨酶底物。 取分析纯α-酮戊二酸29.2mg DL-丙氨酸1.78g克置于小烧杯内,加1mol/L氢氧化钠溶液或1mol/L盐酸调整pH至7.4后,加磷酸缓冲液至100ml。然后加氯仿数滴防腐。此溶液每毫升含α-酮戊二酸2.0μmol,丙氨酸200μmol。[在冰箱内可保存一周]。 4.2,4-二硝基苯肼溶液。 在200ml锥形瓶内放入分析纯2,4-硝基苯肼19.8mg,加100ml 1 mol/L盐酸。把锥形瓶放在暗处并不时摇动,待2,4-二硝基苯肼全部溶解后,滤入棕色玻璃瓶内置[冰箱内保存]。 5.0.4mol/L氢氧化钠溶液。 6.人血清[冰箱内保存]
血清丙氨酸氨基转移酶IFCC推荐方法测定 实验原理 国际临床化学学会(IFCC)推荐的紫外连续监测法。 ALT L-丙氨酸+ -酮戊二酸丙酮酸+L-谷氨酸 LDH(乳酸脱氢酶) 丙酮酸+NADH+H+L-乳酸+NAD++H2O 加入磷酸吡哆醛(P-5-P)是为了稳定ALT活性,避免样品中因内源性磷酸吡哆醛不足造成测定结果假性偏低。(如心肌梗死、肝病和特别监护病人的结果)[1] 2.标本: 2.1病人准备:12小时禁食。 2.2类型:血清,肝素或EDTA血浆。 3.标本存放:3天内的活性损失:2~8℃保存:<10%;15~25℃保存:<17%;标本稳定性:-20℃保存至少可稳定4周。 4.标本运输:常温条件下保存运输。 5.标本拒收标准:标本溶血、细菌污染的标本。 6.实验材料 6.1试剂申能ALT测定试剂盒(货号:141270171701试剂16×64ml 试剂26×16ml) 6.1.1试剂组成 试剂1(R1): Tris缓冲液pH7.5100mmol/L
L-丙氨酸500mmol/L LDH(乳酸脱氢酶)≥1200U/L 试剂2(R2): a-酮戊二酸 15mmol/L NADH 0.18mmol/L 磷酸吡哆醛试剂: Good’s缓冲液pH9.60.7mmol/L 磷酸吡哆醛0.09mmol/L 6.1.2试剂准备:试剂为即用式。 6.1.3试剂稳定性与贮存:试剂保存于2~8℃,若无污染,可稳定至失效期。试剂不可冰冻。 6.1.4变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。 6.1.5注意事项:试剂中含叠氮钠(0.95g/L)为防腐剂。不可入口!避免接触皮肤及粘膜。应采取必要的预防措施使用试剂。 6.2校准品:使用DiaSys公司提供的TruCalU校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。 6.3质控品:具体参见生化检验校准品和质控品.SOP文件。 7.仪器:奥林巴斯AU1000生化分析仪 8.操作步骤 8.1项目基本参数:参见生化检验奥林巴斯AU1000生化分析仪项目测定参数.SOP文件 8.2仪器操作步骤:参见生化检验奥林巴斯AU1000生化分析仪操
2014级12班1组201450557 陆丽霞血清丙氨酸氨基转移酶(ALT)活力测定 实验原理:以丙氨酸和ɑ-酮戊二酸为底物,在血清丙氨酸氨基转移酶的作用下,生成丙酮酸和谷氨酸;丙酮酸产量的多少,即反应酶活性的大小,丙氨酸能与2,4-二硝基苯肼结合,生成丙酮酸二硝基苯腙。丙酮酸二硝基苯腙在碱性溶液中呈现棕色,可用比色测定。 实验步骤: 1.标准曲线绘制: ⑴取6支试管并编号,按表4-16操作; 表4-16 标准曲线的绘制 试剂对照 1 2 3 4 5 2mmol/L丙酮酸标准液0 0.05 0.10 0.15 0.20 0.25 底物溶液0.50 0.45 0.40 0.35 0.30 0.25 PBS缓冲液0.1 0.1 0.1 0.1 0.1 0.1 混匀,37摄氏度水浴5分钟,然后各管加入2,4—二硝基苯肼 2,4——二硝基苯肼0.5 0.5 0.5 0.5 0.5 0.5 混匀,37摄氏度水浴20分钟,然后各管加入0.4mol/L NaOH 0.4mol/L NaOH 5.0 5.0 5.0 5.0 5.0 5.0 相当于ALT活力单位0 28 57 97 150 200 A5200 0.059 0.107 0.167 0.208 0.249 ⑵将所得6支试管混匀,10min后以对照组调零,用520nm波长 比色并读取吸光度; ⑶以吸光度为纵坐标,各管相应的转氨酶单位为横坐标,绘制标 准曲线
2.酶活性测定: ⑴取2支试管,编号,按表4-17操作: 表2 ALT活力测定 试剂对照测定 血清——0.1 PBS缓冲液0.1 —— 底物溶液0.5 0.5 混匀,37摄氏度水浴30分钟,然后各管加入2,4——二硝基苯肼2,4—二硝基苯肼0.5 0.5 混匀,37摄氏度水浴20分钟,然后各管加入0.4mol/L NaOH 0.4mol/L NaOH 5.0 5.0 A5200 0.122 ⑵用520nm波长比色,以对照管调零,读取测定管吸光度;实验结果: 由标准曲线方程y=0.0014x,当A520=0.122, 即y=0.122,故x=87 那么测得ALT酶活力单位为87 讨论:
谷丙转氨酶高的治疗方法 对疾病治疗不仅要选择正确的治疗方法,患者和家属对治疗方法也需要进行认识,这样治疗疾病的时候,才会知道该如何做最佳,场景治疗疾病方法就是药物,这样的治疗方式能够很好的控制疾病不在发展,因此是很好选择,那谷丙转氨酶高的治疗方法怎么样呢,下面就详细的介绍下。 谷丙转氨酶高的治疗方法: 1.若长期高酶不降,主要是处方用药不当。包括治则药物配伍及剂量的失误,如原处方苦寒药过多,量过大,而病人
体质较单薄瘦弱,就应适当减量或反佐以少量补肾药物,进行相反方向的调整。另外应删除某些可能会引起转氨酶波动的药物如某些活血药、淡渗药之类。处方的更换不能起伏太大,药物的调整不宜过多。 2.若长期低酶不降,则应考虑用补气助阳养血滋阴药,唯用量不宜过大,适当少佐清解。不能固于清解药降酶。温补药升酶之说而惧于用补。特别具有低酶高絮浊特点的患者,更应用量少平和之方药,避免以大量苦寒药为主.若用补后转氨酶有2次以上连续上升的情况时,再改用清解,若先升后降者,则不必换方。 3.对个别转氨酶升高而以上述方法无效时,可采用停药法。即暂时不服汤药、卧床休息为主,或只服少量中药粉剂(要由医生调配),或配合一些保肝药物。或者用汤药配合服用西药联苯双酯,也能促使转氨酶较快下降.而没有任何毒副作用,对
降酶,改善症状,缓解焦虑心情,均有益处。只是不宜吃吃停停,应坚持一段时间,在医生指导下使用。 4.某些病人一边服汤药,又服用治妇科的或治骨伤科的药物,或自加补药,都会影响转氨酶的下降,因为妇科、骨伤科大夫不一定了解病人有转氨酶的异常,对一些可能妨碍转氨酶下降的药物缺乏研究,因此在使用药物时可能对降酶不利;自己擅加补药时机不宜,也能延缓降酶。 以上就是对谷丙转氨酶高的治疗方法详细介绍,谷丙转氨酶高的治疗不能随意的选择治疗方式,要先对患者病情进行掌握,然后选择适合患者治疗方法,尤其是对岁数的患者,更是要对治疗方法谨慎使用,否则对患者身体会有很大损害。
高中生物常用试剂及其作用 1.斐林试剂:用于检测还原糖。成分:0.1g/ml NaOH(甲液)和0.05g/ml CuSO4(乙液)。 用法:将斐林试剂甲液和乙液等量混合,再将混合后的斐林试剂倒入待测液,现配现用,水浴加热,如待测液中存在还原糖,则呈砖红色。 2.双缩脲试剂:用于检测蛋白质或者多肽(注意:氨基酸不和其发生作用)。成分:0.1g/ml NaOH(甲液)和0.01g/ml CuSO4(乙液)。 用法:向待测液中先加入1ml甲液,摇匀,再向其中加入3~4滴乙液,(先A后B,A大于B)。摇匀。如待测中存在蛋白质,则呈现紫色。 3.苏丹Ⅲ:用于检测脂肪。可将脂肪染成橘黄色 苏丹Ⅳ:用于检测脂肪。可将脂肪染成红色 4.碘液:用于鉴定淀粉的存在。遇淀粉变蓝。遇糖原变红 5.二苯胺:用于鉴定DNA。在沸水浴的条件下,DNA遇二苯胺会被染成蓝色。 6.班氏试剂:由A液(CuSO4溶液)B液(柠檬酸钠和NaCO3溶液)配制而成。作用及检测原理与斐林试剂相似,但班氏试剂可长期使用。 7.甲基绿和吡罗红:甲基绿使DNA呈现绿色,吡罗红使RNA呈现红色。 8.健那绿:检测线粒体,专一性让线粒体染色呈蓝绿色,而细胞质接近无色。活体染色剂 9.龙胆紫溶液或醋酸洋红:碱性染料,用于染色体染色时,前者呈深蓝色,后者呈红色 10.改良苯酚品红染液:检测染色体,红色 11.溴麝香草酚蓝水溶液:检测CO2,由蓝变绿再变黄 12.酸性重铬酸钾溶液:检测酒精,橙色变为灰绿色 13.二氧化硅:在色素的提取的分离实验中研磨绿色叶片时加入,可使研磨充分。 14.碳酸钙:研磨绿色叶片时加入,可中和有机酸,防止色素受破坏。 15.丙酮:用于提取叶绿体中的色素 16.层析液:(成分:20份石油醚、2份丙酮、和1份苯混合而成,也可用93号汽油)可用于色素的层析,即将色素在滤纸上分离开 17.0.3g/mL的蔗糖溶液:相当于30%的蔗糖溶液,比植物细胞液的浓度大,可用于质壁分离实验。 18.胰蛋白酶:①可用来分解蛋白质。②可用于动物细胞培养时分解组织,使组织细胞分散 19.秋水仙素:人工诱导多倍体试剂。用于萌发的种子或幼苗,可使染色体组加倍,原理是可抑制纺缍体的形成。 20.氯化钙:增强细菌细胞壁的通透性,可用于基因工程 21.NaHCO3/ Na2CO3 Na2HPO4/ NaH2PO4:酸碱缓冲对→调节PH 22. 20%的肝脏研磨液、3%的过氧化氢、3.5%的氯化铁:用于比较过氧化氢酶和Fe3+的催化效率。(新鲜的肝脏中含有过氧化氢酶) 23. 台盼蓝:细胞活性染料,用于检测细胞膜的完整性,可以使死细胞变蓝 24.卡诺氏液:固定细胞形态 25.N-1-萘基乙二胺盐酸盐:泡菜制作中测定亚硝酸盐(经酸化,重氮化)的含量,形成玫瑰红色 26. 刚果红:与纤维素形成红色复合物 27.伊红美蓝:大肠杆菌黑色带金属光泽 28.酚红试剂:分离土壤中分解尿素细菌的检测,作用于氨,呈现红色 29.NaHCO3溶液:用于探究环境因素对光合作用强度的影响的试验中,用于提供CO2,或维持反应体系中CO2含量的相对稳定
实验八 肝脏谷丙转氨酶活力测定 实验类型:验证性实验 相关知识 1. 酶活力: 2. 酶活力单位(即酶含量的多少) 国际单位 习惯单位:谷丙转氨酶在37度与底物作用30min 后,能产生2.5ug 的丙酮酸者为一个谷丙转氨酶活力单位 3.转氨酶 4 谷丙转氨酶 一、 实验目的 1. 了解转氨酶的性质及临床意义 2. 掌握谷丙转氨酶活力的测定方法 二、实验原理 丙氨酸及α-酮戊二酸作用为谷丙转氨酶的作用底物,利用内源性磷酸吡哆醛作辅酶,在一定条件下及时间作用后测定所生成的丙酮酸的量来确定酶活力。 丙酮酸能与2,4-二硝基苯肼结合,生成丙酸-2,4二硝基苯腙,后者在碱性溶液中呈现棕色,其吸收光谱的峰为439~530nm ,可用于测定丙酮酸的含量。 α-酮戊二酸也能与2,4-二硝基苯肼结合,生成相应的苯腙,但后者在碱性溶液中吸收光谱为与丙酸-2,4二硝基苯腙的吸光度有差别,在520nm 波长比色时,丙酸-2,4二硝基苯腙吸光度高出3倍。 在520nm 处吸光度增加的程度与反应体系中丙酮酸与α-酮戊二酸的摩尔比基本上呈线性关系,故可以测定谷丙转氨酶的活力。 三、实验器材、试剂、材料 1. 新鲜猪猪脏 2. 722型分光光度计、剪刀、吸管 3. 标准丙酮酸溶液;谷丙转氨酶底物;0.1mol/L 磷酸缓冲液(pH7.4);0.02%2,4-二硝基 苯肼;0.4mol/L NaOH 溶液 2 + 辅基为磷 2 2 + + ‘ ‘
四、实验操作步聚 1.肝匀浆制备 (1)将猪肝脏用生理盐水冲洗,滤纸吸干,称取肝脏0.25g,剪成小块,置于玻璃匀浆管内(或小研砵中),加入2.25ml预冷的pH7.40.1%mol/L磷酸缓冲 液,制成10%肝匀浆。(每四组1份) (2)吸取肝匀浆0.1ml于另一试管中,加入预冷的0.1mol/L磷酸缓冲液(pH7.4) 4.9ml摇匀,为稀释肝匀浆(稀释50倍)(每四组1份) 2.谷丙转氨酶活力测定(每组做1份) 取试管4支按下表加液 五、实验结果与讨论 2.每毫升稀释肝匀浆谷丙转氨酶活力单位(谷丙转氨酶活力计算:规定酶在37度与底物 作用30min后,能产生2.5ug的丙酮酸者为一个谷丙转氨酶活力单位) 3.每克肝脏谷丙氨酶的活力单位。
谷丙转氨酶偏高的饮食应注意以下几个问题: 1、谷丙转氨酶偏高的饮食应注意综合营养,合理搭配,防止偏食。每日要摄取足量的维生素、脂肪、碳水化合物、蛋白质。一日三餐要合理搭配,荤素相间,尽可能少食辛辣等刺激性较强的食物,避免养成偏食的不良习惯。 2、谷丙转氨酶偏高的患者应每天坚持喝一杯牛奶,吃一个鸡蛋、二到三两精瘦肉(猪、牛、羊、鸡、鱼肉均可),一块豆腐,每天两种蔬菜(扁豆、菠菜、油菜、芹菜、黄瓜、香菇、木耳等任选)交换搭配,吃两个水果(苹果、梨、桃、香蕉等不限)。尽可能避免食用麻辣火锅、海鲜发物、油炸油煎、动物内脏等不易消化的食品。 3、谷丙转氨酶偏高的饮食宜食用一些酸性的蔬菜和水果,例如山楂、杏肉、酸枣、西红柿等。另外,香菇、木耳等食用菌含有较为丰富的多糖类物质,对于加强肝病病人机体免疫功能十分有益。绿色食品是保肝养肝的最佳选择,对于新鲜的蔬菜,患者既可以生食,也可以煮汤,每日交换食用。 4、谷丙转氨酶偏高的患者尤其要注意的是:严格禁酒。90%-95%的酒精都是通过肝脏代谢的,饮酒会加重肝脏负担。而且酒精的主要成分乙醇有直接刺激、损害肝细胞的毒性作用,可使肝细胞发生变性、坏死。乙醇的毒性影响肝脏正常代谢及解毒功能,导致严重肝损伤和酒精性肝硬化。因此,谷丙转氨酶偏高的患者不要喝酒,包括红酒、啤酒等酒精性饮料。 此外,需要注意的是,谷丙转氨酶偏高的饮食只是帮助恢复肝功能的一个方面,要想避免谷丙转氨酶反复升高,肝细胞反复受损,必须针对引起谷丙转氨酶偏高的原因进行治疗。在临床上,常见的引起谷丙转氨酶偏高的原因是乙肝大小三阳、酒精肝、脂肪肝、肝硬化等肝脏疾病. 注意事项 谷丙转氨酶偏高表明肝脏受到了损害,是一种较为常见的现象。在谷丙转氨酶升高时要注意肝脏的恢复,增强自身免疫力,一般来说有以下几个注意事项: 1.注意休息,不要熬夜。正常的休息有助于肝功能的修复,要学会抽空休息,消除疲劳。 2.调节情绪,心情要愉快,在种种压力面前“不要生气”这样也有利于提高抗病能力。 3.适当锻炼,避免疲劳。练瑜伽,打坐,打太极拳,游泳等,有利于身体免疫力的提高。
一、颜色反应归纳及拓展 (1)碘应是单质成分,不是离子成分。若用碘来检测叶片光合作用产生的淀粉,则需要先对叶片进行脱色处理。 (2)斐林试剂和双缩脲试剂均由NaOH 溶液和Cu 2SO 4溶液组成,但两者NaOH 溶液的浓度不同,并且两者的使用方法也不同。如斐林试剂甲液和乙液要等量混合均匀后使用,即现用现配,而且要水浴50-60℃加热,而双缩脲试剂在使用时,先加甲液后再加乙液,加的量不同(甲液1mL ,乙液4滴),而且不需要加热。 (3)蛋白质的鉴定是在碱性环境下Cu 2+与蛋白质的肽键结合成特定化合物的紫色反应。而还原糖的鉴定是新制的的Cu(OH)2 与还原糖的醛基反应,生成砖红色的Cu 2O 沉淀。 (4)健那绿染液是专一性染线粒体的活细胞染料。可使活细胞中的线粒体染成蓝绿色,而细胞质接近无色。 (5)观察DNA 和RNA 在细胞中的分布时用的是甲基绿和吡罗红混合染色剂(即吡罗红甲基绿染色剂),而不是单独染色,应该注意的是该试剂应现用现配。 (6)根据石灰水混浊程度或溴麝香草酚蓝水溶液变黄的时间长短,可以定量检测酵母菌培养液中CO 2的产生情况。 (7)染色体(染色质)容易被碱性染料龙胆紫溶液染成深紫色,用高倍显微镜可以观察细胞的有丝分裂过程中染色体的行为。另外,脂肪的鉴定和细胞中线粒体的观察,也需要染色后,再借助显微镜观察。 (8)龙胆紫和醋酸洋红均为碱性染料,染色体被龙胆紫染成紫色,而被醋酸洋红染成红色。 2012·安徽卷)某同学以新鲜洋葱鳞片叶内表皮为材料,经不同处理和染色剂染色,用高倍显微镜观察。下列描述正确的是( ) A .经吡罗红甲基绿染色,可观察到红色的细胞核 B .经吡罗红甲基绿染色,可观察到绿色的细胞质 C .经健那绿染色,可观察到蓝绿色颗粒状的线粒体 D .经苏丹Ⅲ染色,可观察到橘黄色颗粒状的蛋白质 解析:甲基绿能将DNA 染成绿色,吡罗红能将RNA 染成红色,DNA 主要分布在细胞核中,RNA 主要分布在细胞质中,A 、B 项错误;健那绿可将线粒体染成蓝绿色,C 项正确;苏丹Ⅲ可以用来鉴定脂肪,不能用来鉴定蛋白质,D 项错误。 答案:C
实验九&十血液中转氨酶活力的测定(分光光度法) 本实验八人一组(根据分光光度计来确定) 一、目的要求: 1、了解转氨酶的重要作用及其在临床诊断中的意义。 2、学习转氨酶活力测定的原理和方法。 二、原理:(谷丙转氨酶和丙酮酸的反应方程式) 生物体内广泛存在的氨基移换酶也称转氨酶,能催化α-氨基与丙酮酸的α-酮基互换,在氨基酸的合成和分解,尿素和嘌呤的合成等中间代谢过程中有重要作用。转氨酶的最适pH接近7.4,它的种类很多,其中以谷氨酸-草酰乙酸转氨酶和谷氨酸-丙酮酸转氨酶(简称谷丙转氨酶)的活力最强。正常人血清中只含有少量转氨酶,当发生肝炎、心肌梗死等病患时,血清中转氨酶活力常显著增加,所以在临床诊断上转氨酶活力的测定有重要意义。 本实验采用分光光度计法。谷丙转氨酶作用于丙氨酸和α-酮戊二酸后,生成的丙酮酸与2,4-二硝基苯肼作用生成丙酮酸2,4-二硝基苯腙(催化反应方程式)。丙酮酸2,4-二硝基苯腙加碱处理后呈棕色,可用分光光度法(520nm)测定。从丙酮酸2,4-二硝基苯腙的生成量,可以计算酶的活力。 三、操作: 实验九标准曲线的绘制(由于时间关系,只做一组数据,不要重复) 1、向试管中加入试剂(有改动):取6支试管,分别标上0、1、 2、 3、 4、5六个号。按表中所列的次序添加各种试剂(由于后面测定样品时有对照实验,所以不需要加入谷丙转氨酶底物,以蒸馏水补齐;不需要保温10分钟来平衡内外温度)。 2、向各管内加入0.5mL 2,4—二硝基苯肼溶液后37℃保温20分钟。 3、分别向各管内加入0.4mol/L氢氧化钠溶液5mL(丙酮酸2,4-二硝基苯腙加碱处理后呈棕色)。在室温下保温静置30分钟,以0号管做空白,测定A520nm的吸光度。用丙酮酸的摩尔数做横坐标,光吸收值为纵坐标,画出标准曲线。
谷丙转氨酶(GPT)活性的测定预习报告 1.研究背景:转氨酶是体内重要的一类酶。转氨酶催化α–氨基酸的α–氨基与α–酮酸 的α–酮基之间的相互转化,从而生成一种新的氨基酸与一种新的酮酸,这种作用称为转氨基作用。它在生物体内蛋白质的合成,分解等中间代谢过程中,在糖,脂及蛋白质三大物质代谢的相互联系,相互制约及相互转变上都起着很重要的作用。故转氨酶是氮代谢中不可缺少的一种酶,本次实验测定谷丙转氨酶活性不但可以进一步完善了转氨酶活性研究领域,并且对其他种类转氨酶活性测定具有一定指导作用,测得数据还可以作为临床医学参数造福人类。 2.研究目标:由于催化活性是酶的一个独特属性。酶蛋白质质量再多,纯度再高,如果没有活性往往是毫无意义的。实验用赖氏法分别测定兔子肝脏和血清中GPT活性,藉以作为谷丙转氨酶研究的一个基础。 3.研究策略:根据本次酶活力单位和酶比活定义,通过一定技术手段测定在该条件下由酶催化产生的丙酮酸的量,进而间接反应酶的比活。由于丙酮酸与2,4—二硝基苯肼反应所生成的丙酮酸二硝基苯腙,在碱性环境中于520nm下的特异光吸收在一定的浓度范围内符合朗伯比尔定律,故可以用比色法测定丙酮酸的含量,便可以计算出肝脏和血清中谷丙转氨酶的比活。 4.研究方案及可行性分析:现在可以对反应环境可以做到相当准确的控制,pH 值可以通过缓冲溶液控制,反应的温度可以通过恒温水域箱控制,电子天平可以测定万分之一克以及精确的容量瓶这样可以保证标准管丙酮酸的浓度的准确性。虽然这些实验基础具备了但是由于α-酮戊二酸和2,4—二硝基苯对显色的干扰,以致丙酮酸产量与酶量的关系并不始终成线性关系,其理论误差可以控制相应物质浓度尽量减小。同时,在操作过程中酶在相应条件下反应的时间,以及将试管同时放入和取出水浴的时间不能够精确保证,造成进一步的误差。故本次实验虽具有一定的可操作性,但由于其中引入的误差过程比较多,应该注意保证每一步的正确性,同时通过卡门氏单位进行校正,进而减小实验误差对可操作性带来的影响。 5.具体实验设计: 5.1实验材料:家兔的肝脏和血清 5.2实验仪器:722-光栅分光光度计、离心机、电热恒温水浴锅、匀浆机、移液器、100ml 容量瓶若干、15ml具塞刻度试管若干 5.3具体操作步骤 1.肝匀浆液制备:新鲜肝脏用生理盐水冲洗后沥干,取1g以9ml预冷的pH7.4的0.1M磷酸缓冲液在冰浴上充分匀浆(10%肝匀浆),4000转低温冷冻离心15分钟取上清液冰浴中备用,酶活测定时视情况一般还需稀释至少50倍使用。 2. 血清的制备:心脏采血,分装至预先用生理盐水浸润过的离心管中,3000转低温冷冻离心15分钟取血清冰浴中备用。 3.谷丙转氨酶活力的测定
高中生物学实验的各种颜色反应总结 1、斐林试剂(或班氏试剂)检测可溶性还原糖 原理:还原糖+斐林试剂(或班氏试剂)→砖红色沉淀 常见还原糖:葡萄糖、果糖、麦芽糖 注意:斐林试剂的甲液和乙液要等量混合均匀后方可使用,而且是现用现配,条件需要水浴加热。 应用:检验和检测某糖是否为还原糖;不同生物组织中含糖量高低的测定;在医学上进行疾病的诊断,如 糖尿病、肾炎。 2、苏丹Ⅲ、苏丹Ⅳ检测脂肪 原理:苏丹Ⅲ+脂肪→橘黄色; 苏丹Ⅳ+脂肪→红色 注意:脂肪的鉴定需要用显微镜观察。 应用:检测食品中营养成分是否含有脂肪。 3、双缩脲试剂检测蛋白质 原理:蛋白质+双缩脲试剂→紫色 注意:双缩脲试剂在使用时,先加A液再加B液,反应条件为常温(不需要加热)。 应用:鉴定某些消化液中含有蛋白质;用于劣质奶粉的鉴定。 4、碘液检测淀粉 原理:淀粉+碘液→蓝色 注意:这里的碘是单质碘,而不是离子碘。 应用:检测食品中营养成分是否含有淀粉 5、DNA的染色与鉴定 染色原理:DNA+甲基绿→绿色 应用:可以显示DNA在细胞中的分布。 鉴定原理:DNA+二苯胺→蓝色 条件:沸水浴 应用:用于DNA粗提取实验的鉴定试剂。 6、吡罗红使RNA呈现红色 原理:RNA+吡罗红→红色 应用:可以显示RNA在细胞中的分布。 注意:在观察DNA和RNA在细胞中的分布时用的是甲基绿和吡罗红混合染色剂,而不是 单独染色。 7、台盼蓝使死细胞染成蓝色 原理:正常的活细胞,细胞膜结构完整具有选择透过性能够排斥台盼蓝,使之不能够进入胞内;死细胞或细胞膜不完整的细胞,胞膜的通透性增加,可被台盼蓝染成蓝色。 应用:区分活细胞和死细胞;检测细胞膜的完整性。 8、线粒体的染色 原理:健那绿染液是专一性染线粒体的活细胞染料,可以使活细胞中的线粒体呈现蓝绿色,而细胞质接近无色。 应用:可以用高倍镜观察细胞中线粒体的存在。 9、酒精的检测 原理:橙色的重铬酸钾溶液在酸性条件下与酒精发生化学反应,变成灰绿色。
丙氨酸氨基转移酶(ALT)检测试剂盒(单试剂速率法) 简介: 转氨酶是催化α-氨基酸和α-酮酸之间氨基转换反应的一组酶,丙氨酸氨基转移酶(ALT)旧称谷丙转氨酶(GPT)主要存在于肝细胞浆内,细胞内ALT 浓度远高于血清,肝细胞破坏后,血清ALT 立即迅速升高,因此谷ALT 被世界卫生组织推荐为肝功能损害最敏感的检测指标。 Leagene 丙氨酸氨基转移酶(ALT)检测试剂盒(单试剂速率法)其检测原理是丙氨酸氨基转移酶催化丙氨酸与α-酮戊二酸之间的氨基转移反应,丙酮酸与NADH 经LDH 催化成NAD +,上述方法实际为ALT 速率法,在上述偶联反应中,NADPH 的氧化速率与样本中 酶活性呈正比。该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。 组成: 操作步骤(仅供参考): 1、 准备样品: ① 血浆、血清样品:血浆、血清按照常规方法制备,可以直接用于本试剂盒的测定, -20℃保存1个月有效,用于ALT/GPT 的检测。 ② 细胞或组织样品:取恰当细胞或组织进行匀浆,低速离心取上清,-20℃保存1个 月有效,用于ALT/GPT 的检测。 ③ (选做)样品准备完毕后可以用BCA 蛋白浓度测定试剂盒测定蛋白浓度,以便于后续 计算单位蛋白重量组织或细胞内的ALT/GPT 含量。 2、 分光光度计检测:按照下表设置对照管、测定管,溶液应按照顺序依次加入,并注意避 免产生气泡。如果样品中的酶活性过高,可以减少样品用量或适当稀释后再进行测定。 编号 名称 TE0125 100T TE0125 200T Storage ALT 检测液(R) 成分 终浓度 2×50ml 2×100ml 4℃ 避光 Tris 缓冲液 100mM L-丙氨酸 500mM 酮戊二酸 15mM NADH 0.22mM LDH 1700U/L 防腐剂 15mM 使用说明书 1份 加入物 空白管 测定管
高中生物教材盲区知识点归纳03(必修1) 1.低温环境会影响物质的跨膜运输吗?为什么?(必一P73) 提示:低温环境肯定会影响物质的跨膜运输。温度会影响分子运动的速率,影响化学反应的速率,因此,组成细胞膜的分子的流动性也会相应降低,呼吸作用释放能量的过程也会因有关酶的活性降低而受到抑制。这些都会影响物质跨膜运输的速率。 2.胆固醇:构成细胞膜的重要成分,参与血液中脂质的运输; 但当其过量摄入时便会导致高胆固醇血症,会造 成血管堵塞,从而对机体产生不利的影响(必一P33) 3.新宰的畜、禽,如果马上把肉做熟了吃,而口味不好,过一段时间再煮,肉反而鲜嫩。这可能与肌细胞内哪一种细胞器的作用有关?(必一P58) 提示:与溶酶体的作用有关。细胞死亡后,溶酶体膜破裂,各种水解酶释放出来,分解细胞中的蛋白质等物质,这时的畜、禽肉烹饪后更鲜嫩。这个过程需要一定的时间。 4.破伤风由破伤风芽孢杆菌引起,这种病菌只能进行无氧呼吸。皮肤破损较深或被锈钉扎伤后,病菌就容易大量繁殖。(遇到这种情况,需要及时到医院治疗,如清理伤口、敷药并注射破伤风抗毒血清。)(必一P96) 5.烘干一粒种子,然后点燃烧尽后,最终会得到一些灰白色的灰烬,这些灰烬就是小麦种子里的无机盐(必一P35) 6.胞吞和胞吐区别:胞吞细胞膜内陷形成小囊泡,胞吐:细胞内高尔基体形成的囊泡。(必一P72) 7.克劳德利用差速离心法分离细胞内不同组分。该方法至今还用于分离不同密度的固体成分(必一P51) 8.系统是指彼此间相互作用、相互依赖的组分有规律地结合而形成的整体。(必一P4) 系统的一般特征:①有边界;②有系统内各组分的分工合作;③有控制中心起控制作用.(必一P57) 9.健那绿染液是将活细胞中线粒体染色的专一性染料,可以使活细胞中的线粒体呈现蓝绿色,而细胞质无色.(必一P47) 10罗伯特森在电子显微镜下观察到细胞膜清晰的暗-亮-暗的三层结构(必一P66) 11.消化道和呼吸道上皮细胞表面的糖蛋白有保护和润滑作用(必一P68) 12.酸能催化蛋白质脂肪和淀粉水解。(必一P83) 13.唾液PH值6.2~7.4,胃液PH值0.9~1.5,小肠液PH值7.6(必一P83) 14.动物体内的酶的最适温度35℃~40℃,植物体内的酶的最适温度40℃~50℃(必一P85) 15.细胞既是生物体结构的基本单位也是生物体代谢和遗传的基本单位。(必一P55) 16.体外燃烧1g葡萄糖和体内氧化分解1g葡萄糖释放的能量都是16kJ(必一P30) 17.纤维素是多糖,不溶于水,在人和动物体内很难消化既是草食动物也需要借助于某些微生物帮助才能消化。(必一P31) 18.磷脂是一种由甘油、脂肪酸和磷酸等所组成的分子,磷酸“头”部是亲水的,脂肪酸“尾”部是疏水的。(必一P66) 19.请运用相关的化学知识,解释为什么磷脂在空气一水界面上铺展成单分子层,而科学家如何从这一现象推导出“脂质在细胞膜中必然排列为连续的两层”这一结论的。(必一P66) 提示:因为磷脂分子的“头部”亲水,所以在水—空气界面上磷脂分子是“头部”向下与水面接触,尾部则朝向空气一面。科学家因测得单分子层的面积恰为红细胞表面积的2倍,才得出膜中的脂质必然排列为连续的两层这一结论。 20.淡水水域污染富营养化会爆发主要由蓝藻引起的水华现象,影响水质和水生生物的生活(必一P9) 21. 科学研究证实,在精细胞变形为精子的过程中,精子的头部几乎只保留了细胞核,部分细胞质变成精子
实验九肝脏中转氨酶活力的测定 一、实验目的 1. 了解转氨酶的性质和临床意义; 2. 掌握谷丙转氨酶活力的测定方法 二、实验原理 本实验以丙氨酸的氧化脱氨基为例,分别测定谷丙转氨酶,谷氨酸脱氢酶活性外,又通过抑制剂观察肝组织中的联合脱氨基作用。在谷丙转氨酶的催化下,丙氨酸和α-酮戊二酸作用生成丙酮酸和谷氨酸。次反应可逆,平衡点近于1.0无论正向反应或逆向反应皆可用于测定此酶的活性,既可测定所产生的氨基酸,也可以测定生成的酮酸,因此可有多种测定方法。 本实验以丙氨酸和α-酮戊二酸作为谷丙转氨酶作用的底物,利用内源性磷酸吡哆醛作为辅酶,在一定条件及时间作用后测定所生成的丙酮酸的量来确定其酶活力。丙酮酸能与2,4-二硝基苯肼结合,生成丙酮酸2,4-二硝基苯腙,后者在碱性溶液中呈现棕色,其吸收峰为439-530nm,可用于测定丙酮酸的含量。 α-酮戊二酸也能与2,4-二硝基苯肼结合,生成相应的苯腙,但后者在碱性溶液中吸收光谱与丙酮酸二硝基苯腙有差别,在520nm波长比色时,α-酮戊二酸二硝基苯腙的吸光度远较丙酮酸二硝基苯腙为低(约相差3倍)。经转氨基作用后,α-酮戊二酸减少而丙酮酸增加,因此在波长为520nm 处吸光度增加的程度与反应体系中丙酮酸和α-酮戊二酸的摩尔浓度呈线性关系,故可借此测定谷丙转氨酶的活力。 三、实验材料、试剂和仪器 (一)材料与试剂 猪肝脏、乙醇、0.4mol/LNaOH 标准丙酮酸溶液(1mL 相当于500μg):准确称取纯化的丙酮酸钠62.5mg,溶于100mL 的0.05mol/L的H2SO4中,此液需临用前配制。 谷丙转氨酶底物:称取L-丙氨酸0.90g 及α-酮戊二酸29.2mg,先溶于pH7.4 的0.1mol/L 磷酸缓冲液中,然后用1mol/L NaOH 调至pH7.4,再加pH7.4 的0.1mol/L 磷酸缓冲稀释至100mL,贮藏于冰箱内,可保存一周。(试验了一下pH 接近7.5,中间未调整pH 值) 0.1mol/L 的磷酸缓冲液(pH7.4):称取13.97gK2HPO4(如果是K2HPO4·?H2O,则需称取18.31g)和2.69gKH2PO4 溶于1000mL 蒸馏水中。 0.02% 2,4-二硝基苯肼溶液:称取2,4-二硝基苯肼20mg 溶于少量1mol/L 盐酸中,加热溶解后,利用1mol/L 盐酸稀释至100mL。 (二)仪器/器具 电子天平、分光光度计、剪刀、移液管、组织破碎机 四、实验步骤 1. 肝匀浆制备与稀释