乙烯
一.乙烯
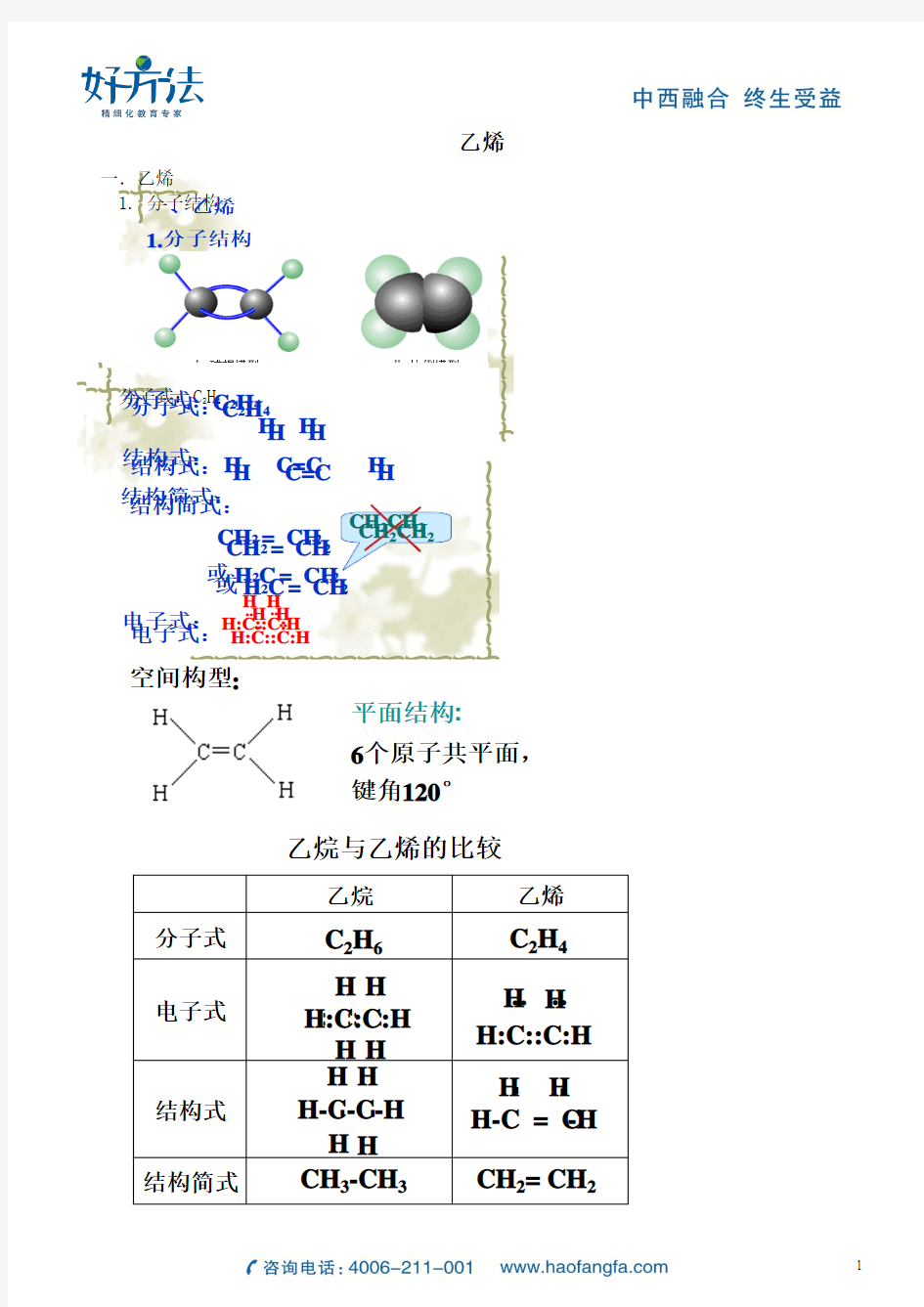
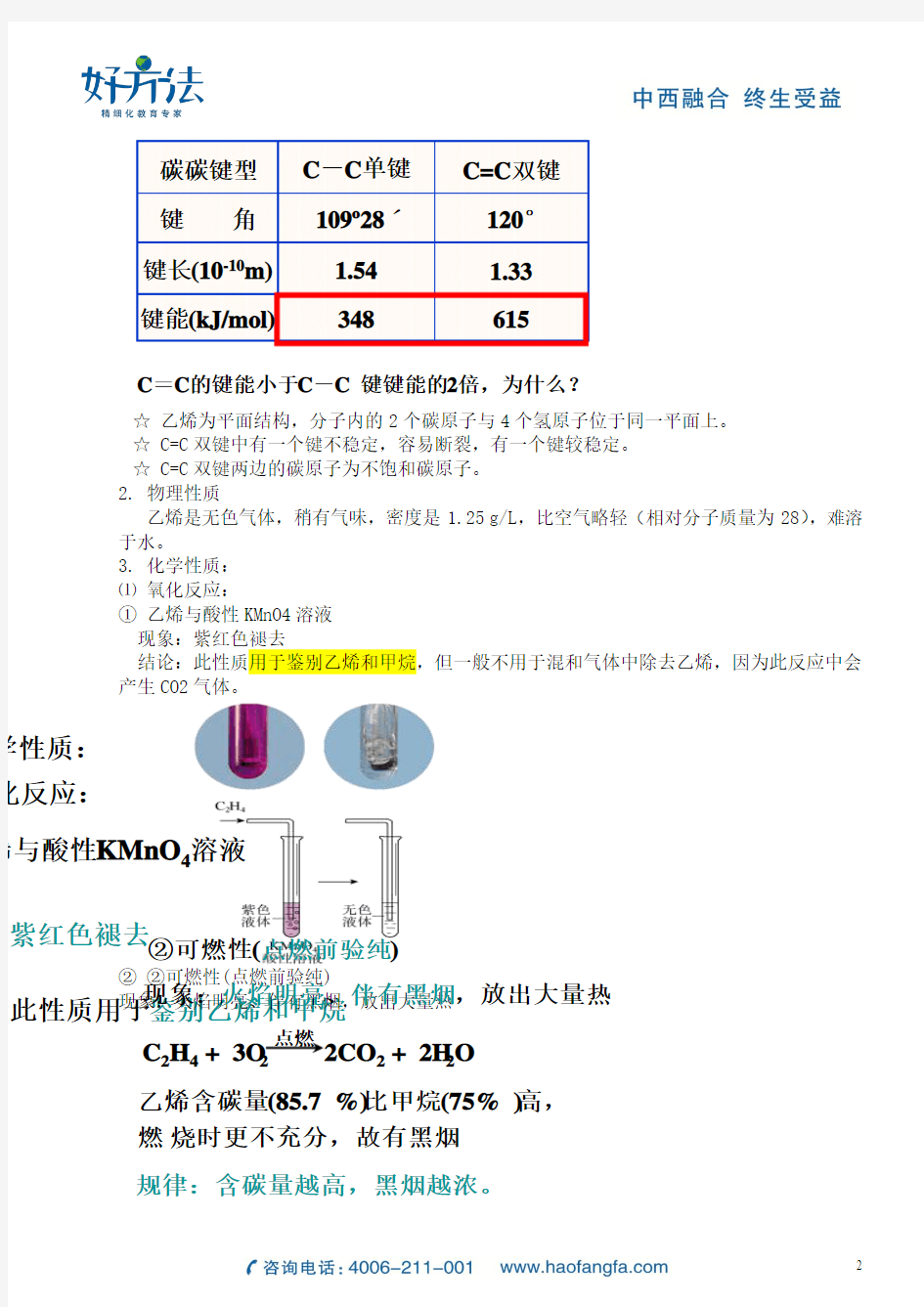
1.分子结构
一、乙烯
1.分子结构
分子式:C
2H 4
分子式:C2H4
结构式:
H H
H C=C H
结构简式:
CH2 = CH2或H2C= CH2CH
2
CH
2
电子式:
H H
.... H:C::C:H
分子式:C2H4
结构式:
H H
H C=C H
结构简式:
CH2 = CH2或H2C= CH2CH
2
CH
2
电子式:
H H
....
H:C::C:H
平面结构:
6个原子共平面,
键角120°
空间构型:
乙烷与乙烯的比较
分子式乙烷C
2
H
6 H H
2. 物理性质
乙烯是无色气体,稍有气味,密度是1.25 g/L ,比空气略轻(相对分子质量为28),难溶于水。
3. 化学性质: ⑴ 氧化反应:
① 乙烯与酸性KMnO4溶液 现象:紫红色褪去
结论:此性质用于鉴别乙烯和甲烷,但一般不用于混和气体中除去乙烯,因为此反应中会产生CO2气体。
学性质:
化反应:
烯与酸性KMnO 4溶液
:紫红色褪去:此性质用于鉴别乙烯和甲烷
② ②可燃性(点燃前验纯)
现象:火焰明亮、伴有黑烟,放出大量热
现象:火焰明亮、伴有黑烟,放出大量热规律:含碳量越高,黑烟越浓。
C 2H 4+ 3O 2
2CO 2+ 2H 2O
点燃
②可燃性(点燃前验纯)
乙烯含碳量(85.7 %)比甲烷(75% )高,燃烧时更不充分,故有黑烟
溶液中)
1,2-二溴乙烷
[ CH
2—CH
2
]
n
二、乙烯的实验室制取
1 、试剂:浓硫酸与无水乙醇(体积比3:1)
控制反应温度,防止制取的乙烯不纯,因为温度过高或过低都会产生气体杂质.因此反应得迅速加热到1700左右;温度计插入液面以下。
加成反应:有机分子中双键(或三键)
问题二:浓硫酸的作用?反应中体现了浓硫酸的什么性质?
浓硫酸起催化剂作用,反应中体现了浓硫酸的脱水性。
问题三:沸石(或碎瓷片)的作用?防止爆沸
问题四:可以用排空气法收集乙烯吗?
不可以,因为乙烯M=28g/mol密度和空气M均=29g/mol密度接近。
5.5.乙烯的用途
重要化工原料乙烯的产量衡量一个国家的石油化工水平;水果的催熟剂。
习题:
1.能用于鉴别甲烷和乙烯的试剂是 ( )
A.溴水
B.酸性高锰酸钾溶液
C.苛性钠溶
D.四氯化碳溶液
2.通常用于衡量一个国家石油化工发展水平的标志是( )
A.石油的产量
B.乙烯的产量
D. 与氧气反应生成二氧化碳和水
5 下列反应中,属于加成反应的是( )
A.乙烯与氢气反应生成乙烷
B.氢气与氧气反应生成水
C.甲烷与氯气反应
D.乙烯与氧气反应生成二氧化碳和水
6下列物质不可能是乙烯加成产物的是()
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH2BrCH2Br
7.在一定条件下,乙烷和乙烯都能制备氯
乙烷CH3CH2Cl。试回答:
1.乙烷制氯乙烷的化学方程式是
___________________________________;
2.乙烯制备氯乙烷的化学方程式是
_______________________________;
3.比较两种方法,________方法制备氯乙烷更好,原因是:
8.实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫(二氧化硫能使酸性高锰酸钾褪色)
C+2H2S04(浓)=2SO2↑+CO2↑+2H2O。
有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回 答下面问题。 (1)下图中①、②、③、④装置可盛放的试剂是:①______;②______;③______;④______
(将序号填入空格内)。 A.品红溶液 B. NaOH 溶液
C.浓H2SO4
D. 酸性KMnO4溶液 烯,常因温度过高而使乙醇和浓量的二氧化硫(二氧化硫能使酸
钾褪色)
(浓)=2SO 2↑+CO 2↑+2H 2O
。
验以确认上述混合气体中有乙烯回答下面问题。、③、④装置可盛放的试剂是:
___;___
内)。OH 溶液性KMnO 4溶液B D △ (2)能说明二氧化硫气体存在的现象是 ______________________。
(3)使用装置②的目的是 _____________________________________。
(4)使用装置③的目的是_______________。
(5)确认含有乙烯的现象是 _________________________________。 8、下述反应中,属于取代反应的是_______________
属于氧化反应的是_____________,属于加成反应的是_______________。
①由乙烯制氯乙烷 ②乙烷在空气中燃烧 ③乙烯使溴水褪色 ④乙烯使酸性高锰酸钾溶液褪色 ⑤乙烷在光照下与氯气反应
9、据碳碳双键结构,推测并写出CH 3CH=CH 2发生加聚反应的化学方程式 ________________________________________________________________ 10.化学方程式:
CH 2BrCH 2Br CH 2=CH 2 CH 3CH 3
CH 3CH 2Br [ CH 2CH 2 ] n
答案:
1.AB
2.B 4. D 5.A 6. B
7. 练习:
在一定条件下,乙烷和乙烯都能制备氯乙烷CH 3CH 2Cl 。试回答:
1.乙烷制氯乙烷的化学方程式是
___________________________________;
2.乙烯制备氯乙烷的化学方程式是
_______________________________;3.比较两种方法,________方法制备氯乙烷更好,原因是_____________________________________。CH 3CH 3+ Cl 2 CH 3CH 2Cl + HCl 光照
取代反应加成反应第2种乙烷与Cl 2发生取代反应,产物中有多种卤代烃;而乙烯与HCl 发生加成反应,产物单一。CH 2=CH 2 + HCl CH 3-CH 2Cl 催化剂
△
8 4.实验室制取乙烯,常因温度过高而使乙醇和浓
H 2SO 4反应生成少量的二氧化硫(二氧化硫能使酸
性高锰酸钾褪色)
C+2H 2S04(浓)=2SO 2↑+CO 2↑+2H
2O 。
有人设计下列实验以确认上述混合气体中有乙烯
和二氧化硫。试回
答下面问题。
(1)下图中①、②、③、④装置可盛放的试剂是:
①______;②______;③______
;④______(将序号填入空格内)。A.品红溶液 B.NaOH 溶液
C.浓H 2SO 4
D.酸性KMnO 4溶液
A B A D △
(2) 装置①中品红溶液褪色
(3) 除去SO2气体,以免干扰乙烯的性质实验 (4) 检验SO2是否除尽
(5) 装置③不褪色,装置④褪色
乙烯 知识点辅导: 一、乙烯的结构: 1、乙烯是一种不饱和烃,分子式C2H4,电子式、结构式 2、乙烯分子里所有原子都在同一平面上,碳氢之间的键角120,双键键长小于乙烷中C-C单键键长,C=C双键的键能比C-C单键的键能小,双键中有一个键较易断裂。 3、碳四键原理:在有机物分子中,碳原子均有四个键与其它原子结合,这是书写有机物结构式,分析有机物分子组成结构关系的重要依据。 4、同系列原理:同系列中的各不同有机物均具有十分相似的化学性质,利用这条原理,可以解决许多的问题。 5、官能团原理:结构决定性质,在有机化学中体现为:原子团决定特性,有机物主要是按原子团进行分类的,所以学习有机化学,从某种意义上说是学习官能团,并且同一物质中的官能团还能相互影响。 二、乙烯的性质: 1、有关有机物的氧化反应: (1)有机化学中,把得氧和失氢的反应称为氧化反应,把得氢或失氧的反应称为还原反应。 (2)在空气中或在氧气中燃烧——完全氧化,绝大多数有机物(除CCl4、CF4、CHCl3等外)都能燃烧,燃烧产物取决于O2是否足量,若O2是足量的,产物为CO2和H2O,若O2不足,产物是C、CO和H2O。燃烧时火焰的明亮程度与分子中含碳量有关,含碳量越高,火焰越明亮,有可能带黑烟。 (3)催化剂存在时被氧气氧化。 (4)被氧化剂氧化,这类氧化反应一般是有机分子中的局部(官能团)被氧化。 2、乙烯能使KM n O4(H+)溶液褪色,用于区别甲烷。
3、在烷烃中只有两种键:C—C单键和C—H键。在反应时,当具有足够的能量时,这两种键都可断裂。若有氧气存在,可燃烧生成CO2和H2O。若无氧气存在,即发生单纯的热分解反应。当受其他反应物质的影响,在不定能量的作用下,只能破坏烷烃中两种化学键中的C—H极性键(C—C键为非极性键),由1价的原子或原子团取代H原子,所以取代反应成为烷烃的特征反应。 4、在不饱和烃中,存在较不稳定的C=C双键(还有CC叁键,在后面将学到),除了化学键可完全断裂在氧气中燃烧生CO2和H2O之外,还可被KM n O4氧化,使KM n O4溶液褪色。不饱和键还可部分打开和一些物质(包括H2、X2、HX、HOH、HClO等)中的1价原子或原子团发生加成反应。在无外界反应试剂时,部分打开的C=C双键,使不饱和碳原子相互连接发生加聚反应,生成高分子化合物。加成反应和加聚反应就成为不饱和烃的特征反应,而不能发生取代反应。 5、加成反应: 双键中的一个键易破裂,溴原子分别加在两个碳原子上。 (1)C=C双键中有一条与烷烃的C-C单键相同,另一条比C-C单键弱易断裂,从而发生加成。 (2)加成反应是不饱和键的特征反应,在后面将学到了CC,C=O,也属于不饱和键,也可发生加成反应。 6、加聚反应(加成聚合反应): (1)聚乙烯是相对分子质量很大的高分子化合物,这种聚合反应也是加成反应,属加聚反应。 (2)高分子化合物可分为两类、一类是天然高分子化合物,如天然橡胶、淀粉、纤维素、蛋白质等,另一类是合成高分子化合物,如聚乙烯合成橡胶等。 三、乙烯的实验室制法: 1、浓H2SO4起催化剂和脱水剂的作用,在反应中会有其它副反应。 2、烧瓶中要加入少量的碎瓷片(或沸石)的作用是防止混合液爆沸。
第一章有理数考点一、实数的概念及分类(3 分) 1、实数的分类 正有理数 有理数零有限小数和无限循环小数实数负有理数 正无理数 无理数无限不循环小数 负无理数 2、无理数:7, 3 2 π ,+8,sin60o 。 3 第二章整式的加减 考点一、整式的有关概念(3 分) 1、单项式 只含有数字与字母的积的代数式叫做单项式。 注意:单项式是由系数、字母、字母的指数构成的,其中系数不能用带分数表示,如- 4 1 a 2 b ,这3 种表示就是错误的,应写成-13 a 2 b 。一个单项式中,所有字母的指数的和叫做这个单项式的次数。如3 -5a3b 2c 是6 次单项式。 考点二、多项式(11 分) 1、多项式 几个单项式的和叫做多项式。其中每个单项式叫做这个多项式的项。多项式中不含字母的项叫做常数项。多项式中次数最高的项的次数,叫做这个多项式的次数。 2、同类项 所有字母相同,并且相同字母的指数也分别相同的项叫做同类项。几个常数项也是同类项。 第三章一元一次方程 考点一、一元一次方程的概念(6 分) 1、一元一次方程 只含有一个未知数,并且未知数的最高次数是1 的整式方程叫做一元一次方程,其中方程 ax +b =(0 x为未知数,a ≠ 0)叫做一元一次方程的标准形式,a 是未知数x 的系数,b 是常数项。 第四章图形的初步认识 考点一、直线、射线和线段(3 分) 1、点和直线的位置关系有线面两种: ①点在直线上,或者说直线经过这个点。 ②点在直线外,或者说直线不经过这个点。 2、线段的性质 (1)线段公理:所有连接两点的线中,线段最短。也可简单说成:两点之间线段最短。 (2)连接两点的线段的长度,叫做这两点的距离。 (3)线段的中点到两端点的距离相等。
地理各模块知识点总结 地理知识点总结了一篇又一篇,每次都是以不一样的视角去告诉学生,如果考试是这样考的,这样的知识点就必须要记住,今天也不例外,每块知识都是从不同角度来分析,这一定就是我们需要掌握的知识! 一、生态问题 1 水土流失问题 我国典型地区:黄土高原、南方低山丘陵地区 产生的原因: (1)自然原因:季风气候降水集中,多暴雨;地表植被稀少;黄土土质疏松黄土高原)。 (2)人为原因:植被的破坏;不合理的耕作制度;开矿。 治理的措施:压缩农业用地,扩大林、草种植面积;植树造林;小流域综合治理。 治理的意义: 有利于因地制宜地进行产业结构的调整,使农林牧副渔全面发展,可以增加农民收入,促进当地经济发展,改善农民生活条件,提高生活质量;有利于改善当地的生态环境,建立良性生态系统;建立生态农业模式,有利于促进生态和经济可持续发展。 2 荒漠化问题 我国典型的地区:西北地区(新疆、青海、内蒙等地) 产生的原因: (1)自然原因:全球变暖,蒸发旺盛;处于内陆地区,降水少;鼠害;蝗害。 (2)人为原因:过度放牧;过度樵采;过度开垦;水资源的不合理利用;交通线等工程建设保护不当。 治理措施: 制定草场保护的法律、法规,加强管理;控制载畜量;营造“三北防护林”建设;退耕还林、还牧;建设人工草场;推广轮牧;禁止采伐发菜等 治理意义: 有利于因地制宜地进行产业结构的调整,使农林牧副渔全面发展,可以增加农民收入,促进当地经济发展,改善农民生活条件,提高生活质量;有利于保护土地资源改善当地的生态环境;有利于促进生态和经济可持续发展。 3 干旱缺水问题 我国典型地区:华北地区、西北、长江中下游地区 华北地区:
九年级上册数学圆章节知 识点总结 Prepared on 21 November 2021
与圆相关的基本知识和计算 一、知识梳理: (一):圆及圆的有关概念 1.圆:到顶点的距离等于定长的点的集合叫做圆; 2.弧:圆上任意两点间的部分叫做圆弧,简称弧。圆的任意一条直径的两个端点把圆分成两条弧,每一条弧都叫做半圆,大于半圆的弧叫做优弧,小于半圆的叫做劣弧; 3.弦:连接圆上任意两点的线段叫做弦。经过圆心的弦叫做直径,它是圆的最长的弦; 4.等圆:能够完全重合的两个圆叫做等圆;等弧:在同圆或等圆中,能够互相重合的弧叫做等弧; 5.圆心角:顶点在圆心的角叫做圆心角;圆周角:顶点在圆上且两边与圆相交的角叫做圆周角; (二)圆的有关性质: 1.对称性:圆是中心对称图形,其对称中心是圆心;圆是轴对称图形,其对称轴是直径所在的直线; 2.垂径定理及其推论: (1)、垂径定理:垂直弦的直径平分弦,并且平分弦所对的弧; (2)、推论:平分弦(不是直径)的直径垂直于弦,并且平分弦所对的弧;3.圆心角、弧、弦之间的关系 (1)定理:在同圆或等圆中,相等的圆心角所对的弧相等,所对的弦也相等;(2)推论:在同圆或等圆中,如果两条弧相等,那么他们所对的圆心角相等、所对的弦相等。在同圆或等圆中,如果两条弦相等,那么它们所对的圆心角相等、所对的弧相等。 4.圆周角与圆心角的关系 (1)在同圆或等圆中,同弧或等弧所对的圆周角相等,都等于这条弧所对的圆心角的一半;
(2)推论:半圆(或直径)所对的圆周角是直角,0 90的圆周角所对的弦是直径; 5.圆内接四边形对角互补。 (三)点与圆的位置关系 1、点和圆的位置关系 如果圆的半径为r,已知点到圆心的距离为d,则可用数量关系表示位置关系. (1)d>r点在圆外;(2)d=r点在圆上;(3)d<r点在圆内. 2、确定圆的条件:不在同一直线上的三个点确定一个圆. (四)直线与圆的位置关系 1、(1)直线与圆的位置关系有关概念 ①相交与割线:直线和圆有两个公共点时,叫做直线和圆相交,这条直线叫做圆的割线. ②切线与切点:直线和圆有惟一公共点时,叫做直线和圆相切,这条直线叫做圆的切线,惟一的公共点叫做切点. ③相离,当直线和圆没有公共点时,叫做直线和圆相离. (2)用数量关系判断直线与圆的位置关系 如果⊙O的半径为r,圆心O到直线l的距离为d,那么: (1)直线l和⊙O相交d<r(如图(1)所示); (2)直线l和⊙O相切d=r(如图(2)所示); (3)直线l和⊙O相离d>r(如图(3)所示). 2、切线 (1)切线的判定定理:经过半径的外端并且垂直于这条半径的直线是圆的切线. (2)切线的性质:圆的切线垂直于过切点的半径. (3)切线长:圆的切线上某一点与切点之间的线段的长叫做这点到圆的切线长. (4)切线长定理:从圆外一点可以引圆的两条切线,它们的切线长相等.这一点和圆心的连线平分这两条切线的夹角. (五)三角形的外接圆和内切圆 1、三角形的外接圆 (1)定义:经过三角形的三个顶点可以做一个圆,这个圆叫做三角形的外接圆.
乙烯 一.乙烯 1. 分一子、结乙构烯 1.分子结构 分子子式式: :C 2H C 4 2H 4 分子式: C 2H 4 H H H H 结构式: 结构式: H H C=C C=C H H 结构简式: 结构简式: CH 2=CH 2 CH 2=CH 2 或 H 2C=CH 2 或 H 2C = CH H H ..H ..H 电子式: H:C::C:H .... 电子式: H:C::C:H CH CH CH 2 2 CH 2 2 2 空间构型 : 平面结构 : 6个原子共平面, 键角 120° 乙烷与乙烯的比较 乙烷 乙烯 分子式 C 2H 6 C 2H 4 电子式 H H :H :H H:C:C:H :::: H:C::C:H H H -H -H H H 结构式 H-C-C-H - - - - H-C = C-H H H 结构简式 CH 3-CH 3 CH 2= CH 2
碳碳键型C- C单键C=C 双键键角109o28ˊ120°键长 (10-10m) 1.54 1.33键能 (kJ/mol)348615 C=C的键能小于 C-C 键键能的 2倍,为什么? ☆乙烯为平面结构,分子内的 2 个碳原子与 4 个氢原子位于同一平面上。☆C=C双键中有一个键不稳定,容易断裂,有一个键较稳定。☆C=C双键两边的碳原子为不饱和碳原子。 2.物理性质 乙烯是无色气体,稍有气味,密度是 1.25 g/L ,比空气略轻(相对分子质量为 28),难溶于水。 3.化学性质: ⑴ 氧化反应: ①乙烯与酸性 KMnO4溶液 现象:紫红色褪去 结论:此性质用于鉴别乙烯和甲烷,但一般不用于混和气体中除去乙烯,因为此反应中会产生 CO2气体。 学性质: 化反应: 烯与酸性KMnO 4溶液 紫:红色褪去 ②可燃性 (点燃前验纯) ② ②可燃性 ( 点燃前验纯 ) 现象:火焰明亮、伴有黑烟,放出大量热 现象:火焰明亮、伴有黑烟,放出大量热 :此性质用于鉴别乙烯和甲烷 C2H4+3O2点燃 2CO2+2H2O 乙烯含碳量(85.7 %) 比甲烷 (75% ) 高,燃烧时更不充分,故有黑烟 规律:含碳量越高,黑烟越浓。
物理知识点归纳总结 物理知识点归纳总结 1.磁性:物体吸引铁、镍、钴等物质的性质。 2.磁体:具有磁性的物体叫磁体。它有指向性:指南北。 3.磁极:磁体上磁性最强的部分叫磁极。 ①任何磁体都有两个磁极,一个是北极(N极);另一个是南极(S极) ②磁极间的作用:同名磁极互相排斥,异名磁极互相吸引。 4.磁化:使原来没有磁性的物体带上磁性的过程。 5.磁体周围存在着磁场,磁极间的相互作用就是通过磁场发生的。 6.磁场的基本性质:对入其中的磁体产生磁力的作用。 7.磁场的方向:在磁场中的某一点,小磁针静止时北极所指的方向就是该点的磁场方向。 8.磁感线:描述磁场的强弱和方向而假想的曲线。磁体周围的磁感线是从它北极出来,回到南极。(磁感线是不存在的,用虚线表示,且不相交) 9.磁场中某点的磁场方向、磁感线方向、小磁针静止时北极指的方向相同。 10.地磁的北极在地理位置的南极附近;而地磁的南极则在地理位置的北极附近。(地磁的南北极与地理的南北极并不重合,它们的交角称磁偏角,这是我国学者:沈括最早记述这一现象。) 11.奥斯特实验证明:通电导线周围存在磁场。
12.安培定则:用右手握螺线管,让四指弯向螺线管中电流方向,则大拇指所指的那端就是螺线管的北极(N极)。 13.安培定则的易记易用:入线见,手正握;入线不见,手反握。大拇指指的一端是北极(N极)。 14.通电螺线管的性质:①通过电流越大,磁性越强;②线圈匝数越多,磁性越强;③插入软铁芯,磁性大大增强;④通电螺线管 的极性可用电流方向来改变。 15.电磁铁:内部带有铁芯的螺线管就构成电磁铁。 16.电磁铁的特点:①磁性的有无可由电流的通断来控制;②磁性的强弱可由改变电流大小和线圈的匝数来调节;③磁极可由电流 方向来改变。 17.电磁继电器:实质上是一个利用电磁铁来控制的开关。它的作用可实现远距离操作,利用低电压、弱电流来控制高电压、强电流。还可实现自动控制。 18.电磁感应:闭合电路的一部分导体在磁场中做切割磁感线运动时,导体中就产生电流,这种现象叫电磁感应,产生的'电流叫感 应电流。 19.产生感生电流的条件:①电路必须闭合;②只是电路的一部 分导体在磁场中;③这部分导体做切割磁感线运动。 20.感应电流的方向:跟导体运动方向和磁感线方向有关。 21.电磁感应现象中是机械能转化为电能。 22.发电机的原理是根据电磁感应现象制成的。交流发电机主要 由定子和转子。 23.高压输电的原理:保持输出功率不变,提高输电电压,同时 减小电流,从而减小电能的损失。 24.磁场对电流的作用:通电导线在磁场中要受到磁力的作用。 是由电能转化为机械能。应用是制成电动机。
英语初二上册重点知识点讲解 Module 1 How to learn English 1.pair n. (相关的)两个人,一对,一双,一副 a pair of socks一双袜子 a pair of gloves一副手套two pairs of trousers两条裤子 e.g.A pair of teenage boys are watching a football game.两个青少年正在看足球赛。 2.correct (1)v. 改正,纠正 e.g.The teacher returned to her room to correct exercise books.老师回到房间去改练习本。 Correct the spelling.纠正拼写。 (2)adj.正确的;恰当的 e.g.correct pronunciation 正确发音 Do you have the correct time?你的表走得准吗? 3.advice (1)n.意思是“意见,建议”,为不可数名词,可用some,much,a piece of,pieces of等修饰,不能说an advice或many/a few advices。 (2)表示“有关……的建议”时,用介词on,接名词、代词或由疑问词引导的不定式。 advice on what to do next. 我们去征求一下他的意见下一步该怎么办。 e.g.Let’s ask for his 常见搭配: take/follow one’s advice接受某人的建议 ask for advice 征求意见 接受(拒绝)某人的建议 accept/refuse one’s advice offer advice to sb. 向某人提供建议 拓展: advise vt.建议 常见搭配:advise sb. to do sth.
5.1 圆 课程标准要求 1.理解圆的有关概念. 2.经历探索点与圆的位置关系的过程,会运用点到圆心的距离与圆的半径之间的数量关系判断点与圆的位置关系. 3.理解弧、弦、半圆、优弧、劣弧等与圆有关的概念, 1.圆概念(重点) 把线段OP的一个端点O固定,使线段OP绕着点O在平面内旋转1周(如图5 -1-1所示),另一个端点P运动所形成的图形叫做圆,其中,定点O叫做圆心,线段OP叫做半径,以点O为圆心的圆,记作“⊙O”,读作“圆0”.2.点与圆的位置(难点) 点与圆的位置关系有三种:点在圆内、点在圆上、点在圆外,设⊙0的半径为r,点P到圆心0的距离为d,用图形表示点与圆的位置关系如图5-1-2所示 3.与圆有关的概念 ①弦:连接圆上任意两点的线段叫做弦,如图5-1-3中的弦 AB,BC。 ②直径:经过圆心的弦叫做直径,如图5-1-3中的弦AB为⊙0的直径直径等于半径的两倍。 ③弧、优弧、劣弧:圆上任意两点间的部分叫做圆弧,简称弧,弧用符号“⌒”表示;圆的任意一条直径的两个端点分圆成两条弧,每条弧都叫做半圆;小于半圆的弧叫做劣弧,如图5 -1-3中以B、C为端点小于半圆的 劣弧“”;大于半圆的弧叫做优弧,优弧要用三个字母表示,如图5~1—3中的优弧“”. ④等圆、同心圆:能够互相重合的两个圆叫做等圆,如图5 -1-4中的⊙和⊙是等圆;圆心相同,半径不相等的两个圆叫做同心圆,如图5—1—5中的两圆, 5.2 圆的对称性
课程标准要求. 1.理解圆的对称性及有关性质. 2.理解同圆或等圆中,圆心角、弧、弦各组量之间的关系,并会应用. 3.探索垂径定理并会应用其解决有关问题. 1.圆是轴对称图形(重点) 通过折叠与旋转的方法,我们可以得到: 圆是轴对称图形,其对称轴为任意一条过圆心的直线; 圆是中心对称图形,其对称中心是圆心. 2.圆心角,弧,弦之间的关系(重点) 在同圆或等圆中,相等的圆心角所对的弧相等,所对的弦相等。 在同圆或等圆中,如果两个圆心角、两条弧、两条弦中有一组量相等,那么它们所对应的其余各组量都分别相等。 (1)在具体运用以上定理解决问题时,可根据需要选择,如“在等圆中,相等的弧所对的圆心角相等”. (2)不能忽略“在同圆或等圆中”这个前提条件,如果丢掉这个前提条件,即使圆心角相等,所对的弧、弦也不一定相等. (3)要结合图形深刻理解圆心角、孤、弦这三个概念和“所对应的”一词的含义,因为一条弦所对的弧有两条,所以由“弦等”得出“弧等”,这里的“弧等”指的是对应的劣弧和劣弧相等,对应的优弧和优弧相等。3.圆心角的度数与它所对的弧的度数的关系 (1)1°的弧:将顶点在圆心的周角等分成360份时,每一份的圆心角是1°的角.因为同圆中相等的圆心角所对的弧相等,所以整个圆也被等分成360份.我们把1°的圆心角所对的弧叫做1°的弧.(2)圆心角的度数与它所对的弧的度数的关系:圆心角的度数与它所对的弧的度数相等. 1.垂径定理的应用(难点) (1)垂径定理:垂直于弦的直径平分这条弦,并且平分弦所对的弧, 垂径定理的表现形式:如图5-2-8所示, 5.3 圆周角 课程标准要求 1.经历探索圆周角的有关性质的过程. 2.理解圆周角的概念及其相关性质,并能运用相关性质解决实际问题. 3.体会分类、转化等数学思想方法,学会用数学的思想方法思考问题. 1.识别圆周角 顶点在圆上,并且两边都和圆相交的角叫做圆周角. 2.圆周角定理的应用 定理:同弧或等弧所对的圆周角相等,都等于该弧所对的圆心角的一半。 3.圆周角定理的推论(难点) 直径(或半圆)所对的圆周角是直角90°的圆周角所对的弦是直径. 本文档部分内容来源于网络,如有内容侵权请告知删除,感谢您的配合!
专题复习16--甲烷乙烯苯知识点总结 核心知识图 1.烃的分类、通式和主要化学性质 氧化:燃烧 饱和烃:烷烃C n H2n+2(n≥1) 甲烷取代结构:链状、碳碳单键裂解 链烃氧化:燃烧、使KMnO4(H+)褪色 (脂肪烃) 烯烃C n H2n(n≥2) 乙烯加成:H2、X2、HX 、H2O等 结构:链状、碳碳双键加聚 氧化:燃烧、使KMnO4(H+)褪色 炔烃C n H2n-2(n≥2) 乙炔加成 不饱和烃结构:链状、碳碳叁键加聚 氧化:燃烧、使KMnO4(H+)褪色 烃二烯烃C n H2n-2 (n≥3) 1,3—丁二烯加成:1,2加成、1,4加成 结构:链状、两个碳碳双键加聚 饱和环烃:环烷烃C n H2n (n≥3) 结构:环状、碳碳单键氧化:燃烧、不能使KMnO4(H+)褪色,不能因反应使反应使溴水褪色 苯加成 环烃取代:卤代、硝化、磺化 苯及其同系物C n H2n-6 (n≥6) 结构:环状、大 键 不饱和环烃:芳香烃氧化:燃烧、使KMnO4(H+)褪色 稠环芳烃:萘、蒽甲苯取代 加成 甲烷的化学性质 通常情况较稳定,与强酸、强碱、KMnO4等均不反应。 (1)氧化反应甲烷燃烧的热化学方程式为: (2)取代反应 ①定义:有机物分子里的某些被其他 所替代的反应。 ②甲烷与Cl2反应 乙烯烯烃知识点总结 一、乙烯的组成和结构 乙烯分子的结构简式:CH2〓 CH2 乙烯分子的结构: 键角约120°,分子中所有原子在同一平面,属平面四边形分子。 二、乙烯的制法 工业上所用的大量乙烯主要是从石油炼制厂和石油化工厂所生产的气体中分离出来的。
实验室制备原理及装置 三、乙烯的性质 1.物理性质:无色、稍有气味、难溶于水、密度小于空气的密度。 2.化学性质 (1)氧化反应 a.燃烧 CH 2=CH 2+3O 2??→?点燃 2CO 2+2H 2O (火焰明亮,并伴有黑烟) b.使酸性KMnO 4溶液褪色 (2)加成反应:有机物分子中双键(或叁键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。 (溴的四氯化碳溶液的红棕色褪去) 乙烯除了与溴之外还可以与H 2O 、H 2、卤化氢、Cl 2等在一定条件下发生加成反应,如工业制酒精的原理就是利用乙烯与H 2O 的加成反应而生成乙醇. 3)聚合反应 n CH 2==CH 2???→?催化剂[— CH 2—CH 2 ]— n ( 聚乙烯) 其中 CH 2=CH 2 为单体 —CH 2—CH 2— 为链节 n 为聚合度 四、乙烯的用途 作植物生长的调节剂,还可以作催熟剂;可用于制酒精、塑料、合成纤维、有机溶剂等, 五、烯烃 1.烯烃的概念:分子里含有碳碳双键的一类链烃 2.烯烃的通式:C n H 2n (n ≥2) 最简式:CH 2 可见,烯烃中碳和氢的质量分数别为85.7%和14.3%,恒定不变 环烷烃的通式与烯烃的通式相同,故通式为C n H 2n 的烃不一定是烯烃,如右图中其分子符合C n H 2n ,但不是烯烃而是环烷烃。 (环丁烷) 一般,我们所说的烯烃都是指分子中只含一个碳碳双键的不饱和烃,所以也叫单烯烃,也还有二烯烃:CH 2=CH - CH=CH 2 苯及其同系物知识点 苯 分子结构 分子式:C 6H 6 最简式:CH 结构式: 结构简式:或 比例模型: 球棍模型: 空间构型: 1、具有平面正六边形结构,所有原子共平面 2、键角都是120°。 3、不存在单双键交替排列,6个碳碳键完全相同,是一种介于单键和双键之间的独特的化学键。
六年级知识点归纳总结 第一单元分数乘法 1.分数乘整数的意义和整数乘法的意义相同,就是求几个相同加数的和的简便运算。2.分数乘整数的计算法则:分数乘整数,用分数的分子和整数相乘的积作分子,分母不变。 (为了计算简便,能约分的要先约分,然后再乘。) 注意:当带分数进行乘法计算时,要先把带分数化成假分数再进行计算。 3.一个数与分数相乘,可以看作是求这个数的几分之几是多少。 4.分数乘分数的计算法则:分数乘分数,用分子相乘的积作分子,分母相乘的积作分母。 5.整数乘法的交换律、结合律和分配律,对分数乘法同样适用。 乘法交换律: a × b = b × a 乘法结合律: ( a × b )×c = a × ( b × c ) 乘法分配律:( a + b )×c = a c + b c a c + b c = ( a + b )×c 6.乘积是1的两个数互为倒数。 7.求一个数(0除外)的倒数,只要把这个数的分子、分母调换位置。 1的倒数是1。0没有倒数。 真分数的倒数大于1;假分数的倒数小于或等于1;带分数的倒数小于1。 注意:倒数必须是成对的两个数,单独的一个数不能称做倒数。 8.一个数(0除外)乘以一个真分数,所得的积小于它本身。 9.一个数(0除外)乘以一个假分数,所得的积等于或大于它本身。 10.一个数(0除外)乘以一个带分数,所得的积大于它本身。 11.分数应用题一般解题步骤。 (1)找出含有分率的关键句。
(2)找出单位“1”的量(以后称为“标准量”)找单位“1”:在分率句中分率的前面;或“是”、“占”、“比”、“相当于”的后面 (3)画出线段图,标准量与比较量是整体与部分的关系画一条线段即可,标准量与比较量不是整体与部分的关系画两条线段即可。(4)根据线段图写出等量关系式:标准量×对应分率=比较量。求一个数的几倍:一个数×几倍; 求一个数的几分之几是多少:一个数×几 几 。 写数量关系式技巧: (1)“的”相当于“×”“占”、“是”、“比”相当于“ = ” (2)分率前是“的”:单位“1”的量×分率=分率对应量 (3)分率前是“多或少”的意思:单位“1”的量×(1 分率)=分率对应量(5)根据已知条件和问题列式解答。 12.乘法应用题有关注意概念。 (1)乘法应用题的解题思路:已知一个数,求这个数的几分之几是多少?单位“1”×对应分率=对应量 (2)找单位“1”的方法:从含有分数的关键句中找,注意“的”前“是、比、相当于、占、等于”后的规则。 (3)甲比乙多几分之几?计算方法是:(甲-乙)÷乙= 甲÷乙-1甲比乙少几分之几?计算方法是:(甲-乙)÷甲 = 1-乙÷甲 (4)“增加”、“提高”、“增产”等蕴含“多”的意思,“减少”、“下降”、“裁员” 等蕴含“少”的意思,“相当于”、“占”、“是”、“等于”意思相近。 (5)当关键句中的单位“1”不明显时,要把关键句补充完整,补充成“谁是谁的几分之几之几”或“甲比乙多几分之几”、“甲比乙少几分之几”的形式。(6)乘法应用题中,单位“1”是已知的。 (7)单位“1”不同的两个分率不能相加减,加减属相差比,始终遵循“凡是
第十一章三角形 一、知识框架: 二、知识概念: 1.三角形:由不在同一直线上的三条线段首尾顺次相接所组成的图形叫做三角形. 2.三边关系:三角形任意两边的和大于第三边,任意两边的差小于第三边. 3.高:从三角形的一个顶点向它的对边所在直线作垂线,顶点和垂足间的线段叫做三角形 的高. 4.中线:在三角形中,连接一个顶点和它对边中点的线段叫做三角形的中线. 5.角平分线:三角形的一个内角的平分线与这个角的对边相交,这个角的顶点和交点之间 的线段叫做三角形的角平分线. 6.三角形的稳定性:三角形的形状是固定的,三角形的这个性质叫三角形的稳定性. 7.多边形:在平面内,由一些线段首尾顺次相接组成的图形叫做多边形. 8.多边形的内角:多边形相邻两边组成的角叫做它的内角. 9.多边形的外角:多边形的一边与它的邻边的延长线组成的角叫做多边形的外角. 10.多边形的对角线:连接多边形不相邻的两个顶点的线段,叫做多边形的对 角线. 11.正多边形:在平面内,各个角都相等,各条边都相等的多边形叫正多边形. 12.平面镶嵌:用一些不重叠摆放的多边形把平面的一部分完全覆盖,叫做用 多边形覆盖平面, 13.公式与性质: ⑴三角形的内角和:三角形的内角和为180° ⑵三角形外角的性质: 性质1:三角形的一个外角等于和它不相邻的两个内角的和. 性质2:三角形的一个外角大于任何一个和它不相邻的内角. n-·180° ⑶多边形内角和公式:n边形的内角和等于(2) ⑷多边形的外角和:多边形的外角和为360°. n-条对角 ⑸多边形对角线的条数:①从n边形的一个顶点出发可以引(3)
线,把多边形分成(2)n -个三角形.②n 边形共有(3)2 n n -条对角线. 第十二章 全等三角形 一、知识框架: 二、知识概念: 1.基本定义: ⑴全等形:能够完全重合的两个图形叫做全等形. ⑵全等三角形:能够完全重合的两个三角形叫做全等三角形. ⑶对应顶点:全等三角形中互相重合的顶点叫做对应顶点. ⑷对应边:全等三角形中互相重合的边叫做对应边. ⑸对应角:全等三角形中互相重合的角叫做对应角. 2.基本性质: ⑴三角形的稳定性:三角形三边的长度确定了,这个三角形的形状、大小就全确定,这个性质叫做三角形的稳定性. ⑵全等三角形的性质:全等三角形的对应边相等,对应角相等. 3.全等三角形的判定定理: ⑴边边边(SSS ):三边对应相等的两个三角形全等. ⑵边角边(SAS ):两边和它们的夹角对应相等的两个三角形全等. ⑶角边角(ASA ):两角和它们的夹边对应相等的两个三角形全等. ⑷角角边(AAS ):两角和其中一个角的对边对应相等的两个三角形全等. ⑸斜边、直角边(HL ):斜边和一条直角边对应相等的两个直角三角形 全等. 4.角平分线: ⑴画法: ⑵性质定理:角平分线上的点到角的两边的距离相等. ⑶性质定理的逆定理:角的内部到角的两边距离相等的点在角的平分线上. 5.证明的基本方法: ⑴明确命题中的已知和求证.(包括隐含条件,如公共边、公共角、对顶 角、角平分线、中线、高、等腰三角形等所隐含的边角关系)
《圆》章节知识点 一、圆的概念 1.平面内到定点的距离等于定长的所有点组成的图形叫做圆。其中,定点称为圆心,定长称为半径,以点O为圆心的圆记作“O”,读作“圆O”。 2.确定圆的基本条件:(1)、圆心:定位置,具有唯一性,(2)、半径:定大小。 3.半径相等的两个圆叫做等圆,两个等圆能够完全重合。 4.①连接圆上任意两点的线段叫做弦,经过圆心的弦叫做直径,②圆上任意两点间的部分叫做圆弧,简称弧,弧用符号“?”表示,圆的任意一条直径的两个端点分圆成为两条等弧,每一条弧都叫做半圆,大于半圆的弧称为优弧,小于半圆的弧称为劣弧。③在同圆或等圆中,能过重合的两条弧叫做等弧。理解:弧在圆上,弦在圆及圆上:弧为曲线形,弦为直线形。 5.不在同一直线上的三个点确定一个圆且唯一一个。 6.①三角形的三个顶点确定一个圆,经过三角形各顶点的圆叫做三角形的外接圆,外接圆的圆心是三角形三边垂直平分线的交点,叫做三角形的外心,这个三角形叫做这个圆的内接三角形。②与三角形三边都相切的圆叫做这个三角形的内切圆,内切圆的圆心是三角形三条角平分线的交点,叫做三角形的内心。三角形的内切圆是三角形内面积最大的圆,圆心是三个角的角平分线的交点,他到三条边的距离相等:内心到三顶点的连线平分这三个角。 (补充)圆的集合概念 1、圆可以看作是到定点的距离等于定长的点的集合; 2、圆的外部:可以看作是到定点的距离大于定长的点的集合; 3、圆的内部:可以看作是到定点的距离小于定长的点的集合 轨迹形式的概念: 1、圆:到定点的距离等于定长的点的轨迹就是以定点为圆心,定长为半径的圆; 2、垂直平分线:到线段两端距离相等的点的轨迹是这条线段的垂直平分线(也叫 中垂线); 3、角的平分线:到角两边距离相等的点的轨迹是这个角的平分线; 4、到直线的距离相等的点的轨迹是:平行于这条直线且到这条直线的距离等于定 长的两条直线; 5、到两条平行线距离相等的点的轨迹是:平行于这两条平行线且到两条直线距离 都相等的一条直线。
圆的知识点归纳总结大全 一、圆的定义。 1、以定点为圆心,定长为半径的点组成的图形。 2、在同一平面内,到一个定点的距离都相等的点组成的图形。 二、圆的各元素。 1、半径:圆上一点与圆心的连线段。 2、直径:连接圆上两点有经过圆心的线段。 3、弦:连接圆上两点线段(直径也是弦)。 4、弧:圆上两点之间的曲线部分。半圆周也是弧。 (1)劣弧:小于半圆周的弧。 (2)优弧:大于半圆周的弧。 5、圆心角:以圆心为顶点,半径为角的边。 6、圆周角:顶点在圆周上,圆周角的两边是弦。 7、弦心距:圆心到弦的垂线段的长。 三、圆的基本性质。 1、圆的对称性。 (1)圆是轴对称图形,它的对称轴是直径所在的直线。 (2)圆是中心对称图形,它的对称中心是圆心。 (3)圆是旋转对称图形。 2、垂径定理。 (1)垂直于弦的直径平分这条弦,且平分这条弦所对的两条弧。 (2)推论: ?平分弦(非直径)的直径,垂直于弦且平分弦所对的两条弧。 ?平分弧的直径,垂直平分弧所对的弦。 3、圆心角的度数等于它所对弧的度数。圆周角的度数等于它所对弧度数的一半。
(1)同弧所对的圆周角相等。 (2)直径所对的圆周角是直角;圆周角为直角,它所对的弦是直径。 4、在同圆或等圆中,两条弦、两条弧、两个圆周角、两个圆心角、两条弦心距 五对量中只要有一对量相等,其余四对量也分别相等。 5、夹在平行线间的两条弧相等。 6、设⊙O 的半径为r ,OP=d 。 7、(1)过两点的圆的圆心一定在两点间连线段的中垂线上。 (2)不在同一直线上的三点确定一个圆,圆心是三边中垂线的交点,它到三 个点的距离相等。 (直角三角形的外心就是斜边的中点。) 8、直线与圆的位置关系。d 表示圆心到直线的距离,r 表示圆的半径。 直线与圆有两个交点,直线与圆相交;直线与圆只有一个交点,直线与圆相切; 直线与圆没有交点,直线与圆相离。 2 9、平面直角坐标系中,A (x 1,y 1)、B (x 2,y 2)。 则AB=221221)()(y y x x -+- 10、圆的切线判定。 (1)d=r 时,直线是圆的切线。 d = r 直线与圆相切。 d < r (r > d 直线与圆相交。 d > r (r 八年级上册英语外研版各模块知识点归纳总结 Module 1 How to learn English advice take/follow one’s advice接受某人的建议ask for advice 征求意见accept/refuse one’s advice接受(拒绝)某人的建议 offer advice to sb. 向某人提供建议 try to (1)try to do sth .努力做某事try doing sth.试着做某事 try/do one’s best to do sth. 尽某人的全力做某事 5.as…as possible/one can time at a time一次,每一次at one time曾经,一度 at times /from time to time 有时,偶尔on time 准时 all the time 总是,一直in time及时,迟早 ①It’s time for sb. to do sth./It’s (high) time sb. did sth. Suggest (2)形容词比较级用法 ①表示两者进行比较时用形容词比较级,最明显的提示词是than,其结构为“A…+比较级+than+B”。 ②有表示程度的副词a little,a bit,a few,a lot,much,even,still,far,rather,any等修饰时,用形容词比较级。 ③比较级前面可以加上表示具体数量差别的结构,表示具体“大多少”,“小多少”,“长多少”,“短多少”等。 ④表示“两者之间最……一个(of the two)”时,常用“the+比较级”结构。 ⑤表示“越来越……”,用比较级重叠结构,即“比较级+and+比较级”,多音节词和部分双音节词时用“more and more+形容词原级”。 ⑥表示“越……就越……”时,用“the+比较级,the+比较级”结构。 Module 4 Planes, ships and trains 形容词最高比较级用法 ①表示三者或三者以上的人或物进行比较时,用最高级形式。形容词最高级前必须加定冠词the,句末常跟一个in/of短语来表示范围。(of表示同范围,in 表示不同范围) 圆与方程知识点总结-标准化文件发布号:(9556-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII 圆梦教育中心 圆与方程知识点总结 1. 圆的标准方程:以点),(b a C 为圆心,r 为半径的圆的标准方程是222)()(r b y a x =-+-. 特例:圆心在坐标原点,半径为r 的圆的方程是:222r y x =+. 2. 点与圆的位置关系: (1). 设点到圆心的距离为d ,圆半径为r : a.点在圆内 d <r ; b.点在圆上 d=r ; c.点在圆外 d >r (2). 给定点),(00y x M 及圆222)()(:r b y a x C =-+-. ①M 在圆C 内22020)()(r b y a x <-+-? ②M 在圆C 上22020)()r b y a x =-+-? ( ③M 在圆C 外22020)()(r b y a x >-+-? (3)涉及最值: ① 圆外一点B ,圆上一动点P ,讨论PB 的最值 min PB BN BC r ==- max PB BM BC r ==+ ② 圆内一点A ,圆上一动点P ,讨论PA 的最值 min PA AN r AC ==- max PA AM r AC ==+ 思考:过此A 点作最短的弦( 此弦垂直AC ) 3. 圆的一般方程:022=++++F Ey Dx y x . (1) 当0422>-+F E D 时,方程表示一个圆,其中圆心??? ??--2,2E D C ,半径2 422F E D r -+=. (2) 当0422=-+F E D 时,方程表示一个点??? ??--2,2 E D . (3) 当0422<-+ F E D 时,方程不表示任何图形. 第一章、裂解炉单元 1 裂解炉出口温度对裂解反应有什么影响 对于一个已定型的裂解炉,其出口温度反映了它的裂解深度,故裂解炉出口温度能影响裂解产物的分布和炉子结焦情况。一般地乙烯、丙烯的收率随炉出口温度升高而增加,达到最大值后,温度再升高,则收率呈下降趋势。丁二烯的收率随炉出口温度变化不明显,甲烷、氢、重质燃料油的收率一般也随温度的升高而增大。 2 乙烷裂解炉为什么要加硫 乙烷裂解炉的原料来自乙烯精馏塔塔釜,它不含硫及硫化物,而SRT裂解炉炉管是由Gr、Ni合金构成,如在物料中加入硫化剂,它可与Gr、Ni形成一种保护膜,防止炉管渗碳后脆裂。同时,加入硫化剂,还可以减少裂气中CO的含量,降低甲烷化反应器的负荷 3 裂解炉烟道气中氧含量过高有什么危害 1.烟气中氧含量高,CO 在对流段容易发生二次燃烧,损坏炉管 2.氧含量高,进入炉子的风量就大,对流段温度升高,影响对流段炉管寿命,同时使排 烟温工升高,降低了炉子的热效率 3.由于氧含量高,炉管表面易氧化,缩短了炉管寿命 4 裂解炉进料量超过设计值有什么影响 若进料量提高,超过设计值,炉出口温度仍然不变,必然会增加炉子的热负荷,炉管温度也会相应提高,增大了结焦趋势,同时炉管耐温极限的限制,影响炉管寿命,因此,进料量不能超过设计值太多。 5管式裂解炉有什么优点 主要优点有: 结构简单,工艺成熟,技术可靠,便于操作,运转稳定性好,烯烃收率高。 6裂解炉节能的主要途径有哪些 1.保持最优的空气过剩系数 2.最低限度地降低排烟温度 3.减少炉壁散热损失 4.提高裂解炉运转周期 7裂解原料中砷和铅有什么危害 裂解原料中砷和铅的含量过高,会加速炉管的结焦,且能污染产品,并可使碳二、碳三加氢催化剂中毒。此外,铅、砷还可与炉管形成低共熔物,损坏炉管。 8 蒸汽-空气在线清焦有何优点 1.裂解炉没有升、降温过程,延长了炉管的寿命 2.由于在线清焦只需几十个小时,提高了开工率 3.老装置只需做不大的改动,就可实现不停炉清焦。 9裂解炉横跨温度的设计依据是什么 不同的裂解原料其横跨温度不同,其依据为某原料的起始裂解温度,最高温度不超过某 第一章 有理数 考点一、实数的概念及分类 (3分) 1、实数的分类 正有理数 有理数 零 有限小数和无限循环小数 实数 负有理数 正无理数 无理数 无限不循环小数 负无理数 2、无理数:32,7, 3 π +8,sin60o 。 第二章 整式的加减 考点一、整式的有关概念 (3分) 1、单项式 只含有数字与字母的积的代数式叫做单项式。 注意:单项式是由系数、字母、字母的指数构成的,其中系数不能用带分数表示,如b a 2 3 14-,这种表示就是错误的,应写成b a 2 3 13- 。一个单项式中,所有字母的指数的和叫做这个单项式的次数。如c b a 235-是6次单项式。 考点二、多项式 (11分) 1、多项式 几个单项式的和叫做多项式。其中每个单项式叫做这个多项式的项。多项式中不含字母的项叫做常数项。多项式中次数最高的项的次数,叫做这个多项式的次数。 2、同类项 所有字母相同,并且相同字母的指数也分别相同的项叫做同类项。几个常数项也是同类项。 第三章 一元一次方程 考点一、一元一次方程的概念 (6分) 1、一元一次方程 只含有一个未知数,并且未知数的最高次数是1的整式方程叫做一元一次方程,其中方程 )为未知数,(0a x 0≠=+b ax 叫做一元一次方程的标准形式,a 是未知数x 的系数,b 是常数项。 第四章 图形的初步认识 考点一、直线、射线和线段 (3分) 1、点和直线的位置关系有线面两种: ①点在直线上,或者说直线经过这个点。 ②点在直线外,或者说直线不经过这个点。 2、线段的性质 (1)线段公理:所有连接两点的线中,线段最短。也可简单说成:两点之间线段最短。 (2)连接两点的线段的长度,叫做这两点的距离。 (3)线段的中点到两端点的距离相等。 乙烯_烯烃知识点汇总(全) -标准化文件发布号:(9556-EUATWK-MWUB-WUNN-INNUL-DDQTY-KII 乙烯 烯烃知识点总结 一、乙烯的组成和结构 乙烯分子的结构简式:CH 2 〓 CH 2 乙烯分子的结构: 键角约120°,分子中所有原子在同一平面,属平面四边形分子。 二、乙烯的制法 工业上所用的大量乙烯主要是从石油炼制厂和石油化工厂所生产的气体中分离出来的。 实验室制备原理及装置 ① 浓H 2SO 4的作用:催化剂、脱水剂。 ② 浓硫酸与无水乙醇的体积比:3∶1。配制该混合液时,应先加5 mL 酒精,再将15 mL 浓硫酸缓缓地加入,并不断搅拌。 ③ 由于反应温度较高,被加热的又是两种液体,所以加热时容易产生暴沸而造成危险,可以在反应混合液中加一些碎瓷片加以防止。(防暴沸) ④ 点燃酒精灯,使温度迅速升至170℃左右,是因为在该温度下副反应少,产物较纯。 ⑤ 用排水法收集满之后先将导气管从水槽里取出,再熄酒精灯,停止加热。 〖讨论〗此反应中的副反应,以及NaOH 溶液的作用 ①乙醇与浓硫酸混合液加热会出现炭化现象,使生成的乙烯中含有CO 2、SO 2等杂质。SO 2也能使高锰酸钾酸性溶液和溴的四氯化碳溶液褪色,因此,检验乙烯气体之前,应该使气体先通过NaOH 溶液,除去CO 2和SO 2。 ②乙醇与浓硫酸共热到140℃,乙醇发生分子间脱水,生成乙醚(C 2H 5-O-C 2H 5) 三、乙烯的性质 1.物理性质:无色、稍有气味、难溶于水、密度小于空气的密度。 2.化学性质 (1)氧化反应 a.燃烧 CH 2=CH 2+3O 2??→?点燃 2CO 2+2H 2O (火焰明亮,并伴有黑烟) b.使酸性KMnO 4溶液褪色 (2)加成反应:有机物分子中双键(或叁键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。八年级上册英语外研版各模块知识点归纳总结
圆与方程知识点总结
乙烯装置基础知识
初中数学知识点归纳总结(精华版)
乙烯_烯烃知识点汇总(全)