
一次性使用无菌导尿包
适用范围:该产品适用于医院导尿治疗过程的一次性使用。
1.1产品规格及其划分说明
一次性使用无菌导尿包由:一次性使用无菌导尿管(普通型)、一次性使用无菌导尿管(超滑型)、一次性使用集尿袋、尿培养试管、垫单、检查手套、塑料镊子、注水器包(一次性使用无菌注射器不带针头带塑料帽)、碘伏棉球包、润滑剂包、纱布块、大托盘、中托盘、小托盘、卡子、别针组件。
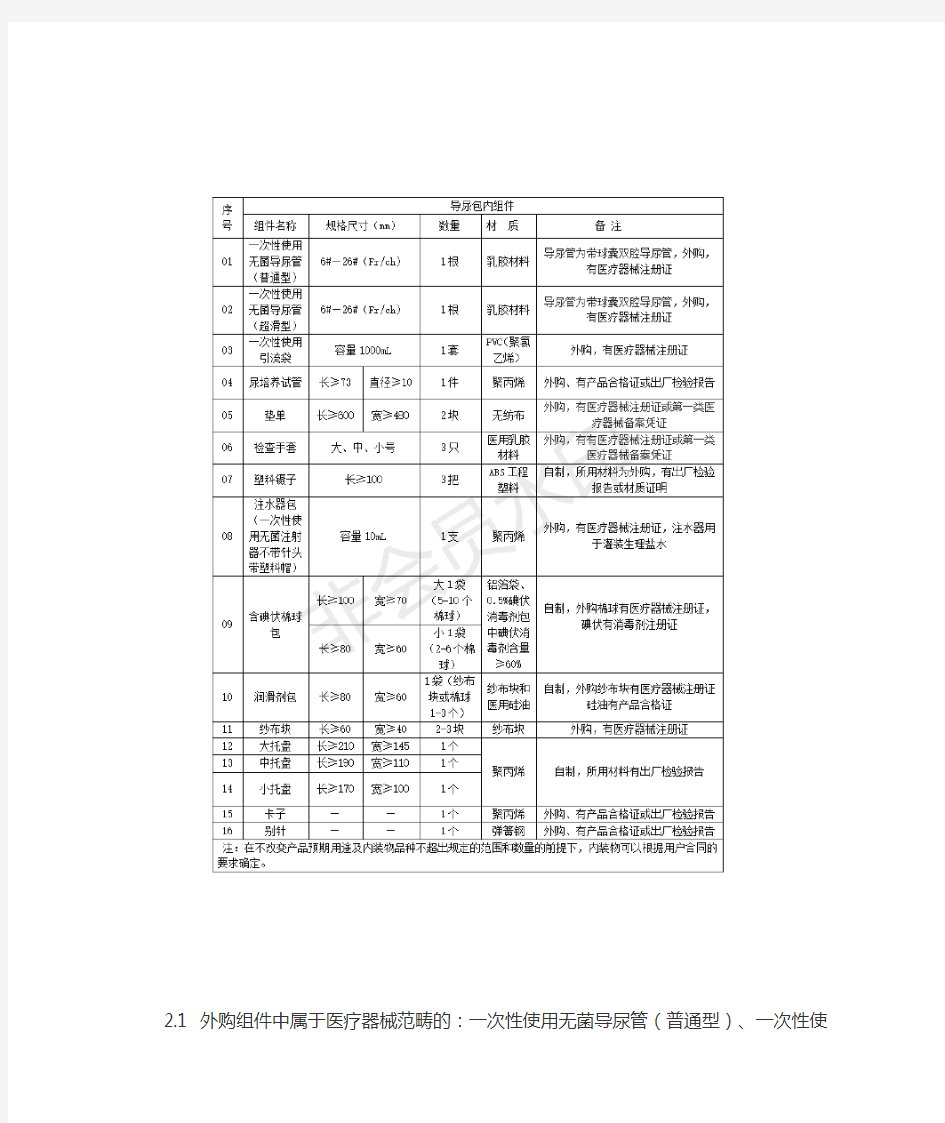
1.2 导尿包组件规格尺寸及数量见表。
表1导尿包组件规格
2.1 外购组件中属于医疗器械范畴的:一次性使用无菌导尿管(普通型)、一次性使用无菌导尿管(超滑型)、一次性使用引流袋、垫单、检查手套、注水器包(一次性使用无菌注射器不带针头带塑料帽)、纱布块,应有供方提供的医疗器械产品注册证或第一类医疗器械备案凭证。
2.2 外购组件中不属于医疗器械范畴的:尿培养试管、卡子、别针,应有供方提供的合格证。
2.3 自制组件的规格尺寸及数量应符合表1中的要求。
2.4 导尿包表1中的塑料镊子、碘伏棉球包、润滑剂包、大托盘、中托盘、小托盘等组件均属自制。其中所用材料棉球、纱布块需要外购,应有供方提供的医疗器械产品注册证或第一类医疗器械备案凭证;所用材料ABS工程塑料、碘伏、硅油、聚丙烯也需要外购,应有供方提供的产品合格证或出厂检验报告。碘伏的出厂报告应符合中国药典的规定。
2.5 导尿包表1中的塑料镊子头端部位应恢复性能良好,自然状态开口尺寸≥10mm。
2.6 外观
2.6.1导尿包内外包装应无破损,包内应清洁无杂质。润滑剂袋不得渗漏。
2.6.2一次性使用无菌导尿管表面应平整、光滑、头端和孔口应无毛刺。
2.6.3导尿包内塑料组件外表面应光滑、圆整,不得有变形、裂纹、锋棱、麻点、砂眼等缺陷。
2.6.4垫单外观不应有破损、污沁、应无落屑、附着物等缺陷。
2.7注水器包(一次性使用无菌注射器不带针头带塑料帽)、润滑剂包,经钴六零灭菌后,应无菌。
2.8 导尿包采用双层密封包装,经环氧乙烷灭菌后应无菌。
2.9 产品出厂时,环氧乙烷残留量≤10μg /g。
一次性使用无菌手术包技术指导原则 辽宁省食品药品监督管理局技术审评中心
目次 一、适用范围 (1) 二、内容与要求 (1) (一)产品名称 (1) (二)产品的结构和组成 (1) (三)产品应适用的相关标准 (1) (四)产品的主要风险 (3) (五)产品的主要技术性能指标 (4) (六)产品的检测要求 (6) (七)产品的临床要求 (7) (八)该类产品的不良事件历史记录 (7) (九)产品说明书、标签和包装标识 (8) (十)注册单元划分的原则 (8) (十一)审查关注点 (9)
前言 根据《医疗器械注册管理办法》(国家食品药品监督管理局令第16号)的要求并结合一次性无菌手术包产品的特点,制定本技术审查指导原则。 本指导原则用于指导和规范一次性使用无菌手术包产品注册申报过程中审查人员对注册材料的技术审评。 本指导原则适用于以非织造布及医用脱脂纱布为主要原料加工制成的一次性使用无菌手术包(以下简称手术包),该产品用于临床手术中使用。 本指导原则由辽宁省食品药品监督管理局技术审评中心提出。 本指导原则起草单位:辽宁省食品药品监督管理局技术审评中心。 本指导原则主要起草人:迟戈、李非。
一次性使用无菌手术包 技术指导原则 一、适用范围 本指导原则适用于以非织造布及医用脱脂纱布为主要原料加工制成的一次性使用无菌手术包(以下简称手术包),该产品用于临床手术中使用。 二、内容与要求 (一)产品名称 产品的名称应统一以“一次性使用无菌手术包”命名。(二)产品的结构和组成 1.产品的结构和组成 手术包一般由手术衣、帽子、口罩、洞巾、大单、中单、台布、方巾、床垫、手套、脱脂纱布等组成,可由用户订货合同要求,企业可另行确定手术包中的物品种类和数量,如增加换药碗、镊子等。 2.产品的规格尺寸 由企业根据市场需要制定合适的规格尺寸。 (三)产品应适用的相关标准 产品适用及引用标准的审查可以分为两步来进行。首先对引用标准的齐全性和适宜性进行审查,也就是在编写注册产品标准
附件4: 一次性使用无菌导尿管产品注册技术审查指导原则 本指导原则旨在指导和觃范一次性使用无菌导尿管产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。 本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新迚展,考虑产品的更新和变化。 本指导原则不作为法觃强制执行,不包括行政审批要求。但是,审评人员需密切关注相关法觃的变化,以确认申报产品是否符合法觃要求。 一、适用范围 本指导原则的适用范围为《医疗器械分类目录》中第二类一次性使用无菌导尿管产品,类代号现为6866。 二、技术审查要点 (一)产品名称的要求 一次性使用无菌导尿管产品的命名应采用《医疗器械分类目录》或国家标准、行业标准上的通用名称,或以产品结构和应用范围为依据命名。产品名称中可带有表示材质或管腔数等描述性词语,例如“硅橡胶”、“三腔”等。
(二)产品的结构和组成 产品所用材料有天然乳胶、硅橡胶和PVC(聚氯乙烯)等。典型产品外形结构见图1(三腔导尿管)。 图1 典型有球囊三腔导尿管 (三)产品的工作原理 本产品工作原理与作用机理基本相同,在作用机理中描述。 (四)产品的作用机理 一次性使用无菌导尿管利用膀胱的压力使尿液通过导尿管排出体外,双腔和三腔导尿管的球囊在注入水后可以膨起,在留置导尿时用于固定导尿管。三腔导尿管还可用于膀胱的冲洗。 使用时首先润滑导尿管管身部分,将润滑后的导管小心揑到膀胱(此时有尿液排出)然后再揑入一定距离,使球囊完全迚入膀胱。握住阀门外套,用不带针头的注射器揑入阀门内,注入额定的无菌水,使膨胀了的球囊卡住膀胱。握住阀门的外套,缓慢的拔出注射器,此时橡胶阀门自动密封,保持球囊膨胀。取出导管时,用不带针头的空注射器揑入阀门内,抽吸球囊内的无菌水,
医疗器械产品技术要求编号: 一次性使用PVC导尿管 1. 产品型号/规格及其划分说明 规格型号 一次性使用超滑导尿管按外径尺寸规格分为6FR、8FR、10FR、12FR、14FR、16FR、18FR、20FR、22FR、24FR、26FR、28FR、30FR,共13种规格。 划分说明 一次性使用PVC导尿管示意图 一次性使用PVC导尿管尺寸规格采用国内外最常见的法国规格表示,这是以导管的周长表示的规格系列。导管周长=πD≈3D,法国规格除以3即为导管外径(mm)。 2. 性能指标 物理指标 外观 当用正常视力或矫正视力在倍放大条件下检验时,管身、尖部、球囊和孔眼应无外来物质。 尺寸 一次性使用PVC导尿管的公称外径应精确到,公差为±,全长和有效长度应符合YY0325-2002中表1的要求。 强度 按YY 0325—2002 附录A 所给方法试验时,尖部和锥形接口应与管身连为
一体,管身应无断裂。 耐弯曲性能 按附录A的规定对管身进行耐弯曲性能试验时,试验段长度为150mm,管身不得出现打折现象。 流量 按YY 0325—2002 附录E 所给方法试验时,应符合YY0325-2002中表2的规定。 化学指标 环氧乙烷残留量 一次性使用超滑导尿管若经环氧乙烷灭菌,其环氧乙烷残留量≤10μg/g。生物指标 无菌 应一经确认的灭菌过程使一次性使用超滑导尿管无菌 3. 检验方法 按附录B检验判定依据表进行检验判定,以下检验项目应符合要求 物理指标 3.1.1外观 以目力观察,应符合2.1.1的要求。 3.1.2 尺寸 以通用量具测量应符合的2.1.2要求。 强度 按YY 0325—2002中附录A 所给方法试验,应符合要求。 耐弯曲性能 按附录A的规定方法对管身进行耐弯曲性能试验,应符合要求。 流量 按YY 0325—2002 中附录E 所给方法试验,应符合要求。 化学指标 环氧乙烷残留量试验 按GB/T 中9章的规定进行,结果应符合的要求。
食药监械监〔2016〕37号附件 一次性使用无菌注射器等25种医疗器械生产环节风险清单和检查要点
目录 一、一次性使用无菌注射器生产环节风险清单和检查要点 (1) 二、一次性使用输液器生产环节风险清单和检查要点 (7) 三、一次性使用静脉留置针生产环节风险清单和检查要点 (13) 四、一次性使用真空采血系统-采血管生产环节风险清单和检查要点(1) (17) 一次性使用真空采血系统-静脉采血针生产环节风险清单和检查要点(2) (20) 五、骨接合植入物(金属接骨板、金属接骨螺钉)生产环节风险清单和检查要点 (23) 六、脊柱内固定金属植入物生产环节风险清单和检查要点 (27) 七、人工关节风险清单和检查要点 (31) 八、人工晶状体生产环节风险清单和检查要点 (36) 九、血管支架生产环节风险清单和检查要点 (38) 十、乳房植入体生产环节风险清单和检查要点 (40) 十一、医用透明质酸钠凝胶(鸡冠提取法)生产环节风险清单和检查要点 (43) 十二、同种异体骨植入物生产环节风险清单和检查要点 (46) 十三、天然胶乳橡胶避孕套生产环节风险清单和检查要点 (52) 十四、血液净化用设备生产环节风险清单和检查要点 (57) 十五、血液净化用器具(接触血液的管路)生产环节风险清单和检查要点 (59) 十六、血液净化用器具(过滤/透析/吸附器械)生产环节风险清单和检查要点 (63) 十七、透析粉、透析浓缩液生产环节风险清单和检查要点 (66) 十八、中心静脉导管生产环节风险清单和检查要点 (69) 十九、封堵器系统产品生产环节风险清单和检查要点 (73) 二十、角膜接触镜生产环节风险清单和检查要点 (76) 二十一、麻醉系统生产环节风险清单和检查要点 (80) 二十二、医用防护服生产环节风险清单及检查要点 (83) 二十三、医用防护口罩生产环节风险清单及检查要点 (89) 二十四、一次性使用非电驱动式输注泵生产环节风险清单和检查要点 (94)
护理技术操作考核评分标准目录 第一项一般洗手操作考核评分标准 (1) 第二项无菌技术操作考核评分标准 (2) 第三项生命体征监测技术操作考核评分标准 (3) 第四项口腔护理技术操作考核评分标准 (4) 第五项鼻饲技术操作考核评分标准 (5) 第六项女病人导尿技术操作考核评分标准 (6) 第七项胃肠减压技术操作考核评分标准 (7) 第八项大量不保留灌肠技术操作考核评分标准 (8) 第九项鼻塞(鼻导管)吸氧技术操作考核评分标准 (9) 第十项换药技术操作考核评分标准 (10) 第十一项雾化吸入技术操作考核评分标准 (11) 第十二项血糖监测技术操作考核评分标准 (12) 第十三项口服给药技术操作考核评分标准 (13) 第十四项密闭式输液技术操作评分标准 (14) 第十五项密闭式静脉输血技术操作考核评分标准 (15) 第十六项静脉留置针技术考核评分标准 (16) 第十七项静脉采集血标本技术操作考核评分标准 (17) 第十八项静脉注射技术操作考核评分标准 (18) 第十九项经外周插管的中心静脉导管(PICC)护理技术操作考核评分标准 19 第二十项动脉血标本的采集技术操作考核评分标准 (20) 第二十一项肌内注射技术操作考核评分标准 (21) 第二十二项皮内注射技术操作考核评分标准 (22) 第二十三项皮下注射技术操作考核评分标准 (23) 第二十四项酒精拭浴降温技术操作考核评分标准 (24) 第二十五项心肺复苏技术操作考核评分标准 (25) 第二十六项经鼻/口腔吸痰法技术操作考核评分标准 (26) 第二十七项气管切开(呼吸机)病人吸痰技术操作考核评分标准 (27) 第二十八项心电监测技术操作考核评分标准 (28) 第二十九项血氧饱和度监测技术操作考核评分标准 (29) 第三十项输液泵/微量输注泵的使用技术考核评分标准 (30) 第三十一项除颤技术操作考核评分标准 (31)
附件13 一次性使用无菌手术包类产品注册技术审查指导原则 本指导原则旨在指导和规范一次性使用无菌手术包类产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。 本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变 化。 本指导原则不作为法规强制执行,不包括行政审批要求。但 是,审评人员需密切关注相关法规的变化,以确认申报产品是否 符合法规要求。 一、适用范围 本指导原则适用于根据临床需求,将医疗器械产品包装在一起的一次性使用无菌器械包类产品(以下简称手术包)。 本指导原则不适用于含有山类医疗器械产品的手术包。 二、技术审查要点 (一)产品名称的要求 产品的名称应以体现产品组成、功能用途为基本原则。手术包是根据临床需求将不同的医疗器械产品组成医疗器械包,包内的组件可以由不同生产制造商提供,并且组件名称也不同,但组
成手术包后就只能有一个产品名称,一般应以其主要预期用途来命名,如:用于外科手术的包就称作手术包,用于产科手术的包 就称为产包,用于导尿的包就称作导尿包。 手术包类产品均为一次性使用,产品名称中应加入“一次性使用”字样,是无菌级别的应加入“无菌”字样,如“一次性使用无菌手术包”、“一次性使用无菌产包”。 (二)产品的结构和组成 手术包组成(一般以组件形式体现)应满足以下条件: 第一,组件不应含有药物(如酒精、灌洗创口用生理盐水等)C 手术包组件管理类别最高为二类。 第二,组件可以是外购具有医疗器械注册证的产品,如外购 的外科手术口罩、手套等。作为手术包的组件其预期用途不应改变,应与审批通过的预期用途一致。 第三,组件可以是尚未注册的医疗器械产品。作为手术包的组件时其安全有效性要求应与单独注册该组件基本一致,如导尿包中的导尿管,应符合单独注册导尿管的技术审评要求。 第四,手术包必须包含在其申报的生产地址所生产的二类组 件,如手术包企业生产的手术衣等。 常见的手术包组件有:手术衣、帽子、口罩、洞巾、大单、 中单、小单、手套、脱脂纱布等。 依据临床用途的不同,不同注册单元的手术包配置也不同,
精心整理 男病人导尿技术操作标准 2015年12月修订
应掌握的知识点:
一()、目的:、收集患者尿标本做细菌培养。 、为尿潴留病人引流尿液,减轻痛苦。 、用于患者术前膀胱减压以及下腹、盆腔器官手术中持续排空膀胱,避免术中误伤。 、患者尿道损伤早期或者手术后作为支架引流,经导尿管对膀胱进行药物灌注治疗。、检查膀胱功能,测膀胱容量、压力及残余尿量。 、鉴别尿闭和尿潴留,以明确肾功能不全或排尿机能障碍。 、诊断及治疗膀胱和尿道的疾病,如进行膀胱造影或对膀胱肿瘤病人进行化疗等。、患者昏迷、尿失禁或者会阴部有损伤时,留置导尿管以保持会阴清洁干燥,避免尿液刺激。、抢救休克或者危重患者,准确记录尿量、比重,为病情变化提供依据。 (二)、指导要点:、操作前告知患者导尿的目的和意义。 、指导患者放松,在插管过程中协调配合,避免污染。、指导患者在留置尿管期间保证充足入量,预防发生感染和结石。 、指导患者在留置尿管期间防止尿管打折,弯曲,受压,脱出等情况发生,保持通畅。、指导患者保持尿袋高度低于耻骨联合水平,防止逆行感染。 、指导长期留置尿管的患者进行膀胱功能训练及骨盆底肌的锻炼,以增强控制排尿的能力。(三)、注意事项: 、严格执行无菌技术及消毒制度,防止医源性感染。导尿管一经污染或拔出均不得再使用。、在操作中注意保护患者隐私,并采取适当的措施防止着凉。 、初步消毒顺序为阴阜、阴茎、阴囊,然后暴露尿道口,旋转擦拭尿道口、龟头、冠状沟。、插管时将阴茎提起,使之与腹壁成60°角,可以使耻骨前弯消失,利于尿管插入。 、插管长度约20-22cm,见尿后再插。、男性尿道较长,又有三个狭窄、两个弯曲,插管时略有阻力,应嘱患者深呼吸,切忌用力过快过猛。、为男性患者插尿管时,遇有阻力,特别时经尿道内口、膜部、尿道外口三个狭窄部、耻骨前弯和耻骨下弯时,嘱患者深呼吸,慢慢插入尿管。、插入、拔出导尿管时,动作要轻、慢、稳、切勿用力过重,以免损伤尿道粘膜。、对膀胱高度膨胀且又极度虚弱的病人,第一次导尿量不可超过1000ml,以防大量放尿,导致腹腔内压突然降低,大量血液滞留于腹腔血管内,造成血压下降,产生虚脱,亦可因膀胱突然减压,导致膀胱粘膜急剧充血,引起血尿。 0、患者尿管拔除后,观察患者排尿时的异常症状。 (四)、留置尿管的操作要点及注意事项:、保持尿道口清洁,每日会阴护理1—2 次。 、定时更换尿袋,及时排空尿袋内尿液,并记录尿量。、每周更换导尿管一次,硅胶尿管可酌情延长更换日期。 、鼓励患者多饮水,保证充足入量,预防发生感染和结石,达到自然冲洗尿道的目的。 精心整理 、训练膀胱反射功能,定时夹闭尿管,3~4h开放1 次,使膀胱定时充盈和排空,促进膀胱功能恢复。、注意患者主诉,观察尿液情况,发现尿液混浊,沉淀,有结晶时,及时处理。长期留置
男病人留置导尿术操作评分标准 科室:姓名:得分: 项目总分考核内容标分扣分 准备(20分)1.仪表端庄,服装整洁。 2.了解病情、膀胱充盈度、会阴皮肤黏膜情况。 3.了解患者自理、合作程度、耐受力及心理反应。 4.向患者解释导尿目的、方法及指导配合,语言文明,态度和蔼。 5.无长指甲,洗手,戴口罩。 6.备齐用物(治疗车、屏风、无菌导尿包,一次性垫单、快速手消毒 剂、医疗垃圾筒等)、并按顺序放置。 2 3 3 3 3 6 操作步骤(70分)1.备齐用物携至病人床旁,核对病人信息后向病人解释。操作前要关 闭门窗,用屏风遮挡注意保护病人隐私。 2.病人取屈膝仰卧位,两腿自然分开,暴露外阴,脱左侧裤腿盖右侧, 盖被遮挡上身及左下肢,减少暴露,于病人臀下垫一次性垫单。 3.无菌方法打开初步消毒包,弯盘放于病人两腿之间,操作者左手戴 无菌手套。右手持血管钳夹取消毒棉球消毒外阴。方法如下: 1)阴阜:横向由远及近由上至下3次。 2)阴茎背部:近根部→阴茎远端。 3)阴茎腹侧:(左手持纱布提起阴茎)阴茎远端→近根部→阴囊。 4)后推包皮暴露尿道口,自尿道口、龟头、冠状沟螺旋消毒3次。 5)每个棉球只用一次,消毒完毕脱去手套。 4.打开导尿包,戴无菌手套,铺孔巾,检查导尿管及引流袋是否完好, 用无菌石蜡油润滑导尿管18-20厘米放入弯盘里备用(不需留标本 可先连接引流袋),暴露尿道口,再次消毒。左手持纱布提起阴茎, 暴露尿道口,螺旋消毒尿道口至龟头至冠状沟3次。 5.将放置导尿管的弯盘移至近会阴处,提起阴茎使之与腹壁约成60度 角,一手持血管钳将导尿管轻轻插入尿道18-20厘米,见尿后再插入 5-7厘米,血管钳夹住导尿管末端,气囊注生理盐水10-15毫升,轻轻 牵拉导尿管遇阻力即可。根据需要留取尿标本,接引流袋,并妥善 固定于床边,观察尿液量、颜色、性质。 6.操作完毕后移去用物,脱手套,协助病人穿好裤子,整理床单位, 将标本及时送检。告知病人留置尿管的注意事项。 7.整理用物,洗手、记录。 5 4 5 15 15 20 3 3 注意事项(10分)1.严格遵守无菌操作,防止感染。 2.操作须轻巧,避免损伤尿道或增加病人痛苦。 3.导尿管前端插入部分应涂抹足润滑剂。 4.导尿管管径大小适当,不宜过粗。男性成年人以F14-18号为宜。 5.若膀胱高度膨胀,病员又极度虚弱时,第一次放尿不应超过1000ml, 此时应缓慢而分次地放出尿液,反复多次,逐渐将膀胱放空。 10 考核日期:考核者:
水凝胶涂层乳胶导尿包 组成:1.导尿包的组成部件:水凝胶涂层乳胶导尿管、引流袋或集尿袋、注水器、无菌水、纱布、碘伏棉球、孔巾、无粉检查手套、铺巾、塑料镊子、导管夹、塑料试管、腰盘、外消毒组件(纱布、塑料镊子、碘伏棉球、无粉检查手套)。 2.导尿包内部件结构 1) 导尿包内注水器与无菌水组合一起时,注水器部件内装有规定容量的无菌水,包装袋采用铝箔或镀金属包装材料。 2) 导尿包内配无菌水独立部件时,无菌水部件内装注射用水,包装袋采用铝箔或镀金属包装材料。空的注水器不进行独立包装。 3) 碘伏棉球部件内装入规定数量的碘伏棉球,包装袋采用镀金属包装材料。 4) 在不改变导尿包产品预期用途及内装品种不超过规定范围的前提下,可以根据用户要求增加或减少导尿包内组成部件。 预期用途:供临床常规导尿用,三腔导尿管还可用于膀胱的冲洗。 1.1材质及导尿管组成 1.1.1导尿管基管材质:导尿管基管材质为天然乳胶,阀材质为聚丙烯。 1.1.2导尿管涂层:水凝胶,涂层主要成分为聚乙二醇、卵磷脂、异丙醇、纯化水。 1.1.3儿童用导尿管所配导丝(如有)材质为聚酰胺。 1.1.4冲洗腔塞子(如有,简称三腔塞子)材质为聚丙烯(PP)、聚乙烯(PE)、聚氯乙烯(PVC)。 1.1.5导尿管组成: 双腔球囊导尿管主要由管身、尖部、球囊、侧孔、排泄锥形接口、充起锥形接口、阀组成; 三腔球囊导尿管主要由管身、尖部、球囊、侧孔、排泄锥形接口、充起锥形接口、阀、冲洗锥形接口组成; 儿童用导尿管(8Fr、10Fr)配有导丝,三腔球囊导尿管配有冲洗腔塞子(三腔塞子)。 1.2产品型号规格 1.2.1产品型号:
1)双腔球囊、三腔球囊 2)儿童用、成人用 1.2.2产品规格: 导尿管规格分为:8Fr、10Fr、12Fr、14Fr、16Fr、18Fr、20Fr、22Fr、24Fr 导尿管最小全长:儿童用220 mm,成人用360 mm。 最小管身长度:儿童用150 mm,成人用275 mm。详情见表1。 球囊容积应以毫升(mL)表示。导尿管的示意图见图1 图1导尿管示意图 1.排泄锥形接口;2—充起锥形接口;3—阀;4—冲洗锥形接口;5—尖部;6—侧孔; 7—球囊;8—管身;L—全长;S—最小管身长度 表1导尿管型号规格信息表
一次性使用无菌溶药注射器带针 产品技术报告 一、产品简介 1.概述 1.1 一次性使用无菌溶药注射器(以下简称溶药注射器)及一次性使用无菌溶药针(以下简称溶药针)的结构、各部件名称如图1所示。本产品的所有部件及加工材料均采用符合医用要求的材料。 1.2 溶药注射器各部分的名称术语如图1所示 1-零刻度线;2-分度容量线;3-公称容量刻度线;4-总刻度容量线; 5-基准线;6-外套卷边; 7-锥头孔;8-锥头;9-针座;10-连结部;11-针管; 12-护套;13-外套;14-活塞; 15-芯杆;16-按手 注:本示意图仅说明溶药注射器的结构,并非为标准规定的唯一型式。 图1 溶药注射器(带溶药针)示例 1.3 主要材料 聚丙烯、橡胶活塞、不锈钢管 2. 结构组成 产品的所有部件及加工材料均采用符合医用要求的材料,其结构组成如图1(示例)构成 3. 预期用途 主要用于供临床配制药液、加药、溶药以及抽取药液时使用。 4.工作原理 溶药注射器的工作原理与普通注射器相同,是利用活塞和针筒的抽吸和注射原理,依靠手工进行配制药液工作。 5.产品特点 溶药注射器具有使用方便、安全等优点,已被广泛地应用到临床当中,产品经环氧乙烷灭菌,为一次性使用无菌产品。 二、技术指标或主要性能要求确定的依据 GB6682—1992 分析实验室用水规格和试验方法 GB15810—2019 一次性使用无菌注射器 GB15811—2019 一次性使用无菌注射针 GB/T1962.1—2019 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头第1部分通用要求GB/T1962.2—2019 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头第2部分锁定接头GB/T2828.1—2019 计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划 GB/T2829—2019 周期检验计数抽样程序及表C适用于对过程稳定性的检验 GB/T14233.1—2019 医用输液输血注射器具检验方法第1部分:评价与试验 GB/T14233.2—2019 医用输液输血注射器具检验方法第2部分:生物试验方法 GB/T18457—2019 制造医疗器械用不锈钢针管
一次性使用无菌注射器1 ml技术规格 1公称容量:1 ml 2外观 2.1 注射器不得有毛边、毛刺、塑流、缺损等缺陷。 2.2 注射器的内表面(包括橡胶活塞),不得有明显可见的润滑剂汇聚。 3注射器的标尺 3.1 最大残留容量:0.05 ml 3.2 计量数字间的最大增量:0.1 ml 4标尺的刻度容量线 4.1 分度值表明刻度容量线。 4.2 零位线的印刷位置应与外套封底的内边缘线相切,当芯杆完全推入外套封底端时零位线应与活塞上的基准线重合,其误差必须在最小分度间隔的四分之一范围以内。 5标尺上的计量数字 5.1 将注射器垂直握住,锥头向上,计量数字应成正立字形。 5.2 计量数字的排列顺序,应从外套封底端的零位线开始,“零”字可以省略。 6标尺的印刷 6.1 中头式注射器:其标尺应印在外套卷边短轴的任意一侧。 6.2 标尺的分度容量线及计量数字印刷应完整,字迹清楚,线条清晰,粗细均匀。 7外套 7.1 注射器外套的最大可用容量的长度至少比公称容量长度长10%。 7.2 注射器外套的开口处应有卷边,以确保注射器任意放置在与水平成10°夹角的平面上时不得转过180°。 8按手间距: 当芯杆完全推入到外套封底时,使活塞的基准线与零位线重合, 从卷边内表面到按手外表面的优选最小长度为8 mm。 9活塞 9.1 橡胶活塞应无胶丝、胶屑、外来杂质、喷霜,应符合YY/T 0243的规定,其他材料制成的活塞应符合相应标准的规定。 9.2 活塞与外套的配合,当注射器被注入水后,保持垂直时,芯杆不得因其自身重量而移动。 10锥头
10.1 锥头孔直径应不小于1.2mm。 10.2中头式注射器,锥头应位于外套封底端的中央,与外套在同一轴线上。11物理性能 11.1 滑动性能:良好。 11.2 器身密合性:将注射器吸入公称容量的水,用规定的轴向压力及侧向力,对芯杆作用30s,外套与活塞接触的部位不得有漏液现象。 11.3 残留容量:当芯杆完全推入到外套封底时,其残留在外套内的液体体积不得超过0.07 ml。 12生物性能3] 12.1 注射器应无菌。 12.2 注射器应无致热原。 13配用针: 0.45、0.50号针头或0.6号针头,带针头帽。针头固定于外套。注射针的针尖应锋利。 14单包装: 单包装上至少应有下列标志: 14.1 内装物的说明, 包括公称容量; 14.2 无菌”、“无热原”字样; 14.3 “一次性使用”或相当字样; 14.4 如果需要,提供对溶剂不相容性的警告; 14.5 批号以“批”字开头; 14.6 制造厂或供应商的名称和地址; 14.7 失效日期的年和月; 14.8 免费及湖北免费规划标识; 14.9 在使用前检查每一单包装完整性的警示; 14.10 有利于环保。 15中包装: 中包装上应有下列标志: 15.1 内装物的说明, 包括公称容量和数量; 15.2 “无菌”字样; 15.3 “一次性使用”或相当字样; 15.4 批号以“批”字开头; 15.5 失效日期的年和月; 15.6 制造厂或供应商的名称和地址; 15.7 免费及湖北免费规划标识; 16大包装: 大包装上应有下列标志:
医疗器械产品技术要求编号: 一次性使用PVC导尿管 1、产品型号/规格及其划分说明 1、1 规格型号 1、1、1一次性使用超滑导尿管按外径尺寸规格分为6FR、8FR、10FR、12FR、14FR、16FR、18FR、20FR、22FR、24FR、26FR、28FR、30FR,共13种规格。 1、2 划分说明 1、2、1 一次性使用PVC导尿管示意图 1、2、2一次性使用PVC导尿管尺寸规格采用国内外最常见的法国规格表示,这就是以导管的周长表示的规格系列。导管周长=πD≈3D,法国规格除以3即为导管外径(mm)。 2、性能指标 2、1 物理指标 2、1、1 外观 当用正常视力或矫正视力在2、5倍放大条件下检验时,管身、尖部、球囊与孔眼应无外来物质。 2、1、2 尺寸 一次性使用PVC导尿管的公称外径应精确到0、1mm,公差为±0、33mm,全长与有效长度应符合YY0325-2002中表1的要求。 2、1、3 强度 按YY 0325—2002 附录A 所给方法试验时,尖部与锥形接口应与管身连为一体,管身应无断裂。 2、1、4耐弯曲性能
按附录A的规定对管身进行耐弯曲性能试验时,试验段长度为150mm,管身不得出现打折现象。 2、1、5 流量 按YY 0325—2002 附录E 所给方法试验时,应符合YY0325-2002中表2的规定。 2、2 化学指标 2、2、1 环氧乙烷残留量 一次性使用超滑导尿管若经环氧乙烷灭菌,其环氧乙烷残留量≤10μg/g。 2、3 生物指标 2、3、1 无菌 应一经确认的灭菌过程使一次性使用超滑导尿管无菌 3、检验方法 按附录B检验判定依据表进行检验判定,以下检验项目应符合要求 3、1 物理指标 3、1、1外观 以目力观察,应符合2、1、1的要求。 3、1、2 尺寸 以通用量具测量应符合的2、1、2要求。 3、1、3 强度 按YY 0325—2002中附录A 所给方法试验,应符合2、1、3要求。 3、1、4耐弯曲性能 按附录A的规定方法对管身进行耐弯曲性能试验,应符合2、1、4要求。 3、1、5 流量 按YY 0325—2002 中附录E 所给方法试验,应符合2、1、5要求。 3、2 化学指标 3、2、1环氧乙烷残留量试验 按GB/T 14233、1-2008中9章的规定进行,结果应符合2、2、1的要求。 3、3 生物指标
一、产品简介 1.概述 1.1 一次性使用无菌溶药注射器(以下简称溶药注射器)及一次性使用无菌溶药针(以下简称溶药针)的结构、各部件名称如图1所示。本产品的所有部件及加工材料均采用符合医用要求的材料。 1.2 溶药注射器各部分的名称术语如图1所示 1-零刻度线;2-分度容量线;3-公称容量刻度线;4-总刻度容量线; 5-基准线;6-外套卷边;7-锥头孔;8-锥头;9-针座;10-连结部;11-针管; 12-护套;13-外套;14-活塞;15-芯杆;16-按手 注:本示意图仅说明溶药注射器的结构,并非为标准规定的唯一型式。 图1 溶药注射器(带溶药针)示例 1.3 主要材料 聚丙烯、橡胶活塞、不锈钢管 2. 结构组成 产品的所有部件及加工材料均采用符合医用要求的材料,其结构组成如图1(示例)构成3. 预期用途 主要用于供临床配制药液、加药、溶药以及抽取药液时使用。 4.工作原理 溶药注射器的工作原理与普通注射器相同,是利用活塞和针筒的抽吸和注射原理,依靠手工进行配制药液工作。 5.产品特点 溶药注射器具有使用方便、安全等优点,已被广泛地应用到临床当中,产品经环氧乙烷灭菌,为一次性使用无菌产品。 二、技术指标或主要性能要求确定的依据 GB6682—1992 分析实验室用水规格和试验方法 GB15810—2001 一次性使用无菌注射器 GB15811—2001 一次性使用无菌注射针 GB/T1962.1—2001 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头第1部分通用要求GB/T1962.2—2001 注射器、注射针及其他医疗器械6%(鲁尔)圆锥接头第2部分锁定接头GB/T2828.1—2003 计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划 GB/T2829—2002 周期检验计数抽样程序及表C适用于对过程稳定性的检验 GB/T14233.1—1998 医用输液输血注射器具检验方法第1部分:评价与试验 GB/T14233.2—2005 医用输液输血注射器具检验方法第2部分:生物试验方法 GB/T18457—2001 制造医疗器械用不锈钢针管 GB 9969.1-1998 工业产品使用说明书总则 GB/T16886.1-2001 医用器械生物学评价第1部分:评价与试验 YY 0242—1996 医疗输液输血注射器用聚丙烯专用料 YY/T0243—2003 一次性使用无菌注射器用活塞 YY/T0296—1997 一次性使用注射针识别色标 YY/T0313—1998 医用高分子制品包装、标志、运输和贮存 YY0466-2003 医疗器械用于医疗器械标签、标记和提供信息的符号 三、产品设计控制、开发、研制过程
技术操作考核评分标准 操作者姓名科室总分 操作名称留置导尿技术 总 分 实得分 操作项目操作内容 标 准 分 扣原 分因 得分 一、操作 目的1.采集患者尿标本做细菌培养。 2.为尿潴留患者引流尿液,减轻痛苦。 3.用于患者术前膀胱减压以及下腹、盆腔器官手术中持续排空膀胱,避免术 中误伤。 4.患者尿道损伤早期或手术后作为支架引流,经导尿管对膀胱进行药物灌注 治疗。 5.患者昏迷、尿失禁或会阴部有损伤时,留置尿管以保持局部干燥、清洁, 避免尿液的刺激。 6.抢救休克或危重患者,准确记录尿量、比重,为病情变化提供依据。 7.为患者测定膀胱容量、压力及残余尿量,向膀胱注入造影剂或气体等以协 助诊断。 5 二、评估 患者1.询问患者身体状况:①病情、意识状态、生命体征、合作程度;②生活自理能力;③膀胱充盈度及会阴部皮肤粘膜情况。 2.向患者解释导尿的目的、方法、注意事项和配合要点。 3.了解患者膀胱充盈度及局部皮肤情况。 三、实施 要点操作要点:65 1、仪表:淡妆上岗、端庄大方、衣帽整洁。 2 2、操作用物: 治疗盘、一次性导尿包(治疗碗2个、镊子2把、0.5%碘棉球2袋、石蜡油 1袋、手套2双、气囊导尿管1根、洞巾1块、20毫升一次性注射器内盛灭 菌水10毫升、纱布、尿袋、无菌标本瓶、弯盘)、无菌持物钳、剪刀、一次 性中单、弯盘、便盆、浴巾、必要时屏风 5 3、操作步骤: 1)核对医嘱,准备用物。 2 2)核对患者床号、姓名、住院号、评估患者,根据患者自理能力嘱其清洁 外阴。 10 3)洗手,戴口罩。检查导尿包有效期,有无漏气、破损、潮湿。 2 4)携用物至病人床旁,再次核对、解释。关闭门窗,屏风遮挡。 2 5)松开床尾盖被,协助病人脱去对侧裤腿盖在近侧腿上,并盖上浴巾,用 盖被遮盖对侧腿。 2 6)协助患者取屈膝仰卧位,双腿略外展,露出外阴。 2 7)将一次性中单垫于臀下,弯盘置于会阴处,再次检查导尿包。 2 8)打开导尿包外层,取出治疗碗放于患者两腿之间,初步还原无菌包。 2 9)左手戴手套,将活力碘棉球倒入治疗碗内,右手持镊夹取棉球消毒阴阜、 对侧大阴唇、近侧大阴唇、对侧大小阴唇之间、近侧大小阴唇之间。 3 10)左手拇、食指分开大阴唇,消毒对侧小阴唇、近侧小阴唇、尿道口至肛 门。消毒完毕,脱下手套置弯盘内,将治疗碗、弯盘一并移至床尾。开导尿 包,将无菌导尿包上半幅垫于臀下。 3
一次性使用无菌导尿管产品注册技术审查指导原则 本指导原则旨在指导和规范一次性使用无菌导尿管产品的技术审评工作,帮助审评人员理解和掌握该类产品原理/机理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。 本指导原则所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。 本指导原则不作为法规强制执行,不包括行政审批要求。但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。 一、适用范围 本指导原则的适用范围为《医疗器械分类目录》中第二类一次性使用无菌导尿管产品,类代号现为6866。 二、技术审查要点 (一)产品名称的要求 一次性使用无菌导尿管产品的命名应采用《医疗器械分类目录》或国家标准、行业标准上的通用名称,或以产品结构和应用范围为依据命名。产品名称中可带有表示材质或管腔数等描述性词语,例如“硅橡胶”、“三腔”等。 (二)产品的结构和组成
产品所用材料有天然乳胶、硅橡胶和PVC(聚氯乙烯)等。典型产品外形结构见图1(三腔导尿管)。 图1 典型有球囊三腔导尿管 (三)产品的工作原理 本产品工作原理与作用机理基本相同,在作用机理中描述。 (四)产品的作用机理 一次性使用无菌导尿管利用膀胱的压力使尿液通过导尿管排出体外,双腔和三腔导尿管的球囊在注入水后可以膨起,在留置导尿时用于固定导尿管。三腔导尿管还可用于膀胱的冲洗。 使用时首先润滑导尿管管身部分,将润滑后的导管小心插到膀胱(此时有尿液排出)然后再插入一定距离,使球囊完全进入膀胱。握住阀门外套,用不带针头的注射器插入阀门内,注入额定的无菌水,使膨胀了的球囊卡住膀胱。握住阀门的外套,缓慢的拔出注射器,此时橡胶阀门自动密封,保持球囊膨胀。取出导管时,用不带针头的空注射器插入阀门内,抽吸球囊内的无菌水,当注射器中水的容量与注入时的容量接近时即可缓慢的拔出导
男病人导尿技术操作标准 2015年12月修订 项目操作流程操作标准 分 值 扣分细则 分 数 仪 表 2分 报告 姓名 语言流畅 2 分 1.紧张,不自然, 语言不流畅 2.着装不符合医院 要求 - 1 - 1操作 项目 举止符合要求 操 作 前1 2 分 双人 查对 确认医嘱无误,打印治疗单并再次核 对:患者床号、姓名、留置尿管医嘱 3 分 3.未正确核对 4.未了解患者情况 - 2 - 1 个人 准备 七步洗手法洗手 戴口罩 4 分 5.未洗手 6.洗手方法有误 7.未戴口罩 8.戴口罩方法有误 - 1 - 1 - 1 - 1检查 物品质量 检查一次性使用物品的名称、有效期 2 分 9.未检查 - 2 物品 准备 ①治疗车上层备:速干手消毒液、尿 管标识、医嘱执行单、笔、一次性使用无 菌导尿包、一次性治疗巾、大浴巾、弯盘、 薄膜手套、必要时备无菌手套一副 ②治疗车下层备:便盆、便盆巾 必要时备屏风 3 分 10.用物准备不全 11.用物放置不合 理 - 1 - 2 操作中 携用 物至床旁 评估 一般情况 核对床号、姓名、腕带、治疗单,评 估患者的意识状态(清醒、嗜睡、昏迷) 及自理能力,了解患者目前排尿情况询问 患者是否接受过类似治疗、是否存在前列 腺增生,请其放松配合,再通过触诊或叩 诊评价患者膀胱充盈度,观察外阴部皮肤 卫生情况,指导或协助患者清洗外阴,向 患者解释并告知患者操作中配合方法。请 家属离开病房(异性导尿留一位陪床家 属),并谢谢配合 1 0分 12.核对不全面 13.评估不全面 14.未评估膀胱充 盈情况 15.未观察外阴部 皮肤情况 - 2 - 2 - 1 - 2 - 1
一次性使用无菌导尿包 适用范围:本品适用于临床导尿。1.1产品型号/规格: A型(内装乳胶双腔导尿管),含规格:6Fr、8Fr、10Fr、12Fr、14Fr、16Fr、18Fr、20Fr、22Fr、24Fr。 B型(内装硅胶双腔导尿管),含规格:6Fr、8Fr、10Fr、12Fr、14Fr、16Fr、18Fr、20Fr、22Fr、24Fr。 C型(内装乳胶双腔超滑导尿管),含规格:6Fr、8Fr、10Fr、12Fr、14Fr、16Fr、18Fr、20Fr、22Fr、24Fr。 D型(内装 PVC单腔导尿管),含规格:6Fr、8Fr、10Fr、12Fr、14Fr、16Fr、18Fr、20Fr、22Fr、24Fr。 E型(内装乳胶三腔导尿管),含规格16Fr、18Fr、20Fr、22Fr、24Fr。 F型(内装硅胶三腔导尿管),含规格:16Fr、18Fr、20Fr、22Fr、24Fr。 1.2产品型号/规格划分说明: 根据导尿管材质、结构差异划分型号。 根据导尿管外周长尺寸差异划分规格。 2.1导尿包 a) 导尿包产品应符合本《技术要求》,并按规定程序所批准的图样及文件 制造。 b) 导尿包经环氧乙烷灭或辐照灭菌,应无菌。 c) 导尿包环氧乙烷残留量应小于10μg/g。 d) 导尿包外观应无破损。 e) 产品包装标识应清晰。 2.2外购件 2.2.1一次性医用包布(治疗巾或无纺布辅料替代)、一次性医用洞巾、引流袋、注水器(注射器替代)、导尿管、检查手套、医用脱脂纱布块、棉球 属II类医疗器械产品,采购时应有供方提供的有效《医疗器械注册证书》,规格、材料应符合附录A。
2.2.2卡子、注射器帽、试管、双面胶、别针 属非医疗器械产品,采购时应有供方提供的《出厂检验合格证》,规格、材料应符合附录A。 a)卡子、注射器帽表面应无飞刺及制造缺陷,卡死及放开灵活可靠,用于6#-24#导尿管均能起到止水作用。 b)双面胶宽10±0.3mm,1800剥离强度≥6.5F/(N/25mm)。 2.2.3 托盘、腰盘 属食品容器,采购时应有供方提供的有效《全国工业产品生产许可证》并包含“食品用塑料包装容器制品”内容,规格、材料应符合附录A。 2.2.4 医用镊 a) 医用镊由聚苯乙烯材料注塑加工而成,其结构形式和基本尺寸应在医用 镊的设计图中做出规定,医用镊的结构形式分为I型(见图1)和II型(见图2)。I型是两片连接结构,II型是整体注塑结构,基本尺寸见表1 医用镊基本尺寸。 b) 医用镊应对称,外表应光滑、不得有锋棱、毛刺、裂纹、麻点。 c) 医用镊应有良好的弹性,按YY/T 0295.1 -2005 附录A检验其变形量应 ≤1.6mm。 d) 医用镊如采用两片结构,按YY/T 0295.1 -2005 附录C检验两片连接应 牢固。 e) 医用镊的唇头齿应清晰完整,不应有缺齿,烂齿的缺陷。 f) 医用镊全部闭合时,唇头齿自头端向下至少在其全长三分之二的长度内 应吻合,不张口。 g) 医用镊的导向应牢固,当医用镊开闭时,应灵活,不应有卡塞现象。 h) 医用镊的柄花应清晰完整,不应有缺花、烂花。 医用镊的捏合力为2-4N。
女病人导尿术操作及评分标准 科室:姓名:得分: 项目内容分值评分标准扣分扣分理由 目的1. 取尿液作细菌培养,观察尿量、比重、残余尿以 助诊断。 2. 尿潴留病人放出尿液,以解除痛苦。 3. 盆腔术前排空膀胱,避免手术中误伤。 4. 昏迷、手术、尿失禁或会阴部有损伤时保留导尿 管,以保持局部清洁干燥。 5. 抢救休克和危重病人,正确记录尿量、尿比重, 以观察肾功能。 5 少一点 1 用物治疗车、治疗盘、一次性导尿包、挂钩、棉垫、免洗 手消毒液、毛毯 6 少一件-1 评估1.询问、了解患者的身体状况、心理状况。 2.向患者解释导尿的目的、注意事项,取得患者的 配合。 3.了解患者膀胱充盈度情况。 5 缺一项 -2 操作步骤1.操作前剪指甲、洗手、戴口罩。仪表符合要求。 4 少一件-1 2.备齐用物(检查一次性导尿包的型号、有效期、密 闭性)。推车至床尾,核对床号、姓名;向病人解释, 关门窗、围屏风,注意保护病人的隐私。 8 未解释 未遮挡 未检查 -2 -3 -3 3.将挂钩挂于床沿上。 1 -1 4. 松被尾,将病人的右手放在胸腹部,上衣上拉, 脱下左腿裤盖在病人右腿上,左腿用棉被遮盖,右腿 用毛毯保暖,病人取仰卧位,两腿屈膝自然分开,充 分暴露外阴,注意保暖。 4 位置不适 未保暖 -2 -2 5. 病人臀下垫一次性尿布垫。 1 未备-1 6.打开导尿包,取第一次消毒盘,倒出碘伏棉球,左 手戴手套,开始消毒,其原则从上至下,从远至近, 从外至内消毒,每一个棉球只用一次。消毒毕后,脱 去手套,移去用物,置于治疗车底下。 8 未戴手套 消毒污染 用物处置有 误 -2 -3 -3 7. 在病人两腿之间打开导尿包内包布,戴无菌手套, 铺洞巾,倒碘伏棉球、镊子置于小弯盘中。检查引流 袋、气囊导尿管、试气、气囊有无漏气,将导尿管与 一次性引流袋连接、关紧引流袋下口、用镊子润滑导 尿管前端5-6cm,妥善置于弯盘内。 10 污染 未检查 未试气 未润滑 -4 -3 -2 -1 8. 小弯盘移至病人会阴处: 女病人:术者左手食指、中指分开小阴唇向上提并固 定、右手持镊子夹取棉球消毒尿道口、小阴唇、尿道 口后,右手移去用物。 10 未固定 消毒不全 -3 -7
一次性使用超滑抗菌导尿包 适用范围:该产品用于不能自主排尿患者的临时导尿或留置导尿,也可以用于泌尿外科手术时的压迫止血和膀胱冲洗。 1.1一次性使用超滑抗菌导尿包的基本配置见表1 表1 导尿包基本配置 1.2按导尿管腔数分为三种型号;按管径不同又分多种规格;球囊容积分为3ml、5ml、30ml。
符合本标准要求的导尿包的产品标记为: 2.1配件要求 2.1.1塑料镊子 2.1.1.1塑料镊子应对称,外表应光滑、不得有锋棱、毛刺、裂纹、麻点、 砂眼。 2.1.1.2塑料镊子的唇头齿应清晰完整,不应有缺齿,烂齿的缺陷。 2.1.1.3塑料镊子的导向销、定位销固定应牢固,当镊子开闭时,应灵活, 不应有卡塞现象。 2.1.2导管夹在使用过程中能起到使液体通断的性能。 2.1.3塑料试管应清洁干燥,能盛液体并且不漏。 2.1.4 腰盘应清洁干燥。 2.2导尿管物理性能 2.2.1外观 导尿管要求外形应整齐美观,表面清洁光滑、不得有伤斑、裂纹等缺陷并具有一定的柔性。供使用状态下的导尿管,管身、尖部、球囊和孔眼应无外来物质。
2.2.2尺寸 导尿管的外径、最小全长(L)和最小管身(S)应按表2的规定。 表2导尿管规格
2.2.3强度 导尿管的尖部和排泄锥形接口应与管身连为一体,管身应无断裂。 2.2.4连接器分离力 导尿管的排泄锥形接口应不与试验连接器分离。 2.2.5球囊 2.2.5.1球囊容积 球囊容积应按表2的规定。 2.2.5.2球囊可靠性 2.2.5.2.1球囊应无泄露,并且不应影响排泄孔。未充起球囊,其两端外 形应与管身平滑地连为一体,在其周围环境温度下,球囊充入水至规定的容积后,应呈现基本对称地鼓起。 2.2.5.2.2球囊和充起腔用水充满后,在重力作用下放出球囊中的水,水 的回收率应不低于表3的规定。