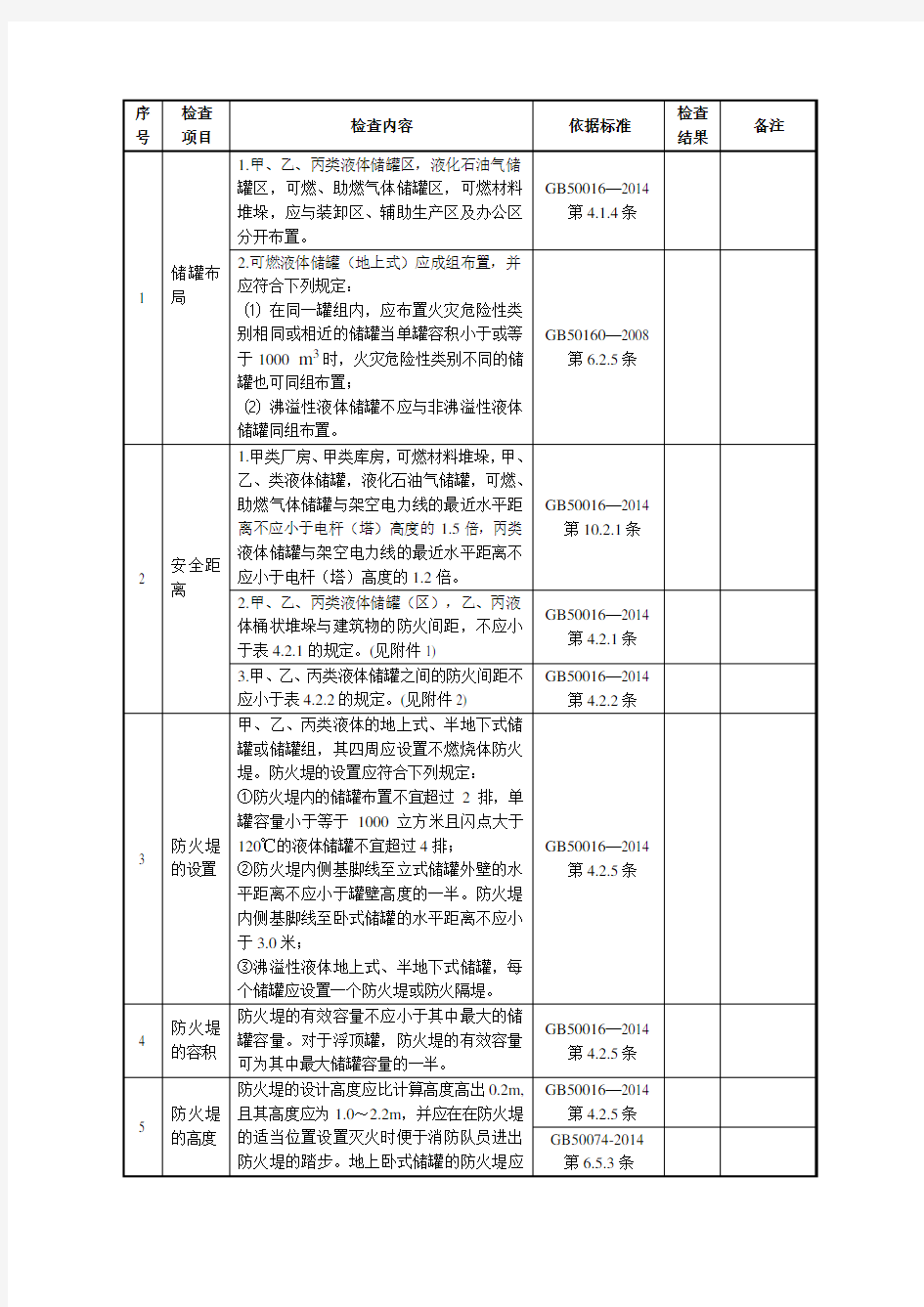
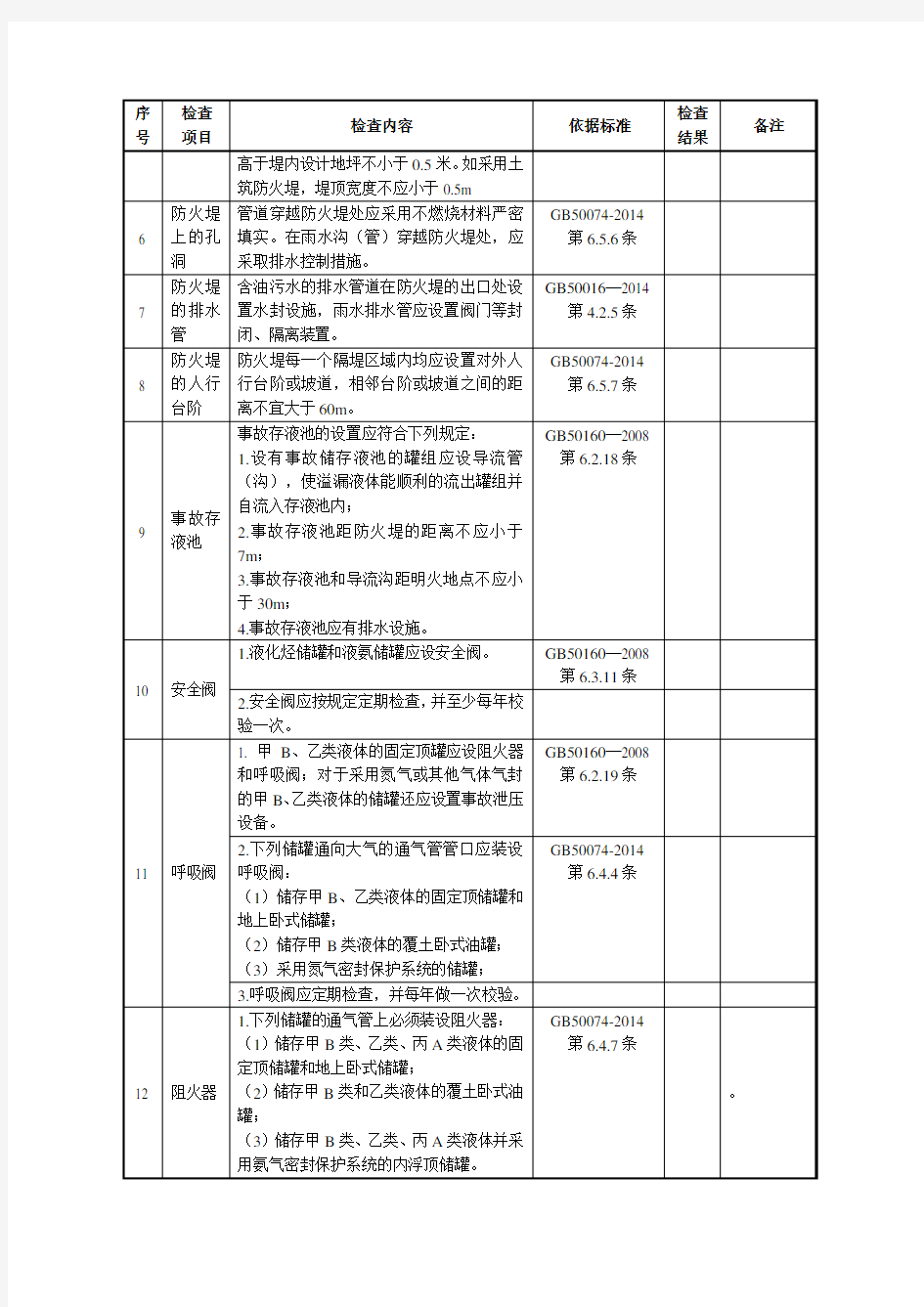
车间班组日常安全检查表 检查人员:日期:年月日项 目 检查内容是否备注 人员作业人员是否遵守安全操作规程 从业人员是否掌握紧急情况下的应急措施,是否有不会使用消防灭火器的人员 特种作业人员持证上岗情况 有无酒后上班;无嬉戏、打闹、饮食等 有无脱岗、睡岗、串岗等 使用无安全装置的设备、工具 有无在车间吸烟违章进入作业场所 有无攀坐或依靠机械、电器、设备等不安全位置有无在车间内穿脱工作衣服 有无在上班时间长期打电话聊天的 是否有轻伤事故发生 是否有(其他)的不安全行为 有无积极对公司提出合理化建议、有实效的; 机械设备设施车间设备是否处于正常运转状态 储罐设备等应无裂纹和渗漏,无跑、冒、滴、漏和腐蚀、锈蚀现象。 管道应无裂纹和渗漏,管道应保持畅通,密封良好,无跑、冒、滴、漏和腐蚀现象。 机器运转时加油、修理、检查、调整(非允许部位)、焊接、清扫等工作 运转设备防护罩是否完好;有无防护罩未在适当位置或防护装置调整不当情况 有无设备带“病”运转或超负荷运转 有无维修调整不良或保养不当、设备失灵情况设备设施是否定期进行维护保养与检修 检修施工作业是否遵守有关规定和标准执行(检修传动设备要先停电、挂警示牌上护栏;试转要站旁边) 特种设备是否按照国家有关规定取得检验、检测合格证,并在有效期间内 维修、调整不良或保养不当、设备失灵等情况监测、监视装置(仪表)是否有效、合格。 机械设备有无跑、冒、滴、漏及腐蚀现象 电器设备电器设备电器设备的金属外壳绝缘是否良好 机械设备接地、接零是否完整良好 有无绝缘不良、绝缘强度不够 有无电气装置带电部分裸露 有无开关、插座、接触器等有无因接触不良而严重发热 电器开关外壳是否完整可靠,有无破损 电线电缆是否用固定装置固定使用 是否超过线缆额定电流量(最大负荷) 有无电线电缆乱拉乱接(架设符合规范),临时用电线路是否及时拆除 临时线路需用良好的橡套电缆,长度不宜超过10m,线上不得有接头 特殊环境(潮湿、粉尘、腐蚀性、易燃易爆)的照明(密封、防爆式);是否使用安全电压和选用合适的漏电保安器。
附件1 医用氧注册申请生产现场检查要点 一、安全生产证明性文件 液态氧(以空气为原料):医用氧(液态)药品生产许可证、安全生产许可证及低温液体贮罐(或槽车)充装许可证等。 气态氧(以空气为原料):医用氧(气态)药品生产许可证、安全生产许可证及气瓶充装许可证、钢瓶检验资质证明等。 气态氧(以液态氧为原料):医用氧(气态)药品生产许可证、危险化学品经营许可证、气瓶充装许可证、钢瓶检验资质证明、液态氧原料运输单位的的资质证明及与运输企业签署的协议等证明文件。 二、对起始原料进行控制 当以空气为起始原料时,需要关注是否对空气质量进行了控制,如何控制;应提供环境监测机构出具的申请人厂区周围环境监测报告材料或环境空气监测报告。 当以液态氧为起始原料时,必须采用已获得国家批准文号的氧,应提供相关的证明性文件。 三、对生产过程的控制 (一)当采用低温空气分离法时,生产过程控制主要包括以下方面: 1.空气的净化过程:是否对空气质量进行控制,如何除去灰尘及机械杂质。一般可采用空气净化设备进行净化。
2.空气的压缩过程:关注压缩机种类,应使用非油压缩机。如果采用油压缩机,应关注对可能引入的杂质的控制。 3.除杂过程:在分馏前如何除去空气中水分、二氧化碳及部分烃类物质。所采用的设备情况,相关设备有无监测指标。一般可采用分子筛净化吸附。 4.分馏过程。 按照申报单位提供的工艺描述和工艺参数,进行动态生产现场检查。 (二)当采用液氧分装法时,关注升温、气化、充装过程,按照申报单位提供的工艺描述和工艺参数,进行动态生产现场检查。 四、包装材料的监管 需关注采用何种包材(液态氧:低温液体储罐或槽车;气态氧:耐压无缝钢瓶等),包材的来源和质量标准是否符合国家相关行业的要求,压力容器有无制造和/或许可证,在生产充装前如何对包材进行处理,如何测定包装的密封性。 五、质量检测 液态氧和气态氧均应执行中国药典2010年版氧标准,包括含量、性状、鉴别、酸碱度、一氧化碳、二氧化碳、其他气态氧化物质。申报时已由省所检验了3批样品,故不再进行现场抽样检验,但应结合中国药典2010年版氧标准中各项检查项目,评价申请人是否具备医用氧的检验能力。
表C.0.1储罐交工验收证书 (项目名称)储罐交工验收证书 单项工程名称: 单项工程编号:单位工程名称单位工程编号 储罐公称容积储罐编号 结构形式罐体材料 设计单位盛装物料 开工日期竣工日期 验收意见: 该工程经有关部门共同检查和鉴定,确认符合设计及《立式圆筒形钢制焊接油罐施工及验收规范》(GB50128-2014)要求,同意交工验收。 建设单位监理单位质量监督单位承包单位 代表: (公章) 年月日总监理工程师: (公章) 年月日 现场代表: (公章) 年月日 质量检查员: 技术负责人: (公章) 年月日
表C.0.2储罐基础复测记录 (项目名称)储罐基础复测记录单项工程名称:单项工程编号: 单位工程编号单位工程编号 储罐名称复测日期 储罐公称容积 M3储罐直径 M 检查项目允许值 (㎜) 实测值 (㎜) 检查项目 允许值 (㎜) 实测值 (㎜) 基础中心标高差环墙周 向标高 差10m内任意两点 基础中心轴线偏差全圆周内任意两点 基础单面倾斜度偏差 沥青砂 表面平 整度倾斜基础平行线 基础直径偏差周向基础环梁宽度偏差径向 同心圆编号计 算 标 高 ㎜ 实测点标高(㎜) P 1 P 2 P 3 P 4 P 5 P 6 P 7 P 8 P 9 P 1 P 1 1 P 1 2 P 1 3 P 1 4 P 1 5 P 1 6 P 1 7 P 1 8 P 1 9 P 2 P 2 1 P 2 2 P 2 3 P 2 4 任意两点 最大高差 (mm) 相邻两点 最大高差 (mm) C1 C2 C3 复测结果确认: 附:储罐基础同心圆及测点编号布置图: 监理单位接受单位交出单位 监理工程师: 年月日技术负责人: 年月日 技术负责人: 年月日
附件2-5 欧阳光明(2021.03.07) 新版GMP认证报告 医用氧发现质量缺陷情况通报 目录 一、机构与人员2 二、厂房与设施、设备3 三、物料与产品6 四、确认与验证7 五、文件管理8 六、生产管理13 七、质量保证15 八、质量控制19
一、机构与人员(共5条) 1.企业配备的质量保证部门人员不足,不能满足实际生产需求。(第18条) 2.缺少质量受权人职责。(第18条) 3.质量受权人对产品放行进行了转授权,对其它质量管理活动没有转授权,不能保证正常参与质量管理活动。(第25条) 4.培训内容不全,培训效果不理想,如: (1)2015年设备验证前未对相关人员进行培训;未及时进行GMP(2010年修订)医用氧附录培训;2014年未对员工进行有关卫生要求的培训;(第27条) (2)人员《药品生产质量管理规范》(2010年版)培训效果不佳,例如质量授权人对变更、偏差、纠正预防等新版GMP概念及应用不熟悉,履职能力不强;(第27条) (3)车间操作人员不能严格按照操作规程进行操作,如充装过程中未按要求采取气瓶防倒措施;(第27条) (4)与氧生产和质量有关的人员GMP学习培训不够,缺少对培训效果的评估;未定期对岗位培训效果进行评估;(第27条)(5)人员培训档案内容不全,现场检查时相关人员回答问题和操作情况不佳;(第27条) (6)企业2015年未对个别从事医用氧生产的人员进行医用氧相关知识培训;部分生产操作员工2015年培训档案中,未归档对医用氧附录的培训考核内容。(医用氧附录第8条) 5.人员健康管理不足,如:
(1)未建立人员健康档案;(第31条) (2)部分质量检验人员的健康查体未对视力、辨色力进行检查;(第31条) (3)2013年相关人员健康查体资料未归档;李某缺少2015年度健康体检报告;(第31条) (4)取样人员未配备防护镜;充装岗位人员未按规定穿工作鞋进行气瓶充装。(医用氧附录第9条) 二、厂房与设施、设备(共16条) 1.空瓶清洗消毒区无水源及下水设施。(第38条) 2.生产区缺少通风、防静电措施,如:(医用氧附录第11条) (1)企业分装车间未安装通风设施; (2)生产区无人员静电释放设施; (3)充装车间无通风和防静电设施; (4)医用氧(气态)生产区未安装静电释放设施。 3.仓储区区域划分不合理,空间不足,缺乏有效的隔离:如: (1)医用氧成品库储存区域未设置待检区、合格区、不合格区;工业氧与医用氧发货操作区隔离杆不固定,有被移动的风险;(第61条) (2)空瓶验收区面积过小,未设置独立不合格空瓶存放区;不合格的空瓶存放区无有效的隔离措施;(第61条)
解决方案编号:LX-FS-A26138 医用氧生产企业安全管理控制措施 标准范本 In the daily work environment, plan the important work to be done in the future, and require the personnel to jointly abide by the corresponding procedures and code of conduct, so that the overall behavior or activity reaches the specified standard 编写:_________________________ 审批:_________________________ 时间:________年_____月_____日 A4打印/ 新修订/ 完整/ 内容可编辑
医用氧生产企业安全管理控制措施 标准范本 使用说明:本解决方案资料适用于日常工作环境中对未来要做的重要工作进行具有统筹性,导向性的规划,并要求相关人员共同遵守对应的办事规程与行动准则,使整体行为或活动达到或超越规定的标准。资料内容可按真实状况进行条款调整,套用时请仔细阅读。 医用氧气态生产企业应选址在远离人员居住区的地方,需要由具有医药化工资质的设计单位进行设计,依据《氧气站设计规范》和《建筑防火设计规范》的要求液氧储罐与充装厂房的距离需大于12米,液氧储罐与办公楼及住宿生活楼距离大于20米,相邻储罐的距离大于较大储罐的半径。 多数医用氧生产企业在生产医用氧的同时还生产工业氧、氩气等其他工业气体,所以医用氧生产车间需使用实体墙或其它措施与工业氧生产车间隔离开,最好不要使用地标线(因为使用地标线时员工有时会
医用氧文件目录总
医用氧GMP文件目录 第一部分机构与人员 机构和人员管理文件目录 文件编码文件名称SMP-JR-001-00 公司组织机构图 SMP-JR-002-00 生产管理部职责 SMP-JR-003-00 质量管理部职责 SMP-JR-004-00 办公室职责 SMP-JR-005-00 供销部职责 SMP-JR-006-00 财务部职责 SMP-JR-007-00 充装车间职责 SMP-JR-008-00 维修车间职责 SMP-JR-009-00 气瓶检验站职责 SMP-JR-010-00 总经理职责 SMP-JR-011-00 生产管理部部长职责 SMP-JR-012-00 质量管理部部长职责 SMP-JR-013-00 办公室主任职责 SMP-JR-014-00 供销部部长职责 SMP-JR-015-00 财务部部长职责 SMP-JR-016-00 QC质检员职责 SMP-JR-017-00 QA质监员职责 SMP-JR-018-00 质量受权人职责 SMP-JR-019-00 车间主任职责 SMP-JR-020-00 工艺员职责 SMP-JR-021-00 采购员职责 SMP-JR-022-00 销售员职责 SMP-JR-023-00 统计员职责 SMP-JR-024-00 仓库管理员职责 SMP-JR-025-00 设备管理员职责 SMP-JR-026-00 维修工职责 SMP-JR-027-00 洗衣工职责 SMP-JR-028-00 车间操作工职责 SMP-JR-029-00 人员培训管理制度 SMP-JR-030-00 人员教育档案管理制度 SMP-JR-031-00 人员体检管理制度 SMP-JR-032-00 特种作业人员管理制度 机构和人员记录目录 文件编码文件名称JL-JR-001-00 年度培训计划
医用氧生产企业安全管理控制 措施(2021年) Safety management is an important part of enterprise production management. The object is the state management and control of all people, objects and environments in production. ( 安全管理 ) 单位:______________________ 姓名:______________________ 日期:______________________ 编号:AQ-SN-0000
医用氧生产企业安全管理控制措施(2021 年) 医用氧气态生产企业应选址在远离人员居住区的地方,需要由具有医药化工资质的设计单位进行设计,依据《氧气站设计规范》和《建筑防火设计规范》的要求液氧储罐与充装厂房的距离需大于12米,液氧储罐与办公楼及住宿生活楼距离大于20米,相邻储罐的距离大于较大储罐的半径。 多数医用氧生产企业在生产医用氧的同时还生产工业氧、氩气等其他工业气体,所以医用氧生产车间需使用实体墙或其它措施与工业氧生产车间隔离开,最好不要使用地标线(因为使用地标线时员工有时会把工业氧瓶与医用氧瓶混淆),医用氧生产区用于存储空瓶和不同阶段产品的气瓶的区域面积应适应生产能力(旧版GMP认
证时很多企业的储存空瓶和不同阶段产品的气瓶区域都是一个形式)。 医用氧生产企业最好是从具有医用液氧生产资质的企业采购原料药,具有医用液氧生产资质企业的医用液氧槽车是专用的,可以最大限度的减少运输过程的污染。对购入的医用液氧进行全检,检验合格后才能卸车,因医用液氧储槽和工业液氧储槽的卸液接口是一种型号,为避免卸错储槽需要对医用液氧储槽的卸液接口进行加锁管理,开锁需要QA确认。 生产设施:低温液氧泵最好安装三道保护装置,一是温度联锁,即当气化器出口的温度低于安全值时(安全值是指气化器能把液氧完全气化时的温度值)能自动停机,二是加装压力联锁,即当充装压力超过允许充装的最高压力时能自动停机,三是加装急停按钮,即在紧急情况下,操作人员可以在充装控制台处可以对低温泵进行停机。 充装管道需进行静电接地,在充装控制阀门与低温泵之间的管道可以使用304不锈钢管或铜管,在充装控制阀之后的管道最好是
J4—2017 储罐试漏检查记录工程名称:中国石油内蒙古乌兰浩特油库安全隐患整改工程 单位工程名称:储运系统工程 设备名称钢制储罐设备位号0321-TK-001A 型号规格5000m3试漏日期2011年5月1日 试漏方法简述: 罐底真空箱法严密性实验在油罐施工中也称真空试漏,是罐底、浮顶单盘板、船舱底板及内浮盘板焊缝的最主要的检验方法。首先将焊缝表面打磨光亮无毛刺杂质,待检焊缝涂抹肥皂溶液,将真空箱盖待检焊缝并抽真空,在达到规定的真空度(53KP)时,焊缝无泄漏(表面无肥皂泡沫产生)为合格。该试验采用焊缝上面处于真空状态时,空气可从焊缝纰病处穿过的原理。 试漏检查情况: 当实验负压值≥53KP时,经目测肥皂溶液表面无泡沫产生,真空压力表读数稳定无变化。此焊缝无渗漏为合格。 结论: 施工单位监理单位 记录人: 作业负责人: 技术负责人: 年月日代表: 年月日
J4—2017 储罐试漏检查记录工程名称:中国石油内蒙古乌兰浩特油库安全隐患整改工程 单位工程名称:储运系统工程 设备名称钢制储罐设备位号0321-TK-001B 型号规格5000m3试漏日期2011年5月5日 试漏方法简述: 罐底真空箱法严密性实验在油罐施工中也称真空试漏,是罐底、浮顶单盘板、船舱底板及内浮盘板焊缝的最主要的检验方法。首先将焊缝表面打磨光亮无毛刺杂质,待检焊缝涂抹肥皂溶液,将真空箱盖待检焊缝并抽真空,在达到规定的真空度(53KP)时,焊缝无泄漏(表面无肥皂泡沫产生)为合格。该试验采用焊缝上面处于真空状态时,空气可从焊缝纰病处穿过的原理。 试漏检查情况: 当实验负压值≥53KP时,经目测肥皂溶液表面无泡沫产生,真空压力表读数稳定无变化。此焊缝无渗漏为合格。 结论: 施工单位监理单位 记录人: 作业负责人: 技术负责人: 年月日代表: 年月日
医用氧生产企业GMP认证申报资料技术要点 生产企业名称: 申请认证范围:医用氧(含气态□、液态□) 受理号: 一.认证申请书 企业名称与许可证是否一致。□ 注册地址是否与许可证上的注册地址一致。□ 生产地址是否与许可证上的生产地址一致。□ 注册地址是否与营业执照上的地址一致。□ 申请认证范围是否在许可证范围内。□ 申请范围的填写是否正确。□ 是否有液态氧生产车间。□ 是否有气态氧生产车间。□ 表格内容是否每一项均填写(凡未发生项,文字填“无”,数字填“0”)。□ 生产剂型和品种表 药品生产企业许可证范围全部剂型和品种表: 是否含品名、□规格、□批准文号。□ 本次认证范围剂型和品种表: 该表是否含品名□、规格□、执行标准□、批准文号□、是否注 明常年生产品种。□ 申请认证的品种的生产批准证明文件复印件是否齐全。□ 本次认证品种名称、规格、批准文号、生产地址与药品批准证明文件中的是否一致。□ 二、安监处形式审查意见单 认证范围是否与企业申报表中的范围一致。□ 认证的有效期限是否正确。□ 有无需要说明的问题。□ 三、许可证、营业执照复印件 证照是否在有效期内。□ 四、企业生产管理和质量管理自查情况 1.企业概况和历史沿革情况:
是否有企业原名或前身,改为现公司的时间。□ 是否企业有占地面积,绿化面积,绿化率。□ 是否有本次申请认证车间的竣工时间,制氧生产区总面积,年设计生产能力,车间生产品种的情况。□ 2.企业GMP实施情况 是否有人员培训情况。□ 是否有企业负责人、生产、质量管理人员及其他技术人员情况。□ 是否有本次认证品种相对应的制氧方法及设备情况。□ 化学法□深冷空分法□分子筛空分法□膜式空分法□ 是否有液态氧生产情况: 日产量_____立方, 储罐单个容积______立方, ______个数 是否有气态氧充装间情况: 汇流排位置□、充装头个数____、日充装能力______瓶, 设备是否专用□。 充装间是否与其它气体共用□,如有, ____气体。 是否有仓储情况。□ 是否有化验室情况。□ 是否有公用设施,水、电、汽供应情况。□ 是否有物料管理情况。□ 是否有气瓶管理情况。□ 自有气瓶数______个, 托管气瓶数______个 是否有卫生管理情况。□ 是否有生产管理情况。□ 是否有质量管理情况。□ 是否有验证情况。□ 是否有安全消防情况。□ 是否有三废处理情况。□ 五、组织机构图 机构图是否合理。□ 质量管理部门负责人与生产部门负责人是否兼任。□ 是否注明各部门名称、相互关系、部门负责人。□ 六、公司人员情况 主管生产和质量的企业负责人是否有相关专业大专以上学历或中级以上职称并具有相应的管理经验。□ 生产管理部门负责人是否有相关专业大专以上学历,或中级以上的专业技术职称,并具有医用气体生产的实践经验。□ 质量管理部门负责人是否有相关专业大专以上学历,或中级以上的专业技术职称,并具有医用气体生产的实践经验。□ 是否有企业负责人、部门负责人简历。□ 药学及相关专业技术人员登记表是否含姓名、□学历、□毕业院校、□ 专业、□职称、□职务、□从药年限。□ 高、中、初级技术人员占全体员工的比例情况表。□
车间安全检查表 检查人员:日期:年月日项 目 检查内容是否备注 人员作业人员是否遵守安全操作规程 从业人员是否掌握紧急情况下的应急措施,是否有不会使用消防灭火器的人员 特种作业人员持证上岗情况 有无酒后上班;无嬉戏、打闹、饮食等 有无脱岗、睡岗、串岗等 使用无安全装置的设备、工具 有无在车间吸烟违章进入作业场所 有无攀坐或依靠机械、电器、设备等不安全位置有无在车间内穿脱工作衣服 有无在上班时间长期打电话聊天的 是否有轻伤事故发生 是否有(其他)的不安全行为 有无积极对公司提出合理化建议、有实效的; 机械设备设施车间设备是否处于正常运转状态 储罐设备等应无裂纹和渗漏,无跑、冒、滴、漏和腐蚀、锈蚀现象。 管道应无裂纹和渗漏,管道应保持畅通,密封良好,无跑、冒、滴、漏和腐蚀现象。 机器运转时加油、修理、检查、调整(非允许部位)、焊接、清扫等工作 运转设备防护罩是否完好;有无防护罩未在适当位置或防护装置调整不当情况 有无设备带“病”运转或超负荷运转 有无维修调整不良或保养不当、设备失灵情况设备设施是否定期进行维护保养与检修 检修施工作业是否遵守有关规定和标准执行(检修传动设备要先停电、挂警示牌上护栏;试转要站旁边) 特种设备是否按照国家有关规定取得检验、检测合格证,并在有效期间内 维修、调整不良或保养不当、设备失灵等情况监测、监视装置(仪表)是否有效、合格。 机械设备有无跑、冒、滴、漏及腐蚀现象 电器设备电器设备的金属外壳绝缘是否良好 机械设备接地、接零是否完整良好 有无绝缘不良、绝缘强度不够 有无电气装置带电部分裸露 有无开关、插座、接触器等有无因接触不良而严重发热 电器开关外壳是否完整可靠,有无破损 电线电缆是否用固定装置固定使用 是否超过线缆额定电流量(最大负荷) 有无电线电缆乱拉乱接(架设符合规范),临时用电线路是否及时拆除 特殊环境(潮湿、粉尘、腐蚀性、易燃易爆)的照明(密封、防爆式);是否使用安全电压和选用合适的漏电保安器。
附件2 医用氧 第一章范围 第一条本附录中所述医用氧是指空气经低温分离制备的液态氧、气态氧。 第二条本附录适用于医用氧工业化生产过程,不包括医疗机构内部医用氧的处置。 第三条其他医用气体的工业生产要求参照本附录执行。 第二章原则 第四条医用氧的生产、贮存、运输、销售应符合国家有关部门的规定,并取得相关证件。 第五条医用氧生产和质量控制须满足其质量及预定用途的要求,应当最大限度降低污染、交叉污染、混淆及差错的风险。 第三章人员 第六条企业的生产管理负责人应具有相关专业(如化工、药学、化学、机械和工业工程等)大专以上学历或中级专业技术职称,具有三年以上的医用氧的生产和质量管理经验,其中至少一年的医用氧生产管理经验。 第七条企业的质量管理负责人和质量受权人应具有相关专业(如化工、药学、化学、机械和工业工程等)大专以上(含大专)
学历(或中级专业技术职称),具有三年以上医用氧生产和质量管理经验,其中至少一年的医用氧质量管理经验。 第八条从事医用氧生产的人员应定期接受医用氧相关知识培训,涉及特种设备操作人员应按国家规定持有有效的并与医用氧生产相适应的资格证书。 第九条应根据需要,为员工配备相应的工作服和安全防护用品。 第四章厂房与设备 第十条医用氧生产企业的生产环境应整洁。生产、质量检验、行政、生活和辅助区总体布局应合理。 第十一条厂房应按医用氧生产工艺流程要求合理布局。生产区和储存区应有与生产规模相适应的面积和空间,并有通风、照明、防火、防爆、防雷、防静电等设施。 应有足够的储存区域用于存放空瓶和不同阶段产品的气瓶(如待清洁、待充装、待检、合格、不合格等),不同储存区域应采用有效方法或明显标识区分,如:地标线、隔断、围栏和标志牌等。 第十二条医用氧充装生产车间应保持整洁,地面平整、耐磨防滑,并设置专用更衣室;充装生产车间应与维修车间分开。 第十三条用于生产和检验用的设备、仪器应经定期确认和校准。 第十四条生产和检验设备应定期进行维护。维护和维修应做好记录。生产设备的任何维护和维修工作不得影响医用氧的质量。
医用氧GMP文件目录 第一部分机构与人员 机构和人员管理文件目录 文件编码文件名称SMP-JR-001-00 公司组织机构图 SMP-JR-002-00 生产管理部职责 SMP-JR-003-00 质量管理部职责 SMP-JR-004-00 办公室职责 SMP-JR-005-00 供销部职责 SMP-JR-006-00 财务部职责 SMP-JR-007-00 充装车间职责 SMP-JR-008-00 维修车间职责 SMP-JR-009-00 气瓶检验站职责 SMP-JR-010-00 总经理职责 SMP-JR-011-00 生产管理部部长职责 SMP-JR-012-00 质量管理部部长职责 SMP-JR-013-00 办公室主任职责 SMP-JR-014-00 供销部部长职责 SMP-JR-015-00 财务部部长职责 SMP-JR-016-00 QC质检员职责 SMP-JR-017-00 QA质监员职责 SMP-JR-018-00 质量受权人职责 SMP-JR-019-00 车间主任职责 SMP-JR-020-00 工艺员职责 SMP-JR-021-00 采购员职责 SMP-JR-022-00 销售员职责 SMP-JR-023-00 统计员职责 SMP-JR-024-00 仓库管理员职责 SMP-JR-025-00 设备管理员职责 SMP-JR-026-00 维修工职责 SMP-JR-027-00 洗衣工职责 SMP-JR-028-00 车间操作工职责 SMP-JR-029-00 人员培训管理制度 SMP-JR-030-00 人员教育档案管理制度 SMP-JR-031-00 人员体检管理制度 SMP-JR-032-00 特种作业人员管理制度 机构和人员记录目录 文件编码文件名称JL-JR-001-00 年度培训计划
整体解决方案系列 某医用氧生产企业安全管 理控制措施
编号:FS-QG-11914 某医用氧生产企业安全管理控制措 Safety man ageme nt con trol measures of a medical oxyge n p roduct ion enterp rise 说明:为明确各负责人职责,充分调用工作积极性,使人员队伍与目标管理科学化、制度化、规范化,特此制定 医用氧气态生产企业应选址在远离人员居住区的地方, 需要由具有医药化工资质的设计单位进行设计,依据《氧气站设计规范》和《建筑防火设计规范》的要求液氧储罐与充装厂房的距离需大于12米,液氧储罐与办公楼及住宿生活楼距离大于20米,相邻储罐的距离大于较大储罐的半径。 多数医用氧生产企业在生产医用氧的同时还生产工业 氧、氩气等其他工业气体,所以医用氧生产车间需使用实体墙或其它措施与工业氧生产车间隔离开,最好不要使用地标线(因为使用地标线时员工有时会把工业氧瓶与医用氧瓶混淆),医用氧生产区用于存储空瓶和不同阶段产品的气瓶的 区域面积应适应生产能力(旧版GMP认证时很多企业的储存 空瓶和不同阶段产品的气瓶区域都是一个形式)。 医用氧生产企业最好是从具有医用液氧生产资质的企 业采购原料药,具有医用液氧生产资质企业的医用液氧槽车是专用的,可以最大限度的减少运输过程的污染。对购入的医用液氧进行全检,检验合
格后才能卸车,因医用液氧储槽和工业液氧储槽的卸液接口是一种型号,为避免卸错储槽需 要对医用液氧储槽的卸液接口进行加锁管理,开锁需要QA确认。 生产设施:低温液氧泵最好安装三道保护装置,一是温 度联锁,即当气化器出口的温度低于安全值时(安全值是指 气化器能把液氧完全气化时的温度值)能自动停机,二是加 装压力联锁,即当充装压力超过允许充装的最高压力时能自动停机,三是加装急停按钮,即在紧急情况下,操作人员可以在充装控制台处可以对低温泵进行停机。 充装管道需进行静电接地,在充装控制阀门与低温泵之 间的管道可以使用304不锈钢管或铜管,在充装控制阀之后的管道最好是使用铜管,因为铜管更不容易聚集静电。 充装排组的充装头数每组最好不要少于20个,现在很 多医用氧生产企业的充装排组的充装头数每组在15个以下, 这样每组充装时只能充装15瓶医用氧,因为低温泵最好是在中高速的转速下运行时的性能是最佳的,每组的充装头太 少时,充装的时间不能保证达到30分钟,充装时间达不到 30分钟以上时,容易出安全事故。 医用氧生产前需对充装管道进行置换,对管道内的气体 纯度经检测合格后方可进行充装,充装过程中用激光测温仪逐瓶检测瓶
医用氧生产企业安全管理控制措施示范文本 In The Actual Work Production Management, In Order To Ensure The Smooth Progress Of The Process, And Consider The Relationship Between Each Link, The Specific Requirements Of Each Link To Achieve Risk Control And Planning 某某管理中心 XX年XX月
医用氧生产企业安全管理控制措施示范 文本 使用指引:此解决方案资料应用在实际工作生产管理中为了保障过程顺利推进,同时考虑各个环节之间的关系,每个环节实现的具体要求而进行的风险控制与规划,并将危害降低到最小,文档经过下载可进行自定义修改,请根据实际需求进行调整与使用。 医用氧气态生产企业应选址在远离人员居住区的地 方,需要由具有医药化工资质的设计单位进行设计,依据 《氧气站设计规范》和《建筑防火设计规范》的要求液氧 储罐与充装厂房的距离需大于12米,液氧储罐与办公楼及 住宿生活楼距离大于20米,相邻储罐的距离大于较大储罐 的半径。 多数医用氧生产企业在生产医用氧的同时还生产工业 氧、氩气等其他工业气体,所以医用氧生产车间需使用实 体墙或其它措施与工业氧生产车间隔离开,最好不要使用 地标线(因为使用地标线时员工有时会把工业氧瓶与医用 氧瓶混淆),医用氧生产区用于存储空瓶和不同阶段产品
的气瓶的区域面积应适应生产能力(旧版GMP认证时很多企业的储存空瓶和不同阶段产品的气瓶区域都是一个形式)。 医用氧生产企业最好是从具有医用液氧生产资质的企业采购原料药,具有医用液氧生产资质企业的医用液氧槽车是专用的,可以最大限度的减少运输过程的污染。对购入的医用液氧进行全检,检验合格后才能卸车,因医用液氧储槽和工业液氧储槽的卸液接口是一种型号,为避免卸错储槽需要对医用液氧储槽的卸液接口进行加锁管理,开锁需要QA确认。 生产设施:低温液氧泵最好安装三道保护装置,一是温度联锁,即当气化器出口的温度低于安全值时(安全值是指气化器能把液氧完全气化时的温度值)能自动停机,二是加装压力联锁,即当充装压力超过允许充装的最高压力时能自动停机,三是加装急停按钮,即在紧急情况下,
药品生产监督医用氧气检查重点内容和检查方法指导原则 医用氧气是指采用深冷分离法、分子筛空分法等空分技术将大气中氧气分离以供应医疗救治病人使用的氧气,监督检查时,应重点关注医用氧生产人员的操作技能和安全防护措施,如兼产工业用氧、其他类医用气体时,还应重点关注其防止混淆、交叉污染措施是否完善。 1.人员 检查方法: 根据人员花名册选取相关岗位人员,抽查相关岗位职责、培训档案、健康档案,检查有关资质证件。 检查内容: 1.1从事医用氧生产的人员是否接受医用氧特定操作的有关知识培训,并按国家有关规定取得相关管理部门资格证书(气瓶充装资格证、危险品押运证、安全员证等)。 1.2从事医用氧的生产和质量检验工作是否检查辨色力,是否有色盲患者从事以上工作。
2.厂房设备 检查方法: 现场检查厂房布局及设备,检查相关记录。 检查内容: 2.1气瓶充装区域是否有明显标识,空瓶和不同阶段产品的气瓶(如待充装、已充装、待检、合格、不合格)是否清楚标示并分开放置。 2.2生产区和储存区是否有与生产规模相适应的面积和空间,并有通风、照明、防火、防爆、防静电等设施。 2.3医用氧生产过程中的气体压缩设备活塞密封是否不使用氟塑料制材料。 2.4用液态氧气化充装气态氧是否使用低温液氧泵,加压气化后充装。 2.5医用氧容器(槽车、储罐和气瓶)是否专用,且有与其他气体容器区分的明显标识。 2.6医用氧充装是否使用专用设备,其充装夹具是否有防错装装置。
2.7气瓶储存区域是否清洁、干燥,有良好通风,没有易燃物质。 2.8医用氧是否有相对独立的储存区域,空瓶、实瓶区域是否有隔离。 2.9医用氧的生产、贮存、运输、销售是否符合国家有关部门的规定,并取得相关证件(如:如危化品安全生产许可证或危化品安全经营许可证、危化品运输许可证、永久气瓶充装许可证)。 3.质量管理 检查方法: 抽查气瓶鉴定、饮用水检测报告,检查液氧注册批准文件,检查质量标准、检验记录,检查气瓶管理制度和记录,检查质量控制实验室仪器。 检查内容: 3.1使用的气瓶是否经具有核准资格的单位进行定期检验合格。 3.2用于气瓶静水压测试的水是否至少符合生活饮用水
SY4202-2007石油天然气建设工程施工质量验收规范储罐工程 检验批质量验收记录表格目录 1、表B.2 球形储罐球壳板组装检验批质量验收记录 (2) 2、表B.6 立式储罐基础沥青砂垫层工程检验批质量验收记录 (4) 3、表B.7 立式储罐底板预制检验批质量验收记录 (5) 4、表B.13 立式储罐罐底焊接检验批质量验收记录 (6) 5、表B.14 立式储罐罐壁组装检验批质量验收记录 (8) 6、表B.15 立式储罐罐壁焊接检验批质量验收记录 (9) 7、表B.18 立式储罐浮顶及内浮顶组装检验批质量验收记录 (10) 8、表B.19 立式储罐浮顶焊接检验批质量验收记录 (11) 9、表B.20 立式储罐附件安装检验批质量验收记录 (12) 10、表B.21 立式储罐总体验收检验批质量验收记录 (13) 11、表B.22 外防腐涂料涂装工程检验批质量验收记录 (15) 12、表B.23 立式储罐内防腐工程检验批质量验收记录 (16) 13、表B.24 防火涂料涂装工程检验批质量验收记录 (17) 14、表B.25 绝热工程检验批质量验收记录 (18) 15、表B.26 梯子、平台、栏杆制作安装工程检验批质量验收记录 (20) 16、表E.1 立式储罐单位工程质量控制资料核查记录 (21) 17、表A.1 储罐工程质量检验用计量器具 (22) 备注: 表B.1,表B.3,表B.4,表B.5,表B.8,表B.9,表B.10,表B.11,表B.12,表B.16,表B.17,表D.1未列入。如需使用上述表格,参照验收规范,自行制作!
SY4202-2007石油天然气建设工程施工质量验收规范储罐工程检验批质量验收记录表B.2 球形储罐球壳板组装检验批质量验收记录
应急预案编号:HSHG001 应急预案版本号:第二版 辛集市海顺气体有限公司 (辛集市海立医用氧气厂) 生产安全事故综合应急预案 编制单位:辛集市海顺气体有限公司 颁布日期:年月日
批准页 根据《生产经营单位生产安全事故应急预案编制导则》(GB/T 29639—2013)以及安全生产监督管理部门的相关要求,结合公司实际情况编制了生产事故综合应急预案,本预案经安全生产监督管理部门应急工作人员及其认可的专家组评审通过,现予以发布,自即日起实施。希望全体员工积极贯彻落实,并认真进行演练。 批准人: 发布日期:年月日
目录 1总则............................................................... - 1 - 1.1编制目的. (1) 1.2编制依据 (1) 1.3适用范围 (2) 1.4应急预案体系 (2) 1.5应急工作原则 (3) 2事故风险描述 (4) 3应急组织机构及职责 (6) 4预警及信息报告 (8) 4.1预警 (8) 4.2信息报告 (8) 5应急响应 (10) 5.1响应分级 (10) 5.2响应程序 (11) 5.3处置措施........................................................ - 13 - 5.4应急结束 (17) 6信息公开 (18) 7后期处置 (18) 8保障措施 (20) 8.1通信与信息保障 (20) 8.2应急队伍保障 (20) 8.3物资装备保障 (20) 8.4其他保障 (20) 9应急预案管理 (21) 9.1应急预案培训 (21) 9.2应急预案演练 (21) 9.3应急预案修订 (21) 9.4应急预案备案 (22) 9.5应急预案的实施 (22) 附件 (23)
医用氧生产企业GMP 认证申报资料技术要点生产企业名称:申请认证范围:医 用氧(含气态□、液态□受理号:一.认证申请书企业名称与许可证是否一致。□注册地址是否与许可证上的注册地址一致。□生产地址是否与许可证上的生产地址一致。□注册地址是否与营业执照上的地址一致。□申请认证范围是否在 生产企业名称: 申请认证范围:医用氧(含气态□、液态□ 受理号: 一. 认证申请书 企业名称与许可证是否一致。□ 注册地址是否与许可证上的注册地址一致。□ 生产地址是否与许可证上的生产地址一致。□ 注册地址是否与营业执照上的地址一致。□ 申请认证范围是否在许可证范围内。□ 申请范围的填写是否正确。□ 是否有液态氧生产车间。□ 是否有气态氧生产车间。□ 表格内容是否每一项均填写(凡未发生项,文字填“无”,数字填“0”。□ 生产剂型和品种表 药品生产企业许可证范围全部剂型和品种表: 是否含品名、□规格、□批准文号。□ 本次认证范围剂型和品种表: 该表是否含品名□、规格□、执行标准□、批准文号□、是否注明常年生产品种。□ 申请认证的品种的生产批准证明文件复印件是否齐全。□ 本次认证品种名称、规格、批准文号、生产地址与药品批准证明文件中的是否一致。□ 二、安监处形式审查意见单 认证范围是否与企业申报表中的范围一致。□ 认证的有效期限是否正确。□ 有无需要说明的问题。□ 三、许可证、营业执照复印件 证照是否在有效期内。□ 四、企业生产管理和质量管理自查情况 1. 企业概况和历史沿革情况: 是否有企业原名或前身,改为现公司的时间。□ 是否企业有占地面积,绿化面积,绿化率。□ 是否有本次申请认证车间的竣工时间, 制氧生产区总面积, 年设计生产能力,
附件2-5 新版GMP认证报告 医用氧发现质量缺陷情况通报 目录 一、机构与人员 (2) 二、厂房与设施、设备 (3) 三、物料与产品 (6) 四、确认与验证 (7) 五、文件管理 (8) 六、生产管理 (13) 七、质量保证 (15) 八、质量控制 (19)
一、机构与人员(共5条) 1.企业配备的质量保证部门人员不足,不能满足实际生产需求。(第18条) 2.缺少质量受权人职责。(第18条) 3.质量受权人对产品放行进行了转授权,对其它质量管理活动没有转授权,不能保证正常参与质量管理活动。(第25条) 4.培训容不全,培训效果不理想,如: (1)2015年设备验证前未对相关人员进行培训;未及时进行GMP(2010年修订)医用氧附录培训;2014年未对员工进行有关卫生要求的培训;(第27条) (2)人员《药品生产质量管理规》(2010年版)培训效果不佳,例如质量授权人对变更、偏差、纠正预防等新版GMP概念及应用不熟悉,履职能力不强;(第27条) (3)车间操作人员不能严格按照操作规程进行操作,如充装过程中未按要求采取气瓶防倒措施;(第27条) (4)与氧生产和质量有关的人员GMP学习培训不够,缺少对培训效果的评估;未定期对岗位培训效果进行评估;(第27条)(5)人员培训档案容不全,现场检查时相关人员回答问题和操作情况不佳;(第27条) (6)企业2015年未对个别从事医用氧生产的人员进行医用氧相
关知识培训;部分生产操作员工2015年培训档案中,未归档对医用氧附录的培训考核容。(医用氧附录第8条) 5.人员健康管理不足,如: (1)未建立人员健康档案;(第31条) (2)部分质量检验人员的健康查体未对视力、辨色力进行检查;(第31条) (3)2013年相关人员健康查体资料未归档;某缺少2015年度健康体检报告;(第31条) (4)取样人员未配备防护镜;充装岗位人员未按规定穿工作鞋进行气瓶充装。(医用氧附录第9条) 二、厂房与设施、设备(共16条) 1.空瓶清洗消毒区无水源及下水设施。(第38条) 2.生产区缺少通风、防静电措施,如:(医用氧附录第11条) (1)企业分装车间未安装通风设施; (2)生产区无人员静电释放设施; (3)充装车间无通风和防静电设施; (4)医用氧(气态)生产区未安装静电释放设施。 3.仓储区区域划分不合理,空间不足,缺乏有效的隔离:如: (1)医用氧成品库储存区域未设置待检区、合格区、不合格区;工业氧与医用氧发货操作区隔离杆不固定,有被移动的风险;(第61条)