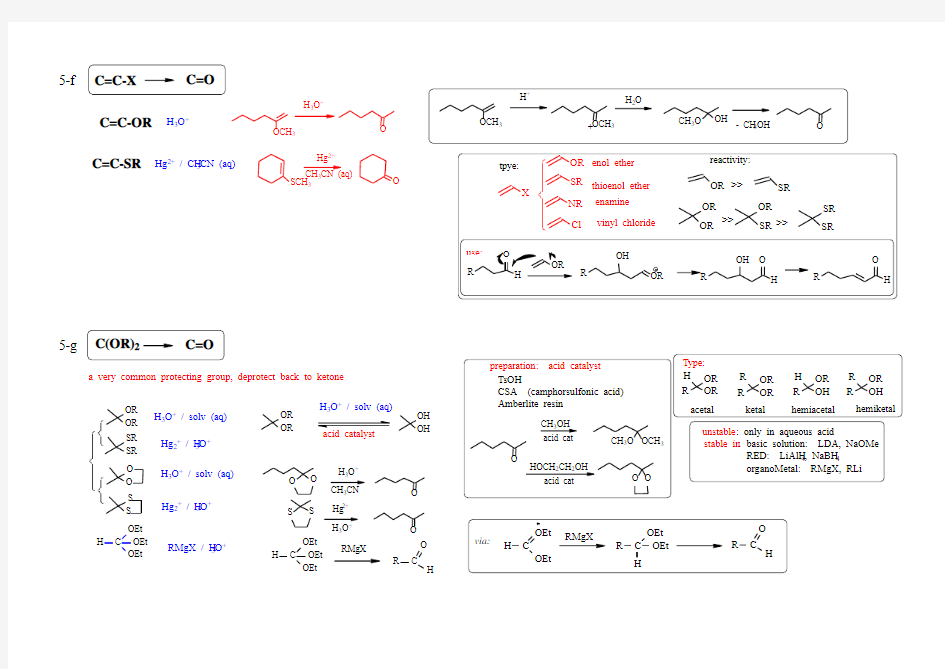

5-f
H 3O +
Hg 2+ / CH 3CN (aq)
C=C-OR C=C-SR
OCH 3
O
H 3O
+
SCH 3
O
Hg 2+
3
O
H 3O Hg 2+3H 3O +O
O O S
S
S S
SR
SR O O OR OR 5-g
Hg 2+ / H 3O +H 3O + / solv (aq)H 3O + / solv (aq)Hg 2+ / H 3O +
OR OR
OH OH
H 3O + / solv (aq)a very common protecting group, deprotect back to ketone
H
C OEt OEt OEt
RMgX / H 3O +
H
C OEt OEt OEt
RMgX
R
C
H
O
N H
+2
Cr 2O 7-2
N HCl
.CrO 3
Ag 2O:
1. a mild oxidizing agent
2. must be freshly prepared: NaOH into AgNO 3 (aq)
3. may involve surface change, react with CO 2, light
Swern oxidation: (DMSO, oxalyl chloride, Et 3N)drawback: react at low T Collins reagent: (CrO 3 - 2 Py)1. drawback: use 6 equivalent, a messy reaction 2. must be very dry, fire easily; purify by CaH 23. an old oxidizing material, isolated by Collin.
i. PCC
ii. PDC
ix. K 2R C OH
O aldehyde
1st alcohol
2nd alcohol
1st alcohol
R C OH
O
R C R
O
R C H
O 5-h i. PCC ii. PDC
JOC, 1985, 50, 1332.
N OCH 3
OH
PDC (pyridinium dichormate)
(H 2Cr 2O 7 + 2 Py)
PCC (pyridinium chlorochromate) (Py-HCl-CrO 3)
most widely used use 1 - 1.2 eq.
Pfitzner-Moffatt oxidation
O
O Br
DMSO
O O
O
H
360 %
Synth. Commun., 1986, 16, 1343.
JOC, 1977, 42, 1991.
Synthesis, 1981, 165.O I O
OAc
AcO
pH 6: weak acid buffer, avoid interfere with ketal group
McMurray reaction
i. Corey approach: subtituted-quinone // H 3O +ii. Watt approach
a. PhCHO // MCPBA // H 3O +
b. ArPhO // MCPBA // H 3O +
c. NBS // KOH // H 3O +
Ph
O
Ph Ph
O
Ph
NH 2
Ph Ph
NH 2
N
C O H // H 3O +
O O
5-i.15-i.2i. Et 3N // H 3O +
Nef reaction
ii. TiCl 3 / pH 1 or 6iii. SiO 2 / NaOH // H 3O +
JACS, 1977, 99, 3861.
iv. LDA / MoO 5-Py -v. NaOH // CH 3O O
H 3O +vi. KMnO 4 / KOH
Chem. Rev. 1955, 55, 137.
5-k I
O
O
OH O
(3 eq.)JACS, 2001, 123, 3183.
CH 3CHO
2. DDQ / TFA.
Synthesis, 1979, 537.
JCS, 1932, 1875.
Ph-F / DMSO 3.
1. SeO 2
a select oxidant
indrect: change to RC-OH followed by oxidation direct:
1. DMAPO / DBU / CH 3CN i. DMSO / AgBF 4R
Br DMSO / AgBF 4- Me 2S
Bull Soc. Jpn., 1981, 54, 2221.
THL, 1974, 917.2. NaIO 4 / DMF
O Br
84 %
o
NaIO 4 / DMF a new method 3. DMSO reagents:
ii. DMSO / ZnS
RCHBrMe
RC(O)Me
DMSO Br
OH O
OH JACS, 2003, 68, 2480.
R
O
AgBF
THL, 1975, 4467.
C C R CHOH
R
R C C H
C C R R'R C C H
R C C Ar
R C C H
C C R Ph
R C C H
steric base, prevent Nu attack n -BuLi: not MeLi, or t -BuLi, fire easily RX: R-Br, R-TOS, RCHO, RC(O)R
n -BuLi / R'CHO // Ac 2O // KO t Bu
Cl
OMe
N Li
iii.
ii. (Ph 3P)2PdCl 2, CuI, Et 2NH / PhI
i. n-BuLi / RX
6-b
6-a b c d e g 6-a
C C
C C
C C
sulfonic acid: PhSO 3H; sulfinic acid: PhSO 2H; sulfenic acid: PhSOH
iv. CuI, NaI, Na 2CO 3, R
C C CH 2Cl
R C C H
Cl CH 2C
C R'
R
C
C
CH 2C
C
R'
Synthesis, 2000, 691.
RCH 2-SO 2Ph RC CH
h f i
RCH(CO 2H)-CH 3-C(O)-CH 3
O O
O
X
CRR'=CHX
in fact: convert to C=C firstly
ii. protect - deprotect
i. move to terminal 6-c
NH 2NHK
use: KAPA
use: Co (CO)8 // Fe(NO 3)3, EtOH
JACS, 1975, 97, 891.
6-d
use: i. Br 2 / CCl 4 // KO t Bu
6-e
use: Pb(OAc)4, LiCl // KO t Bu // Br 2/CCl 4 // KO t Fe(NO 3)3: weak oxidizing agent
ii. Br 2 // KOH
JA CS, 1941, 63, 1180.
Ph
Ph
Ph
Ph
6-f
i. NaBH 4, H 3O +, Br 2, KOtBu
ii. NH 2OH, NaNO 2 / H 2SO 4 // Ac 2O / DMAP
iii. LDA, ClPO(OEt)2
O
N N
O
DMAP:
4-N,N-D i m ethyl a minop y ridine
mixture of
Ac 2O / DMAP:
N N
C CH 3
O
6-g
use: TsNHNH 2 / EtOH, heat
THL, 1967, 3943.
OH
O
3(l)
O
(MVK)
CH 3CH CH 2
Robinson Annulation German invention, as acylating agent
LDA: Li N(iPr)2, ignored a long time, re-introduced by Michigan State U. became famous, appeared every week
HO
R
LiNH 2 / NH 3 (l)
RX
use: LiNH 2 / NH 3 (l) / R-X
O Cl
6-h
6-i.
JA CS, 1958, 80, 4599.
JA CS, 1955, 77, 3293.Me Ph
H
OSO 2CF 3Me C C Ph
via:
Me C
Ph
JOC, 1978, 43, 364.
Ar
Ar'H Br Ar C C Ar'
NaOEt
via:
Ar Ar'
Br i. NaOEt (when X = Br)
ii. BuLi (when X = -OSO 2CF 3)
?
heat
RCH=CH 2
:PBu RCH 2CH 2-O-PBu 3
RCH 2CH 2-OH
Ph-Se-PBu 3Ph-Se-CN
mechanism:
MCPBA OAc CO 2Me
OAc
MeO MeO 2C
NO 2Se
N
OAc
CO 2Me
OAc MeO
MeO 2C
minor
applied for reactions: without rearrangement;
no regiosiomer
C
C (CO 2H)2 / benzene
OH Ph
Ph
O
O Cl Cl
Cl
Cl
O
Cl Cl NC NC
O iii. Pd-C; or Ni; Pt, Rh
ii. chloronail
i. DDQ use base: DBN
i. CH 3I / Ag 2ii. HCHO / HCO 222use: heat
use: heat
b 7-i. p-TSOH.H 2O or CSA ii. weak acid: HOAc; HCO 2H; H 2C 2O 4use:
C C H
I
C C H NH 2
C C H OC(S)SMe C C H OAc C C H OMs C C H OH a
7-i h g
C
C
X C C C C
C CH
C O C C
f e d
c b a 7--C(O)-CH 3
CH-CH CH-CX C-OH
j
CX-CY
NaI / Zn (Cu)
i. Zn / acetone
i. CSCl 2
/
C C
OMs OMs C C Br
Br
C
C
OH OH
c
7-C
C
OH I
ii. CSCl 2 / P(OMe)3
P N
N
Ph
POCl 3 / py // Sn
via:
C C I
I
application: i. protect alkene: via Br 2 // Zn
CCCCC 36 o C CCCC=C 31 o C CCCC C Cl Cl
148 o C
S OR OR
C C Br
OAc
Zn / HOAc
O
AcO AcO
AcO
Br
OAc
Zn O
OAc OAc
OAc
JOC, 1978, 43, 364.
HOAc
https://www.doczj.com/doc/e915102442.html,, 1998, 2113.
ii. In / MeOH ii. purify compound
d
7-
e
7-
i. WCl 6 / RLi ii. LiPPh 2 / CH 3I product retention product inversion
Na R C H
C H
CH 2CH 2CH 2OH O
Cl
R
iii. Na
(special structure):
7-d.7-d.S R 1
R 2
R 1
R 2
(EtO)3P
use: (EtO)3P
Synthesis , 1977, 1134.
via : betaine, oxaphosphetane (NMR)O
not good for Ph 3P=CH 2function as base:
expensive
difficult to prepare
O
Et
CN
PPh 3
CN
PPh 3H O
PPh 3O CO 2Me
+not
Ph 3P CH Et
H C O
CO 2Me not
Ph 3P CH CO 2Me
Et
H O
+
+++stable ylid gives trans (E)
unstable ylid gives cis (Z)water soluble, removed by extraction
(comparison: O=PPh 3 highly soluble in organic solvent)
use:Li
Ph S
O
N Me
CH 2// Al (Hg)
Me 3SiCHR -Li +
Ph 3SiCH 2-Li + === Ph 3SiCH 2Br + n-BuLi (exchange)Me 3SiC -H-MgBr === Me 3SiCH 2Cl + Mg (metal reduction)
Ph 3SiC -HCH 2Ph === Ph 3SiCH=CH 2 + PhLi (addition to vinylsilane)Me 3SiC -HCO 2Et === Me 3SiCH 2CO 2Et + Li (metalation)Me 3SiCH=PPh 3 === Me 3SiCH 2PPh 3+ X - + KH
RO = MeO-, EtO-
use: (RO)2PO-CHR'
use: Ph 3P-CHR'vi. Sulfoximide (Johnson C.)iii. Silyl Wittig Reaction (Peterson Reaction)
ii. Phosphonate Wittig Reaction (Horner-Emmons Modification)i. Wittig Reaction 7-f
7-f.Synthesis, 1984, 384.THL, 1981, 2751.JOC, 1968, 33, 780.
iv. CH 2(ZnI)2
Chem. Lett, 1995, 259.
Synlett, 1988, 12, 1369.
2
CH 2(ZnI)2v. CH 2CHBr 2, Sm, SnI 2 / CrCl 3, THF
R
O R
vii. Grignard reagent:
1. TMSCH MgCl
use: TMSCH 2MgCl
THL, 1973, 3497.
THL, 1988, 4339. 2. NaOAc, AcOH
methylenation
O
C R
R'
3
H advantages over the Wittig:
1. by-products are more easily removed,
2. reaction suffers less from steric effects.
via:
(olefination reaction)
1953 discover
7-f.2
not for Wittig, ylid unstable
JOC, 1978, 43, 3253.
JACS, 1974, 96, 4706.
Chem. Lett, 1973, 1041.TiCl 3-LiAlH 4 / THF TiCl 3 / Mg TiCl 4 / Zn TiCl 4 / K ii. McMurry Coupling
i. use: N 2H 4 / H 2S / Pb(OAc)4
BASF, 1973, 2147.via:
Zn-Cu
P(OEt)1. H 2S
2. Pb(OAc)4
31. H 2S
2. Pb(OAc)4O
O
N S
N N N O
S
N N
S
O
N O
N N
N
S
N N
O
N N
O O
S
O O
N N
O
O O
O O
TiCl 3N 2H 4
有机反应类型与官能团之间的转化 一、有机化学反应类型归纳 1.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。包括:卤代反应、硝化反应、磺化反应、卤代烃的水解反应、酯化反应、酯的水解反应、醇分子间脱水反应等。 2.加成反应:有机物分子中不饱和的碳原子跟其他原子或原子团直接结合生成新的化合物的反应。包括:与氢气的加成反应 (烯、二烯、炔的催化加氢;苯、苯的同系物、苯乙烯催化加氢;醛、酮催化加氢;油脂的加氢硬化)|、与卤素单质的加成反应、与卤化氢的加成反应、与水的加成反应等。 3.脱水反应:有机物在适当条件下,脱去相当于水的组成的氢氧元素的反应。包括分子内脱水(消去反应)和分子间脱水(取代反应)。 4.消去反应:有机物在适当条件下,从一个分子脱去一个小分子(如水、HX等),而生成不饱和(双键或三键)化合物的反应。包括醇的消去反应和卤代烃的消去反应。 5.水解反应:广义的水解反应,指的凡是与水发生的反应,中学有机化学里能够与水发生水解反应的物质,一般指的卤代烃水解、酯的水解、油脂的水解(含皂化)、糖类的水解、肽及蛋白质的水解等。 6.氧化反应:指的是有机物加氧或去氢的反应。包括: (1)醇被氧化:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,去掉氢原子形成C=O键。注意:叔醇(羟基所在碳原子上无H)不能被氧化: ; (2)醛被氧化:醛基的C—H键断裂,醛基被氧化成羧基: ; (3)乙烯氧化:2CH2=CH2+O22CH3CHO; (4)有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。 (5)醛类及含醛基的化合物与新制碱性Cu(OH)2或银氨溶液的反应; (6)苯酚在空气中放置转化成粉红色物质(醌)。 7.还原反应:指的是有机物加氢或去氧的反应。包括: (1)醛、酮、烯、炔、苯及其同系物、酚、不饱和油脂等的催化加氢。 (2) C6H5-NO2 + 3Fe + 6HCl → C6H5-NH2 + 3FeCl2 + 2H2O 8.酯化反应:酸和醇作用生成酯和水的反应。 9.聚合反应:是指由小分子单体相互发生反应生成高分子化合物的反应。包括加聚反应和缩聚反应。 10.裂化反应:在一定条件下,把相对分子质量大、沸点高的长链烃,断裂为相对分子质量小、沸点低的短链烃的反应。深度裂化叫裂解。 11.显色反应、颜色反应: (1)苯酚溶液滴加氯化铁溶液——显紫色。 (2)淀粉溶液加碘水——显蓝色。 (3)蛋白质(分子中含苯环的)加浓硝酸——显黄色 二、官能团之间的转化知识梳理
精心整理有机合成中有机物官能团的引入、消除和转化方法 1.官能团的引入 2.官能团的消去 (1)通过加成反应消除不饱和键。 (2)通过消去反应、氧化反应或酯化反应消除羟基(—OH)。 (3)通过加成反应或氧化反应消除醛基(—CHO)。 (4)通过消去反应或水解反应消除卤素原子。 3.官能团的转化 (1)利用衍变关系引入官能团,如卤代烃伯醇(RCH (2) (3) 1. (1) (2) 2. (1)与 (2) (3) 3. (1) (3) (4) 1. (1) (2) 二元醇―→二元醛―→二元羧酸―→ (3)芳香化合物合成路线: 2.有机合成中常见官能团的保护 (1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH反应,把—OH变为 —ONa(或—OCH3)将其保护起来,待氧化后再酸化将其转变为—OH。 (2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl等的加成反应将其保护起 来,待氧化后再利用消去反应转变为碳碳双键。 (3)氨基(—NH2)的保护:如在对硝基甲苯对氨基苯甲酸的过程中应先把—CH3氧化成—COOH之后,再把
—NO2还原为—NH2。防止当KMnO4氧化—CH3时,—NH2(具有还原性)也被氧化。 有机合成中有机物官能团的引入、消除和转化方法练习【例1】工业上用甲苯生产对羟基苯甲酸乙酯(),其过程如下: 据合成路线填写下列空白: (1)有机物A的结构简式:____________________________________________________, B的结构简式:_____________________________________________________________。 (2)反应④属于__________反应,反应⑤属于____________反应。 (3)③和⑥的目的是__________________________________________________________。 (4) 【例2】 去)。 (1) (2) B: (3) ④ ⑤ ⑥ (4)在NaOH溶液中水解的化学方程式: 【例3】 1,4- A 【例4】 化合物,苯环上只含一个直支链,能发生加聚反应和水解反应。测得M的摩尔质量为 162g·mol-1,只含碳、氢、氧三种元素,且原子个数之比为5∶5∶1。 (1)肉桂酸甲酯的结构简式是。 (2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示 单链或双键)。G的结构简式为。 (3)以芳香烃A为原料合成G的路线如下: ①化合物E中的含氧官能团有________(填名称)。 ②E―→F的反应类型是__________,F―→G的化学方程式为_______________________。
烷烃——无官能团: 1.一般C4及以下是气态,C5以上为液态。 2.化学性质稳定,不能使酸性高锰酸钾溶液,溴水等褪色。 3.可以和卤素(氯气和溴)发生取代反应,生成卤代烃和相应的卤化氢,条件光照。 4.烷烃在高温下可以发生裂解,例如甲烷在高温下裂解为碳和氢气。烯烃——官能团:碳碳双键 1.性质活泼,可使酸性高锰酸钾溶液褪色。 2.可使溴水或溴的四氯化碳溶液褪色,发生加成反应,生成邻二溴代烷,例如乙烯和溴加成生成1,2-二溴乙烷。 3.酸催化下和水加成生成醇,如乙烯在浓硫酸催化下和水加成生成乙醇。 4.烯烃加成符合马氏规则,即氢一般加在氢多的那个C上。 5.乙烯在银或铜等催化下可以被空气氧化为环氧乙烷。 6.烯烃可以在镍等催化剂存在下和氢气加成生成烷烃 7.烯烃可以发生加聚反应生成高聚物,如聚乙烯,聚丙烯,聚苯乙烯等。 实验室制乙烯通过乙醇在浓硫酸作用下脱水生成,条件170℃。 炔烃——官能团:碳碳三键 1.性质与烯烃相似,主要发生加成反应。也可让高锰酸钾,溴水等褪色。 2.炔烃加水生成的产物为烯醇,烯醇不稳定,会重排成醛或酮。如乙
炔加水生成乙烯醇,乙烯醇不稳定会重拍生成乙醛。 3.乙炔和氯化氢加成的产物为氯乙烯,加聚反应后得到聚氯乙烯。 4.炔烃加成同样符合马氏规则 5.实验室制乙炔主要通过电石水解制的(用饱和食盐水)。 芳香烃——含有苯环的烃。 1.苯的性质很稳定,类似烷烃,不与酸性高锰酸钾,溴的四氯化碳反应,与溴水发生萃取(物理变化)。 2.苯可以发生一系列取代反应,主要有: 和氯,溴等卤素取代,生成氯苯或溴苯和相应的卤化氢(条件:液溴,铁或三溴化铁催化,不可用溴水。) 和浓硝酸,浓硫酸的混合物发生硝化反应,生成硝基苯和水。条件加热。 和浓硫酸反应生成苯磺酸,条件加热。 3.苯可以加氢生成环己烷。 4.苯的同系物的性质不同,取代基性质活泼,只要和苯环直接相连的碳上有氢,就可以被酸性高锰酸钾溶液氧化为苯甲酸。如甲苯可以使酸性高锰酸钾溶液褪色,被氧化为苯甲酸。无论取代基有多长,氧化产物都为苯甲酸。 5.苯分子中所有原子都在同一平面上。 6.苯环中不存在碳碳双键,六个碳原子之间的键完全相同,是一种特殊的大π键。
精品 2、按官能团分类 表l 一1 有机物的主要类别、官能团和典型代表物 1、电子式 2、结构式 3、线键式 4、实验式
同分异构体:(碳链异构、官能团异构) ①同分异构现象:化合物具有相同分子式,不同结构式的现象,叫做同分异构现象。 ②同分异构体:具有同分异构现象的化合物之间,互称为同分异构体。 同分异构体之间异同: 分子组成相同、分子量相同、分子式相 同 注意:同分异构体不仅存在于有机化合物中,也存在于无机化合物中。甚至有机化合物与无机化合物之间也存在同分异构体,如无机物氰酸铵[NH4CNO]和有机物尿素[CO(NH2)2]。 同系物:结构相似,分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。如甲烷和乙烷。 有机物命名: 烷烃可以根据分子里所含碳原子数目来命名。碳原子数在十以内的用甲、乙、丙、丁、戊、己、庚、辛、壬、癸来表示。例如,CH4叫甲烷,C5H12叫戊烷。碳原子数在十以上的用数字来表示。例如,C17H36叫十七烷。前面提到的戊烷的三种异构体,可用“正”“异”“新”来区别,这种命名方法叫习惯命名法。由于烷烃分子中碳原子数目越多,结构越复杂,同分异构体的数目也越多,习惯命名法在实际应用上有很大的局限性。因此,在有机化学中广泛采用系统命名法。下面以带支链的烷烃为例,初步介绍系统命名法的命名步骤。 (1)选定分子中最长的碳链为主链,按主链中碳原子数目称作“某烷”。 (2)选主链中离支链最近的一端为起点,用l,2,3等阿拉伯数字依次给主链上的各个碳原子编号定位,以确定支链在主链中的位置。例如: (3)将支链的名称写在主链名称的前面,在支链的前面用阿拉伯数字注明它在主链上所处的位置,并在数字与名称之间用一短线隔开。例如,用系统命名法对异戊烷命名: 2—甲基丁烷 (4)如果主链上有相同的支链,可以将支链合并起来,用“二”“三”等数字表示支链的个数。两个表示支链位置的阿拉伯数字之间需用“,”隔开。 如有侵权请联系告知删除,感谢你们的配合! 精品
有机物常见官能团的变化 江油一中 各类烃及烃的衍生物的相互转化,其实质是官能团之间的互换和变化。 一、 与卤素原子的有关变化: 1、 取代反应: ①烷烃与卤素单质光照下反应:CH 4 + Cl 2 CH 3Cl + HCl + Br 2 + HBr ③苯酚与溴水反应: + 3Br 2 + 3HCl ④ 醇与卤化氢反应:R OH + HBr R Br + H 2O ⑤苯同系物侧链与卤素单质反应: Cl 2 + HCl ⑥苯同系物与卤素单质反应: Br 2 + HBr 2: ① 烯烃与卤素单质加成: CH 2 CH 2 + Br 2 CH 2Br CH 2Br ②烯烃与卤化氢加成:CH 2 CH 2 + HCl CH 3 CH 2Cl ③炔烃与卤化氢、卤素单质加成: CH CH + Br 2 CH CH CH CH + HBr CH 2 CH 2Br 光 Fe OH Br -光照 Fe 催化剂 △ Br 催化剂 △
二、羟基有关的变化: 1、卤代烃碱性条件下水解生成醇: R X + H 2O R OH + HX 2、 氯苯水解制苯酚: + H 2O +HCl 3、烯烃与水加成:CH 2 CH 2 + H 2O CH 3CH 2OH 4、醛、酮还原:R CHO + H 2 R CH 2OH R COR ’ + H 2 R CH R ’ 5、脂水解:RCOOR ’+ H 2O RCOOH + R ’OH ①CH 3COOCH 2CH 3 + H 2O CH 3COOH + CH 3CH 2OH ②+ H 2O + CH 3COOH 1735COOCH 2 ③ + 3H 2O + 3C 17H 35COOH 三、与羰基有关的变化: 1、 氧化反应: ①烯烃氧化:2CH 2 CH 2 + O 2 2CH 3CHO ②醇氧化:2RCH 2OH + O 2 2RCHO + 2H 2O 2R CH R ’ + O 2 2R C R ’ + 2H 2O ③烯烃臭氧分解: RCH CHR ’ RCHO + R ’CHO 2、炔烃水化: CH CH + H 2O CH 3CHO 3、羰基合成:CH 2 CH 2 + CO + H 2O CH 3CH 2CHO △ 碱 3 催化剂 高温、高压 催化剂 催化剂 催化剂 OH 催化剂 稀硫酸 △ 3 催化剂 △ C 17H 35COOCH C 17H 352 催化剂 △ CH 2 CH 2OH CHOH 催化剂 △ △ 催化剂 OH 催化剂 △ O 3 Zn 、H 2O 催化剂 催化剂
有机化学基团名称翻译 A 伸乙烷合萘基;伸二氢苊基 acenaphtheneylene 亚乙烷合萘基;亚二氢苊 基 acenaphthenylidene 醋酰胺基;乙酰胺基 acetamido; acetamino 乙炔基 acetenyl;ethynyl 乙酰乙酰基 acetoacetyl 丙酮基 acetonyl 亚丙酮基 acetonylidene 乙酰氧基 acetoxy 乙酰基 acetyl 乙酰亚胺基 acetylimino 酸硝基 aci-nitro 吖啶基 acridinyl 丙烯酰基 acrylyl; acryloyl 己二酰基 adipoyl; adipyl 脲[基]羰基;脲甲酰基 allophanyl; allophanoyl 烯丙基 allyl 甲脒基 amidino; guanyl 酰胺基 amido 酰胺草酰基;草酰胺酰基 amidoxalyl; oxamoyl 胺基 amino 戊基 amyl; pentyl 伸戊基 amylene 亚戊基 amylidene 亚戊基 amylidene; pentylidene 苯胺基 anilino 大茴香亚甲基;对甲氧苯亚甲基;对甲氧亚苄 基 anisal; anisylidene 甲氧苯胺基 anisidino 大茴香酰基;对甲氧苯甲酰基;对甲氧苄酰 基 anisoyl 大茴香亚甲基;对甲氧亚苄基;对甲氧苯亚甲 基 anisylidene; p-methoxybenzylidene; anisal 邻胺苯甲酰基;邻胺苄酰基 anthraniloyl; anthranoyl 蒽基 anthranyl; anthryl 蒽醌基 anthraquinonyl 伸蒽基;次蒽基 anthrylene 精胺酰基 arginyl 亚胂酸基 arsinico 胂基 arsino 胂酸基 arsono 亚胂基 arsylene 细辛基;2,4,5-三甲氧苯基 asaryl; 2,4,5-trimethoxyphenyl 天[门]冬酰胺酰基 asparaginyl; asparagyl 天[门]冬胺酰基 aspartyl 阿托酰基;颠茄酰基;2-苯丙烯酰基 atropoyl 壬二酰基 azelaxyl 迭氮基;三氮基 azido; triazo 偶氮亚胺基 azimino; azimido 次偶氮基 azino 偶氮基 azo 氧偶氮基 azoxy B 苯亚甲基;亚苄基 benzal 苯甲酰胺基;苄酰胺基 benzamido 苯亚磺酰基 benzene sulfinyl; phenylsulfinyl 苯磺酰胺基 benzenesulfonamido 苯磺酰基 benzenesulfonyl 次苄基 benzenyl; benzylidyne 二苯甲基 benzhydryl; diphenylmethyl 二苯亚甲基 benzhydrylidene; diphenylmethylene 联苯胺基 benzidino 亚苄基;苯亚甲基 benzilidene 二苯羟乙酰基 benziloyl 苯并咪唑基 benzimidazolyl
常见有机化合物官能团 1. 苯基 苯(benzene, C6H6)有机化合物,是组成结构最简单的芳 香烃,在常温下为一种无色、有甜味的透明液体,并具有强烈的芳香气味。可燃,有毒,为IARC 第一类致癌物。苯具有的环系叫苯环,是最简单的芳环。苯分子去掉一个氢以后的结构叫苯基,用Ph 表示。因此苯也可表示为PhH 2. 羟基羟基,又称氢氧基。是由一个氧原子和一个氢原子相连组成的一价原子团,化学式-OH。 在无机物中在无机物中,通常含有羟基的为含氧酸或其的酸式盐。含羟基的物质溶解于水会电离出氢离子,因此含羟基的物质水溶液多成偏酸性。 在有机物中在有机化学的系统命名中,在简单烃基后跟着羟基的称作醇,而糖类多为多羟基醛或酮。 羟基直接连在苯环上的称作酚。 具体命名见OH 原子团的命名注:乙醇为非电解质,不显酸 性。 羟基的性质 1. 还原性,可被氧化成醛或酮或羧酸
2. 弱酸性,醇羟基与钠反应生成醇钠,酚羟基与氢氧化钠反应生成酚钠 3. 可发生消去反应,如乙醇脱水生成乙烯 OH 原子团的命名此原子团在有机化合物中称为羟基,是醇( ROH )、酚(ArOH )等分子中的官能团;在无机化合物水溶液中以带负电荷的离子形式存在(OH-1 ),称为氢氧根。当羟基与苯环相连形成苯酚时,可使苯环致活,显弱酸性。再进基主要进入其邻位、对位。 羟基与氢氧根的区别在很多情况下,由于在示性式中,羟基和氢氧根的写法相同,因此羟基很容易和氢氧根混淆。 虽然氢氧根和羟基均为原子团,但羟基为官能团,而氢氧根为离子。而且含氢氧根的物质在水溶液中呈碱性,而含羟基的物质的水溶液则多呈偏酸性。氢氧根和羟基在有机化学上的共性是亲核性。 有机合成中羟基的保护羟基是有机化学中最常见的官能团之一,无论是醇羟基还是酚羟基均容易被多种氧化剂所氧化。因此在多官能团化合物 的合成过程中,羟基或者部分羟基需要先被保护,阻止它参与反应,在适当的步骤中再被转化。 3. 烃基
无官能团:烷烃—— C4以上为液态。及以下是气态,C51.一般 2.化学性质稳定,不能使酸性高锰酸钾溶液,溴水等褪色。可以和卤素(氯气和溴)发生取代反应,生成卤代烃和相应的卤化3. 氢,条件光照。4.烷烃在高温下可以发生裂解,例如甲烷在高温下裂解为碳和氢气。 烯烃——官能团:碳碳双键 1.性质活泼,可使酸性高锰酸钾溶液褪色。 2.可使溴水或溴的四氯化碳溶液褪色,发生加成反应,生成邻二溴代烷,例如乙烯和溴加成生成1,2-二溴乙烷。 3.酸催化下和水加成生成醇,如乙烯在浓硫酸催化下和水加成生成乙醇。 4.烯烃加成符合马氏规则,即氢一般加在氢多的那个C上。 5.乙烯在银或铜等催化下可以被空气氧化为环氧乙烷。 6.烯烃可以在镍等催化剂存在下和氢气加成生成烷烃 7.烯烃可以发生加聚反应生成高聚物,如聚乙烯,聚丙烯,聚苯乙烯等。 实验室制乙烯通过乙醇在浓硫酸作用下脱水生成,条件170℃。 炔烃——官能团:碳碳三键 1.性质与烯烃相似,主要发生加成反应。也可让高锰酸钾,溴水等褪色。 炔烃加水生成的产物为烯醇,烯醇不稳定,会重排成醛或酮。如乙
炔加水生成乙烯醇,乙烯醇不稳定会重拍生成乙醛。 3.乙炔和氯化氢加成的产物为氯乙烯,加聚反应后得到聚氯乙烯。 4.炔烃加成同样符合马氏规则 5.实验室制乙炔主要通过电石水解制的(用饱和食盐水)。 芳香烃——含有苯环的烃。 1.苯的性质很稳定,类似烷烃,不与酸性高锰酸钾,溴的四氯化碳反应,与溴水发生萃取(物理变化)。 2.苯可以发生一系列取代反应,主要有: 和氯,溴等卤素取代,生成氯苯或溴苯和相应的卤化氢(条件:液溴,铁或三溴化铁催化,不可用溴水。) 和浓硝酸,浓硫酸的混合物发生硝化反应,生成硝基苯和水。条件加热。 和浓硫酸反应生成苯磺酸,条件加热。 3.苯可以加氢生成环己烷。 4.苯的同系物的性质不同,取代基性质活泼,只要和苯环直接相连的碳上有氢,就可以被酸性高锰酸钾溶液氧化为苯甲酸。如甲苯可以使酸性高锰酸钾溶液褪色,被氧化为苯甲酸。无论取代基有多长,氧化产物都为苯甲酸。 5.苯分子中所有原子都在同一平面上。 6.苯环中不存在碳碳双键,六个碳原子之间的键完全相同,是一种特
有机合成中有机物官能团的引入、消除和转化方法 1.官能团的引入 2.官能团的消去 (1)通过加成反应消除不饱和键。 (2)通过消去反应、氧化反应或酯化反应消除羟基(—OH)。 (3)通过加成反应或氧化反应消除醛基(—CHO)。 (4)通过消去反应或水解反应消除卤素原子。 3.官能团的转化 (1)利用衍变关系引入官能团,如卤代烃水解取代伯醇(RCH 2OH)氧化还原醛――→氧化 羧酸。 (2)通过不同的反应途径增加官能团的个数,如 (3)通过不同的反应,改变官能团的位置,如 有机合成中碳架的构建 1.有机成环反应 (1)有机成环:一种是通过加成反应、聚合反应来实现的;另一种是通过至少含有两个相同或不同官能团的有机物脱去小分子物质来实现的。如多元醇、羟基酸、氨基酸通过分子内或分子间脱去小分子水等而成环。 (2)成环反应生成的五元环或六元环比较稳定。 2.碳链的增长 有机合成题中碳链的增长,一般会以信息形式给出,常见的方式如下所示。 (1)与HCN 的加成反应 (2)加聚或缩聚反应,如n CH 2 (3)酯化反应,如CH 3CH 2OH +CH 3COOH 浓 CH 3COOCH 2CH 3+H 2O 。 3.碳链的减短 (1)脱羧反应:R —COONa +NaOH ――→CaO △R —H +Na 2CO 3。
(3)水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。 (4)烃的裂化或裂解反应:C 16H 34――→高温C 8H 18+C 8H 16; C 8H 18――→高温 C 4H 10+C 4H 8。 合成路线的选择 1.中学常见的有机合成路线 (2)一元合成路线 R —CH=CH 2――→HX 卤代烃――→NaOH 水溶液△一元醇――→氧化一元醛――→氧化一元羧酸―→酯 (3)二元合成路线 CH 2=CH 2――→X 2CH 2X-CH 2X ――→NaOH 水溶液△二元醇――→氧化二元醛――→氧化二元羧酸→???? ? 链酯环酯 高聚酯 (3)芳香化合物合成路线: 2.有机合成中常见官能团的保护 (1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH 反应,把—OH 变为—ONa(或—OCH 3)将其保护起来,待氧化后再酸化将其转变为—OH 。 (2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl 等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。 (3)氨基(—NH 2)的保护:如在对硝基甲苯――→合成 对氨基苯甲酸的过程中应先把—CH 3氧化成—COOH 之后,再把—NO 2还原为—NH 2。防止当KMnO 4氧化—CH 3时,—NH 2(具有还原性)也被氧化。 有机合成中有机物官能团的引入、消除和转化方法 练习 【例1】 工业上用甲苯生产对羟基苯甲酸乙酯( ),其过程如下: 据合成路线填写下列空白: (1)有机物A 的结构简式:____________________________________________________, B 的结构简式:_____________________________________________________________。 (2)反应④属于__________反应,反应⑤属于____________反应。 (3)③和⑥的目的是__________________________________________________________。 (4)写出反应⑥的化学方程式:_________________________________________________。 【例2】 由环己烷可制备1,4-环己醇二醋酸酯。下面是有关的8步反应(其中所有无机产物都已略去)。
i 5-7-g f e d c b a e d c b a i h g f e d c b a h g f e d c b a h g f e d c b a 6-4-3-1-2-i h g f e d c b a C=C -C(O)-CH 3 CH-CH CH-CX F u n c t i o n a l G r o u p I n t e r c o n v e r s i o n C=C C C C=C C C RCH 2-SO 2Ph RC CH C C C-NH 2; C-NO 2C-OH C(OR)2; C(SR)2C=C-OR; C=C-SR C C C N C=N-OH, C=N-H C=S C=O C=O C-C(O)Z C=C C=O C-OH C-X C-N C-H C-N C=O C---OH C-OC(O)R C-X C-OCH 2OR C-NH 2 C-OR C-H C-OH C=C C-H C(O)OR C-(OR)2C-OH C-OR C-CHO C-CO 2H C-CN C=C C=O C-S C-X C-OH C-H C=C j C(O)X h C N j k C-H C-Br 8-C-X i C-OH C-OH C(O)Z d c b a e d c b a f C-NH 2C-H j CX-CY C C X C=O h g f i C CH RCH(CO 2H)-CH 3-C(O)-CH 3 O O O X CRR'=CHX j C O C-NH 2C-CN 9-C-CH 3 C-X a e C=O
1-a dry pyridine: from CaH 2 and distilled triflate mesylate tosylate S O O O RCH 2CF 3 S O O O RCH 2CH 3 CH 3 CH 3 CH 3 OH (2). for 3' alcohol: LiAlH 4 (1). for 1', 2' alcohol: 1-i h g f e d c b a C-CHO C-CO 2H C-CN C=C C=O C-S C-NH 2C-X C-OH C-H CH 3 CH 3 CH 3 H n -Bu SnH C S O Ph Cl RCH 2-H CH 3 S O O O RCH 2CH 3 S O O Cl RCH 2OH purification textbook ~ $ 30 / Kg toluenesulfonyl chloride (s)methanesulfonyy chloride (l)~ $ 30 / Kg j C(O)X Ph 2SiHCl / InCl 3 Ph Ph Ph Ph JOC, 2001, 66, 7741. ii. Ph 2SiHCl / InCl 3 i. p -TsCl // LiAlH 4 i. ClC(S)OPh // n -Bu 3SnH Cl 2 via: a unique Lewis acid catalyst, acceleratedeoxgyenation InCl 3 indium trichloride ii. Et 3SiH / Lewis acid J. Org. Chem. 2000, 65, 6179 JOC, 2000, 65, 6179. CHCl 2rt, 3 hr
标准文档 实用文案常见官能团的性质 一. 中学有机化合物分类及常见官能团名称和主要性质
标准文档 实用文案 注:烷烃中的烷基,芳香烃中的苯基都不是官能团。 二. 有机官能团的化学性质与有机基本反应 1. 氧化反应 (1)燃烧。凡是含碳氢的有机化合物燃烧都生成二氧化碳和水。 烃的燃烧通式: 烃的含氧衍生物的燃烧通式: (2)被酸性高锰酸钾氧化。能使酸性高锰酸钾褪色的有机物有: ①不饱和烃、不饱和烃的衍生物(含碳碳双键、碳碳三键); ②苯的同系物(苯基上的烃基易被氧化); ③含醛基的有机物:醛、甲酸、甲酸酯、甲酸盐、葡萄糖; ④石油产品(裂解气、裂化气)。 (3)羟基的催化氧化。某些含羟基的有机物在催化剂的作用下,能被氧气氧化成醛或酮。 当与羟基相连的碳原子上有两个氢原子时,羟基能被氧化成醛基。如: 22232232CHCHOHOCuCHCHOHO 当与羟基相连的碳原子上有一个氢原子时,羟基能被氧化成羰基(碳氧双键)。如:
标准文档 实用文案当与羟基相连的碳原子上没有氢原子时,羟基不能被氧化。 (4)醛基的氧化。有机物中的醛基,不仅可以被氧气氧化成羧基;而且还能被两种弱氧化剂(银氨离子和铜离子)氧化成羧基。 醛基被氧气氧化。如: 22323CHCHOOCHCOOH?????催化剂? ??AgNH32氧化。如: 银镜反应,醛基被?? ??CHCHOAgNHOHCHCOONHAgNHHO33234322223??????????????()△ 醛基被Cu OH()2氧化。如: CHCHOCuOHCHCOOHCuOHO3232222???????()? 2. 取代反应。 有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应。中学常见的取代反应有: (1)烷烃与卤素单质在光照下的取代。如: CHClCHClHCl423?????光 (2)苯与苯的同系物与卤素单质、浓硝酸等的取代。如: (3)酚与浓溴水的取代。如: (4)酯化反应。酸和醇在浓硫酸作用下生成酯和水的反应,其实质是羧基与羟基生成酯基和水的反应。如: CHCH OH CHCOOH323?CH COOCH CHHO3232? (5)水解反应。水分子中的?OH或?H取代有机化合物中的原子或原子团的反应叫水解反应。
有机合成中有机物官能团的引入、消除和转化方法1.官能团的引入
2.官能团的消去 (1)通过加成反应消除不饱和键。 (2)通过消去反应、氧化反应或酯化反应消除羟基(—OH)。 (3)通过加成反应或氧化反应消除醛基(—CHO)。 (4)通过消去反应或水解反应消除卤素原子。 3.官能团的转化 (1)利用衍变关系引入官能团,如卤代烃水解 取代伯醇(RCH2OH) 氧化 还原醛――→ 氧化 羧酸。 (2)通过不同的反应途径增加官能团的个数,如 (3)通过不同的反应,改变官能团的位置,如
有机合成中碳架的构建 1.有机成环反应 (1)有机成环:一种是通过加成反应、聚合反应来实现的;另一种是通过至少含有两个相同或不同 官能团的有机物脱去小分子物质来实现的。如多元醇、羟基酸、氨基酸通过分子内或分子间脱去小分子水等而成环。 (2)成环反应生成的五元环或六元环比较稳定。 2.碳链的增长 有机合成题中碳链的增长,一般会以信息形式给出,常见的方式如下所示。 (1)与HCN的加成反应
(2)加聚或缩聚反应,如n CH 2 (3)酯化反应,如CH 3CH 2OH +CH 3COOH 浓 CH 3COOCH 2CH 3+H 2O 。 3.碳链的减短 (1)脱羧反应:R —COONa +NaOH ――→CaO △ R —H +Na 2CO 3。 (3)水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。 (4)烃的裂化或裂解反应:C 16H 34――→高温C 8H 18+C 8H 16; C 8H 18――→高温C 4H 10+C 4H 8。 合成路线的选择 1.中学常见的有机合成路线 (2)一元合成路线 R —CH=CH 2――→HX 卤代烃――→NaOH 水溶液△一元醇――→氧化一元醛――→氧化一元羧酸―→酯 (3)二元合成路线 CH 2=CH 2――→X 2CH 2X-CH 2X ――→NaOH 水溶液△二元醇――→氧化二元醛――→氧化二元羧酸→???? ? 链酯环酯 高聚酯 (3)芳香化合物合成路线: 2.有机合成中常见官能团的保护 (1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH 反应,把—OH 变为—ONa(或—OCH 3)将其保护起来,待氧化后再酸化将其转变为—OH 。 (2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl 等的加成反应
人0 Xfi 甲 It 草 幺子弍:cooph 胪J2分矣:WSffl *0u 乙氢甲It 耳 分子式:COOK 年屋分类:wsm 0-CH ) *宙:甲丘甲離華 分子式:COOMa 舗產分空:進荃GO COOH 命屋分类: 名 ?: isnJLILM 分子弍:CO(t-Bu) 严厘分类:樓生团 NH 2 塔祢:毎基甲毎基 牙子式:CONH2 胪雇分类:碳基团 "乞 件 名练:异丁 It 狂 分子式:CO(i-Pr) 序酌类:碳荃团 幺祢:乙醉基 另子式:COCH3 所斥分类:O 团 兔?u 宋甲配狂 毎子5:! COPh 豹压分芬:儀荃团 名洽:甲tt^;IE£ 分子式:CHO 所斥分类:os 名冻:★甲狂 分子式:CH2Ph 斯应分癸:襪荃团 RT 名 W : B£ 分子北:CN 所?分as :审棊0= R£H 名祢:乙決基 分子弍:C2H 所匡分卒:谑菇团 Q '5° 名称:三 分孑式:CPh3 所舄分类:碳基匡 名越U 三异丙荃甲基 分孑式:C(i-Pr)3 所床分类:蘇因 CI R ------------ I CI 名三気甲基 分?式:ccim 所廂分类:碳至因 R --------- F r 名称:三気甲基 分子式:CF3 所耳分类:蘇因 名粽:魅內基 分子式:CH=CH2CH2 所泾分25 :強芝团 名稼:乙垛基 分子式:CH=CH2 所至分2$:审棊01 名称:魚甲能基 牙子式:COCI 子居分 类:WSS
R H^C 名徐:异戊基分子式:i-Am 所雇分 类:碳链 平3 R - H3 CH3 名徐:叔丁基分子式:t-Bu 所雇分类:谀链 R I CH3 名徐:仲丁基分子式:s-Bu 所層分类:碳涟 R CH3 H CH3名務:异丁 基分子式:I-BU 所属分类:碳链 CH3 T CH3 名称:异丙基分子式:i-Pr 所 犀分类:碳链 n/W1 名称:正戊基外子式:n?C5 所雇分类:谀 链 名探:正丁基 份孑式:n?C4 所属分类:碳链 :心 名称:正丙基 分子式:n?C3 所犀分类:碳 链 攵徐:环主基分子式:C-C8 所属分类:碳环 乂徐:环霞基 分孑式:C-C7 所属分类:碳环 X称:茏基 分子式:bpn 所属分类:碳环 兔徐:茂基 分子式:C- C5P 所属分类:碳环 名徐:环己基分子式:c? C6 所属分类:碳环名徐:环戊基 分子式:c<5 所属分类:碳环 □ 名徐:环丁基 分子式:c? C4 所属分类:碳环 △ 名青:环丙基 分子式:c<3 所属分类:碳环
有机物官能团与性质 [知识归纳] —R —OH 其中: 1、能使KMnO4褪色的有机物: 烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂 2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂 3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖 4、具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸 5、能发生银镜反应或与新制Cu(OH)2反应的有机物: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖 6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃 7、能发生颜色(显色)反应的有机物:
[有机合成的常规方法] 1.引入官能团: ①引入-X 的方法:烯、炔的加成,烷、苯及其同系物的取代 ②引入-OH 的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和CO 2 ③引入C=C 的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入C=O 2.消除官能团 ①消除双键方法:加成反应 ②消除羟基方法:消去、氧化、酯化 ③消除醛基方法:还原和氧化 3.有机反应类型 常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。能够发生各种反应类型的常见物质如下: ①烷烃、芳香烃与X 2的反应 (1)取代反应 ②羧酸与醇的酯化反应 ③酯的水解反应 ①不饱和烃与H 2、X 2、HX (2)加成反应 的反应 ②醛与H 2的反应 (3)加聚反应:烯烃、炔烃在一定条件下的聚合反应。 C H COOH O O O O C H 2CH 2Br Br C H 2CH O O C OCH 2CH 2O C []n CHO
一、有机物间相互转化关系
二、能与溴水发生化学反应而使溴水褪色或变色的物质
1、有机物: ⑴ 不饱和烃(烯烃、炔烃、二烯烃等) ⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯) 2、无机物: ⑴ -2价的S (硫化氢及硫化物) ⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe 6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 3 6FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 3 2FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2 ⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO 2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3 变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应) △
三、能萃取溴而使溴水褪色的物质 上层变无色的(ρ>1):卤代烃(CCl4、氯仿、溴苯等)、CS2等; 下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和 烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质 1、有机物: ⑴不饱和烃(烯烃、炔烃、二烯烃等) ⑵不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶石油产品(裂化气、裂解气、裂化汽油等) ⑷醇类物质(乙醇等) ⑸含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹天然橡胶(聚异戊二烯) ⑺苯的同系物 2、无机物: ⑴氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵+ 2价的Fe(亚铁盐及氢氧化亚铁)
JA C S, 1972, 94, 7159. L A H ------------ alm ost all: ald, ketone, acie, ester, acyl X, anhydride N aB H4 --------------- not for acid, ester (but L iB H4 w ork for ester) B2H6 --------------- not for ester, acyl X, anhydride; from top: L iA lH4; N aB H4; N a / N H3 A l (O i Pr)3 / i PrO H ----------- M eerw ein-Pondorf-V erley rxn IrC l4 / i P rO H / P(O M e)3 ------ H enbest rxn L iB H(sec Bu)3 ------------------ H. C. B row n from bottom: (2). stereoselective: (1). regioselective: 3-h (3). H C H O reagent: M e C H O M e O H H C H O JA C S, 1935, 511, 903. C H3C H O C(C H2O H)4 2 O rg.Syn, 1925, 4, 53. H C H O / K O H H C H O / C a(O H)2 S ynthesis, 1994, 1007. Ph N O2 O Ph N O2 H O H B H / SM e JO C, 2001, 66, 7514. JO C, 2003, 68, 2030. O B H3 / T H F 99.5 % trans solvent: T H F, S M e2 3-i R3B, H O C H2C H2O H // H2O2 // N aO H JO C, 1986, 51, 4925. C O R R R3B R R R R R3C B O H O C H2C H2O H R3C B O O H2O2 O H R3 H O B O O R3C H2O R3C O H
含氧官能团不同的碳氧键会因其中原子程度的不同而有性质上的差异。sp2杂化的氧原子有,而sp3则有。 分类官能团名称化学式结构式英文前缀英文后缀例子 卤代甲酰基RCOX haloformyl- -oyl halide ROH hydroxy- -ol RCOR' keto-, oxo- -one
RCHO aldo- -al ROCOOR alkyl carbonate RCOO?carboxy- -oate RCOOH carboxy- -oic acid ROR' alkoxy- alkyl alkyl ether RCOOR' alkyl alkan oate ROOH hydroperoxy- alkyl hydroperoxide
ROOR peroxy- alkyl peroxide []含氮官能团 分类官能团名称化学式结构式英文前缀英文后缀例子 -amide RCONR 2carboxamido- -amine RNH 2amino- R NH amino- -amine 2 N amino- -amine R 3
R N+ammonio- -ammonium 4 RC(=NH)R' imino- -imine RC(=NR)R'imino- -imine RC(=NH)H imino- -imine RC(=NR')H imino- -imine RC(=O)NC(=O)R' imido- -imide alkyl azide RN 3azido- R' azo- -diazene RN 2 ROCN cyanato- alkyl cyanate RNC isocyano- alkyl isocyanide
高中常见有机化合物结构与性质总结 物质类别特征结构(官能团)断键位置反应类型试剂条件反应产物烷烃取代X2,光照 烯烃 加成 X2的CCl4溶液 HX H2O,催化剂 加成,还原H2,催化剂 加聚一定条件 ——氧化酸性KMnO4溶液酸性KMnO4溶液褪色 炔烃或 加成 X2的CCl4溶液或 HX,催化剂,加热或加成,还原H2,催化剂或 ——氧化酸性KMnO4溶液酸性KMnO4溶液褪色 芳香烃 取代 X2,FeX3 HNO3,浓H2SO4,加热 加成3H2H2,Ni,加热 取代 HNO3,浓H2SO4,加热 氧化酸性KMnO4溶液 C C H H C C C C X X C C X H C C OH H C C C H H X NO2 R R NO2 NO2 O2N R H H H C H COOH C H H C H H C H X C H X C X X C X X C C H H C C H X C C X X C C C C C C C C H C X C C ]n [ C
物质类别 特征结构(官能团) 断键位置 反应类型 试剂条件 反应产物 卤代烃 —X 取代 NaOH 水溶液(催),加热 消去 NaOH 乙醇溶液(催), 加热 醇 —OH 取代、置换 Na 取代、酯化 羧酸—COOH ,浓H 2SO 4,加热 氧化 O 2,Cu ,加热 取代 浓HX 溶液,加热 消去 浓H 2SO 4,加热 —CH 2—OH —— 氧化 酸性KMnO 4溶液(或酸性K 2Cr 2O 7溶液) —COOH 酚 取代 溴水 取代、置换 Na 中和 NaOH 溶液 —— 氧化 空气 —— 醛 氧化 O 2,催化剂,加热 (或银氨溶液, 或新制 Cu(OH)2 浊液) 羧 加成、还原 H 2,催化剂,加热 羧酸 取代、置换 Na 中和 NaOH 溶液 取代、酯化 醇,浓H 2SO 4,加热 酯 取代、水解 稀H 2SO 4,加热 (或NaOH 溶液,加热) O H ONa OH OH H H H OH Br Br Br O C H ONa C O O C C C C X C O C H H H C O OH C C OH C H O C O H ONa C O OH C O O C R O OH C O H C OH H H C O H C O OH C O C O H C C X C OH C C C X H O C R O HO R OH C O O C R O